基于“宏观辨识与微观探析”高中化学教学设计
——以“乙烯”公开课为例
孙 悦,陆国志
(吉林师范大学 化学学院,吉林 四平 136000)
我国教育部在2018年正式发布的《普通高中化学课程标准(2017年版)》中提出,高中化学教学应以发展学生化学核心素养为主旨,优化教学流程,发展素质教育,促进专业发展,从而实现立德树人的总体目标。宏观辨识与微观探析是化学核心素养的重要组成部分。
宏观辨识与微观探析是从分子、原子层次对物质结构、性质、能量转变及相互关系的基本认识[1]。学生通过学习或观察物质的存在形态、变化特征,用化学符号和文字进行描述就是“宏观辨识”;而从微观角度对物质结构组成、变化特征的本质原因进行探究分析就是“微观探析”。本文以人教版高中化学必修第二册《乙烯》的教学设计为例,设计教学过程并分析如何有效化学核心素养,帮助学生构建相关的化学核心观念。
1 落实宏观辨识和微观探析素养的教学设计构思
课堂教学活动是学生成长发展和培育学生核心素养最重要的途径之一。教学设计是一堂课的前提和基础,高中生化学核心素养的发展离不开化学课程的实施,离不开化学知识的学习,离不开经历化学问题的解决过程[2]。教师在进行教学设计时,可以将“乙烯”的核心知识与实际的生产生活相联系、与多彩的化学实验相结合、与直观的结构模型相对应,通过小组讨论、实验探究、问题解决等课堂活动,培养学生归纳核心知识框架,解决化学问题的能力,最后揭示内在本质,促进学生核心素养形成。
2 落实宏观辨识和微观探析素养的教学设计过程
2.1 基于生活实际提问,激发学生学习兴趣
化学是一门与生活紧密联系的学科。在课堂教学中,教师要创设学生感兴趣的真实问题情境,激发学生学习的积极性,同时在真实情境中培养学生正确的价值观和责任感。
[教学片段]创设情境:19世纪,在亚速尔群岛,有个木匠在工作时无意中将美人蕉的碎屑烧了,结果美人蕉屑燃烧的烟雾弥漫开来后温室中的植物提前开了花[3]。使加速植物开花的气体就是乙烯。本节课我们共同学习乙烯的相关知识。(在课堂最后对乙烯应用的总结中可以回顾此故事情境,体现出前后呼应的整体性)
问题引入:根据预习教材回答问题,乙烯的用途有哪些?乙烯的产量有什么意义?乙烯的主要来源是什么?
学生回答:乙烯是从石油中获得的重要的化工原料,乙烯的产量可以衡量一个国家的石油化工发展水平。
2.2 利用创新微型实验,体现化学宏观价值
化学是一门以实验为基础的科学。教师在进行教学设计时可以在教材实验的基础上,根据学生的学习情况和学校的资源配备,创设有助于培养学生核心素养和发扬学生正确价值观的实验活动。
[教学片段]药品仪器:盛满乙烯的集气瓶、注射器、盛有少量酸性KMnO4溶液的带胶塞的集气瓶、盛有少量溴水的带胶塞的集气瓶、火柴。
实验过程:学生分组实验:①用注射器从集气瓶中抽出乙烯,穿过胶塞注入到盛有少量酸性KMnO4溶液的集气瓶中,振荡后静置片刻,观察现象;②再用注射器从集气瓶中抽出乙烯,穿过胶塞注入到盛有少量溴水的集气瓶中,振荡后静置片刻,观察现象;③用注射器从集气瓶中抽出乙烯,用火柴在针头处点燃,观察现象。
根据实验现象总结乙烯化学性质:乙烯具有可燃性,且能使酸性高锰酸钾溶液、溴水褪色。教师类比前面学过的甲烷是正四面体结构,不能使酸性高锰酸钾溶液和溴水褪色,那乙烯的空间结构又是怎么样的呢?接下来从微观角度对乙烯的结构进行探索。
新型的微型实验既达到探究乙烯性质的实验目的,同时让学生了解化学实验要满足“科学性、安全性、可行性和简约性”等要求,与传统实验进行对比,体现其简化装置、节省时间、节约药品,安全环保等优势。
2.3 利用球棍模型,组建物质微观结构
能从元素和原子、分子水平认识物质的组成、结构、性质和变化,形成“结构决定性质”观念是宏观辨识与微观探析的内涵之一。而有机物的空间结构比较复杂,在化学学习中产生一定的困难。学习的实质是“主动地形成认知结构,并通过把新获得的知识和已有的认知结构联系起来, 积极地建构其知识体系”对于乙烯结构的学习可以从乙烷的空间结构入手[4]。
[教学片段]学生自主拼出乙烷的球棍模型,并根据已学知识完成表1。

表1 实验任务表
学生通过预习教材可知乙烯的分子式是C2H4,与乙烷C2H6相比少了2个氢原子,学生可以将乙烷的球棍模型中拿掉2个代表氢原子的小球,见图1、图2。根据价键理论,在有机物中碳原子形成四个共价键,将拿掉两个氢原子后碳的两个半键连接成一个新的碳碳键,让学生通过对模型的观察完成表格,见表2。

图1 乙烷的结构 图2 乙烷去掉2个氢原子

表2 实验任务表
通过以上教学活动,将乙烯的结构“可视化”,化学模型表征,使学生更容易理解微观结构,“宏观辨识和微观探析”这个素养就是要求培养学生从不同角度理解化学事实和实验现象,体会物质变化的丰富性和多样性。
2.4 学生模拟反应历程,加深反应本质理解
在课堂上,学生参与模拟演示复杂抽象的有机反应历程,使学生对化学知识理解得更透彻。寓教于乐,在教师的解说下,学生既学会了知识,又能从化学的学习中找到乐趣。通过问题的解决、实验探究和归纳讨论等逐渐形成“宏观到微观,微观到符号表征”,最后揭示内在联系或本质,形成概念,从而促进学生核心素养的形成。
[教学片段]教师引导学生思考碳碳双键中的两条键是否相同,并展示表3。(信息:键能表示断裂或形成 1 mol 化学键所吸收或放出的能量)

表3 断键类型和键能
根据表格让学生总结:乙烯碳碳间的两条键键能不同,其中一条键键能小,易断裂,因此乙烯的化学性质活泼,而乙烯使溴水或溴的四氯化碳溶液褪色是因为发生了“加成反应”,那么加成反应的反应历程如何呢?播放视频,通过视频使学生掌握加成反应的反应历程,写出乙烯与Br2、H2、H2O、HBr发生加成反应的方程式。
组织学生课堂上模拟双键断裂-结合见图3~5。

图3 模拟演示乙烯双键

图4 碳碳双键断开一条键,形成两个半键

图5 两个半键分别结合其他原子
3 基于化学核心素养的学习评价
课程标准对“宏观辨识与微观探析”素养目标达成的程度和学习要求提出了具体的评价标准:
1)通过仔细观察和探究讨论,学生能描述化学物质的颜色、形态及变化现象,掌握物质的分类方式;
2)学生能正确书写或辨识物质的分子式、电子式、结构式、结构简式以及重要的化学反应方程式;
3)学生能从微观角度理解反应原理和物质的结构组成、性质应用;形成“结构决定性质、宏观与微观相结合”的观念;
3.1 具体的评价措施
1)学生各小组间交流讨论:思考题①将乙烯通入到溴水溶液中有何现象?如何除去乙烷中的乙烯?能否选择Br2的CCl4溶液?②总结鉴别乙烯和甲烷的方法。这两个思考题意在考查学生对烷烃、烯烃特殊性质的差异性掌握,并将性质应用于解决具体的化学问题。通过学生的思考交流及结果汇报,也可以培养学生化学语言表达和逻辑推理等能力。
2)让学生总结《乙烯》这节课所学的知识点,并推测丙烯可能具有的性质;丙烯既有碳碳双键又有碳碳单键,一定条件下兼具烷烃和烯烃的性质,有助于学生发散性思维的养成。再让学生敢于提出对本节课所学内容存在的问题和疑问,畅所欲言。教师要善于倾听学生在学习中或课程后的反馈,善于挖掘和体会学生表述不清的问题,及时给出解答或提供交流,尊重学生的想法,产生共鸣,才能更好地培养学生学科核心素养。
3)设计一篇当堂检测试卷,要求题型多样,题目数量不能太多;紧扣本节课的重难点、易错易混点;难度适中,既面向全体,又关注差异;规定时间完成,要求独立完成,培养学生独立思考的能力;及时批改,及时反馈。
例如:①判断下列关于乙烯结构描述是否正确?
乙烯的分子式是C2H2;乙烯是立体结构;乙烯的结构简式是CH2CH2;乙烯既存在碳碳单键又存在碳碳双键;乙烯分子中所有原子共线;乙烯分子中都是极性键。
此题可以检验学生对乙烯微观结构的掌握程度,结合课上拼的模型,使学生深刻掌握。
②判断下列反应或现象属于哪种反应类型?
甲烷在光照条件下与氯气混合;乙烷在氧气中燃烧;丙烯与氯气反应生成一氯丙烯;乙烯通入溴的四氯化碳后橙色褪去;乙烯通入酸性高锰酸钾后溶液紫色褪去;乙烯在氧气中剧烈燃烧,产生黑烟。
此题考查学生对烷烃和烯烃的化学性质和反应类型的掌握。
③小明同学设计的制备乙烯并验证乙烯某些性质的实验装置如图6所示。
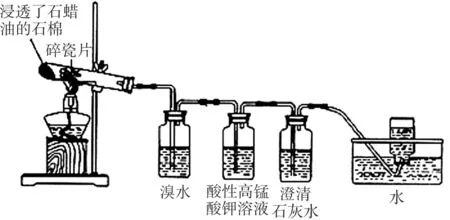
A C D E
(1)A装置中碎瓷片的作用
(2)石油分馏产物之一十六烷可发生如下反应,反应式已配平:

写出甲生成乙的化学方程式:
(3)写出B装置中的化学反应方程式。
(4)能否利用C装置去掉乙烯中乙烷(填“能”或“不能”),若不能,写出理由。
(5)根据装置图可知,实验室用排水集气法收集乙烯,能否用排空气法?为什么?
此题是与教材实验相关的实验主观题,意在让学生了解气体制备和性质检验实验的装置、实验过程、注意事项、重点查考方向等。
3.2 评价结果及分析
1)操作过程:首先选取两个人数和化学基础相差不多的班级,一个为实验班,一个为对照班。实验班按照基于宏观辨识和微观探析素养的教学设计进行课堂活动;对照班按照灌输式教学模式进行课堂活动,然后进行相同的评价,最后分析评价结果。
2)评价方式:课后检测共10道单选题,每道3分;2道非选择题,每道10分,满分50分。

表4 分数段分析
由表4可知,实验班的40~50和30~40分数段人数约占班级总人数的三分之二,大部分学生对本节课的知识点掌握得较好,并且锻炼出了一定的答题能力和信息提取能力。

表5 小分表分析
表5中展示了1~8、11、12题的平均得分,由表5可知实验班1、3、5、6、7、11、12题的平均得分都高于对照班,而2、4、8题经过调查,部分学生没有理解题意,部分学生信息提取不全面而导致失分,但后进生还是取得了很大进步。其中5、6、7题实验班都超过了2分,而对照班只有1分左右,足见差距之大。
4 结语
化学核心素养是学生学习化学后逐步形成的一种隐性品质,表现为以后在处理与化学相关具体事物时的自觉思维习惯[5],但这并非一时一日之功,这需要教师和教研者反复设计和打磨教学模式、教学策略和教学设计等,反复研究学生,让学生成为课堂真正的主体。

