猴痘病原学、流行病学特征及其检测防控技术
李香,杨婧,赵合平
(1.陕西省动物疫病预防控制中心,陕西西安 710002;2.宜君县畜牧业发展中心,陕西宜君 727200)
在新型冠状病毒病(COVID-19)全球流行的同时,另一种人兽共患病——猴痘(monkeypox)正在逼近人类。自2022年5 月7 日英国发现人猴痘病例以来,全球人间猴痘病例数迅速上升,截至2022年12 月14 日,超过100 个国家和地区报告出现82 553 例病例[1],其发病率、死亡率和住院率呈持续增长趋势。全球受猴痘影响最严重的10个国家是美国、巴西、西班牙、法国、英国、德国、哥伦比亚、秘鲁、墨西哥和加拿大[2]。我国首例猴痘病例是2022年6 月24 日在台湾地区发现的,截至2022年10 月,我国已经发现6 例病例,其中台湾4 例,香港和重庆各1例[3]。
猴痘是由猴痘病毒(monkeypox virus)引起的一种病毒性人兽共患病。猴痘病毒最早在猴子身上被发现[4],1970年报告了第一例动物向人传播的猴痘病例[5]。目前猴痘在人间的传播速度超出预期,引起了人们的高度重视。当前,严密监视猴痘全球流行情况并做好防控,阻止猴痘的人际传播以及人与动物间的传播具有重要意义。本文从猴痘的病原学、流行病学、检测技术、防控措施等方面进行综述,以期帮助人们全面认识猴痘,提高防范意识,同时为相关机构做好防控及技术储备工作提供参考。
1 病原学
1.1 病毒分类及命名
根据国际病毒分类委员会(International Committee on Taxonomy of Viruses,ICTV)最新分类,猴痘病毒属于痘病毒科(Poxviridae)脊椎动物痘病毒亚科(Chordopoxvirinae)正痘病毒属(Orthopoxvirus)成员。遗传进化分析显示,猴痘病毒分为两大遗传进化分支(clade):西非分支和刚果盆地(中非)分支[6-7]。其中,刚果盆地分支病毒1970年在刚果民主共和国被发现[8],西非分支病毒1986年在西非国家(塞拉利昂、尼日利亚、利比里亚和科特迪瓦)被报道[9]。研究数据[7]表明:不同分支毒株的全基因组核苷酸差异为0.55%~0.56%;刚果盆地分支病毒对人类的毒力比西非分支更强,西非分支导致的死亡率约为1%,而刚果盆地分支则为10%。猴痘病毒最新基因序列结果显示,2022年全球流行株与2018年和2019年英国流行株一致,均属于西非分支[10-11]。系统发育树见图1-A。猴痘是因在猴子身上被分离出来而命名的,但为了避免病毒名称对任何国家、区域、文化、社会、专业或民族群体等造成伤害,世界卫生组织(World Health Organization,WHO)2022年8 月12 日宣布对猴痘病毒分支重新命名,新名称由罗马数字和小写英文字母组成,使用罗马数字表示病毒分支,用小写字母表示亚分支。将刚果盆地分支称为分支I,西非分支称为分支II。分支II 又包括两个亚分支,即IIa 和IIb,其中IIb 是2022年主要流行的一组病毒变种[12-13]。系统发育树见图1-B。
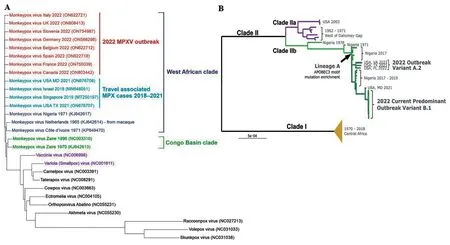
图1 猴痘病毒基因组系统发育树
1.2 病毒形态结构及理化特性
电子显微镜下,猴痘病毒颗粒为椭圆形或圆角砖状,大小200~250 nm,是有包膜的双链DNA病毒,基因组大小约197 kb,约有190 个不重复的ORF,每个ORF 长度均超过180 nt,核苷酸56~120 kb 处的中央编码区序列(CRS)高度保守,两侧包含可变的反向末端重复序列(ITRs),ITR区域至少包含4 个ORF[14-16]。猴痘病毒与所有痘病毒一样,编码病毒复制酶和结构蛋白的基因相对保守,这些基因大部分位于基因组的中心区域,编码病毒DNA 复制、转录、组装和释放所需的所有蛋白质,成熟的病毒颗粒具有哑铃状的核蛋白核心,包含一个大的双链线性DNA 基因组[17]。猴痘病毒与所有痘病毒相似,细胞外包膜病毒(EEV)和细胞裂解过程中释放的细胞内成熟病毒(IMV)两种成熟形式均可感染细胞(图2)[14]。猴痘病毒对宿主细胞的侵袭主要通过吸附、膜融合和核侵3 个步骤完成,在被感染细胞的细胞质中完成复制的全过程[18]。猴痘病毒不耐热,56 ℃处理30 min 可失活;易被甲醛、甲醇、十二烷基磺酸钠(SDS)、苯酚和氯仿等有机溶剂灭活;耐干燥和低温,4 ℃的温度下能长期保持活力[4]。

图2 猴痘病毒粒子结构[14]
2 流行病学
2.1 传染源
猴痘病毒最早于1958年在非洲热带雨林中的一组用于研究的猕猴属食蟹猴身上被分离到[4,19]。目前已发现松鼠、冈比亚鼠、土拨鼠、不同种类的非人类灵长类动物以及人类均能感染猴痘病毒成为传染源[20]。1970年,一名儿童成为第一例人类猴痘病例[21],此后多个国家多次暴发人间猴痘疫情。高风险人群包括未接种牛痘的人员、宠物商店工作人员、宠物爱好者、动物饲养人员、医院传染科医护人员等[22]。
2.2 传播途径
起初的人类猴痘病例主要通过接触、被咬伤、食入猴肉或者松鼠而被感染,由此推测接触被感染动物的皮肤或黏膜伤口、体液、血液等都会感染猴痘病毒[23]。人间传播途径可以是人与人的直接接触传播,也可以通过飞沫、呼吸道分泌物、被感染者污染的用品等传播,还可以通过母婴传播[24-25]。2022年5 月18 日以来,多国的猴痘疫情报告显示,人间也可以通过性传播,并且性传播不局限于男男性行为[26]。2022年流行的猴痘疫情主要是通过性接触传播引起的,多在与男性发生性关系的男性中被诊断出来,特别是有多重性行为的男性[27]。另外,英国的一项新研究表明,感染猴痘病毒的人在出现明显的疾病症状之前,可将病毒传播给他人,而且这种类型的传播在当前国际疫情中占很大一部分[28]。专家们预计,2022年的疫情不会造成像COVID-19 那种的全球破坏,因为猴痘并不像COVID-19 可通过空气传播,也不像天花高度传播,更不像艾滋病在病毒体内持久存在。
2.3 全球疫情现状
2022年5 月,多个无猴痘流行的国家以及有流行的非洲国家发现猴痘病例。之后,全球发现的猴痘病例数量出现了前所未有的增长,美国、英国、西班牙和加拿大等几个过去无猴痘流行的国家也出现了不可控的人际传播病例[29]。目前,猴痘疫情已蔓延到100 多个国家和地区,报告的病例超过8万例[30]。虽然自2022年8 月中旬以来,美国和欧洲确认的猴痘病例数量呈现下降趋势(图3)[31],但是疫情发展势态仍然不明,各国应提高警惕,减少猴痘国际传播对人们造成的恐慌。

图3 2022年5—9 月全球猴痘病例发展趋势[31]
3 临床症状
猴痘患者一般都有相关病毒接触史。如:发病前21 d 内有境外猴痘病例报告地区旅居史;发病前21 d 内与猴痘病例有密切接触;发病前21 d内接触过猴痘病毒感染病例的血液、体液或分泌物等[32]。猴痘的临床症状与天花相似,但是没有天花严重。猴痘潜伏期一般为7~14 d,最长可达21 d。猴痘病毒的感染过程主要分为两个阶段:先是前驱期(0~2 d),患者表现发热、疲劳、严重头痛、淋巴结肿大、肌肉疼痛等症状。之后是典型的皮疹期(7~21 d),患者表现为面部(95%)、手掌和脚底(75%)、口腔黏膜(70%)、生殖器(30%)和结膜(20%)等部位的皮疹[33];皮疹持续2~4 周,从斑块开始,由丘疹变成小泡,然后出现脓疱,最后结痂;严重情况下,病变区域会融合,导致大片皮肤脱落[34]。在2022年的猴痘疫情报告中还出现轻微症状或无症状感染者[35]。猴痘的非典型特征包括潜伏期短、临床表现轻,生殖器和肛周处出现局部有时疼痛的皮疹和病变[36-38]。值得注意的是,免疫功能低下的猴痘患者,如孕妇和儿童,还有可能继发其他疾病。
4 实验室检测
4.1 核酸检测
猴痘的临床症状与天花等痘病毒病临床症状相似,因此确诊猴痘还需通过进一步的实验室检测。猴痘的检测方法有多种,其中实时荧光定量PCR是当前核酸检测中最常用的方法,主要用于早期检测,其灵敏度高,检测速度快,适合出入境检疫工作[39]。通过采集口鼻咽分泌物以及疑似病例的皮疹、疱液、痂皮等标本提取DNA 进行PCR 检测,确定病毒相关基因存在与否。必要时还可以分离病毒进行病毒全基因组测序,确定病毒的种、属、分支以及基因突变情况[40]。目前还建立了环介导等温扩增(LAMP)、限制性长度片段多态性(RFLP)、重组酶聚合酶扩增(RPA)等多种猴痘病毒核酸检测方法[41-44]。
4.2 血清学检测
酶联免疫吸附试验(ELISA)可分别检测猴痘患者感染5 d 和8 d 后血清中的特异性IgM 和IgG抗体[45],尤其在急性期和恢复期血清抗体可增至原来的4 倍,用ELISA 方法较易诊断猴痘。由于猴痘病毒与其他痘病毒存在抗原交叉反应,特异性不足,因此该方法不能准确识别猴痘,常用于流行病学调查[46]。
4.3 其他检测方法
电镜检查、免疫化学分析和多重免疫荧光成像也可用于猴痘病毒的抗原检测[47-48]。为了确定诊断,还需要从患者标本中分离和培养活病毒并对病毒基因组进行分析[40]。
5 防治措施
应对当前的猴痘疫情,WHO 表示应从以下3点加强防控:(1)中断人际传播,优先关注接触风险高的社区;(2)保护处境危险的易感人群;(3)尽量控制人和动物间的传播[49]。另外,各国还应建立完善的猴痘病毒检测系统,做到早发现、早隔离,避免猴痘病毒扩散。
目前还没有专门针对猴痘的特效疫苗,但天花疫苗可以对其提供85%的保护[40]。可使用的天花疫苗有两种:一种是第二代疫苗ACAM2000(减毒活疫苗),另一种是第三代疫苗JYNNEOS(Imvamune、Imvanex、MVA-BN,复制缺陷型减毒疫苗)[50-51]。但WHO 表示,目前不需要也不建议对猴痘进行大规模疫苗接种;建议对高危人群接种初级预防(接触前)疫苗,对病例接触者接种预防性疫苗(PEPV),最好是在首次接触后4 d 内,在没有症状的情况下最多14 d 内接种疫苗[52]。
目前尚无针对猴痘的特效抗病毒药物。抗天花病毒药物可以起到抗猴痘病毒的作用,可以适当减轻患者症状,控制并发症。对于病症严重的患者,建议考虑抗病毒疗法,通常使用Tecovirimat、西多福韦(cidofovir)或布林西多福韦[53],但这些治疗是非正式的,因为没有确切的指南证实此疗法可缓解症状。
6 结语
猴痘病毒是一种类似于天花的病毒,其引起的病死率比天花病毒低,但传播较快,容易引起人们恐慌。目前猴痘不仅在西非和中非国家流行,也在全世界流行开来,是一个值得全世界关注的公共卫生问题。在一些基础设施差、高素质医务人员缺乏、公共卫生体系薄弱、基本医疗保障不足的发展中国家,猴痘更易发生流行,因此这些国家更应该重视猴痘防控。
目前我国虽然只报道了2 例境外输入猴痘病例,但应时刻保持警惕,首选建立科学的猴痘防控策略并不断完善,防止猴痘再次传入国内;其次仍需继续推进快速、特异、高效的猴痘病毒检测技术研究和应用评估。

