ZrO2基双金属氧化物催化CO加氢行为的研究
刘竞舸 闫国春 李 艺 卢卫民 张成华
(1.中国神华煤制油化工有限公司,100011 北京;2.中国科学院山西煤炭化学研究所,030001 太原)
0 引 言
芳烃作为一种重要的化工原料,常见于合成橡胶、树脂、纤维、涂料等行业,市场需求量巨大。目前,芳烃主要来源于石化行业,但是,我国的能源分布呈“富煤、少气、贫油”的格局,通过合成气制备芳烃成为当下研究热点[1-2]。双功能催化剂可以实现合成气到芳烃的一步转化,其中金属氧化物-分子筛双功能催化剂(OX-ZEO)展现出芳烃选择性优异和催化剂使用寿命长等优点,但是催化活性差制约了该型催化剂的进一步发展[3-8]。
OX-ZEO由加氢组分和重整组分两部分组成,其中加氢组分负责合成气的活化和中间物种的形成,ZrO2广泛用作OX-ZEO中的加氢组分。研究表明,通过引入杂元素修饰ZrO2可以显著改善OX-ZEO的催化性能。杨成等[9]在反应温度为400 ℃,压强为3.0 MPa,反应空速为500 mL/(g(催化剂)·h),CO,H2和Ar的物质的量比为5∶5∶1条件下,制备得到的双功能催化剂ZrO2/H-ZSM-5展现出26.2%的CO转化率以及40.7%的芳烃选择性;CHEN et al[5]发现Zn的引入可显著改善双功能催化剂ZrO2/H-ZSM-5的催化活性,在反应温度为430 ℃,压强为3.0 MPa,反应空速为1 500 mL/(g(催化剂)·h),H2和CO的物质的量比为2∶1,在Zn和Zr的物质的量比为1∶1 000条件下,CO转化率为10.0%,Zn和Zr的物质的量比为1∶5条件下,CO转化率增加到45%左右,但是芳烃选择性由80.0%下降到10.0%;ZHOU et al[8]将掺杂Mo的ZrO2用于CO芳构化,结果显示Mo的引入可显著提高CO转化率,当Mo和Zr的物质的量比为1∶68时,双功能催化剂Mo-ZrO2/H-ZSM-5在温度为400 ℃,压强为3.0 MPa,反应空速为3 000 mL/(g(催化剂)·h),H2和CO的物质的量比为2∶1条件下,CO转化率达到22.0%,芳烃选择性达到70.0%,但是此催化剂使用寿命缩短,在100 h的稳定性测试中,催化剂发生明显失活现象。综上,杂元素的引入显著提高OX-ZEO催化活性的同时,对OX-ZEO催化选择性、使用寿命均产生了明显影响。
CHEN et al[5]指出含氧物种(如甲醇、二甲醚等)作为中间产物,对于目标产物芳烃的生成具有重要作用。对此本实验以UiO-66这一含Zr的金属有机框架(MOF)材料为前驱物,利用MOF材料中金属团簇高度分散[10-11]的特性,引入Zn,Cu,Ce,Mn,In等杂元素,拟制备得到高分散纳米M-ZrO2(M分别为Zn,Cu,Ce,Mn,In),研究杂元素的引入对ZrO2催化活性、含氧物种选择性的影响,考察ZrO2基双金属氧化物用作OX-ZEO中加氢组分的潜能。
1 实验部分
1.1 催化剂制备
采用UiO-66为前驱物制备纳米ZrO2,首先需合成UiO-66,具体方法如下:将66.1 g六水硝酸氧锆、杂元素硝酸盐(杂元素分别为Zn,Cu,Ce,Mn,In,杂元素与Zr的物质的量比控制在1∶1)、10.9 g对苯二甲酸溶于200 mL N,N-二甲基甲酰胺(DMF)中,室温下超声溶解30 min后得到澄清溶液,再向溶液中添加一定量醋酸,醋酸添加量控制在Zr4+与醋酸物质的量的比为1∶50。最后将所得溶液密封于聚四氟乙烯涂覆的管弹反应器中,120 ℃下水热24 h,冷却后将生成物过滤、洗涤、干燥,得到的生成物记为M-UiO-66(M分别为Zn,Cu,Ce,Mn,In)[12]。将得到的M-UiO-66在空气气氛(流量为100 mL/min)下于400 ℃焙烧9 h,得到的生成物记为M-ZrO2(M分别为Zn,Cu,Ce,Mn,In)。
1.2 催化剂表征
采用低温N2-物理吸脱附法,在ASAP 2420物理吸附仪(Micromeritics,美国)上对样品织构性能进行测定;采用Bruker X射线衍射仪D2-phaser(Bruker,德国)对催化剂物相组成进行分析;采用ESCALAB 250Xi X射线光电子能谱仪(Thermao Fisher Scientific,美国)对催化剂表面电子结构进行分析;采用电子顺磁谱(EPR),利用Bruker Xenon软件(Bruker德国)对催化剂表面性质进行分析;采用吡啶-红外(Py-IR),在VERTEX 70红外光谱仪(Bruker德国)上对催化剂表面酸性进行定性、定量分析;采用NH3-程序升温脱附(NH3-TPD),在动态化学吸附仪ASAP 2920(Micromeritics,美国)上对催化剂表面酸性位数量、强度进行定量分析;采用TalosTM 200A透射电子显微镜(FEI,美国)对催化剂形貌进行表征。
1.3 催化剂评价
在固定床反应器上对催化剂性能进行评价,具体操作如下:将催化剂压片、造粒、筛分后得到粒径范围为0.212 mm~0.355 mm的成型催化剂,程序升温至目标温度(400 ℃)后开始加氢反应。采用Agilent GC-7890型气相色谱仪(Agilent美国)对气相产物进行在线分析,分别用热阱、冷阱收集蜡相、油相与水相产物,并对收集到的产物进行离线分析。根据CO转化率、CO2选择性、产物选择性、C2~C4烯烷比等指标对催化剂性能进行评价,各物理量计算公式如式(1)~式(3)所示。
(1)
式中,αCO为CO转化率,%;n(COin)为通入原料气中CO的物质的量,mol;n(COout)为尾气中CO的物质的量,mol。
(2)
式中,SCO2为CO2选择性,%;n(CO2out)为尾气中CO2的物质的量,mol。
(3)
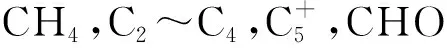
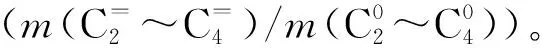
2 结果与讨论
2.1 催化剂相态与形貌
杂元素修饰的UiO-66及其焙烧后所得双金属M-ZrO2的XRD谱如图1所示。由图1a可以看出,在2θ分别为7.4°,8.5°,14.1°,14.7°,17.0°,18.6°和19.1°处均出现明显的UiO-66特征衍射峰,说明杂元素的引入并不影响该MOF材料的形成[13-14]。由图1b可以看出,将杂元素修饰的UiO-66焙烧后所得M-ZrO2在2θ分别为30.2°,35.0°,50.4°,60.0°和62.9°处有明显的衍射峰,分别归属于t-ZrO2(101)晶面,t-ZrO2(110)晶面,t-ZrO2(112)晶面,t-ZrO2(211)晶面和t-ZrO2(202)晶面[15],t为四方相。除了Cu-ZrO2以外,并没有发现杂元素的衍射峰,表明杂元素与Zr呈高度分散。在Cu-ZrO2中,发现除了存在t-ZrO2特征峰外,在2θ分别为35.8°和39.0°处的衍射峰归分别归属于CuO(-111)晶面和CuO(111)晶面,这是由于在焙烧过程中Cu-ZrO2发生相分离,CuO从ZrO2中剥离。采用Sherrerr公式,以2θ为30.2°处的衍射峰为基准得到不同样品的晶粒尺寸(见表1),发现得到的M-ZrO2的晶粒尺寸范围为3.8 nm~5.8 nm,与纯ZrO2的晶粒尺寸4.0 nm相接近,表明杂元素的引入并不影响ZrO2的晶粒尺寸。对于Cu-ZrO2而言,以2θ为35.8°处的衍射峰为基准,采用Sherrerr公式计算得到的CuO晶粒尺寸达到18.8 nm。
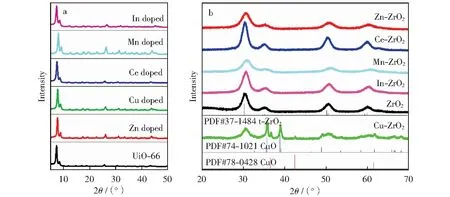
图1 杂元素修饰的UiO-66及其焙烧后所得双金属M-ZrO2的XRD谱Fig.1 XRD spectra of hetero elements doped UiO-66 and M-ZrO2a—Hetero elements doped UiO-66;b—M-ZrO2
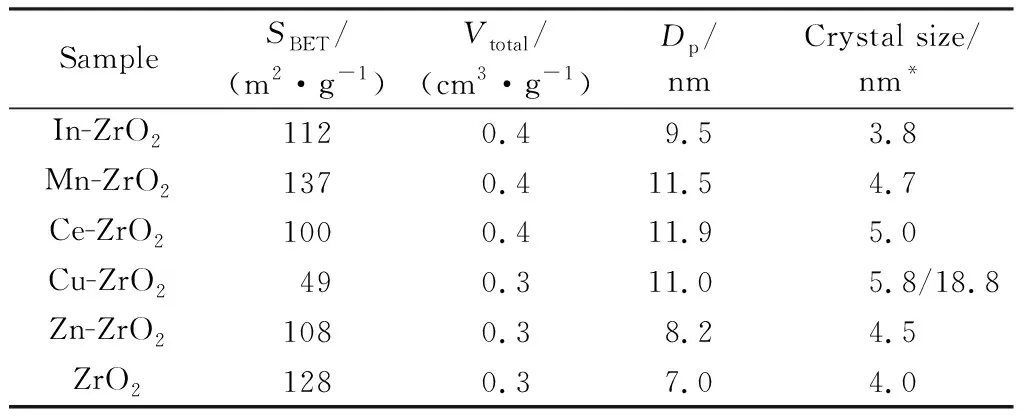
表1 杂元素修饰的双金属M-ZrO2的织构性能Table 1 Texture properties of hetero elements doped M-ZrO2
杂元素修饰的UiO-66及其焙烧后所得双金属M-ZrO2进行N2-物理吸附表征的结果和双金属M-ZrO2的孔径分布如图2所示。由图2a可以看出,M-UiO-66的吸脱附曲线都为Ⅳ型吸-脱附曲线,具有明显的H3回滞环,表明该材料为典型的介孔结构。由图2b可以看出,与M-UiO-66类似,M-ZrO2催化剂也为介孔结构。杂元素修饰的UiO-66的织构性能如表2所示。由表1和表2可以看出,杂元素修饰的UiO-66的比表面积都集中在1 100 m2/g左右、孔径范围在9.5 nm~15.3 nm之间;杂元素修饰的UiO-66焙烧后所得的M-ZrO2,除了Cu-ZrO2外,其余M-ZrO2的比表面积均大于或等于100 m2/g,孔径范围在7.0 nm~11.9 nm之间。对于Cu-ZrO2而言,其比表面积仅为49 m2/g,这是由于Cu和Zr发生分相,CuO受热迁移、聚集、长大(晶粒尺寸达到18.8 nm),导致Cu-ZrO2比表面积下降。
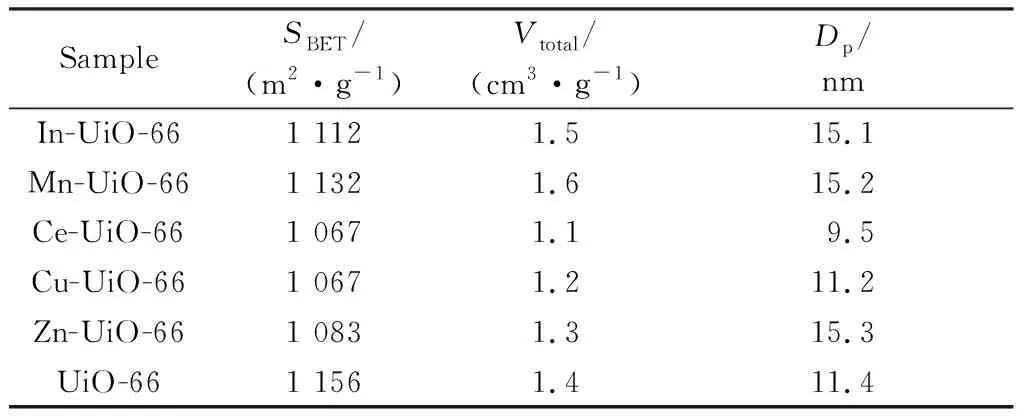
表2 杂元素修饰的UiO-66的织构性能Table 2 Texture properties of hetero elements doped UiO-66
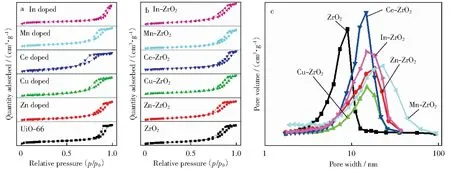
图2 杂元素修饰的UiO-66及其焙烧后所得双金属M-ZrO2进行N2-物理吸脱附表征的结果和双金属M-ZrO2的孔径分布Fig.2 N2 physical adsorption and desorption characterization results of hetero elements doped UiO-66, M-ZrO2 and pore width distribution of M-ZrO2a—Hetero elements doped UiO-66;b—M-ZrO2;c—Pore width distribution of M-ZrO2
采用TEM对M-ZrO2的形貌及其元素分布进行分析的结果以及对样品颗粒尺寸的统计结果如图3所示。由图3可以看出,M-ZrO2的形貌都呈典型的球状。样品的颗粒尺寸范围为4.0 nm~6.0 nm,这与XRD计算结果相一致。由图3b可以看出,在样品Cu-ZrO2中发生烧结现象,有大量黑色斑点出现,对该黑色斑点处的晶格条纹进行测量,其晶格间距为2.71 nm,对应于CuO(110)晶面,这与XRD表征结果相吻合,证明在焙烧的过程中Cu-ZrO2发生相分离,Cu元素以CuO的形式存在于ZrO2表面。对于Zn-ZrO2,Ce-ZrO2,Mn-ZrO2等样品而言,其晶格间距范围为2.93 nm~2.98 nm,对应于ZrO2(101)晶面,ZrO2晶格间距的变化可能是由杂元素引入且与之形成氧化物固溶体所致[16]。对于In-ZrO2,TEM结果显示其晶格间距分别为2.95 nm,2.54 nm和1.81 nm,分别对应于ZrO2(101)晶面;ZrO2(110)晶面和ZrO2(112)晶面。采用TEM-mapping对样品表面元素分布进行表征,在Zr元素富集的区域,相应存在大量杂元素,这些杂元素高度分散在ZrO2中。

图3 M-ZrO2的TEM表征结果及对样品颗粒尺寸的统计结果Fig.3 TEM results of M-ZrO2 and statistical results of sample particle sizea—Zn-ZrO2;b—Cu-ZrO2;c—Ce-ZrO2;d—Mn-ZrO2;e—In-ZrO2
2.2 催化剂表面性质
对双金属M-ZrO2进行吡啶-红外和NH3-程序升温吸脱附表征的结果如图4所示。由图4a可以看出,与纯ZrO2一样,M-ZrO2在1 445 cm-1,1 487 cm-1,1 574 cm-1和1 605 cm-1处均出现红外吸收峰,归属于L酸,没有B酸出现,表明杂元素的掺杂并不影响ZrO2表面酸性位种类[17-18]。采用NH3-程序升温吸脱附对样品表面的酸性进行定量分析,并对表征结果进行拟合且采用外标法对样品表面酸性进行量化,计算结果如表3所示。由表3可以看出,纯ZrO2表面酸性位数量达到345.6 μmol/g。随着杂元素的引入,ZrO2表面酸性位数量逐渐降低,由Zn-ZrO2的335.9 μmol/g减少到Mn-ZrO2的210.3 μmol/g,但是杂元素的引入仅影响ZrO2表面酸性位数量,对ZrO2表面酸性位强度分布影响较小,各样品的弱酸、中酸、强酸质量分数分别都集中在20.0%,70.0%,10.0%左右。
M-ZrO2的Zr3d轨道如图5所示。由图5可以看出,结合能为182.0 eV和184.4 eV分别对应Zr3d5/2轨道和Zr3d3/2轨道,可以看到纯ZrO2和Zn-ZrO2都向低结合能方向发生偏移,造成这一现象的原因在于样品表面阴离子空穴的产生[19-22]。采用XPS对Zn,Cu,Ce,Mn,In等助剂的电子状态进行考察,结果如图6所示。由图6可以看出,在Zn-ZrO2中,结合能为1 044.8 eV和1 021.7 eV分别对应于ZnO2p1/2和ZnO2p3/2轨道;在Cu-ZrO2中,结合能为954.1 eV和934.2 eV分别对应于CuO2p1/2和CuO2p3/2轨道;在Ce-ZrO2中,结合能为882.2 eV对应于CeO23d5/2轨道;在Mn-ZrO2中,结合能为641.6 eV对应于Mn2O33d5/2轨道;在In-ZrO2中,结合能为452 eV和444.3 eV,分别对应于In2O33d3/2和In2O33d5/2轨道。对6组样品的O1s轨道进行分析,结果如图7所示。由图7可以看出,结合能为529.9 eV,531.4 eV和532.4 eV处的信号分别归属于Co(表面氧)、Vo(氧空位)和Lo(晶格氧)[19-22]。M-ZrO2的NH3-程序升温吸附与XPS的量化结果如表3所示。由表3可以看出,除Zn-ZrO2外,杂元素的引入普遍减少了ZrO2中Vo的相对含量,Cu-ZrO2,Ce-ZrO2,Mn-ZrO2,In-ZrO2等样品中Vo的相对含量分别为20.4%,25.8%,15.0%,21.0%。
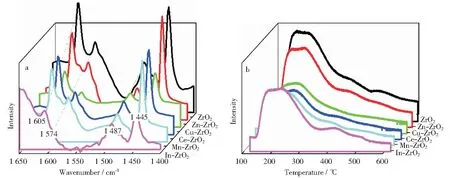
图4 对双金属M-ZrO2进行吡啶-红外和NH3-程序升温吸脱附表征的结果Fig.4 Py-IR and NH3-TPD characterization results of M-ZrO2
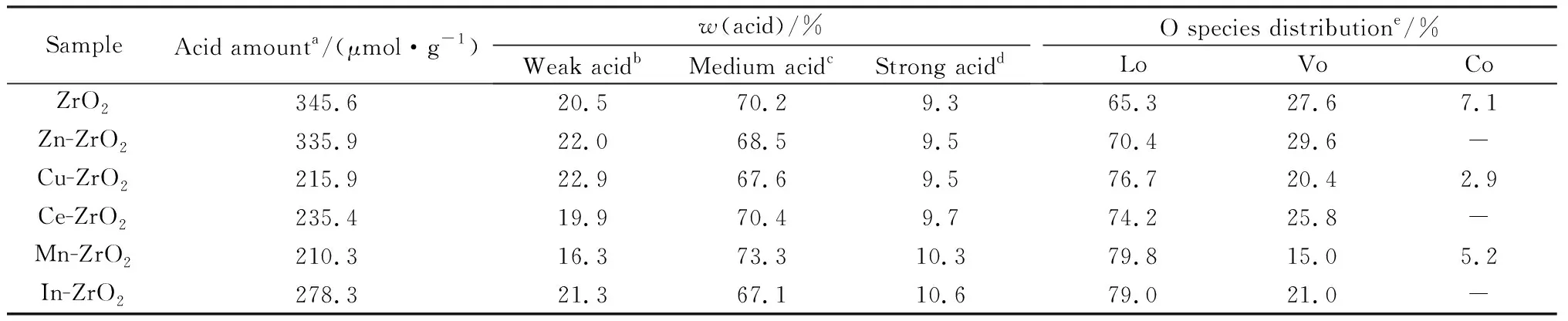
表3 M-ZrO2的NH3-程序升温吸附与XPS的量化结果Table 3 Quantitative results of NH3-TPD and XPS of M-ZrO2
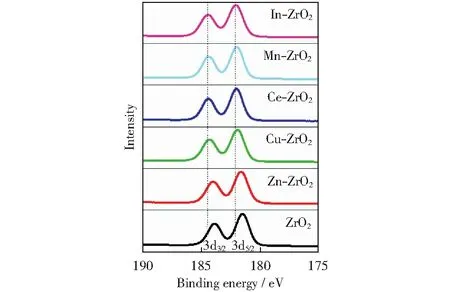
图5 M-ZrO2的Zr3d轨道Fig.5 Zr3d track of M-ZrO2
双金属M-ZrO2的EPR谱如图8所示。由图8a可以看出,引入杂元素对ZrO2表面性质产生了显著影响。对于ZrO2,Zn-ZrO2,Ce-ZrO2和In-ZrO2等样品,在磁场强度范围为3 350 G~3 400 G内均有明显的顺磁性信号,对应g因子为2.00。这是由于以UiO-66为前驱物,400 ℃焙烧条件下得到的M-ZrO2,其表面还残留一些含碳物种,这一信号便归属于这些含碳物种[23]。相较于ZrO2,Zn-ZrO2,Ce-ZrO2和In-ZrO2等样品,Cu-ZrO2和Mn-ZrO2显示出截然不同的EPR谱,其中Cu-ZrO2在磁场强度范围为3 300 G~3 500 G内出现弥散的顺磁信号,表明在Cu-ZrO2中Cu是以+2价形式存在[24];Mn-ZrO2样品中则出现了6组对称信号,这一现象的出现表明部分Mn是以+2价存在于该催化剂中[25]。将ZrO2,Zn-ZrO2,Ce-ZrO2和In-ZrO2等样品在磁场强度范围为3 300 G~3 500 G处的EPR信号进行放大,如图8b所示。由图8b可以看出,样品在磁场强度为3 400 G处均有明显顺磁性信号,对应g因子为1.98,该g因子值对应于Vo[19,26],由于该信号值的强度与Vo相对含量呈正相关,所以样品按Vo相对含量由大到小依次为ZrO2,Ce-ZrO2,Zn-ZrO2,In-ZrO2,这与XPS O1s的拟合结果相一致,表明助剂的添加并没有促进Vo产生,反而起到了削弱作用。
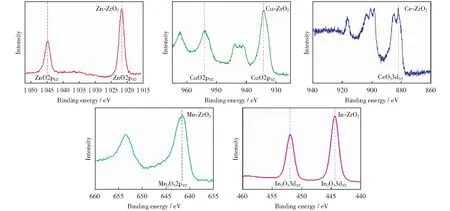
图6 M-ZrO2的电子状态Fig.6 Electronic state of M-ZrO2
2.3 CO加氢反应
双金属氧化物催化剂中的加氢组分应具有良好的CO活化性能及含氧物种选择性[5]。在反应温度为400 ℃,压强为6.0 MPa,反应空速为600 mL/(g(催化剂)·h),H2和CO的物质的量比为1∶1的条件下,对纯ZrO2和M-ZrO2的催化性能分别进行评价,结果如表4所示。由表4可以看出,杂元素的引入对ZrO2催化性能产生明显影响,首先在CO转化率方面:文献[27-28]指出ZrO2表面酸性位是其活化CO位点,结合NH3-TPD表征结果,由于Zn,Ce的引入降低ZrO2表面酸性,相较于纯ZrO235.4%的CO转化率,Zn-ZrO2,Ce-ZrO2等样品的CO转化率发生不同程度的下降,Zn-ZrO2和Ce-ZrO2的CO转化率分别为31.7%和27.4%;Cu-ZrO2,Mn-ZrO2,In-ZrO2等样品的CO转化率明显升高,造成这一现象的原因可能在于杂元素在反应过程中逐渐还原为金属态,提升了ZrO2表面活化氢气的性能,进而拉动CO转化[29]。以Cu-ZrO2为例,XRD与TEM表征结果显示,Cu-ZrO2发生相分离,Cu以CuO的形式存在于样品中,随着反应的进行,CuO逐步还原为单质Cu,使得CO转化率由初始的50.5%增加到61.0%。
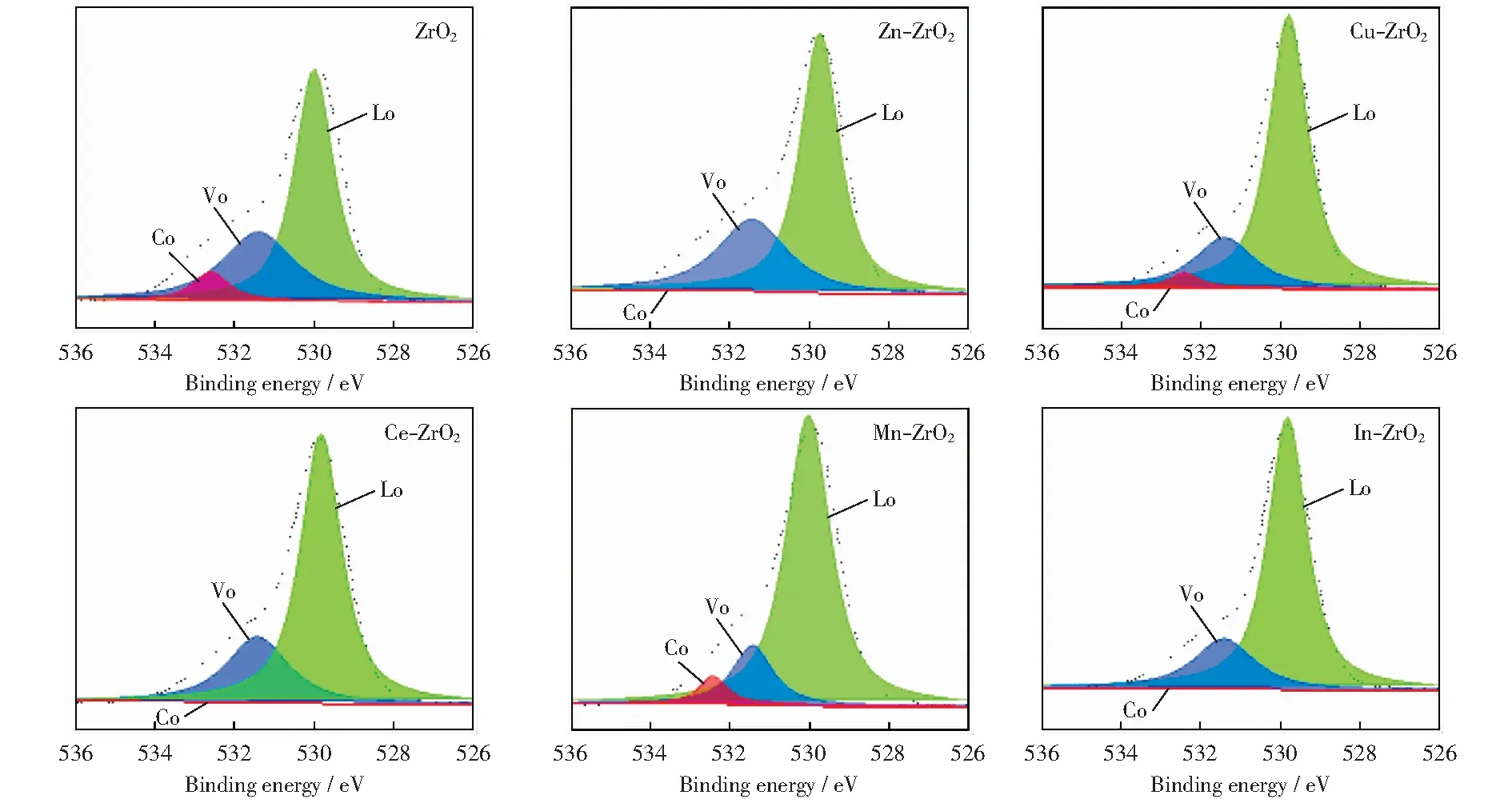
图7 M-ZrO2的O1s轨道Fig.5 O1s track of M-ZrO2
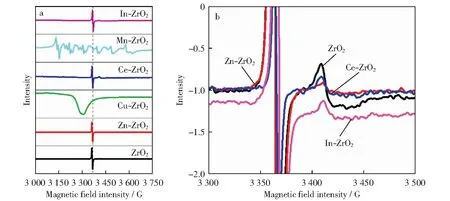
图8 M-ZrO2的EPR谱Fig.8 EPR spectra of M-ZrO2a—Field range is 3 280 G-3 430 G;b—Field range is 3 400 G-3 430 G
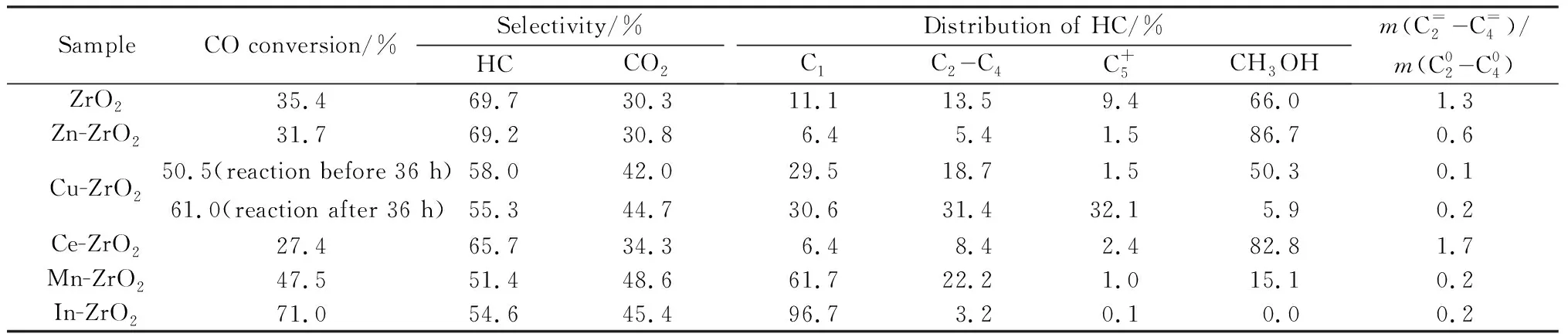
表4 采用UiO-66焙烧法所得ZrO2及M-ZrO2催化性能Table 4 Catalytic properties of ZrO2 and M-ZrO2 derived from UiO-66 as precursor
在之前的研究中,笔者提出ZrO2上氧空穴有利于含氧物种的产生[3,30],EPR与XPS表征结果显示杂元素的引入普遍降低ZrO2氧空穴数量,但是,Zn-ZrO2和Ce-ZrO2样品上CH3OH选择性分别达到86.7%和82.8%,这可能是由于金属氧化物固溶体的形成促进了含氧物种CH3OH产生[5,7]。对于Cu-ZrO2,Mn-ZrO2,In-ZrO2等样品而言,由于Cu,Mn,In等杂元素在反应过程中可能以金属态存在于ZrO2表面,从而提高了ZrO2表面活化H2的能力,因此CO转化率提高的同时,导致CH4大量生成,抑制CH3OH的形成[29]。以In-ZrO2为例,其CO转化率达到71.0%,产物中并未检测到CH3OH,反而有大量CH4产生,且其选择性高达96.7%。对于Mn-ZrO2,Cu-ZrO2也发现同样的规律,产物多以饱和烷烃为主。
3 结 论
1) 杂元素的引入并不影响UiO-66前驱物的形成,焙烧得到的M-ZrO2(M分别表示Zn,Cu,Ce,Mn,In)的晶粒尺寸普遍介于4.0 nm~6.0 nm之间,且杂元素高度分散,可能与ZrO2形成金属氧化物固溶体。
2) 杂元素的引入对ZrO2表面性质产生显著影响,Zn,Cu,Ce,Mn,In显著降低了ZrO2表面酸性位数量,但是并未改变ZrO2表面酸性种类,仍为L酸;其次是表面缺陷位,XPS和EPR表征显示杂元素的引入降低了样品表面Vo的相对含量。
3) 杂元素的引入对ZrO2的催化性能产生显著影响。其中Cu,Mn,In的引入显著提高了ZrO2表面活化H2的能力,CO转化率分别达到35.4%,61.0%和71.0%,但是在活性提高的同时,有大量C1~C4饱和烷烃生成;由于Zn,Ce减弱了ZrO2表面酸性,使得CO转化率有所降低,但是由于金属氧化物固溶体的形成,CH3OH选择性明显提升,分别达到86.7%和82.8%。

