阿替普酶静脉溶栓后早期联合替罗非班治疗轻中度急性缺血性卒中及各TOAST亚型的效果研究
吕洋,柳燕,李宏伟,臧洁,宋金东
卒中是全世界引起死亡和长期残疾的重要原因之一[1],2019年我国卒中发病率为201/10万,居全球首位,卒中所致死亡占全因死亡的20%以上,居我国疾病所致死亡首位[2-3]。急性缺血性卒中(acute ischemic stroke,AIS)占我国卒中的69.6%~70.8%,且呈逐年上升趋势,其发病后3个月和1年的致残率为33.4%、33.8%,发病后3个月和1年的致死率为34.5%、37.1%,是造成患者残疾和死亡的重要原因之一[4-5]。超早期AIS的主要治疗方式之一是阿替普酶静脉溶栓,但其较低的血管再通率和较高的血管再闭塞率导致患者预后不良。替罗非班治疗冠心病有确切疗效,但其联合阿替普酶治疗AIS仍存在争议。既往研究显示,阿替普酶静脉溶栓后早期联合替罗非班静脉泵注可改善AIS患者预后,且不增加颅内出血(intracranial hemorrhage,IH)发生风险[6],所以《替罗非班在动脉粥样硬化性脑血管疾病中的临床应用专家共识》[7]推荐使用替罗非班作为静脉溶栓的辅助治疗是合理的。但也有研究表明,静脉溶栓联合替罗非班不但会增加AIS患者IH发生风险,而且不能改善患者预后[8]。目前还没有针对AIS亚型的相关研究。本研究旨在探讨阿替普酶静脉溶栓后早期联合替罗非班治疗轻中度AIS及各TOAST亚型的有效性和安全性,以期为临床工作提供证据。
1 对象与方法
1.1 研究对象 选取2020—2021年青岛市黄岛区中医医院神经内科收治的轻中度AIS患者300例,按照随机数字表法将其分为常规组和替罗非班组,每组150例。按照TOAST分型将两组患者进一步分别分为小动脉闭塞型(smallartery occlusion,SAO)、大动脉粥样硬化型(large-artery atherosclerosis,LAA)、心源性栓塞型(cardioembolism,CE)、其他已知原因型+不明原因型(其他)亚组,其中常规SAO亚组70例,常规LAA亚组45例,常规CE亚组30例,常规其他亚组5例;替罗非班SAO亚组60例,替罗非班LAA亚组51例,替罗非班CE亚组33例,替罗非班其他亚组6例。纳入标准:(1)符合《中国急性缺血性脑卒中诊治指南2018》[9]中AIS的诊断标准;(2)年龄18~75岁;(3)就诊时美国国立卫生研究院卒中量表(National Institute of Health Stroke Scale,NIHSS)[10]评分为1~15分;(4)新发症状、体征如肢体活动障碍、肢体麻木、共济失调、视野缺损等持续存在1 h以上,且发病时间<4.5 h。排除标准:(1)参照《中国急性缺血性脑卒中诊治指南2018》[9],需要进行机械取栓及其他血管内治疗的患者;(2)静脉溶栓后2 h内出现颅内出血、消化道出血、泌尿系统出血、喉头水肿等患者。本研究经青岛市黄岛区中医医院伦理委员会批准(hdzyyll201912-08),所有患者签署知情同意书。
1.2 治疗方法 所有患者进行阿替普酶(生产厂家:Boehringer Ingelheim Pharma GmbH & Co. KG,国药准字SJ20160054)静脉溶栓治疗,剂量为0.9 mg/kg(最大剂量为90 mg),其中10%在最初1 min内静脉注射,剩余90%静脉滴注1 h。常规组患者在阿替普酶静脉溶栓基础上予以强化降脂、改善侧支循环、控制血糖及早期康复治疗等常规治疗,静脉溶栓24 h后复查颅脑CT,无IH者予以阿司匹林肠溶片(生产厂家:Bayer AG,国药准字H20130340)口服,0.1 g/d,共90 d。替罗非班组在常规治疗基础上,于阿替普酶静脉溶栓后2 h静脉泵注盐酸替罗非班注射用浓溶液(生产厂家:鲁南贝特制药有限公司,国药准字H20090328),剂量为0.4 μg·kg-1·min-1,持续30 min后改为0.1 μg·kg-1·min-1,至静脉溶栓24 h后复查颅脑CT,有HT者停用替罗非班,无HT者继续静脉泵注,共持续24 h;待替罗非班泵注结束时予以阿司匹林肠溶片口服,0.1 g/d,共90 d。所有患者在治疗过程中随时复查颅脑CT以监测病情变化,如有HT则立即停用替罗非班、阿司匹林肠溶片、他汀类药物等。
1.3 观察指标 (1)临床资料。收集患者临床资料,包括年龄、性别、基础疾病(高血压、糖尿病、冠心病、高脂血症)发生情况、心房颤动发生情况、吸烟史(吸烟≥10支/d,持续3年以上定义为有吸烟史)、饮酒史(男性乙醇摄入量≥25 g/d,女性≥12.5 g/d,持续3年以上定义为有饮酒史[11])、入院时血压(收缩压、舒张压)、入院时血糖、入院时低密度脂蛋白、入院时国际标准化比值(international normalized ratio,INR)、发病到开始治疗时间、梗死部位、TOAST分型。(2)NIHSS、改良Rankin量表(modified Rankin Scale,mRS)评分及预后。NIHSS[10]包含意识、语言、运动、感觉、共济运动、眼球运动、视野等方面,总分范围为0~42分,分数越高提示神经功能缺损程度越严重。mRS[12]是评价卒中患者中长期神经功能恢复状态的重要量表,从0级(0分)完全无症状到6级(6分)死亡,其评分越低提示神经功能恢复越好,同时定义mRS评分0~2分为预后良好[13-15],即不遗留明显残疾。本研究记录患者入院时、治疗7 d后NIHSS评分,治疗90 d后mRS评分及治疗90 d后预后良好情况。(3)安全性指标。根据有无临床症状恶化将IH分为两种类型[16]:①无症状性IH:虽然CT检查证实有出血转化,但无与出血转化时间相关的临床症状恶化;②症状性颅内出血(symptomatic intracranial hemorrhage,sICH):CT检查证实有出血转化,且有与出血转化时间相关的临床症状恶化。记录患者IH、sICH发生情况及死亡情况。
1.4 统计学方法 采用SPSS 21.0统计学软件进行数据分析。符合正态分布的计量资料以(±s)表示,组间比较采用两独立样本t检验,组内比较采用配对t检验。计数资料以相对数表示,组间比较采用χ2检验或Fisher's确切概率法。以P<0.05为差异有统计学意义。
2 结果
2.1 常规组与替罗非班组临床资料比较 常规组与替罗非班组年龄、性别、高血压发生率、糖尿病发生率、冠心病发生率、高脂血症发生率、心房颤动发生率、吸烟史、饮酒史、入院时收缩压、入院时舒张压、入院时血糖、入院时低密度脂蛋白、入院时INR、发病到开始治疗时间、梗死部位、TOAST分型比较,差异无统计学意义(P>0.05),见表1。
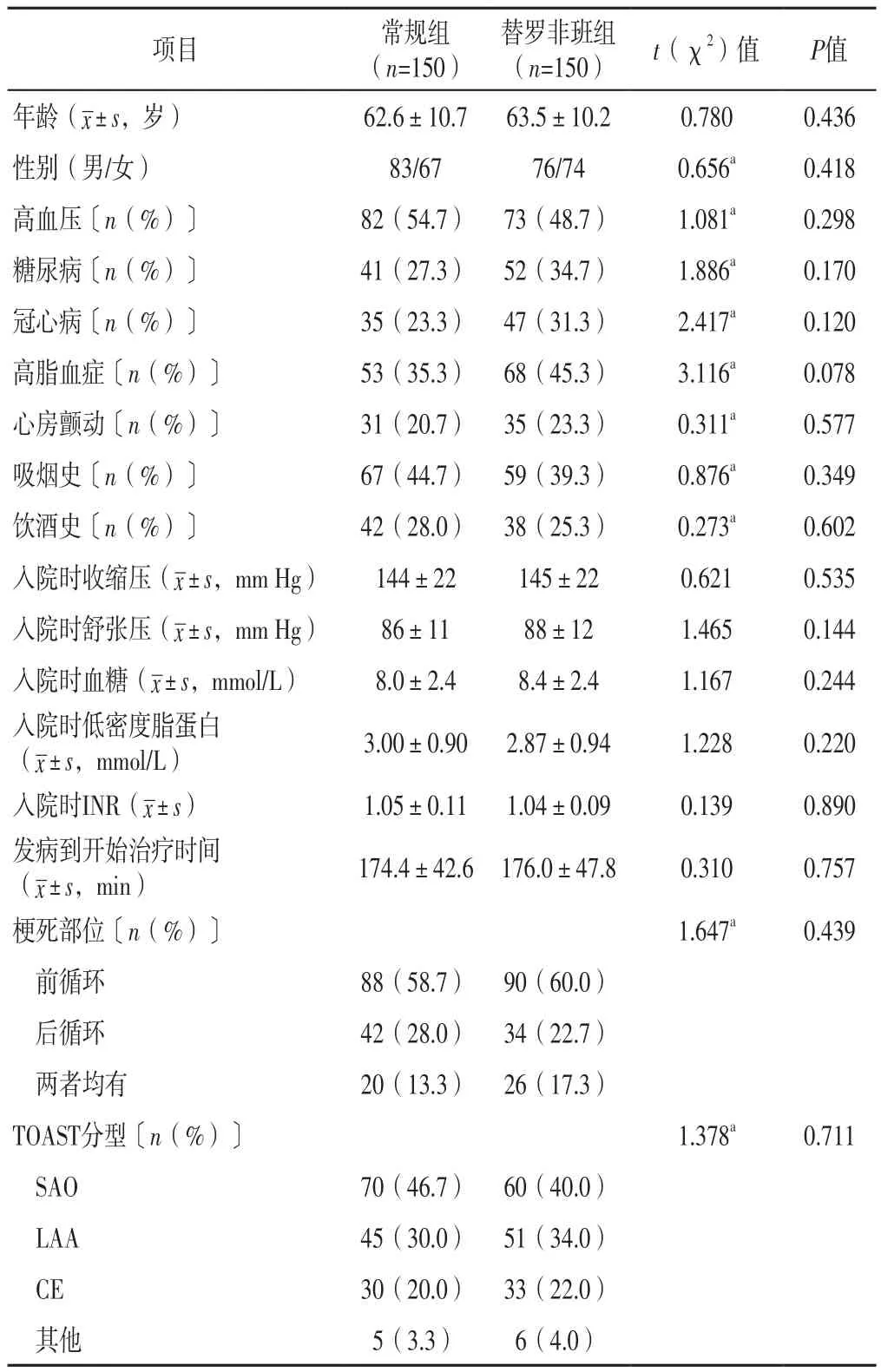
表1 常规组与替罗非班组临床资料比较Table 1 Comparison of clinical data between routine group and tirofiban group
2.2 NIHSS、mRS评分及预后
2.2.1 常规组与替罗非班组 常规组与替罗非班组入院时NIHSS评分比较,差异无统计学意义(P>0.05);常规组、替罗非班组治疗7 d后NIHSS评分分别低于本组入院时,且替罗非班组低于常规组,差异有统计学意义(P<0.05);替罗非班组治疗90 d后mRS评分低于常规组,预后良好者占比高于常规组,差异有统计学意义(P<0.05),见表2。
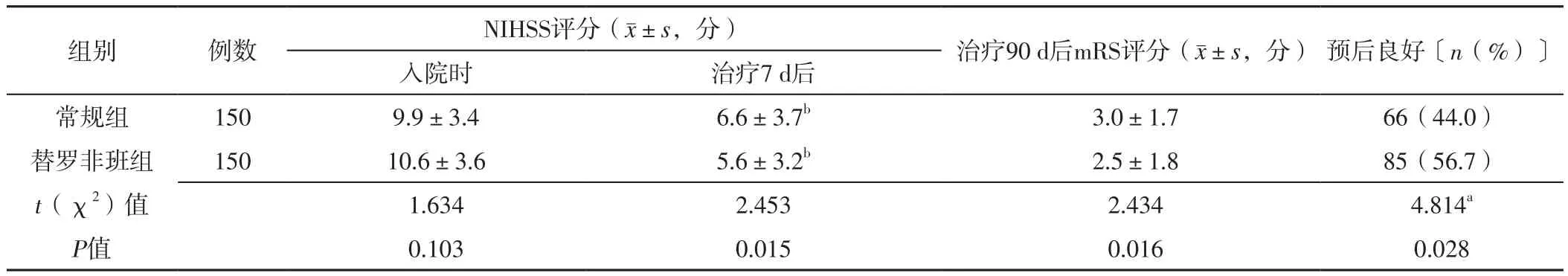
表2 常规组与替罗非班组NIHSS、mRS评分及预后比较Table 2 Comparison of NIHSS and mRS score and prognosis between routine group and tirofiban group
2.2.2 常规SAO亚组与替罗非班SAO亚组 常规SAO亚组与替罗非班SAO亚组入院时NIHSS评分比较,差异无统计学意义(P>0.05);常规SAO亚组、替罗非班SAO亚组治疗7 d后NIHSS评分分别低于本组入院时,且替罗非班SAO亚组低于常规SAO亚组,差异有统计学意义(P<0.05);替罗非班SAO亚组治疗90 d后mRS评分低于常规SAO亚组,预后良好者占比高于常规SAO亚组,差异有统计学意义(P<0.05),见表3。
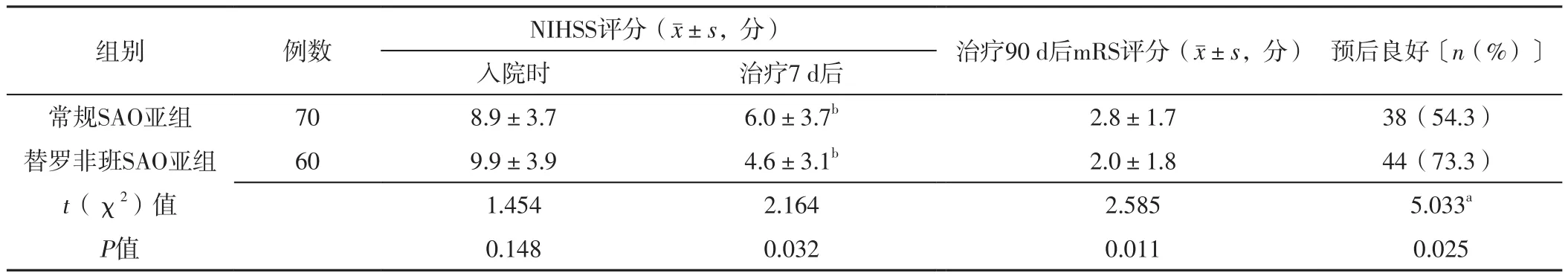
表3 常规SAO亚组与替罗非班SAO亚组NIHSS、mRS评分及预后比较Table 3 Comparison of NIHSS and mRS score and prognosis between conventional SAO subgroup and tirofiban SAO subgroup
2.2.3 常规LAA亚组与替罗非班LAA亚组 常规LAA亚组与替罗非班LAA亚组入院时、治疗7 d后NIHSS评分及治疗90 d后mRS评分、预后良好者占比比较,差异无统计学意义(P>0.05);常规LAA亚组、替罗非班LAA亚组治疗7 d后NIHSS评分分别低于本组入院时,差异有统计学意义(P<0.05),见表4。
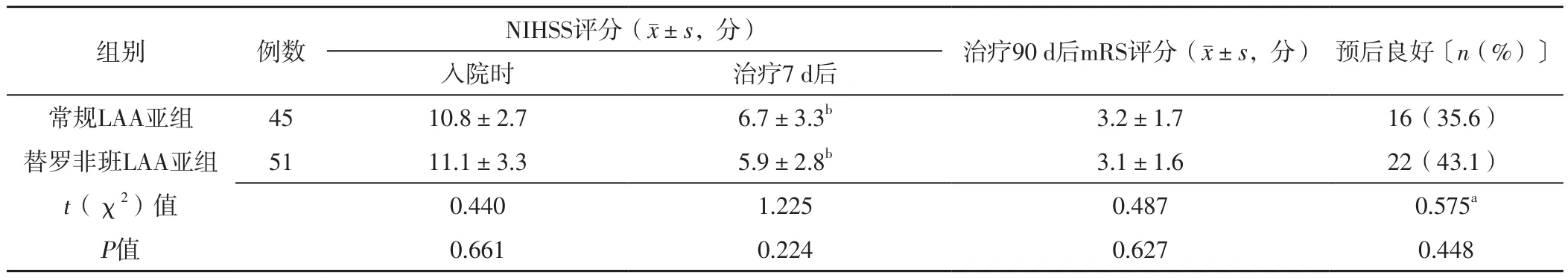
表4 常规LAA亚组与替罗非班LAA亚组NIHSS、mRS评分及预后比较Table 4 Comparison of NIHSS and mRS score and prognosis between conventional LAA subgroup and tirofiban LAA subgroup
2.2.4 常规CE亚组与替罗非班CE亚组 常规CE亚组与替罗非班CE亚组入院时、治疗7 d后NIHSS评分及治疗90 d后mRS评分、预后良好者占比比较,差异无统计学意义(P>0.05);常规CE亚组、替罗非班CE亚组治疗7 d后NIHSS评分分别低于本组入院时,差异有统计学意义(P<0.05),见表5。
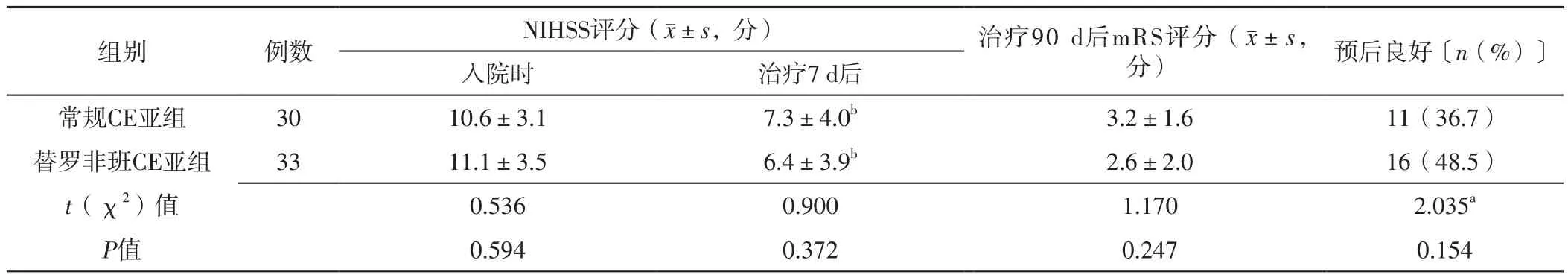
表5 常规CE亚组与替罗非班CE亚组NIHSS、mRS评分及预后比较Table 5 Comparison of NIHSS and mRS score and prognosis between conventional CE subgroup and tirofiban CE subgroup
2.3 安全性指标
2.3.1 常规组与替罗非班组 常规组与替罗非班组IH发生率、sICH发生率、死亡率比较,差异无统计学意义(P>0.05),见表6。

表6 常规组与替罗非班组安全性指标比较〔n(%)〕Table 6 Comparison of safety indexes between routine group and tirofiban group
2.3.2 常规SAO组与替罗非班SAO组 常规SAO亚组有1例发生IH,无sICH、死亡发生;替罗非班SAO亚组无IH、sICH、死亡发生。
2.3.3 常规LAA亚组与替罗非班LAA亚组 常规LAA亚组与替罗非班LAA亚组IH发生率、sICH发生率、死亡率比较,差异无统计学意义(P>0.05),见表7。
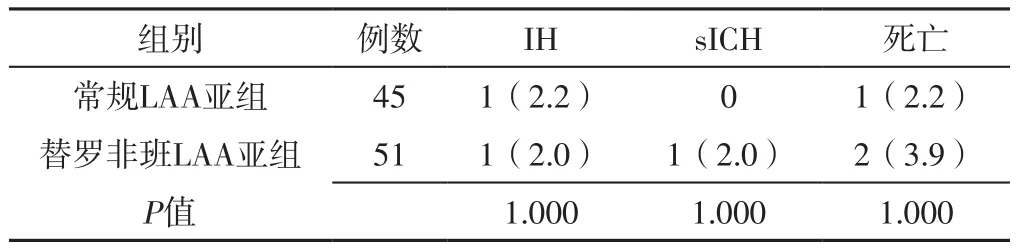
表7 常规LAA亚组与替罗非班LAA亚组安全性指标比较〔n(%)〕Table 7 Comparison of safety indexes between conventional LAA subgroup and tirofiban LAA subgroup
2.3.4 常规CE亚组与替罗非班CE亚组 常规CE亚组与替罗非班CE亚组IH发生率、sICH发生率、死亡率比较,差异无统计学意义(P>0.05),见表8。
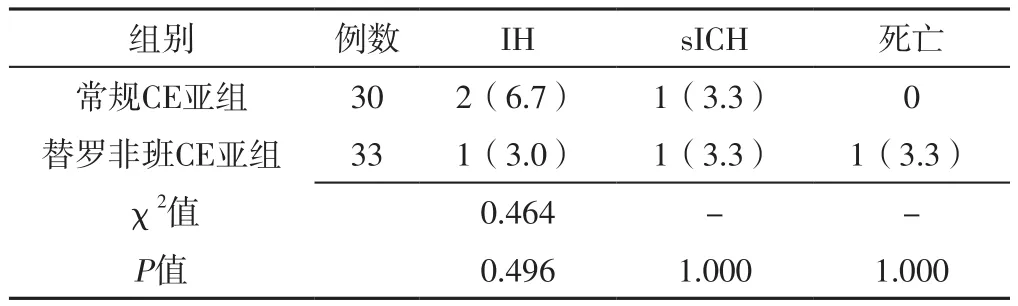
表8 常规CE亚组与替罗非班CE亚组安全性指标比较〔n(%)〕Table 8 Comparison of safety indexes between conventional CE subgroup and tirofiban CE subgroup
3 讨论
阿替普酶静脉溶栓是AIS最重要的治疗方式之一,但一项RCT结果显示,接受静脉溶栓治疗的AIS患者总血管再通率仅为46%,其中颈内动脉和大脑中动脉再通率为10%和25%,且所有血管再通患者中14%~34%会发生血管再闭塞,进而导致预后不良[17-18]。所以,阿替普酶联合其他药物提高血管再通率、降低溶栓后血管再闭塞发生率是目前亟待解决的问题和研究的重点。
替罗非班是一种低分子量的L-酪氨酸修饰结构的非肽类血小板糖蛋白(glycoprotein,GP)Ⅱb/Ⅲa受体拮抗剂[19-20]。GPⅡb/Ⅲa受体在二磷酸腺苷和血栓素A2等多种激活剂作用下活化,之后与纤维蛋白原、血管性血友病因子(von willebrand factor,vWF)等配体结合而导致血小板聚集、血栓形成,这也是血小板活化、聚集的最后通路。因此,阻滞该受体与纤维蛋白原、vWF等配体结合就可以阻滞血小板的活化,避免血栓形成。替罗非班与GPⅡb/Ⅲa受体亲和力高,能竞争性结合80%以上的受体,是最有效的抗血小板聚集药物[21]。静脉给予患者负荷剂量的替罗非班后,5 min内即可抑制90%以上的血小板,且在持续静脉滴注过程中,药物浓度为0.01~25.00 μg/ml即可维持65%的血浆蛋白结合率[22]。替罗非班的血浆t1/2仅为1.5~2.0 h,65%的药物原型从尿液排泄,25%从粪便排泄,而当肌酐清除率<30 ml/min时替罗非班的血浆清除率将降低50%以上[23]。
SEITZ等[24]将符合溶栓指征且无禁忌证的患者分为阿替普酶治疗组(仅予以阿替普酶静脉溶栓治疗)和联合治疗组(予以阿替普酶静脉溶栓后早期联合替罗非班治疗),结果显示,治疗8 d后联合治疗组梗死面积缩小程度大于阿替普酶治疗组,且神经功能改善效果优于阿替普酶治疗组。LI等[6]研究纳入的均为标准剂量(0.9 mg/kg,最大剂量为90 mg)阿替普酶静脉溶栓治疗的患者,部分患者在静脉溶栓后24 h内联合替罗非班(0.4 μg·kg-1·min-1,持续30 min后以0.1 μg·kg-1·min-1静脉泵注,持续24 h)治疗(联合治疗组),结果显示,联合治疗组溶栓后血管再闭塞率明显低于对照组(仅阿替普酶静脉溶栓治疗者),治疗7 d后NIHSS评分明显低于对照组,治疗90 d后预后良好占比明显高于对照组。本研究结果显示,替罗非班组治疗7 d后NIHSS评分低于常规组,治疗90 d后mRS评分低于对照组,预后良好者占比高于常规组,提示阿替普酶静脉溶栓后早期联合替罗非班治疗轻中度AIS有效。亚组分析结果显示,替罗非班SAO亚组治疗7 d后NIHSS评分低于常规SAO亚组,治疗90 d后mRS评分低于常规SAO亚组,预后良好者占比高于常规SAO亚组;而替罗非班LAA亚组与常规LAA亚组、替罗非班CE亚组与常规CE亚组入院时、治疗7 d后NIHSS评分及治疗90 d后mRS评分、预后良好者占比比较,无统计学差异。分析原因如下:(1)替罗非班可降低阿替普酶静脉溶栓后血管再闭塞率,根据文献报道,血管再闭塞的患者中SAO者占比较高[25]。阿替普酶溶栓后再通的血管在原来血栓位置仍有少部分血栓残留和/或该处因原血栓形成而受损的血管内皮细胞在血栓大部分溶解后被暴露、血液流经溶栓后再通位置时为涡流、血栓溶解过程中降解产物等因素可激活血小板,引发血小板聚集等一系列反应,导致血管再次狭窄或闭塞[26-27]。替罗非班可通过竞争性地结合GPⅡb/Ⅲa受体而阻断血小板的活化,进而避免静脉溶栓后的血管再闭塞[28-29]。(2)进展性卒中发病机制不详,但血小板的活化、聚集是其重要发生机制,且是SAO亚型进展的主要机制,而替罗非班可通过抑制血小板聚集而改善进展性卒中SAO亚型的进展[30]。多项研究证实,替罗非班可明显提高进展性卒中SAO亚型患者治疗7 d时NIHSS评分及治疗90 d时预后良好率,而对进展性卒中LAA、CE亚型患者无改善效果[31-32]。(3)SUN等[33]研究证实,心源性栓子富含红细胞,而替罗非班对富含红细胞的栓子无效,可能导致其对LAA、CE亚型患者的临床疗效、预后无改善作用。(4)LAA亚型有低灌注/微栓子清除障碍等多种发生机制,而替罗非班对这些机制无效[34]。(5)可能与LAA、CE亚组样本量较小有关。
研究表明,低剂量到标准剂量阿替普酶静脉溶栓后早期联合替罗非班均不增加AIS患者IH、sICH发生率及死亡率[6,19,26,35-36]。WU等[27]纳入121例静脉溶栓后早期联合替罗非班治疗患者(替罗非班组)和66例不联合替罗非班治疗患者(非替罗非班组),结果显示,替罗非班组和非替罗非班组sICH发生率和死亡率比较,差异无统计学意义。一项荟萃分析显示,阿替普酶静脉溶栓后早期联合替罗非班组和未联合替罗非班组IH、sICH发生率及死亡率比较,差异无统计学意义[8]。牙龈、消化系统、泌尿系统是报道比较多的除颅脑以外的出血部位,PRISM-PLUS试验显示,替罗非班组牙龈、消化系统、泌尿系统等部位出血总发生率为4%,与对照组(不应用替罗非班而应用肝素治疗)比较差异无统计学意义[37]。本研究结果显示,替罗非班组和常规组以及两组中对应的SAO亚组、LAA亚组、CE亚组IH发生率、sICH发生率及死亡率比较均无统计学差异,证实阿替普酶静脉溶栓后早期联合替罗非班不增加轻中度AIS及各TOAST亚型患者死亡率及IH发生率、sICH发生率,是安全的,与既往研究结果一致[7,25,38]。
综上所述,阿替普酶静脉溶栓后早期联合替罗非班治疗轻中度AIS患者安全有效,尤其是SAO患者,建议在阿替普酶静脉溶栓后2 h联合替罗非班(静脉泵注,0.4 μg·kg-1·min-1,持续30 min后改为0.1 μg·kg-1·min-1,共持续24 h)以降低致死率、改善患者预后。但本研究为小样本量、单中心研究,未来需要大样本量、多中心的研究进一步验证本研究结论。
作者贡献:吕洋进行文章的构思与设计、负责文章的质量控制及审校;吕洋、柳燕、李宏伟进行研究的实施与可行性分析;柳燕、李宏伟进行资料收集;柳燕、李宏伟、臧洁进行资料整理;吕洋、柳燕撰写论文;李宏伟、臧洁进行统计学处理;吕洋、宋金东进行论文的修订,对文章整体负责、监督管理。
本文无利益冲突。

