总有机碳检测法在五味子提取清洁验证中的应用
徐婷 陶金 岳镭


摘 要:为了证明总有机碳(total organic carbon, TOC)检测法可用于中药材五味子提取设备的清洁验证。采用淋洗法与擦拭法取样,并验证TOC检测法的线性、精密度与准确度、检测限(LOD)与定量限(LOQ)、取样回收率与稳定性,评价总有机碳法用于中成药清洁验证的效果。结果表明,五味子浓度(x)在0.024~0.960 mg/L范围内时,其与TOC值(y)呈良好的线性关系,回归方程为y=218.8x-0.033,r2=0.999;精密度与准确度的相对标准偏差(RSD)均不超过4%;检测限(LOD)为3.84μg/L,定量限(LOQ)为11.5 μg/L;采用两种方式取样,在低、中、高浓度淋洗法平均取样回收率分别为63.91%、81.00%、81.11%,擦拭法平均取样回收率分别为87.50%、83.33%、106.94%;样品溶液分别在0、4、8、24、28、48 h进行TOC检测,RSD为5.21%;应用于生产中减压浓缩罐设备残留量计算,结果符合限度浓度要求。TOC法可用于五味子提取生产清洁验证,可广泛应用于多活性成分的中药制药生产。
关键词:总有机碳检测法,五味子,清洁验证,擦拭法取样,淋洗法取样
DOI编码:10.3969/j.issn.1002-5944.2023.19.038
Application of Total Organic Carbon Method in Cleaning Validation for Extraction of Schisandra chinensis
XU Ting TAO Jin YUE Lei*
(Shanghai Hutchison Pharmaceuticals)
Abstract: To prove that the total organic carbon (TOC) method can be applied in cleaning validation (CV) for extraction of Schisandra chinensis. Sampling by rinsing and swabbing methods the TOC method was verifi ed for linearity, precision and accuracy, limit of detection (LOD) and limit of quantitation (LOQ), sampling recovery rate, stability, which was used for evaluating the effectiveness of facilities cleaning of Chinese patent medicine. The Schisandra chinensis extract concentration(x) at a range of 0.024~0.960 mg/L showed good linear relationship to TOC value (y), of which the linear regression equation was y=218.8x-0.033, r2=0.999. Both the RSDs in accuracy and precision tests were less than 4%. LOD was 3.8 μg/L, LOQ was 11.5 μg/L.Sampling by two methods, the average sampling recoveries of rinsing method at low, medium and high concentrations were 63.91%, 81.00% and 81.11% respectively, and those of swabbing method were 87.50%, 83.33% and 106.94% respectively. The test solutions were detected at 0, 4, 8, 24, 28, and 48 h respectively by TOC method, with RSD of 5.21%. When applied in the production, the residual concentration of vacuum concentration tank residues were lower than allowable level. The TOC method can be used for CV of Schisandra chinensis extract, which means that it can be widely used for CV of traditional Chinese medicine production with complex components.
Keywords: total organic carbon (TOC) method, Schisandra chinensis (Turcz.) Baill., cleaning validation, swabbing sampling, rinsing sampling
0 引 言
五味子為木兰科植物五味子Schisandra chinensis(Turcz.)Baill.的干燥成熟果实,习称“北五味子”,收录于2020年版《中华人民共和国药典》(以下简称《中国药典》)[1]与2012年《可用于保健食品的物品名单》[2]中,五味子中目前已知的活性成分达203种[3-4],主要成分有五味子醇甲[5]、五味子甲素、五味子乙素等木质素类成分[6],萜类[7],挥发油[8],多糖、黄酮类[9]及有机酸[10]等。
《药品生产质量管理规范》(Good Manufacturing Practice,GMP)要求企业对制药设备进行有效清洗以最大限度防止药品污染和交叉污染[11],为保证清洗后的设备中各种残留物的总量低至不影响共线产品规定的疗效、质量和安全性,需要对设备进行清洁验证[12],即通过科学的方法采集足够的数据,以证实按规定方法清洁后的设备,能始终如一地达到预定的清洁标准[13]。
五味子提取后设备清洁残留成分多、限度低于目视标准(1~4 μg/cm2),难以界定溶解度最小或颜色最深的目标化合物[14],新兴起的总有机碳(total organic carbon,TOC)法[15]可检测到所有含碳化合物,结果以碳的质量浓度表示,包括清洁剂乙醇等都能被检出,该法检测范围广,灵敏度高,检测时间短,更适用于中药生产过程清洁验证[16-18]。
1 仪器与材料
GE Sievers M9 型总有机碳TOC分析仪(美国通用电气GE公司);XS205DU型电子分析天平(梅特勒-托利多METTLER TOLEDO 仪器上海有限公司);五味子(批号J200301,上海真仁堂药业有限公司);蔗糖对照品(批号111507-202105,中国食品药品检定研究院);1,4对苯醌对照品(批号101197-201904,中国食品药品检定研究院);超纯水(实验室自制,Millipore A10水纯化系统)。
2 方 法
2.1 系统适用性实验

2.2 線性
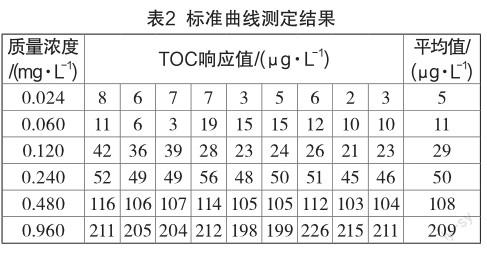
用超纯水溶解60 mg五味子浸膏,并定容至500 mL,配置浓度为120 mg/L的标准储备液体,再用超纯水稀释至质量浓度分别为0.024、0.060、0.120、0.240、0.480、0.960 mg/L的溶液,以超纯水为空白对照,分别进行TOC检测,重复测定TOC结果的平均值(μg/L)作为y值,以五味子质量浓度(mg/L)为x值,进行线性回归,计算相关系数(r2)。
2.3 精密度与准确度
将上述质量浓度分别为0.24 mg/L、0.48 mg/L、0.96 mg/L的样品溶液再进行TOC检测,重复测定9次,计算RSD,9次检测结果的平均值与带入线性方程所得的TOC响应值之比为回收率结果。
2.4 检测限与定量限
在10个取样瓶中分别加满纯化水,重复测定3次,计算平均值,由t99(n-1)×SD得到检测限(Limit of detection, LOD),将检测限乘以3,得出定量限(Limit of quantitation, LOQ)[18]。
2.5 取样回收率
2.5.1 淋洗法回收率
吸取56.00 mg/L的五味子样品溶液6 mL,定量装入干净的喷雾器中,分别从阀门的左右两侧均匀喷在管内壁,内表面目视干燥后用700 mL纯化水淋洗,在干净的烧杯中收集淋洗水并检测其TOC响应值,用扣除背景的TOC响应值代入方程换算出样品溶液浓度(mg/L),并计算平均浓度(mg/L),除以理论浓度(mg/L)得到淋洗法平均取样回收率(%),用0.5倍残留浓度与1.5倍残留浓度的样品溶液重复上述实验。
2.5.2 擦拭法回收率
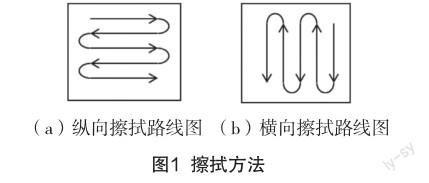
准备一块平整光滑的不锈钢板,在其表面划出25 cm2×4的区域,配置浓度为19.20 mg/L的五味子样品溶液,定量装入干净的喷雾器中,在不锈钢表面上均匀喷洒10 mL溶液,液体不得越过边界,静置过夜,自然晾干。取样人员手部清洁,在目视检查合格后用分别用两支TOC专用棉签进行擦拭取样,取样面积为25 cm2。取样前,棉签使用少量纯化水润湿,按图1(a)的路线用棉签的一侧擦拭,尽量覆盖全部取样面积,取样时注意折弯棉签头取样,然后翻转棉签使其另一面按图1(b)的路线进行擦拭,应尽可能采用相同的力度[20]。
将现场取样擦拭完毕的TOC专用棉签头折断,浸入装有100 mL纯化水的烧杯中,轻摇并放置10 min,使有关物质溶出后测定,用扣除背景的TOC响应值代入线性回归方程换算出样品溶液的平均浓度值(mg/L),除以理论浓度(mg/L)得到擦拭法取样回收率(%),用0.5倍残留浓度与1.5倍残留浓度的五味子浸膏溶液重复上述实验并测定。
2.6 样品溶液稳定性
将质量浓度为0.48 mg/L的样品溶液保存在常温环境中,分别在0、4、8、24、28、48 h测定其TOC响应值,平行测定3次,以其平均值计算RSD。
2.7 方法在车间的应用

3 结 果
3.1 系统适用性实验
系统适用性实验的响应效率(R)为94%,在85%~115%之内,符合要求,数据见表1。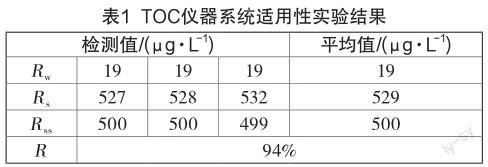
3.2 线性
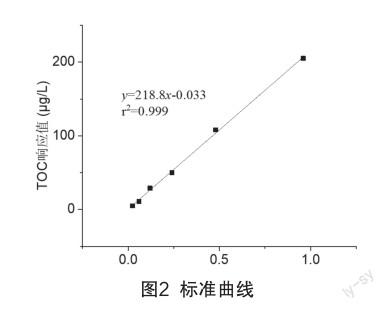
超纯水空白的TOC响应值<0.03 μg/L,当样品溶液的浓度(x)在0.024~0.960 mg/L范围内时,其与TOC响应值(y)呈较好的线性关系,标准曲线的回归方程为y=218.8x-0.033,相关系数r2=0.999。
3.3 精密度与准确度
样品溶液在低、中、高浓度对应的回收率在90%~110%范围内,相对标准偏差分别为3.4%、2.9%,2.1%,表明精密度与准确度好,如表3所示。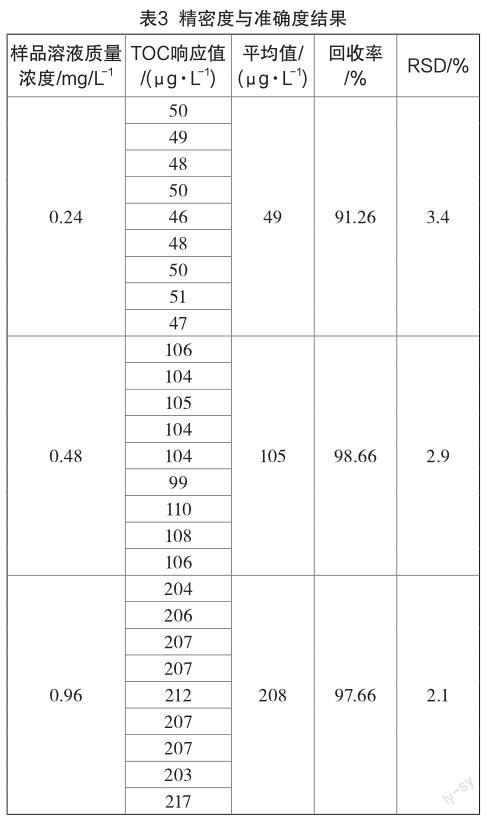
3.4 检测限与定量限
淋洗水的TOC平均值为0.78 μg/L,SD为1.09μg/L,LOD=SD×t99(n-1)=1.09×3.52=3.84 μg/L,LOQ=3SD×t99(n-1)=11.5 μg/L。
3.5 取样回收率
3.5.1 淋洗法回收率
0.24 mg/L(0.5倍残留浓度)、0.48 mg/L(1.0倍残留浓度)、0.72 mg/L(1.5倍残留浓度)的淋洗水样品平均回收率分别为63.91%、81.00%、81.11%,淋洗法取样回收率均大于60%,见表4。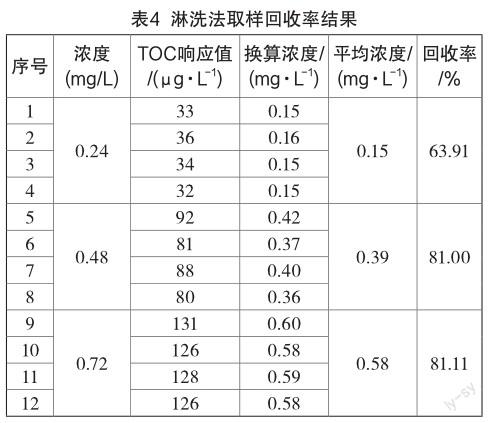
3.5.2 擦拭法回收率
0.24 mg/L(0.5倍残留浓度)、0.48 mg/L(1.0倍残留浓度)、0.72 mg/L(1.5倍残留浓度)的擦拭样品溶液平均回收率分别为87.50%、83.33%、106.94%,见表5。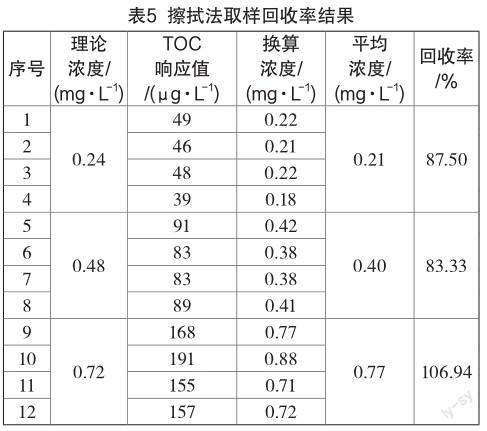
3.6 稳定性
放置了48 h的样品溶液分别在6个时间段进行TOC检测,RSD为5.21%,样品送检后应在48 h内完成检测。供试品溶液稳定性验证如图3所示。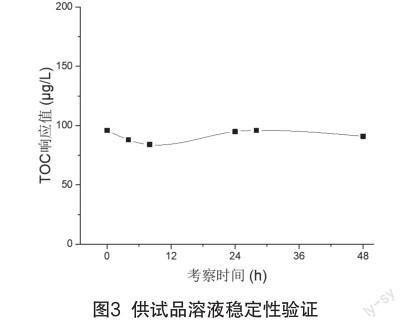
3.7 方法在车间的应用
分别根据减压浓缩罐设备与干燥设备清洗后的样品溶液TOC响应值,代入线性公式折算,所得样品溶液浓度均小于标准限度浓度,说明减压浓缩罐与干燥设备中五味子浸膏的残留量符合限度要求。
4 讨 论
中药设备清洁方法验证是对生产取样人员操作、棉签选择、溶剂选择等的全面模拟考察,进行方法验证时保证擦拭取样人员与车间生产取样人员一致,若无法保证,可考察不同人员擦拭后的效果,TOC检测法应使用专用棉签,避免棉签影响取样回收率,擦拭溶剂应与取样溶剂一致,注意擦拭溶剂不应干扰TOC检测结果。
取样方面,对于易擦拭的设备表面采用棉签擦拭法,对于不易擦拭的表面及卫生球阀采用淋洗法,仅在0.24 mg/L的浓度时,淋洗法取样平均回收率<70%,其余擦拭法与淋洗法平均回收率在80%~110%范围内,当两种取样方法均适用时建议优先采用擦拭法,尤其在指标成分含量极低时,擦拭法取样回收率更好,回收率不符合要求的主要原因包括人员擦拭力度不够、擦拭路径未包含全部取样面积、棉签与取样表面的接触角度过大导致接触面积不足等。
在药品生产设备清洁过程中,一般选择溶解度小、毒性高的指标成分进行验证,对于不含毒性成分且有效成分残留含量极低的中药产品,TOC法凸显优势,该法能更全面检测中药品种中多指标成分的残留量,具有很大的应用空间。本次验证TOC法检测限低至3.8 μg/L,且样品检测耗时仅10 min,检测时间短、灵敏度高,样品溶液质量浓度与TOC响应值呈现良好的线性关系,r2=0.999,检测精密度好、准确可靠,稳定性考察结果表明样品溶液较为稳定,可至少放置48 h。但TOC法检测也有一定的局限性,其仅能检测水溶性物质的碳含量,且清洗要求高,检测结果易受残留物影响。
5 结 论
以五味子提取设备清洁为例采用TOC法检测中药生产设备的清洁残留浓度,该方法操作简便、灵敏度高、准确度和精密度好,更适用于基质复杂、指标成分含量低于1 mg/kg的中药生产设备清洁验证,通过建立科学合理的清洁验证检验方法,满足不含毒性成分的中药产品中低浓度、多指标组分的检测要求,为中药制剂生产清洁验证工作提供方法学研究参考。
参考文献
[1]国家药典委员会.中华人民共和国药典,一部[M].北京:中国医药科技出版社,2020:68,255.
[2]于新.药食同源物品使用手册(可用于保健食品的物品)[M].北京:中国轻工业出版社,2012.
[3]YANG, S Y, YUAN C H. Schisandra Chinensis: A comprehensive review on its phytochemicals and biological activities [J].Arabian Journal of Chemistry, 2021(14) : 103310.
[4]YANG Y C, WEI J C, LIU L Q, et al. A new norsesquiterpenoid from Schisandra chinensis.[J]. China journal of Chinese Materia Medica, 2022, 47(6) :1582-1586.
[5]鄭宏春,张珍,刘扬.五味子中五味子醇甲含量与成熟程度的关系研究[J].中文科技期刊数据库(文摘版)医药卫生,2022(2):4.
[6]王志明,刘久石,郭耀杰,等.五味子果实不同部位中木脂素成分的分布规律[J].中国实验方剂学杂志,2015,21(18):35-39.
[7]白文宇,王厚恩,王冰瑶,等.五味子化学成分及其药理作用研究进展[J].中成藥,2019,41(9):2177-2183.
[8]THINH B B,THANH V Q, HANH D H,et al. Chemical Composition and Antioxidant Activity of Essential Oil from Fruit of Schisandra perulata[J]. Chemistry of Natural Compounds, 2022, 58(4).
[9]穆开朗,程昆木,王正旺,等.南北五味子及其藤茎中多糖与黄酮类成分含量差异的研究[J].山东化工,2021, 50(14):114-115+117.
[10]金银萍,曲正义,崔丽丽,等.五味子不同部位黄酮和酚酸类成分的含量测定及抗氧化活性[J].中国实验方剂学杂志,2018,24(19):79-84.
[11]卫生部.卫生部令第79号 药品生产质量管理规范(2010年版)[EB/OL].(2011-01-17) [2023-04-10].https://www. gov.cn/govweb/gongbao/content/2011/content_1907093.htm.
[12]国家食品药品监督管理局食品药品审核查验中心.口服固体制剂与非无菌吸入制剂:药品GMP指南[M].北京,中国医药科技出版社,2023:328.
[13]叶笑,王立杰,颜若曦.清洁验证中活性物质残留限度标准探讨[J].中国药物评价,2022,39(3):227-231.
[14]吴斌,相婷,牟娜.中药共线生产的风险评估和清洁验证[J].现代药物与临床,2023,38(2):464-466.
[15]邹大光,袁曦.一种清洁验证新方法—TOC法[J].中国药事,2002,16(1):19-20.
[16]周庆凯,孙巍,曹凤兰,等.总有机碳法用于复方丹参装囊滴丸清洁验证的可行性研究[J].中成药,2012,34(11): 2114-2117.
[17]谢姗姗,廖丹,杨勇,等.总有机碳检测法在无细胞百日咳疫苗生产清洁验证中的应用[J].中国生物制品学杂志, 2017,30(11):1196-1202+1206.
[18]冯潇,戈玲,刘晨鸣,等.总有机碳分析在制药设备清洁验证中的应用[J].微生物学免疫学进展,2016,44(3):43-48.
[19]国家药典委员会.中华人民共和国药典(四部)[S].北京:中国医药科技出版社,2020:92.
[20]齐鹤.关于化学药品制剂生产车间清洁验证的几点思考[J].黑龙江医药,2022,35(1):45-48.
作者简介
徐婷,硕士,主要从事中药标准化研究。
岳镭,通信作者,高级工程师,主要从事中药生产及质量管理研究工作。
(责任编辑:袁文静)

