手性纳米材料:生物成像、生物传感与治疗
卢美如,张宏宇,石百媚,孙茂忠,徐丽广,胥传来,匡 华
(江南大学食品科学与技术国家重点实验室,无锡 214122)
手性是生物系统的一个重要的特征,广泛存在于分子与细胞水平,在维持正常的生物和生理过程中起着至关重要的作用[1].作为一种手性超分子体系,生物系统在吸收、合成、传感及代谢等生化过程中也表现出极强的手性特异性,生物分子的手性决定了其结合特性,这对许多生物事件都产生了显著影响[2].纳米技术的快速发展和进步使得大量人工手性纳米材料得以构建,引入手性的方式包括表面配体介导的手性[3]、不对称手性形态[4]和自组装纳米手性[5].作为一种新兴的纳米技术,手性无机纳米材料因具有独特的光学性质、对映选择性以及良好的生物相容性等特点[6,7],已被广泛应用于生物医学领域,特别是生物成像与治疗.
无机纳米颗粒可以解决小分子药物无法解决的许多挑战,例如较高的渗透性和保留效应.然而在实际应用中仍面临许多挑战和局限性,如长期肝肾的积累、毒性及生物化学稳定性等,手性配体的表面修饰可以在一定程度上改善这些关键问题[8~12].迄今,科学工作者已经构建了多种基于手性的纳米材料,并将其应用于生物成像与诊疗领域.基于手性的生物成像被用于可视化和监测生物过程,并通过安全、无创的光学成像方法原位诊断疾病[13].结合手性、荧光和拉曼多重信号的手性自组装纳米结构[13,14]也被用于全方位的深层疾病诊疗.此外,一些手性纳米粒子的对映体结构可以选择性地识别与调控疾病相关蛋白的构象转变,这更深入地扩展了手性纳米材料在重大疾病治疗领域的应用.Kuang等[15]合成了具有切角四面体构型的手性碲化镉量子点,其可以特异性识别并结合双链脱氧核糖核酸(DNA)中的GATATC片段,并在光的激发下产生羟基自由基,导致双链DNA中GAT^ATC位点的特异性剪切.Zhang等[16]制备的手性硒化铜铁纳米粒子可选择性地与β-淀粉样纤维结合,并触发β-淀粉样组装体的解聚.手性调控机体免疫应答已成为现阶段的研究热点.Xu等[17]利用强手性金纳米粒子作为佐剂与抗原呈递细胞表面的G蛋白偶联受体进行特异性结合,激活炎症小体通路,同时诱导细胞免疫应答和体液免疫应答,为未来新型疫苗佐剂研发找到了根本性突破口.手性结构的优异性能极大地扩展了无机纳米材料的应用领域.然而,手性纳米材料进入临床试验还有很长的路要走,包括对其安全性、毒理学和靶向效率的评估.因此,开发高效、稳定且安全的新型手性纳米材料在药物研发和创新中发挥着重要作用.
本文阐述了手性纳米材料在生物医学领域的研究现状,重点介绍了手性金属和手性半导体纳米结构的光学特性,如圆二色性和对映选择性光热性能,并概述了基于手性的生物成像、生物传感、疾病诊断和疾病治疗的发展和优势.最后,探讨了未来手性纳米材料在生物医学领域应用所面临的挑战与前景.
1 手性无机纳米材料的种类及功能特性
近10年来,具有各种尺寸和形貌的手性纳米材料的合成已经取得了重大进展.手性纳米材料利用其独特的光学性质,有潜力成为改善临床早期疾病诊断以及光治疗方法的有力工具[18].根据手性来源,本文将近年来广泛用于生物医学领域的手性纳米材料主要分为表面配体介导的手性、不对称手性形态和自组装纳米手性等3种.本文总结了以上3种手性纳米材料的构建方法以及基于手性的生物检测策略.
1.1 表面配体介导的手性
配体诱导的手性是基于手性分子与单个纳米粒子的整合,其机制非常广泛[19,20].Jiang等[21]利用表面配体交换的方式合成了手性氧化钨纳米粒子,左手性及右手性氧化钨纳米粒子的圆二色光谱呈现出完美的镜像对称[图1(A)].Balaz等[20]合成了非手性硒化镉量子点,用其修饰左旋或右旋半胱氨酸配体后诱导产生了镜像对称的圆二色光谱信号[图1(B)].Kotov等[3]利用左旋或右旋半胱氨酸作为表面配体合成了手性四氧化三钴纳米粒子,其强手性源自配体引起的晶格手性畸变[图1(C)].值得注意的是,表面配体诱导手性作为获得手性无机纳米材料最便捷最常见的途径,已经分别从材料的性质(尺寸、形态及元素等)和手性配体的性质(种类和构象等)方面进行了深入的研究,合成的手性纳米粒子已广泛应用于光学偏振和基于手性的生物检测和疾病诊疗等交叉领域.然而,这种手性无机纳米材料合成方式单一,难以通过高分辨透射电子显微镜或扫描电子显微镜来识别这种手性结构,限制了对手性与生物界面相互作用机制的进一步探索.
1.2 不对称手性形态
为了获得可控的手性形态,氨基酸、肽及圆偏振光等通常作为手性源引入纳米粒子的合成过程中,导致其不对称形态的演变.这种不对称手性形态具有良好的可调性,其圆二色信号和各向异性因子通常较强,有利于进一步探索手性结构与生物界面相互作用的机制.Kuang等[15]在手性碲化镉纳米粒子合成过程中引入左旋或右旋半胱氨酸配体形成了独特的不对称切角四面体结构,并用于特异性剪切双链DNA中的GATATC片段[图1(D)].Nam等[4]通过两步法设计合成了具有特定形态和强光学活性的手性等离子体螺旋结构.首先,合成了尺寸均匀的低米勒指数表面的金纳米粒子作为种子.在之后的生长步骤中,手性半胱氨酸或基于半胱氨酸的肽被编码在金纳米粒子中.手性配体与金纳米粒子的相互作用导致形成强手性的螺旋体结构[图1(E)].Xu等[17]使用圆偏振光来控制左旋或右旋半胱氨酸-苯丙氨酸二肽诱导的非手性金纳米三角片的还原生长,成功制备了不对称因子(g值)高达0.44的镜像手性纳米颗粒[图1(F)].

Fig.1 Morphology and spectroscopy of chiral nanoparticles
1.3 自组装纳米手性
不对称纳米组装体显示出直观的立体构象、可控的等离子体增强的手性活性和优异的多重性能[22,23],这极大地增强了其在生物传感中的应用潜能.近年来的研究大多使用DNA[24~26]、蛋白质及多肽[27]等生物分子作为连接物,并赋予组装体二聚体、金字塔、卫星结构或螺旋结构等空间几何结构及光学性质.Sun等[25]将上转换纳米颗粒内嵌入贵金属纳米颗粒组装的手性四面体中获得手性纳米结构,通过监测圆二色光谱信号和上转换发光信号,实现了细胞自噬程度的定量分析以及细胞自噬过程的可视化表征[图2(A)].Li等[26]利用上转换纳米粒子与金纳米粒子为基元通过DNA进行组装,制备了手性金字塔结构并成功应用于活细胞内的microRNA精准测定[图2(B)].

Fig.2 Structure and spectroscopy of chiral nano-assemblies
除上述几种常见的自组装结构外,一些手性纳米贵金属或半导体材料可在生物分子或光的调控下自组装形成具有特定螺旋方向的纳米超结构[28~30].圆偏振光在特定位置照射下可诱导等离子体纳米立方体周围的扭曲电场分布,并通过扭曲电场将电介质部分电化学沉积到立方体的特定位置上作为电子振荡助推器,由此制备出具有特定扭曲方向的手性纳米结构[31].Kotov等[32]发现碲化镉量子点的手性使其对圆偏振光的吸收有选择性.用左旋和右旋圆偏振光照射碲化镉量子点可分别诱导形成左旋和右旋扭曲纳米带.这表明不同偏振光处理可改变量子点与配体的相互作用,进一步导致量子点自组装形成手性纳米超结构[图2(C)].有趣的是,Kotov等[29]又利用超分子相互作用,实现了金纳米棒与人胰岛淀粉样多肽的精准共组装,构建了具有类似于手性液晶的长程有序的纳米螺旋纤维结构,其不对称因子(g值)高达0.12[图2(D)].液晶的颜色变化可直观地反应纳米棒的纤维化,这为检测疾病相关淀粉样蛋白提供了新思路.
本章阐述了不同对映体结构的构建及手性来源,这些手性来源包括手性氨基酸配体、多肽、DNA、蛋白质以及圆偏振光.这表明不同的纳米材料有不同的手性诱导机制和手性发生.各种不同的对映体结构有望被应用于对映选择性光催化剂、高灵敏度手性传感器、光子材料甚至临床生物医学检测与治疗,推动生命科学与技术的发展.
2 生物应用
2.1 生物成像与传感
生物成像能够揭示细胞和生物的结构和生理功能,从而实现疾病的筛查、诊断和治疗.目前使用的生物成像方法包括光学成像(PAI)、磁共振成像(MRI)、超声成像(USI)及X射线计算机断层扫描(CT)[33]等.基于手性的生物成像越来越受到重视.本章将全面探讨手性无机纳米材料在生物成像与传感中的应用.
2.1.1 PAI方法 PAI作为一种新型生物成像技术,具有非电离、无创、高对比度和高分辨率等特点[33].近年来,随着手性纳米技术的发展,手性纳米造影剂已被广泛应用于肿瘤组织的光声成像.与传统造影剂相比,手性纳米颗粒造影剂具有在深层组织的成像能力和增强的对比度.此外,许多研究将热疗与PAI结合,基于手性纳米粒子独特的光学性质,实现PAI引导的肿瘤协同诊断和治疗.Xu等[34]首次构建了DNA驱动的金(核)-银(壳)卫星纳米自组装体作为手性光敏剂.通过在其表面修饰半胱氨酸的对映体,使其在可见光区展现出强烈的手性等离子体活性.在各种合成的手性卫星纳米组装体中,右旋半胱氨酸修饰的金15(核)-银(壳)卫星纳米组件(金15:直径为15 nm的金纳米粒子)在静脉注射24 h后,在肿瘤部位表现出较强的光学信号[图3(A)].此外,在圆偏振光辐照下,右旋半胱氨酸修饰的金15(核)-银(壳)卫星纳米组件具有较强的活性氧生成能力,从而表现出良好的抗肿瘤活性.结果表明,该手性纳米组件在圆偏振光辐照下,实现了PAI引导的实时肿瘤监测与治疗.
2.1.2 MRI方法 MRI是目前生物医学领域常用的一种诊断方法,一些磁性纳米粒子作为造影剂已显示了增强的磁共振诊断信号以实现靶向治疗的巨大潜力[35,36].Li等[37]合成了具有强手性和独特磁性的磁手性氢氧化钴纳米颗粒,并首次利用手性氢氧化钴纳米颗粒的圆二色光谱和MRI双重信号检测和监测活细胞中的活性氧.当二价钴离子与活性氧相互作用后,其氧化为三价钴离子导致圆二色光谱信号降低,T1信号强度增加.右旋天冬氨酸封端的氢氧化钴纳米颗粒的圆二色光谱和T1信号表明其在胞内检测活性氧的有效范围为0.673~612.971 pmol/106cell,检测限分别为0.087和0.179 pmol/106cell,该检测限分别是左旋天冬氨酸封端的氢氧化钴纳米颗粒的17%和29%,这归因于右旋天冬氨酸封端的氢氧化钴纳米颗粒具有更高的细胞积累.此外,该纳米颗粒能够通过荧光和MRI信号量化小鼠肿瘤内的活性氧水平[图3(B)].
2.1.3 荧光成像方法 基于手性纳米探针的荧光共振能量转移效应已广泛应用于生物检测与成像.Dong等[38]利用含“锦环”的DNA将小分子染料与金纳米粒子自组装,通过DNA“锦环”部分与microRNA的竞争结合使得染料猝灭的荧光恢复,并通过检测染料分子的荧光变化实现对胞内microRNA的可视化检测.然而,背景自发荧光和染料分子的光学不稳定性严重限制了microRNA的细胞内定量.本课题组[14,26,39]利用上转换纳米粒子代替小分子染料,将手性纳米材料与上转换纳米粒子自组装,构建了具有圆二色和上转换发光双重信号的检测探针,该策略可有效避免生物自发荧光的干扰.Hao等[14]制备了上转换纳米粒子(核)-手性硫化镍纳米粒子封装的沸石咪唑酯骨架结构材料-8(壳)纳米组装体.该纳米组件在440和530 nm处显示出强烈的圆二色性信号,而上转换纳米粒子在540 nm处的上转换发光信号被手性硫化镍纳米粒子猝灭,并且在660 nm处的上转换发光信号几乎不变.利用手性光学信号和荧光信号,实现了对活细胞和体内活性氧的超灵敏和选择性检测[图3(C)].Sun等[39]利用多黏菌素对敏感菌株和耐药菌株的亲和力的不同,通过抗原抗体反应设计了金壳-上转换纳米粒子异质二聚体结构,利用圆二色光谱以及上转换发光双信号实现了对大肠杆菌多黏菌素耐药性的检测[图3(D)].Li等[26]利用上转换纳米粒子与金纳米粒子为基元通过核酸杂交进行组装,制备了手性金字塔结构.利用金字塔结构的圆二色信号以及上转换发光信号,成功实现了活细胞内的microRNA精准测定.这些基于手性纳米粒子与上转换纳米粒子自组装结构的双模态探针为一些疾病的早期诊断提供了强有力的支撑.
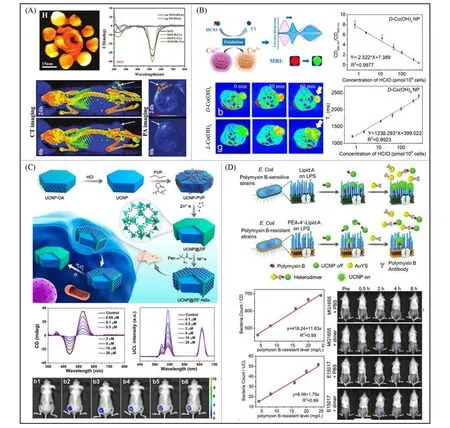
Fig.3 Bioimaging and sensing of chiral nanostructures
2.2 肿瘤治疗
近年来,手性无机纳米材料在肿瘤治疗领域已得到了广泛的应用.手性无机纳米结构,因其表面等离子体共振效应和独特的光学性质可以很大程度地增强其光转换性能,并且基于手性的选择性吸收性能,可以帮助实现精准治疗[40].本章阐述了手性无机纳米材料在肿瘤光疗以及肿瘤免疫治疗中的应用.
2.2.1 光疗方法 目前最常见的光疗方法是光热疗法(PTT)[40~43]和光动力疗法(PDT)[44,45],它们可以通过光吸收产生局部热能或活性氧来有效杀死癌细胞.一些手性贵金属纳米材料,由于其表面等离子体共振和激子耦合效应可以大大增强纳米结构中的手性光学活性,已广泛应用于光治疗肿瘤领域.有趣的是,手性纳米材料对圆偏振光的吸收能力强于线偏振光,因此圆偏振光辐照可提高其光转换效率并提高其治疗效果.此外,手性对圆偏振光的选择性吸收性能还可以减少治疗过程中对正常细胞与组织的损伤[46,47].Xia等[43]利用配体交换制备了具有近红外光学活性的手性硫化铜纳米晶体.在无光照射下,右手性和左手性硫化铜纳米晶体均能在极低浓度下产生活性氧并诱导肿瘤细胞自噬.而在近红外光照射下,硫化铜纳米晶体产生的光热效应进一步增强了肿瘤细胞的消融.右手性硫化铜纳米晶体进入HepG2和HeLa肿瘤细胞的量是其对映体的3倍,这导致了右手性硫化铜纳米晶体对肿瘤细胞的消融效率明显高于其对映体[图4(A)].该工作对肿瘤细胞消融的体外机制进行了广泛的研究,但对其在体内的作用尚未进行探讨.Xu等[34]利用金(核)-银(壳)卫星纳米自组装体作为手性光敏剂.这些手性卫星纳米组装物在相应的圆偏振光下对活性氧的生成显示出更强的对映选择性.其中,右旋半胱氨酸修饰的金15(核)-银(壳)卫星纳米组件表现出最强的光动力效应,并在右旋圆偏振光照射15 d后,彻底消除了小鼠的肿瘤组织[图4(B)].

Fig.4 Applications of chiral nanoparticles in tumor therapy
2.2.2 免疫治疗 引起具有特异性和安全性的全身抗肿瘤反应的肿瘤免疫治疗是目前癌症治疗方向的热点与前沿[48~52].纳米粒子的表面手性配体修饰或对映结构会影响它们与细胞、生物分子和生物系统之间的相互作用.然而,关于手性影响免疫反应的机理还需要进一步深入研究.最近,本研究组[53]首次利用强手性金纳米佐剂诱导细胞免疫应答和体液免疫应答以达到治疗和预防肿瘤的目的.研究发现,该手性纳米佐剂可选择性与树突细胞表面的G蛋白偶联受体家族(CD97和EMR1)结合,并在内吞的过程中诱导钾离子外流,激活炎症小体途径,刺激树突细胞的成熟,最终引起细胞免疫应答和体液免疫应答.与右手性纳米佐剂相比,左手性纳米佐剂与CD97和EMR1之间较高的亲和力诱导了更强烈的树突状细胞成熟和促炎细胞因子表达,这进一步促进了自然杀伤细胞和CD8 T淋巴细胞的活化与瘤内浸润,从而发挥更强的抗肿瘤及预防肿瘤效应[图4(C)].手性与免疫细胞之间的对映选择性相互作用为将来手性纳米佐剂在治疗性疫苗上的应用上提供了理论支持和方向.

Fig.5 Application of chiral nanomaterials in neurodegenerative disease treatment
2.3 神经退行性疾病治疗
随着纳米技术的发展,手性纳米材料在疾病诊疗中的应用已逐渐从肿瘤扩展至神经退行性疾病,如帕金森病(PD)和阿尔茨海默病(AD).神经退行性疾病的病理通常包括细胞内或细胞外错误折叠蛋白/多肽的聚集,氧化应激诱导的神经损伤和细胞凋亡[54~59].最近,一些基于手性的纳米材料在缓解神经退行性疾病的病理症状方面取得了重要进展.Zhang等[16]合成了手性硒化铜铁纳米粒子可选择性与β-淀粉样纤维结合,而右手性纳米粒子与β-淀粉样纤维的亲和性比左手性纳米粒子更高,在近红外光激发下产生活性氧,最终加速β-淀粉样纤维的分解[图5(A)].Tang等[60]发现,右手性金纳米粒子比左手性金纳米粒子更能有效防止β-淀粉样蛋白聚集,这归因于右手性金纳米粒子对β-淀粉样蛋白的亲和力更高.在AD模型小鼠中,右手性金纳米粒子显示出更有效的血脑屏障渗透,并导致AD小鼠认知的恢复[图5(B)].Hao等[59]使用手性苯丙氨酸作为结构导向剂制备了手性多孔氧化铜纳米簇.这些手性多孔氧化铜纳米簇在功能上具有多种类酶活性,可以清除活性氧,保护细胞免受氧化应激,抑制神经细胞毒性,并挽救PD模型小鼠的记忆缺陷[图5(C)].此外,当合成中不使用手性苯丙氨酸配体时,获得了不具有显著类酶活性的片状纳米结构,表明手性苯丙氨酸配体在决定最终纳米簇结构中产生了至关重要的作用.这些研究表明手性纳米材料在治疗神经退行性疾病方面有巨大的应用前景.
3 总结与展望
手性纳米材料是一种新兴的纳米结构,在过去的几年里吸引了科学界越来越多的关注.由于具有独特的光学性质和良好的生物相容性,手性纳米材料在生物学和生物医学领域备受关注.手性依赖现象在生命系统中普遍存在,这决定了手性与手性之间的结合特异性.因此,开发新型安全的手性纳米材料对纳米生物以及纳米医学的发展具有重要意义.本文对近10年来手性纳米材料在生物传感、生物成像和疾病诊断与治疗领域的一些重点研究进行了总结,并展望其未来发展前景.
尽管已经报道了手性纳米材料在生物应用中的可行性和优越性,但目前手性无机纳米材料在生物医学中的研究仍然处于初步阶段,仍有一些问题亟待解决.(1)高产率制备有明确手性构型以及强手性光学性质的手性纳米材料仍具有很大的挑战性.如何将合成过程可控化、标准化、简单化,并实现大规模生产以满足市场需求是未来需重点解决的问题.(2)手性纳米材料通过对圆偏振光的选择性吸收激发其特异性功能,如生物成像、生物传感、疾病诊断与治疗.目前大多数手性材料可以被可见光激发,然而,可见光穿透人体组织的深度有限,难以治疗位于组织深处的靶点,尤其是肿瘤或脑部疾病.因此,为了促进具有独特光学性质的手性纳米材料的临床转化,开发更多可被近红外光激发的手性纳米材料是非常重要的.(3)生物相容性、安全性和靶向性是临床试验前的主要考虑因素.尽管手性的引入可以降低纳米材料的生物毒性,增强其生物相容性及靶向性,但其临床应用往往受到很多未知因素的影响,如长期生物毒性和体内代谢.基于这些担忧,应优先从合成材料所需的元素、溶剂和配体方面进行调控,开发高效、稳定、安全的新型手性纳米材料.此外,手性纳米材料的临床试验迫在眉睫.随着生物技术的发展,研究者致力于解析不同纳米药物的生物机制.然而,与人体相关的基因组学、蛋白质组学及代谢组学等高通量技术研究却很匮乏.将这些技术与手性纳米医学相结合,深度解析其相关性,可以加速手性纳米医学向临床医学的转化,推动手性纳米技术的发展.
尽管存在上述挑战,但在生物学和医学的许多领域,手性纳米材料相对于其它非手性纳米材料的优势非常显著.生物分子对手性无机纳米材料的不同偏好以及不同响应为其生物应用提供了广阔的机会和光明的前景.通过更好地理解手性纳米材料的性质以及新的合成方法,可以大规模生产具有特定性质的手性纳米材料,使其在一系列科学领域发挥前沿作用.

