金贝口服液制备过程中指标成分黄芪甲苷的传递研究
张爱均,严嘉伟,丁 琳,陶 凯,张良棕,孟兆青
(1.山东宏济堂制药集团股份有限公司,山东 济南 250100;2.山东省中医药治疗呼吸系统疾病技术创新中心,山东 济南 250100;
3
.山东中医药大学附属医院,山东 济南 250014)
金贝口服液由黄芪、北沙参等12味中药组成,具有益气养阴、祛瘀化痰的作用,主要用于特发性肺纤维化属气阴两虚兼痰瘀交阻证,症见气短、乏力、喘促、咳嗽、胸痛、紫绀等。该制剂来源于山东中医药大学附属医院陶凯主任医师的经验方,临床以汤剂给药效果明显。黄芪为本制剂处方君药,主要含有多糖、黄酮类化合物及三萜皂苷[1],其中黄芪甲苷(黄芪皂苷Ⅳ)为黄芪的主要活性成分,具有抗炎、抗肝纤维化、抗氧化、抗哮喘、降血糖、免疫调节和心肌保护等多重功效[2],是本制剂内控质量标准的指标成分。
本研究以金贝口服液君药黄芪中黄芪甲苷为指标,对制备过程各工序中黄芪甲苷的传递情况进行考察,得到影响黄芪甲苷传递的主要工艺和因素,获得了科学合理的制备工艺和控制参数,保证了金贝口服液质量的均一性。
1 仪器与试药
1.1 仪器
高效液相色谱仪(Waters,e2695),超高效液相色谱仪(安捷伦,UHPLC-1290),电热恒温水浴锅(上海树立仪器仪表,DFD-700),型号十万分之一电子天平(Mettler-toledo公司,XS105),十功能自动煎药机(北京东华原医疗设备有限公司,YJD20D-GL),旋转蒸发仪(郑州长城科工贸有限公,R-1020),循环水式多用真空泵(郑州长城科工贸有限公司,SHB-Ⅲ),恒温磁力搅拌器(德国IKA,RET basic),pH计[梅特勒-托利多仪器(上海)有限公司,FiveEasy Plus],灌装机(山东青州市精诚医药装备制造有限公司,ZG-30A),压力蒸汽灭菌器(山东博科生物产业有限公司,BKQ-B100II)。
1.2 试药
黄芪甲苷(中国食品药品检定研究院,批号110781-201717,含量96.9%),色谱乙腈(德国Merck公司,批号JA097830),色谱甲醇(德国OMNI公司,批号190150329M22),其他试剂均为分析纯。金贝口服液为中试产品(批号1912001、1912002、1912003)。
2 方法
2.1 金贝口服液的制备流程图及取样点
见图1。
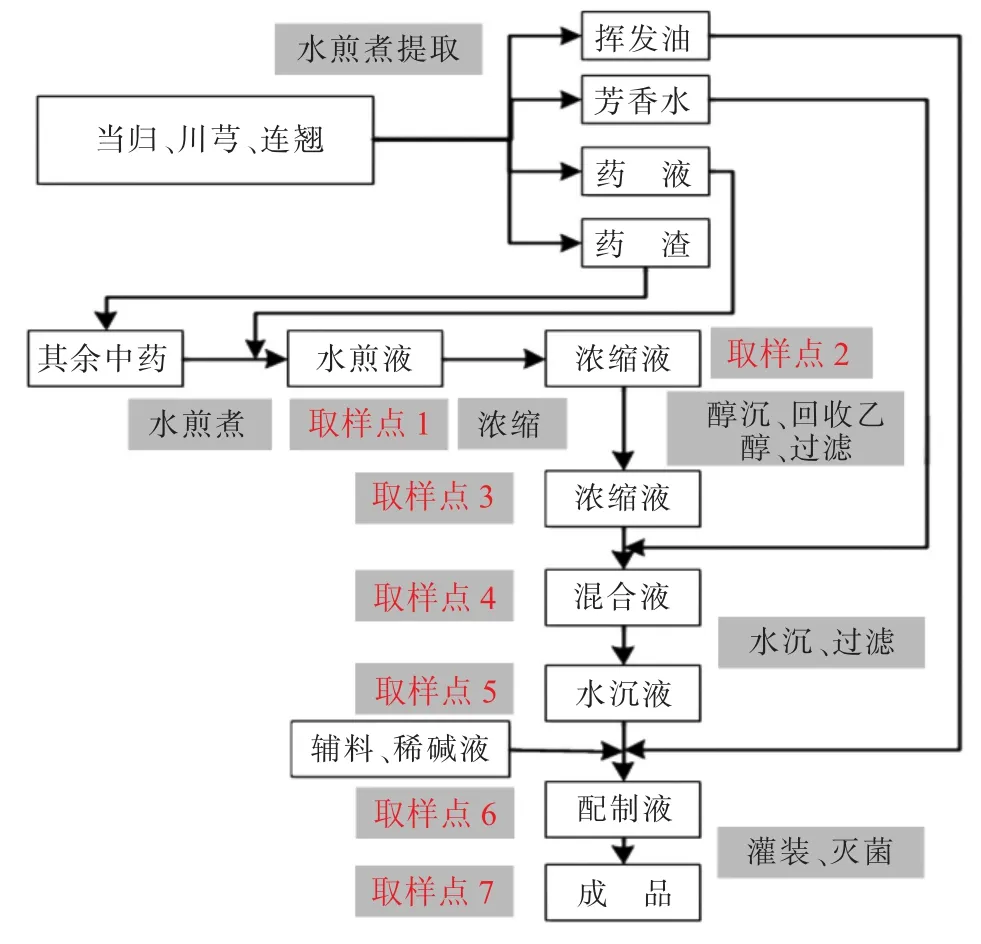
图1 金贝口服液制备流程
2.2 样品的制备、色谱条件及黄芪甲苷含量测定方法学研究
2.2.1 样品制备
对照品溶液的制备:称取黄芪甲苷对照品适量,精密称定,加甲醇使溶解,配制成质量浓度为0.5612mg/mL的对照品溶液,备用。
黄芪甲苷含量测定供试品溶液的制备:精密量取各取样点溶液(相当于成品20 mL,折合中药饮片14.24 g,折合黄芪1.32 g),用水饱和正丁醇提取3次,每次30 mL,合并正丁醇提取液,用1%氢氧化钠洗涤两次,每次30 mL,弃去氢氧化钠液,再用正丁醇饱和的水30 mL洗涤1次,弃去水液,正丁醇提取液蒸干,残渣加甲醇溶解,定量转移至2 mL量瓶中,加甲醇至刻度,摇匀,滤过,续滤液作为供试品溶液。
指纹图谱研究供试品溶液的制备:精密量取金贝口服液20mL,置具塞锥形瓶中,精密加入50%色谱甲醇60mL,称定质量,超声(300W,40kHz)处理30min,放至室温,补重,摇匀,滤过,取续滤液,即得。
黄芪饮片供试品溶液的制备:参照《中国药典》2020年版黄芪中供试品制备的方法[3]。
2.2.2 色谱条件及方法学研究
2.2.2.1 色谱条件
Agilent Eclipse Plus C18(5μm,4.6mm×250mm)色谱柱,流动相为乙腈-水(34∶66),流速1.0 mL/min,柱温25℃,进样量10μL,蒸发光检测器,气体流速25 psi,漂移管温度60℃,增益值2。
Agilent InfinityLab Poroshell 120 SB-C18(2.1mm×150 mm,2.7μm)色谱柱,柱温25℃;流动相为乙腈(A)-0.2%磷酸水溶液(B),梯度洗脱64 min,流速0.2 mL/min,进样量1μL,检测波长254 nm。见表1。

表1 金贝口服液制备指纹图谱流动相线性梯度表
2.2.2.2 方法学考察
线性范围考察:精密称取黄芪甲苷对照品适量,加甲醇分别制成每1 mL含0.968 50 mg、0.484 30 mg、0.193 70 mg、0.096 85 mg、0.038 74 mg、0.019 37 mg的对照品溶液,取10μL进样,如法测定,以峰面积对数值对黄芪甲苷进样量的对数值进行线性回归。
专属性试验:按照处方的比例和制备工艺,制备不含黄芪的金贝口服液阴性对照样品,再按供试品溶液的制法制成阴性对照。吸取供试品溶液、阴性对照溶液、黄芪甲苷对照品溶液和空白溶剂(甲醇),依法测定。
重复性试验:精密量取已知含量的成品(批号1912001)6份,每份20 mL,按供试品溶液制备方法制备供试品溶液,测定黄芪甲苷的含量,计算相对标准偏差(RSD)。
稳定性试验:精密量取已知含量的成品(批号1912001)20 mL,按供试品溶液制备方法制备,分别于配制后0、3、6、8、16、20、24 h测定黄芪甲苷的含量,计算RSD。
准确度试验:精密量取已知含量的成品(批号1912001)10 mL,按1∶1比例精密加入黄芪甲苷对照品,照供试品制备方法制成供试品溶液并测定黄芪甲苷的含量,以回收率计算黄芪甲苷平均回收率。
2.3 各取样点样品中黄芪甲苷含量测定
吸取各取样点溶液,依照同供试品溶液制法配制供试品溶液,计算黄芪甲苷转移率。
2.4 乙醇沉淀(醇沉)工艺的优化
醇沉时,加乙醇速度、搅拌速度、醇沉温度对成分转移率有较大影响,因此分别对各因素进行参数优化。
2.4.1 加乙醇速度和搅拌速度的优化
取同一批次金贝口服液浓缩液18份,分6组,每组3份平行样品。1、2、3组控制加乙醇速度,分别为50 mL/s、150 mL/s、250 mL/s,搅拌速度300 r/min,醇沉温度2℃,醇沉时间24 h;4、5、6组控制变量搅拌速度,分别设定为300 r/min、600 r/min、900 r/min,醇沉温度2℃,醇沉时间24 h,加醇速度50 mL/s。如法取样,测定黄芪甲苷的含量,计算转移率。
2.4.2 醇沉温度的优化
取同一批次金贝口服液浓缩液12份,分4组,每组平行3份,边搅拌边加入乙醇至醇浓度为65%,分别使药液降至不同温度(0℃、2℃、4℃、6℃),静置24 h,滤过,得滤液。如法取样,测定黄芪甲苷的含量,计算转移率。
2.5 灭菌前pH值的优化
取9份同一批次金贝口服液水沉液,分成3组,每组平行3份,分别按处方量加入辅料后用8%氢氧化钠水溶液调酸碱度,pH值分别调至5.70、6.00、6.70,分别灌装,于105℃环境灭菌30 min。灭菌前后分别如法取样测定,同时测定灭菌前后pH值变化。
2.6 灭菌温度和灭菌时间的优化[4]
中药制剂生产中灭菌条件选择不仅需要考虑微生物杀灭效果,还需要从整体上考虑灭菌对化学成分的影响。取同一批次金贝口服液灌装后灭菌前样品9份(灌装前pH值调至6.00),分别以不同条件进行灭菌操作。以黄芪甲苷转移率、超高效液相色谱(UPLC)指纹图谱、澄清度以及微生物限度为评价指标,考察不同灭菌条件对金贝口服液的指标成分转移率、化学成分、微生物及澄清度的影响。
鉴于口服制剂工业生产中灭菌温度一般选择为115℃、110℃、105℃三个温度点,灭菌时间一般为15 min、20 min、30 min,故本次研究共进行了三个温度点不同灭菌时间的考察。
2.7 不同灭菌条件的优化
灭菌前后分别取一定体积的样品(相当于成品20 mL,折合生药材14.24 g,折合黄芪药材1.32 g),按2.2.1项下样品制备方法及2.2.2.1项下色谱条件分别进行黄芪甲苷含量测定,并计算灭菌后成品中黄芪甲苷相对于灭菌前配制液的转移率。按2.2.1项下指纹图谱样品制备方法及2.2.2.1项下指纹图谱色谱条件分别进行指纹图谱测定。
3 结果
3.1 方法学考察
3.1.1 线性范围考察
以所测得黄芪甲苷色谱峰面积对数值和黄芪甲苷进样量的对数值进行线性回归,计算得回归方程Y=0.6324X-3.3055,相关系数r=0.999 9。结果见图2。
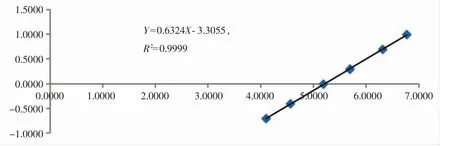
图2 金贝口服液黄芪甲苷含量标准曲线
3.1.2 专属性试验
空白溶剂和阴性对照溶液在黄芪甲苷色谱峰位置处未见吸收峰。结果见图3。

图3 黄芪甲苷含量检测专属性图谱
3.1.3 重复性试验
6份供试品中黄芪甲苷含量RSD为1.76%。结果见表2。

表2 不同供试品黄芪甲苷含量检测重复性试验结果
3.1.4 稳定性试验
供试品溶液分别于配制后0、3、6、8、16、20、24 h黄芪甲苷含量RSD为2.59%。结果见表3。

表3 不同时间点黄芪甲苷含量检测稳定性试验结果
3.1.5 准确度试验
供试品中黄芪甲苷平均回收率为92.59%。结果见表4。
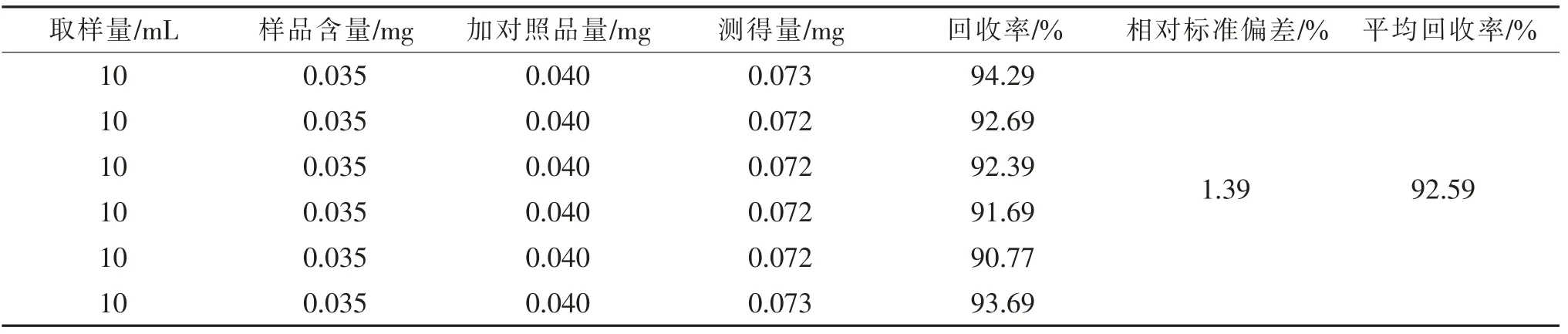
表4 黄芪甲苷回收率测定结果
3.2 各取样点样品中黄芪甲苷含量测定
计算各取样点溶液中黄芪甲苷的转移率。结果见表5、表6、图4。

图4 金贝口服液制备过程中黄芪甲苷转移率变化曲线
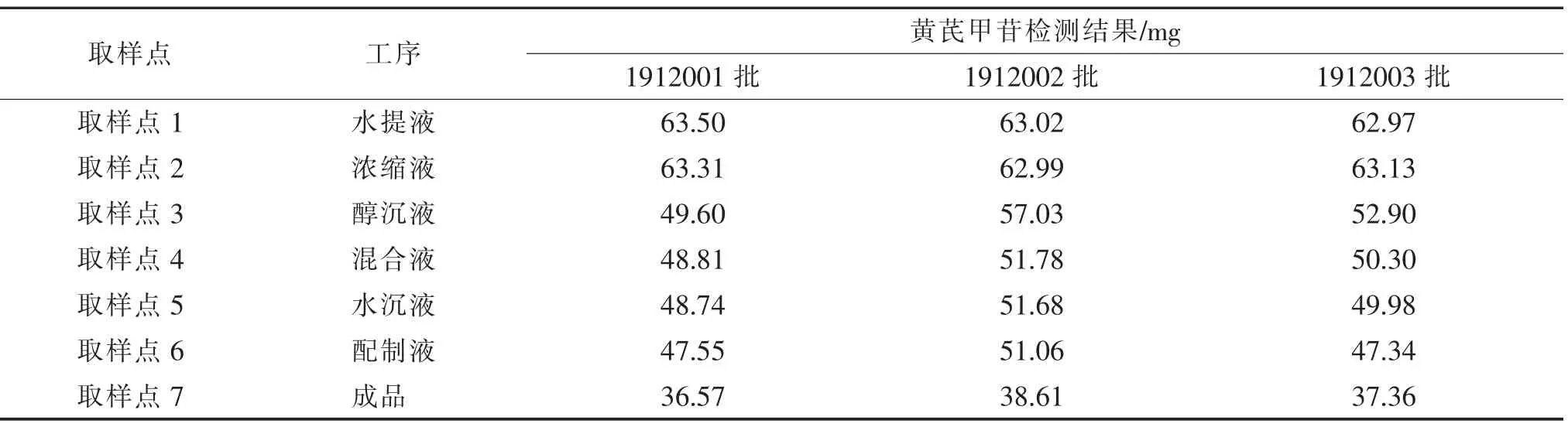
表5 各取样点黄芪甲苷检测结果
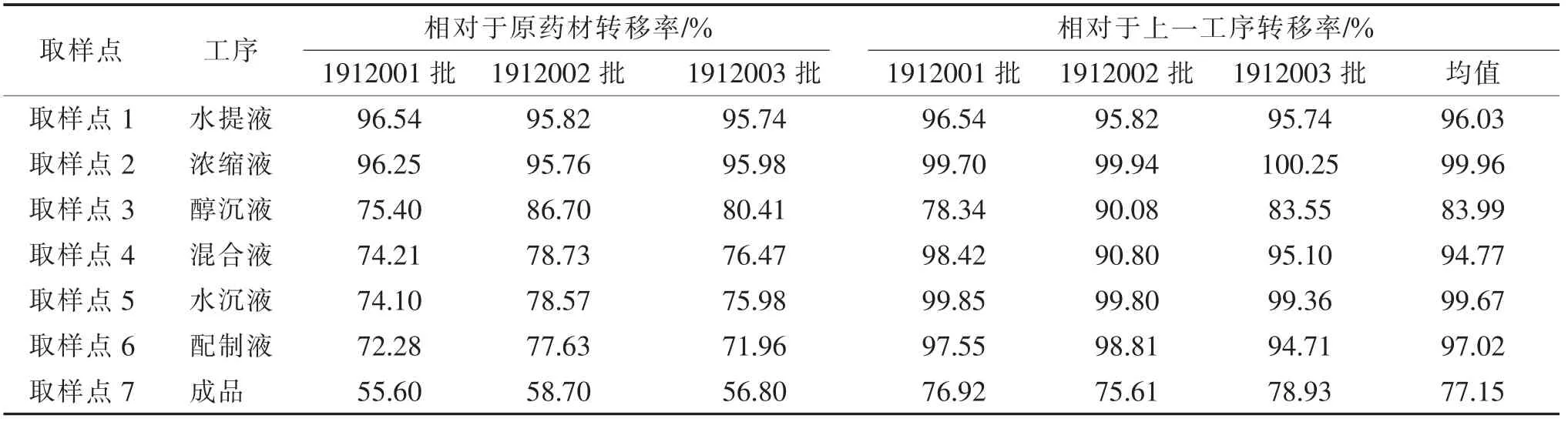
表6 黄芪甲苷转移率计算结果
3.3 乙醇沉淀工艺的优化
3.3.1 加乙醇速度和搅拌速度的优化
各样品溶液中黄芪甲苷的转移率,见表7。

表7 不同加醇方式下金贝口服液醇沉液中黄芪甲苷的转移率比较
3.3.2 醇沉温度的优化
各样品溶液中黄芪甲苷的转移率,见表8。

表8 不同醇沉温度下金贝口服液中黄芪甲苷转移率比较
3.4 灭菌前pH值的优化
各样品溶液pH值、黄芪甲苷含量及转移率,见表9。
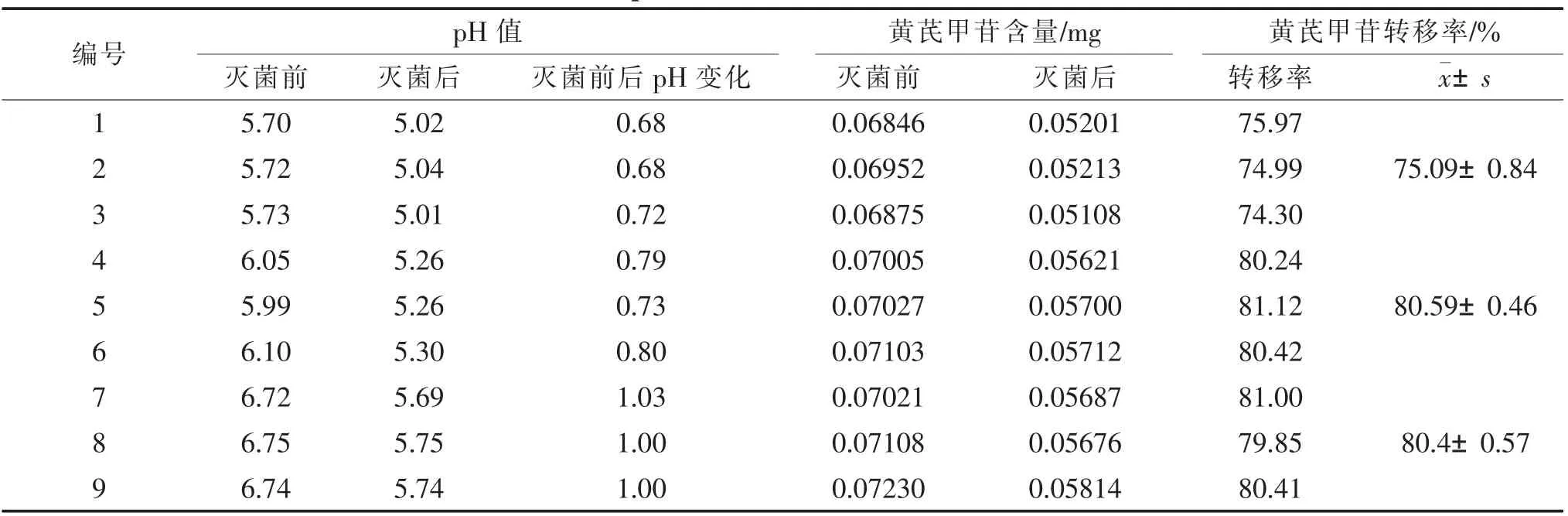
表9 不同配制液pH值下金贝口服液中黄芪甲苷转移率比较
3.5 灭菌温度和灭菌时间的优化
各供试品黄芪甲苷含量测定及转移率见表10。指纹图谱见图5,相似度分析结果见表11。

表11 金贝口服液不同灭菌条件下黄芪甲苷含量的相似度分析
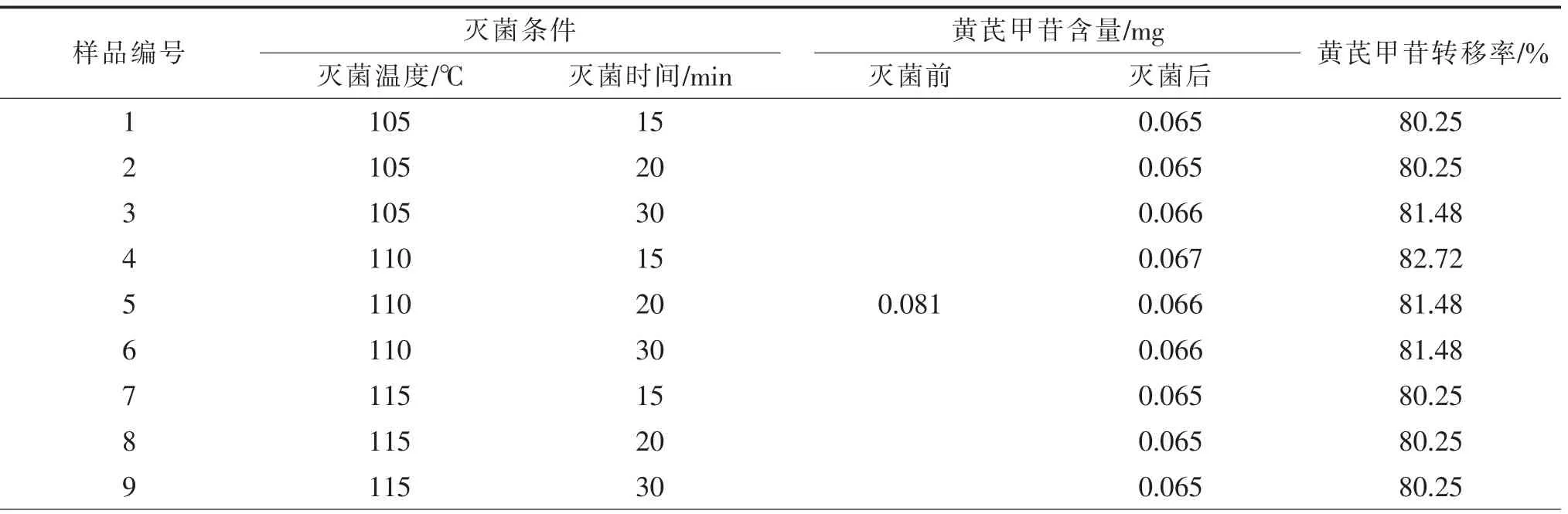
表10 不同灭菌条件下金贝口服液中黄芪甲苷转移率比较
4 讨论
本次研究对供试品溶液的制备及检测方法进行了方法学考察,研究结果显示,黄芪甲苷进样量在0.1937~9.6850μg内具有良好的线性关系,专属性、重复性良好,供试品溶液在24 h内稳定,方法准确。
醇沉工序相对前工序黄芪甲苷转移率为78.34%~90.08%,平均转移率为83.99%;灭菌工序相对前工序黄芪甲苷转移率为75.61%~78.93%,平均转移率为77.15%;其余工序黄芪甲苷相对前一工序转移率均大于90%,说明本制剂制备中影响黄芪甲苷量质传递的关键工序是醇沉和灭菌工序,优化醇沉及灭菌参数是稳定黄芪甲苷转移率的关键工序。
不同的加乙醇速度和搅拌速度均对醇沉工序相对上一工序黄芪甲苷转移率具有显著影响。研究结果显示加乙醇速度50 mL/s、搅拌速度600 r/min时,可以达到较为理想的醇沉效果。不同醇沉温度条件下,静置24 h,黄芪甲苷转移率在4℃、6℃条件下较0℃和2℃条件下稍低,考虑到产品质量、醇沉效果、能耗等因素,确定醇沉温度控制在(2±1)℃。故金贝口服液醇沉工序参数是乙醇加速度50 mL/s、搅拌速度600 r/min、乙醇沉淀温度(2±1)℃。
随着配制液pH升高,黄芪甲苷转移率逐渐升高;当pH上升至5.99后,黄芪甲苷转移率基本平缓。黄芪皂苷主要有黄芪皂苷Ⅰ~Ⅶ、乙酰黄芪皂苷Ⅰ、异黄芪皂苷Ⅰ~Ⅳ等,其中黄芪皂苷Ⅳ又称为黄芪甲苷,随着药液pH升高,黄芪皂苷Ⅰ~Ⅱ等皂苷成分可发生酯水解反应转化为黄芪甲苷[5-7]。故在配制液pH值调节过程中,可能存在部分黄芪皂苷Ⅰ及其衍生物转化为黄芪甲苷,考虑到皂苷成分转化和生产可操作性,建议金贝口服液配制液最佳pH范围为6.00±0.05。黄芪甲苷转移率研究结果显示,不同灭菌条件对黄芪甲苷转移率影响并不明显,说明黄芪甲苷在一定温度条件下具有一定的稳定性;指纹图谱研究结果显示,不同灭菌条件下的指纹图谱无指纹峰丢失,与对照指纹图谱相比,相似度均大于0.996,说明9个灭菌条件下样品整体化学成分一致性均较好,且灭菌前后成分种类基本无变化,灭菌对金贝口服液整体化学成分影响并不显著。因此从化学成分、灭菌效果以及澄清度等因素整体考虑,确定金贝口服液灭菌前配制液pH值为6.00±0.05、灭菌温度为105℃、灭菌时间为30 min。
本研究证实了金贝口服液制备过程中黄芪甲苷含量变化呈整体下降趋势,以黄芪甲苷在金贝口服液制备过程中的传递为依据,表明醇沉、灭菌工序是制备中的关键环节。
本研究对金贝口服液醇沉工序进行了参数优化,结果显示温度低时,黄芪甲苷和鞣质、蛋白质等杂质溶解度及转移率降低,但杂质去除率较高;反之,除杂效果较差。研究过程发现醇沉静置期间温度越高,沉淀物越松软,上清液越难以过滤,所得过滤液越少,黄芪甲苷转移率越低。搅拌速度过快和快搅时间过长,形成的絮体细小,沉降或过滤困难,除增大絮体和药液分离的难度以外,还会造成已经被絮凝剂高分子吸附的脱附,大絮体被强剪切力撕裂成小絮体,絮凝后药液浊度上升,所以在保证絮凝高分子和药液快速混合均匀的条件下,快搅速度尽量小,快搅时间尽量短[8]。另醇沉前浸膏的组成和性质也可能因原药材产地、气候、采集时间等差异而存在质量波动,关于这些潜在质控风险因素对醇沉效果的影响程度还有待一步研究。
本研究以黄芪甲苷转移率、灭菌效果、指纹图谱、澄清度等为考察指标对灭菌前配制液pH范围、灭菌温度、灭菌时间等进行了研究,结果表明配制液最适宜酸碱度是6.00±0.05,在该pH范围内既可以保证黄芪甲苷转移率,又可以满足金贝口服液质量标准要求。通过对不同灭菌温度和灭菌时间的考察,未发现二者对金贝口服液化学成分有明显影响,但对澄清度和微生物限度有一定的影响:灭菌温度越高,时间越长,澄清度越差,微生物限度恰与之相反。为保证制剂质量,应全面考虑灭菌温度和时间参数,本制剂最适宜灭菌温度为105℃,灭菌时间30 min。
中药成分的复杂性决定了单味中药材就是一个复方制剂,金贝口服液由12味中药组成,其成分复杂性可想而知。本次研究是以主要有效成分黄芪甲苷为指标考察金贝口服液制备过程中成分的传递,从而对金贝口服液进行关键参数优化。虽然优化后的制备工艺可以保证黄芪甲苷有较为理想的转移率,但并不能完全说明本次研究所优化参数为最佳参数,与药效相关联的、更深入的工艺优化研究与金贝口服液物质基础及体内作用物质研究有待进一步开展。在新药研究及产品全生命周期内均应持续进行关键工艺及关键参数的优化研究。

