儿童中枢性尿崩症在朗格汉斯细胞组织细胞增生症中的临床特点及预后
熊婷,杨玉,吴崇军,杨利,徐忠金,张东光,吴主强,叶瑶
(南昌大学附属儿童医院江西省儿童医院1.内分泌遗传代谢科;2.血液科;3.影像中心,南昌 330000)
朗格汉斯细胞组织细胞增生症(Langerhans Cell Histiocytosis,LCH)是一种罕见的克隆性疾病,其特征在于具有CD1a和CD207阳性未成熟树突状细胞表型的细胞增殖[1]。LCH是儿童中最常见的组织细胞疾病,最近,LCH被定义为一种由错误引导的骨髓分化引起的疾病[2],并且中国LCH患儿的临床特征具有高度异质性,高达60%的病例存在MAPK通路突变[3]。 本病可能侵及骨骼、皮肤、淋巴结或实质器官,如肝、脾、骨髓,并且本质上分为单病灶损害和多病灶损害,出现典型皮疹、溶骨性损害、肝脾及淋巴结肿大、外耳道流脓、肝功能损害、血细胞减少等。多病灶LCH分为两种类型:单系统多病灶(SS-m)和多系统(MS)。按风险器官(RO)受累(高(RO+)或低(RO-)风险组)进行分层,在LCH-III试验中,RO-MS-LCH和RO+MSLCH患儿的五年生存率分别提高到99%和84%[3]。我们前期的研究也显示改良LCH-Ⅲ方案对LCH的治疗化疗结束反应率为84.21%,效果理想[4]。但是,仍有部分患儿出现复发,尤其部分LCH会带来各种永久性损害,从而导致生活质量的长期损害。其中中枢性尿崩症(CDI)是在LCH患者中观察到的最常见的中枢神经系统(CNS)相关永久后果,且被认为是神经退行性中枢神经系统疾病(NDCNS)的不可逆和危险因素[1]。因此如何早期判别、预防及治疗合并CDI的LCH患者是提高LCH患儿治疗效果及生存质量的关键。
1 资料和方法
1.1 病例来源 回顾2016年10月至2021年10月在江西省儿童医院就诊,并经病理检查确诊的LCH合并中枢性尿崩症8例,其中3例在外院诊断及治疗。分析患者的临床资料,包括一般情况、症状和体征、影像学表现、病理诊断、治疗方案和随访结果。
1.2 诊断LCH诊断主要依据于病理诊断;CDI是根据临床特征(多饮、多尿),禁水试验和脑部MRI表现综合诊断的[1]。将在LCH诊断前发生的CDI定义为CDI之前,将在LCH诊断后发生的CDI和开始治疗后的CDI定义为CDI之后。
1.3 化疗方案 采用LCH III方案/SCMC-LCH-2018方案进行化疗,分别在6周、12周、26周及52周化疗后进行评估[5]。
1.4 疗效评估 根据脏器损害情况,分为好转、中间反应和加重。其中好转(better)包括完全缓解(CR)和消退,即无活动病变(NAD)和活动病变,好转(AD better)。中间反应(intermediate)包括混合型(mixed)和稳定型(stable),即有的病变消退,但有新的病变出现/不变。加重(worse)即进展(progression),单个脏器骨受累患者,进展定义为出现新的骨病变或新的病变累及骨以外器官。
2 结果
2.1 一般资料8例患儿中,男性5例,女性3例;中位年龄为3岁11月、6岁7月(1岁8月~14岁3月),所有患儿都经病理诊断确诊为LCH。其中ID3、ID7、ID8在外院诊断及治疗,仅在本院复查;ID1、ID2、ID4、ID5全程在本院治疗;ID6系第一次因发热、皮疹诊断LCH,经治疗后缓解,后停药1年后出现头部包块,考虑复发,在外院给予化疗后停药3年,出现多饮、多尿,结合垂体MRI,考虑尿崩症。其中3例中枢性尿崩症出现在LCH诊断之前,3例同时诊断,2例系在诊断LCH后3年出现。
2.2 治疗情况 在本院治疗的病例中,ID1、ID2、ID4、ID5四例在治疗初始阶段均按多系统高危组方案执行,根据尿崩出现的时间,给予醋酸去氨加压素口服;其中ID1、ID2、ID4病例采取LCH III方案(VP-MTX-6-MP),ID5采用的是SCMC-LCH-2018方案(VP-Ara-C-6-MP)进行化疗。期间根据当时条件和家属医院,ID1、ID2、和ID5完善BRAF V600E基 因 检 测,ID2 BRAF V600E基 因 检 测 阴性,ID1和ID5基因检测阳性;ID5在治疗6周后处于中间反应状态,给予加用达菲拉尼口服。ID3、ID7、ID8系在外院诊断及治疗,其中ID3目前在给予二线化疗方案,ID7和ID8治疗方案不详;ID6给予醋酸去氨加压素口服后较前尿崩症状较前好转,后至上海儿童医学中心就诊,建议内分泌科随诊,未予化疗。
2.3 评估、预后及随访 随访最长4年,3例失访,3例已经结束化疗,2例化疗中,5例随访患儿均在口服醋酸去氨加压素。ID1在给予LCH III方案化疗后,目前已经停止化疗1年余,随访至今,考虑好转,处于CR,未给予靶向药物治疗,醋酸去氨加压素在减量中;ID2已经停止化疗,目前好转,疾病处于消退状态;该患儿在治疗之初,反复出现电解质紊乱,目前多饮、多尿症状较前改善,电解质稳定,口服醋酸去氨加压素中;ID4目前处于维持化疗阶段,患儿在初始治疗6周处于中间反应状态,给予达拉非尼口服,多饮多尿症状改善,口服醋酸去氨加压素中。ID5目前仍在化疗中。ID6给予醋酸去氨加压素口服后尿崩较前好转,未予化疗。ID3、ID7、ID8失访。
3 讨论
LCH是以单核-巨噬细胞系统中朗格汉斯细胞(Langerhans cell,LC)克隆性增殖为特征的疾病,于1865年由Smith首次发现并报道,1953年Lichtenstein提出将其命名为组织细胞增生症,直到1987年国际组织细胞协会才将其更名为LCH[6]。目前诊断依据2009年国际组织细胞协会分布的LCH评估与治疗的新版指南[7],本组病例都是基于病理结果诊断。该病临床罕见,好发于儿童,儿童发病率为2~10/10万,男性多于女性[8]。在本组8例患儿中,男性5例,女性3例,与既往报道相符[9]。本组病例中位年龄为3岁11月、6岁7月,提示该病可发生在任何年龄阶段,但该病发病高峰年龄为1~4岁[10]。
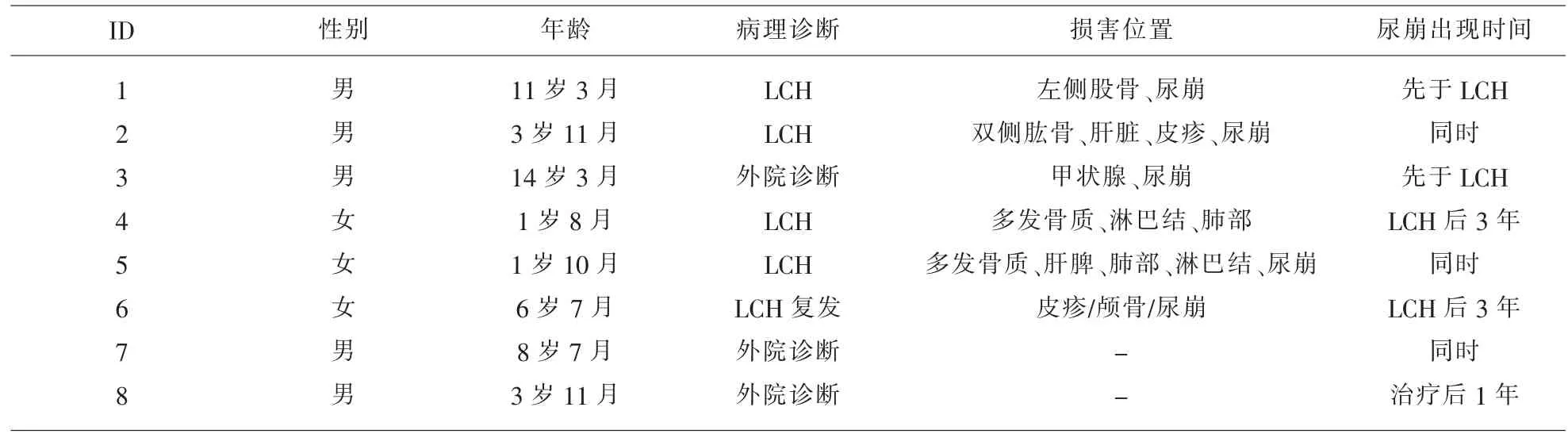
表1 8例LCH合并尿崩症患儿一般资料
LCH致病机制尚不明确,目前主要有炎症反应性假说和肿瘤增生性假说,因BRAF V600E基因支持该病为髓源性组织细胞肿瘤样增生性疾病,因此更倾向于肿瘤增生性病变[11]。在本组中ID1、ID2、和ID5完 善BRAF V600E基 因 检 测,ID2 BRAF V600E基因检测阴性,ID1和ID5基因检测阳性。在儿童LCH BRAF V600E基因阳性率方面,黄俊彬等[12]报道的阳性率为33.3%,曹静等[13]报道的阳性率为59.2%,左华楚等[14]报道阳性率为11.36%,冯楚础报道的阳性率为70.3%[15],各家报道阳性率不同,可能受样本保存条件及检测方法的影响,但所选对象大部分为多系统受累且高危险度。
LCH临床表现多样,发展过程常难以预测,轻者仅累及皮肤及骨骼,重者累及多器官(肝、脾、造血系统等)并造成重要脏器功能损害[16],其中CNS受累范围为,下丘脑-垂体轴受累伴尿崩症、头颅骨损害伴团块影、脑实质团块影以及脑桥、小脑脚、脑白质受累的神经退行性疾病[17]。国内外均有LCH相关的报道,但以尿崩症为首发表现,且累及骨、肺、皮肤及垂体等多个器官的病例报道较少见,该类型起初临床表现单一,仅表现为多饮多尿,易误诊为单纯性尿崩症。在一组145例患儿中,共有11例(11/145,7.6%)存在中枢神经系统受累[16],但仅2.8%患儿初诊时出现垂体受累。本组3例中枢性尿崩症出现在LCH诊断之前,3例同时诊断。3例在LCH诊断之前存在尿崩症的患儿在给予醋酸去氨加压素治疗后控制不佳,这些提示中枢性尿崩症可能是LCH早期唯一表现。
章亚威等[16]将LCH患儿中存在垂体受累者按年龄分组,≤1岁组未出现垂体受累病例,1~3岁组有1例患儿出现垂体受累,≥4岁者有3例患儿出现垂体受累,三组差异无统计学意义。本组病例年龄区间为1岁8月~14岁3月,支持垂体是否受累与发病年龄无关。Haupt等[18]将颅面骨定义为CNS风险部位,但穹窿病变除外,并建议这些部位的LCH病变有发展CDI和ND-CNS的风险。本组病例中ID4、ID6均系在颅骨损害之后出现尿崩症,进一步支持颅骨的LCH病变有发展CDI的风险。同时我们发现在LCH后出现尿崩症患儿均系复发病例,进一步说明疾病复发有发展CDI的风险。要减少或预防CDI后的发展,更有效的LCH治疗以使患者保持稳定的无复发状态至关重要,同时化疗开始后中枢神经系统危险部位复发的患者发生CDI后的发生率显着增加[1]。 在LCH患者中观察到的最常见的中枢神经系统(CNS)相关永久后果是中枢性尿崩症(CDI)[1]。ID1、ID2、ID4在给予化疗后尿崩症状均有不同程度改善,与章亚威[16]的数据相符,9例尿崩症均予以口服去氨加压素治疗,症状控制尚可。国内也有报道垂体LCH患者在规律化疗后,停用去氨加压素,症状控制尚可[19]。但邵明玮[8]的3例患者在经过放疗和化疗后,尿崩症状均未获得改善,可能需要长期激素替代治疗。
多系统LCH多以化疗为主,其中LCH-III方案应用最为广泛[9]。本组4例在本院治疗病例中有3例采用的是LCH III方案(VP-MTX-6-MP)。对于存在BRAF基因突变的难治性LCH患儿,应用BRAF基因突变抑制药成为有效治疗方案又一选择。本组ID5采用的是SCMC-LCH-2018方案(VP-Ara-C-6-MP)进行化疗,在治疗6周后处于中间反应状态,给予加用达菲拉尼口服,目前在维持治疗中,效果有待进一步观察。CDI损伤不可逆,因此CDI不是系统治疗的指针,活动期才需系统治疗[11]。本组ID6系第一次因发热、皮疹诊断LCH,经治疗后缓解,后停药1年后出现头部包块,考虑复发,给予化疗后停药3年,出现多饮、多尿,结合垂体MRI,考虑尿崩症,未予化疗,仅给予醋酸去氨加压素口服后较前好转。
综上所述,在LCH患者中观察到的最常见的CNS相关永久损害是CDI,垂体是否受累与发病年龄无关,CDI发生率低,可发生在LCH诊断前,也可发生在治疗后,且CDI可以是LCH早期唯一表现,疾病复发和颅骨损害有发展CDI的风险,预后有待长期随访。

