高静压协同酶法制备交联多孔淀粉及其性质研究
张甜甜,侯梦醒,刘培玲
(内蒙古工业大学化工学院 呼和浩特 010000)
天然来源的淀粉材料具有安全性强、生物可降解等特性,然而,溶解性较差、易回生、吸附能力弱、黏度很高及热不稳定等缺点,使天然淀粉的应用受到很大的限制[1]。对淀粉进行改性可以改善淀粉的性能,拓展淀粉的应用[2]。多孔淀粉(porous starch)是指用物理、化学或生物方法处理淀粉形成的一种具有孔道结构的变性淀粉[3]。其颗粒呈现多孔状,从表面到中心均有丰富的微孔,相比于原淀粉,具有更高的孔隙率和比表面积,较低的颗粒密度和堆积密度,良好的吸附性能等性能[4]。多孔淀粉可有效防止被包埋物质自氧化,一些对温度、光和氧不稳定的物质可被多孔淀粉保护。其也可作为微胶囊芯材、吸附载体和包埋剂等[5]。
目前多孔淀粉的制备方法主要有物理法、化学法、酶解法及复合法[6]。这些方法中,酶解方法因高效的催化能力和温和的反应条件而被广泛应用于制备多孔淀粉,研究表明:不同的酶催化效果不同,同时使用α-淀粉酶和糖化酶进行反应制备效果较好[7-8]。然而,单一的制备方法存在各自的缺陷,复合法成为目前多孔淀粉制备的主要方式,即先进行物理或化学前处理,后通过复合酶水解制备多孔淀粉。物理或化学处理后的淀粉更易被酶水解,其结构也较稳定[9]。OLIYAEI 等[10]在酶水解前用湿热预处理的方法制备小麦多孔淀粉,结果表明经重复湿热预处理得到的多孔淀粉吸附能力、比表面积和总孔容积均得到显著提高。吴丽荣等[11]和MAHSA 等[12]研究表明超声可以提高α-淀粉酶和淀粉葡萄糖苷酶的催化效率,提高多孔淀粉的制备效果。
高静压(high hydrostatic pressure,HHP)技术属于物理变性技术,具有安全性、经济性高和稳定性强等独特优势。其作用机理为淀粉分子与水分子在高压作用下的水合作用使淀粉的颗粒结构发生变化,并由此导致淀粉性质发生改变,达到改性的目的[13]。Herman 等[14],Liu 等[15]和Li 等[16]发现HHP 在一定程度上使淀粉特征性质发生变化,如破坏淀粉颗粒表面,改变结晶度和糊化性质等。交联可使颗粒表面机械性和结构稳定性增加。徐正康等[17]研究表明低中等交联度的变性淀粉可以满足中高温制备多孔淀粉的要求。利用三偏磷酸钠(sodium trimetaphosphate,STMP)交联,可在保证颗粒稳定性的基础上,使颗粒多孔增加,从而提高吸附率[18]。
本研究以玉米淀粉为原料,通过对高压多孔淀粉与高压交联多孔淀粉的分析,研究制备高压交联多孔淀粉的工艺参数,并对其性质进行研究,为多孔淀粉在食品加工中的应用提供参考。
1 材料与方法
1.1 试验材料
1.1.1 材料与试剂 玉米淀粉,沽源县盛邦农业有限责任公司。三偏磷酸钠,上海精纯试剂有限公司;糖化酶,北京酷来搏科技有限公司;α-淀粉酶,北京索莱宝科技有限公司;氯化钠、氢氧化钠、盐酸、磷酸钠缓冲液干粉、溴化钾均为分析纯级,天津永晟精细化工有限公司。
1.1.2 仪器与设备 ALB-224 分析天平,赛多利斯科学仪器有限公司;S-3400N 扫描电子显微镜,日本厥场制作所;Quarasorb-SI3030606 比表面积与孔径分析仪,贝士德仪器科技(北京)有限公司;XRD-6000X 射线衍射仪,上海实验仪器有限公司;ETIR-33FTIR 光谱仪,上海美谱达仪器有限公司;XRD-6000X 射线光电子能谱分析仪,日本理学株式会社;HHP-750 高静压设备,包头科发高压技术有限公司;TDL-5-A 离心机,上海安亭器有限公司;ALB-224 数显恒温水浴锅,金坛市江南仪器厂;101A-2 鼓风干燥箱,上海实验仪器有限公司;SHA-B 恒温震荡仪,江苏常州国华有限公司;SHB-B95 循环水真空泵,郑州长城科工贸有限公司;DHT 恒温电热套,上海帅登仪器有限公司。
1.2 试验方法
1.2.1 多孔淀粉的制备
1)高压多孔淀粉制备 准确称取20 g 玉米淀粉,加入磷酸钠缓冲溶液配成20%的玉米淀粉乳液,装入聚乙烯袋中,抽真空塑封,用高静压分别在0,100,200,300,400 MPa 下压制30 min。将制备的玉米淀粉乳装入烧杯中,在50 ℃恒温水浴中预热10 min,加入α-淀粉酶与糖化酶比例为4∶1的复合酶,添加量为淀粉基的2.0%。反应4 h 后,加入4%的NaOH 使酶失活。离心、抽滤,用去离子水洗涤3 次后在鼓风干燥箱干燥18 h,研磨,过100 目筛,制得高压多孔淀粉[19]。
2)高压交联多孔淀粉制备 称取5 g 高压多孔淀粉与去离子水配制成20%的淀粉乳,在烧杯中放入NaOH(淀粉基的2%)和NaCl(淀粉基的6%),用磁力搅拌器搅拌,使其溶解。40 ℃水浴中加热1 h,使其碱化。加入三偏磷酸钠(淀粉基的3%)交联剂后,在不同温度下用恒温振荡仪140 r/min 反应3 h,然后,加入适量的盐酸,调节pH 为中性。抽滤,洗涤3 次。在恒温干燥箱内干燥18 h,研磨,过100 目筛,制得高压交联多孔淀粉[20-21]。
1.2.2 多孔淀粉颗粒形貌的测定 将导电胶粘于扫描电子显微镜的载物台上,粘取少量样品,放入离子溅射镀金仪中真空喷金20 min 后观察,加速电压为20 kV[22]。
1.2.3 多孔淀粉比表面积与孔径的测定 采用全自动物理吸附设备对样品的比表面积和孔径进行分析。将样品置于样品管中经105 ℃、2 h 的真空脱气脱水,然后,将样品管放入盛有液氮的样品台中通入氮气,以氮气为吸附气体。比表面积可由BET 方程(Brunauer Emmett Teller)计算得出,样品的孔径、孔体积由BJH 法(Barrett Joyner Halenda)分析得出[23-24]。

式中,V——平衡压力为P 时,吸附氮气的总体积,L;Vm——样品表面覆盖第1 层满时所需氮气的体积,L;P——氮气在吸附温度下平衡时的压力,Pa;Ps——饱和蒸汽压力,Pa;C——吸附常数。
1.2.4 多孔淀粉X 射线衍射 取0.5 g 淀粉样品置于模具的圆形螺纹处,用光滑的玻璃片压平。对淀粉样品用X-射线衍射仪测试,扫描范围5°~40°,步长0.02°,扫描速度2°/min。样品的相对结晶度用MDI-Jade 6.0 软件计算得出[25]。
1.2.5 多孔淀粉红外光谱扫描 将淀粉样品与KBr 在105 ℃的鼓风干燥箱中干燥至恒重,消除样品中水分子对红外吸收峰的干扰。淀粉样品与KBr 按1∶100 的比例混合,研磨成细粉,在5 MPa的压力下压成圆形透明片。以KBr 为背景,在4 000~400 cm-1范围内记录光谱。用OMNIC 8.0软件计算吸光度比,1 047/1 022 cm-1,表征淀粉的短程有序度,1 022/995 cm-1表示淀粉无定型区域的结构变化。
1.2.6 多孔淀粉X 射线光电子能谱测定 使用单色化的AlKα 射线(能量1 486.6 eV))作为激发源,真空度5×10-9Pa,发射电压15 kV,发射功率150 W。采用的全谱和窄谱扫描通能分别为160 eV 和40 eV,其步长分别为1 eV 和0.1 eV。用XPS Peak 4.1 软件进行数据处理。
1.2.7 吸油率与吸水率的测定
1)吸油率测定 准确称取2.0000 g 样品于烧杯中,加入5 mL 葵花籽油,室温下用恒温电热套搅拌30 min,将搅拌后的样品置已知质量的砂芯漏斗中,用循环水真空泵抽滤直至没有油滴滴下。记录砂芯漏斗与样品的质量,计算吸油率A。每组样品测定3 次,取平均值。

式中,A——吸油率,%;B——样品质量,g;C——砂芯漏斗的质量,g;D——漏斗与样品的质量,g。
2)吸水率测定 准确称取2.0000 g 样品于烧杯中,加入5 mL 去离子水,在室温下用恒温电热套搅拌30 min。将搅拌后的样品置已知质量的砂芯漏斗中,用循环水真空泵抽滤直至没有水滴滴下。记录砂芯漏斗与样品的质量,计算吸水率A。每组样品测量3 次,取平均值。
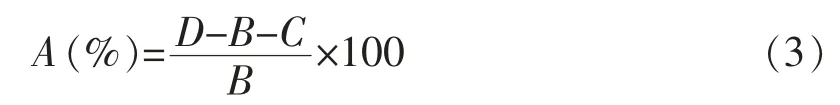
式中,A——吸油率,%;B——样品质量,g;C——砂芯漏斗的质量,g;D——漏斗与样品的质量,g。
1.2.8 透光率的测定 称取适量的样品加入去离子水,配成1%的淀粉溶液,在水浴锅中沸水加热搅拌15 min,同时保持溶液体积不变,结束反应后将样品冷却至室温,去离子水为空白溶液,用紫外-可见分光光度计在波长620 nm 处测定淀粉糊的吸光度,计算透光率[26]。每组样品测定3 次,取平均值。
1.2.9 冻融稳定性的测定 准确称取1.5000 g 样品,与25 mL 去离子水配成6%的淀粉乳,在85℃水浴锅中水浴5 min,取出冷却至室温。在离心管(质量为M0)中加入一定质量的淀粉糊(M1),冷冻(约-2 ℃)24 h。解冻后在离心机中4 000 r/min离心15 min,称量离心管与沉淀物的质量M2,沉淀物的质量记为M3。样品析水率记为W[27]。每组样品测量3 次,取平均值。
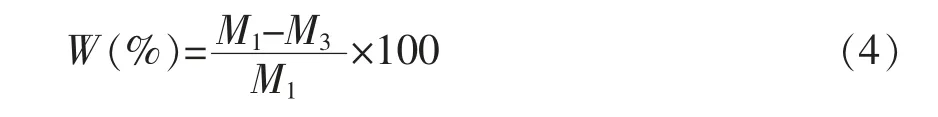
式中,M1——离心管中的淀粉糊质量,g,M1=M-M0;M3——管内沉淀物的质量,g,M3=M2-M0。
1.2.10 溶解度和膨胀度的测定 称取0.5000 g样品放于已知质量的离心管中。加入10 mL 去离子水,在80 ℃水浴锅中水浴30 min,反应过程中不断摇晃。反应结束后冷却到室温,3 000 r/min 离心5 min,将上清液倒入预先称量过的培养皿中,并立即称量沉淀物。记录沉淀物与离心管的质量,上清液置于已知质量的培养皿中,用60 ℃的鼓风干燥箱干燥24 h 后立即称其质量[28]。每组样品测定3 次,取平均值。计算样品的溶解度(S),膨胀度(B)。

式中,M1——离心管的质量,g;M2——沉淀物与离心管的质 量,g;M3——培养皿的质量,g;M4——干燥后上清液的质量,g。
1.2.11 高压交联多孔淀粉最佳工艺的确定
1.2.1 1.1 单因素实验
1)反应温度对多孔淀粉交联度的影响 固定压强200 MPa,反应pH 10,反应时间4 h,探讨反应温度对交联度的影响。
2)pH 值对多孔淀粉交联度的影响 固定压强200 MPa,反应温度40 ℃,反应时间4 h,探讨pH 值对交联度的影响。
3)三偏磷酸钠用量对多孔淀粉交联度的影响
固定压强200 MPa,反应pH 10,反应温度40℃,反应时间4 h,探讨三偏磷酸钠用量对交联度的影响。
4)压力强度对多孔淀粉交联度的影响 固定反应pH 10,反应温度40 ℃,反应时间4 h,选择压力强度分别为0,100,200,300,400 MPa,考察压力强度对交联度的影响。
1.2.1 1.2 正交试验 根据单因素实验结果,固定反应时间4 h。选取反应温度(A)、反应pH(B)、三偏磷酸钠用量(C)、反应压强(D)4 个因素,用spss软件设计L9(34)正交试验,以沉降积为指标,确定最佳试验条件。
1.2.12 多孔淀粉交联度的测定 通过测定多孔淀粉的沉降积来间接表示交联度,交联度与沉降积呈负相关。交联度越大,沉降积越小;反之,交联度越小,沉降积越大[29]。
称取0.5000 g 高压交联多孔淀粉,与25 mL蒸馏水搅拌均匀,放入恒温水浴锅中,85 ℃保温2 min,冷却至室温。将所得糊液在4 000 r/min 离心5 min,准确记录上清液体积,用下式计算其沉降积[30]。每组试验重复3 次。

式中,V——上清液的体积,mL;Vs——沉降积,mL。
2 结果与讨论
2.1 多孔淀粉颗粒SEM 扫描分析
原玉米淀粉颗粒呈多面体形,表面不光滑,有凹陷和通向颗粒中心的细孔[31]。经过酶解和交联而未进行高压处理的淀粉颗粒(A1、B1)的表面形成孔道结构,孔径较小。经100 MPa 压强处理的淀粉颗粒(A2、B2)表面几乎看不到孔道结构,可能是因为此压力对淀粉颗粒表面有紧致作用。200 MPa 时淀粉颗粒(A3、B3)表面孔道结构增多,孔径变大;300 MPa 时高压多孔淀粉(A4)颗粒表面的孔径无明显变化,而高压交联多孔淀粉(B4)表面出现沟壑,孔径增大;400 MPa 时淀粉颗粒(A5、B5)的孔径明显增大,孔与孔相连在一起,部分淀粉颗粒出现塌陷现象。高压交联多孔淀粉与高压多孔淀粉相比,孔道孔径更大。

图1 多孔淀粉的扫描电镜照片Fig.1 Electron microscopy of porous starch
2.2 多孔淀粉比表面积与孔径的分析
由表1 可看出,在压强作用下高压多孔淀粉和高压交联多孔淀粉的平均孔径与孔体积均呈现先下降后升高的趋势,且在相同压强下,高压交联多孔淀粉的孔体积均大于高压多孔淀粉,说明交联反应可以增加多孔淀粉的孔体积。天然玉米淀粉的比表面积较小,约0.339 m2/g,经高静压处理的高压多孔淀粉的比表面积变大,呈先升高后降低的趋势,当压强200 MPa 时多孔淀粉的比表面积最大,高压交联多孔淀粉与高压多孔淀粉有同样的趋势,只是高压交联多孔淀粉的比表面积比多孔淀粉大。一方面可能是由于交联反应作用在淀粉颗粒的表面,使孔道的直径变大,另一方面可能是交联反应在淀粉颗粒间发生团聚现象。
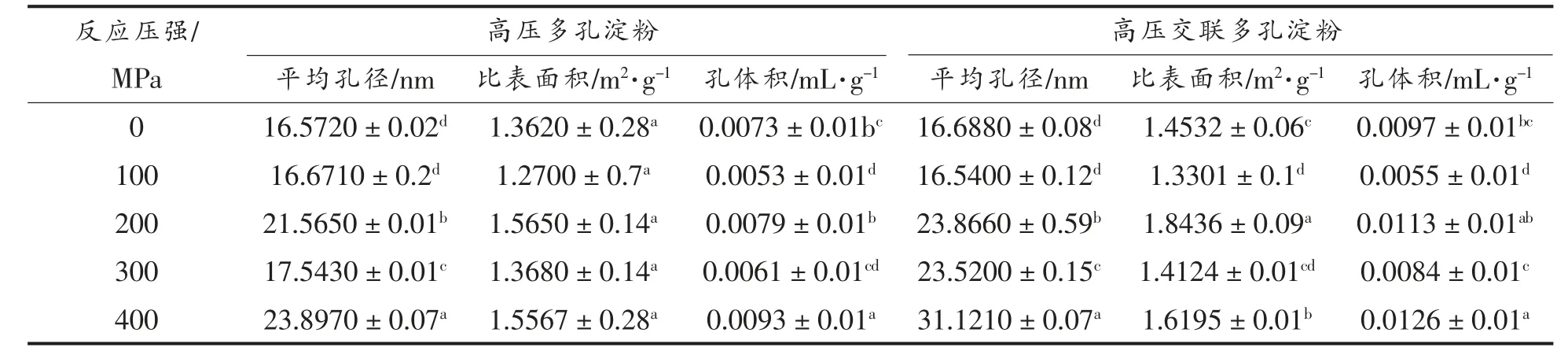
表1 多孔淀粉比表面积与孔径测定结果Table 1 Determination of specific surface area and pore size of porous starch
2.3 多孔淀粉X 射线衍射分析
由图2 可知,高压多孔淀粉和高压交联多孔淀粉的特征峰均没有发生变化,说明它们的晶型未发生变化,是典型的A 型淀粉。2θ 在17.1,18.2处的双峰峰强度有变化,表现出很高的结晶度,说明高压可能使淀粉晶体结构发生变化,交联反应也影响淀粉颗粒的晶体结构。通过MDI Jade 软件进行相对结晶度的计算[32]。由表2 可知,高压交联多孔淀粉的相对结晶度均低于高压多孔淀粉,说明高压交联多孔淀粉具有疏松的内部孔道结构,更利于吸收及吸附。
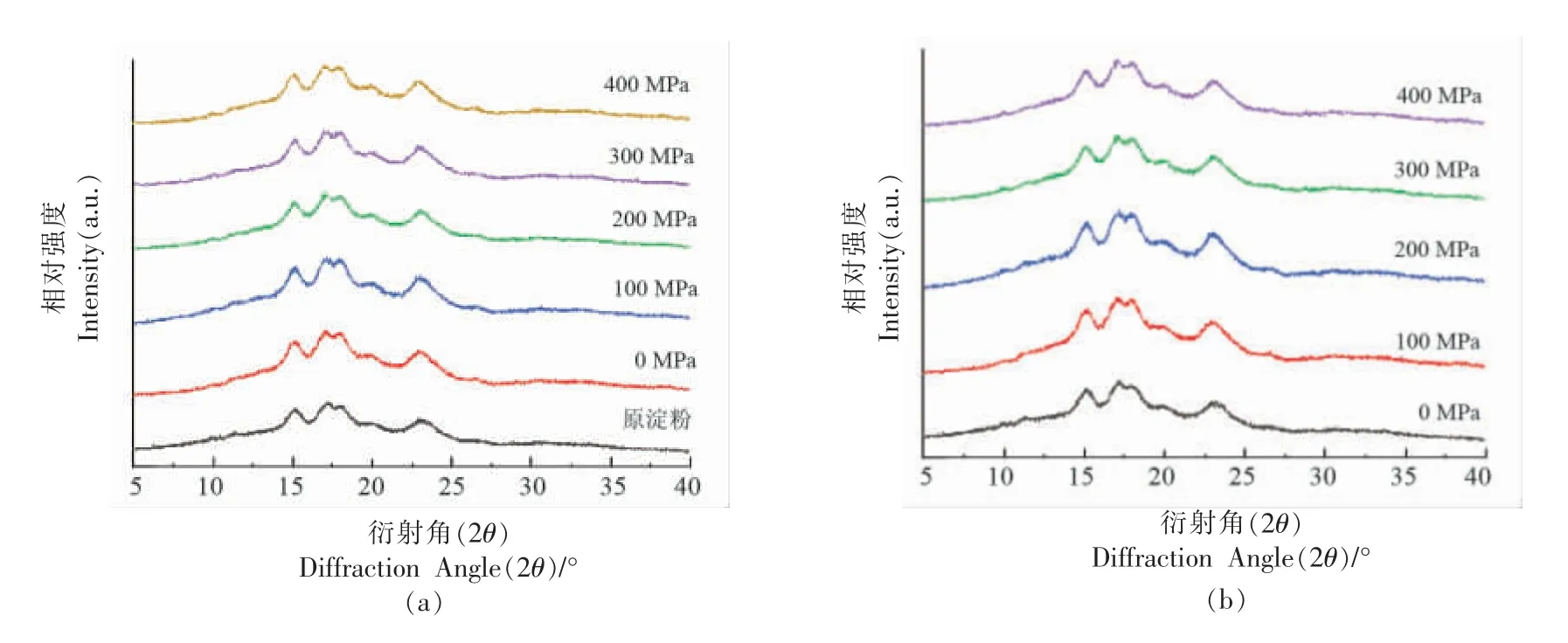
图2 多孔淀粉的XRD 图谱(a:高压多孔淀粉;b:高压交联多孔淀粉)Fig.2 XRD patterns of porous starch(a:high pressure porous starch;b:high pressure cross-linked porous starch)
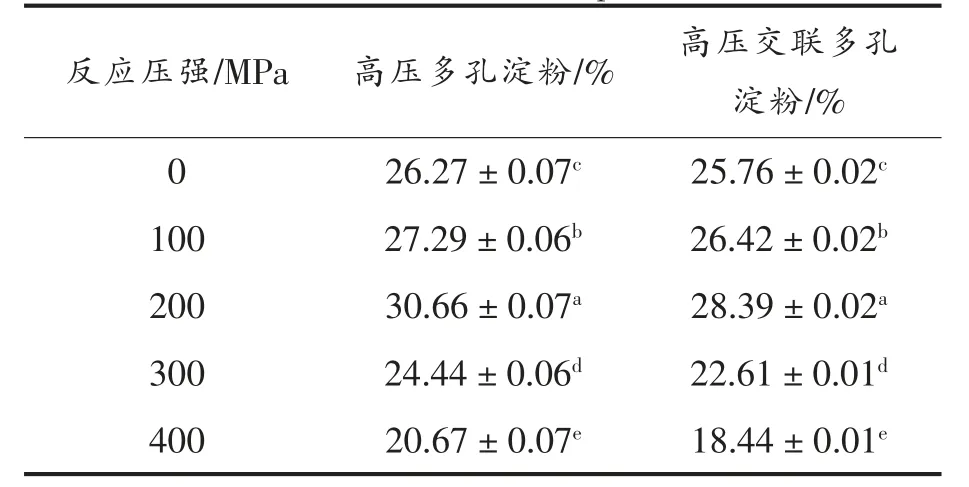
表2 不同压力下多孔淀粉的相对结晶度Table 2 Relative crystallinity of cross-linked porous starch under different pressures
2.4 多孔淀粉红外光谱扫描分析
图3 的红外光谱中,3 400 cm-1处的特征峰对应O-H 的伸缩振动,1 248 cm-1处的特征峰对应O-H 的弯曲振动,1 365~1 413 cm-1区域的吸收带是由C-H 弯曲振动引起的,2 945 cm-1处的吸收带是由于C-H 的伸缩振动,1 242 cm-1处是P=O的特征吸收,1 025 cm-1处是P-O-C 的特征吸收。可以看出高压多孔淀粉与高压交联多孔淀粉的红外光谱与原淀粉的大致相同,没有新的峰出现,说明均没有新的官能团生成。1 047 cm-1和1 022 cm-1附近的红外波段分别与淀粉的结晶区和非晶区有关,1 047 cm-1和1 022 cm-1处的吸光度比值通常用来表征淀粉的近程分子顺序[33]。交联改性后,多孔淀粉样品的有序结构值(1 047/1 022)略有降低,表明交联反应破坏了多孔淀粉样品的近程分子顺序,这与XRD 结果一致。

图3 多孔淀粉的FTIR 图谱Fig.3 FTIR profiles of porous starch
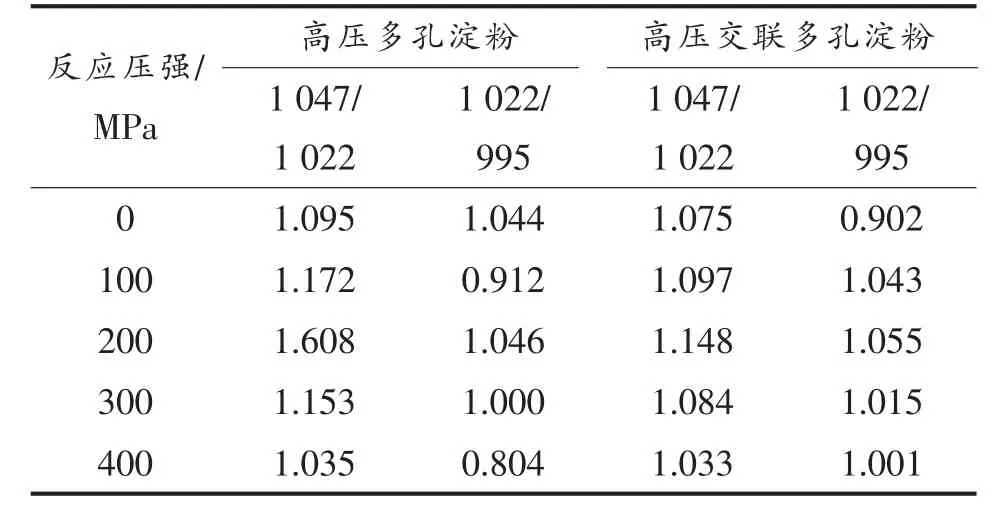
表3 不同压力下多孔淀粉的1 047/1 022,1 022/995 比值Table 3 Ratio of 1 047/1 022,1 022/995 of porous starch under different pressures
2.5 多孔淀粉的X 射线光电子能谱分析
图4 为经200 MPa 处理和3%交联剂优化的高压多孔淀粉和高压交联多孔淀粉的XPS 光谱,可以看出,碳和氧是淀粉的主要成分,峰分别出现在约286.3 eV 和532.8 eV 处。从图4B 可以看出,高压交联多孔淀粉在133.4 eV 处有新的峰,表明磷酸基团被引入改性淀粉样品中。从图4C 可以看出,高压多孔淀粉样品中C1s 在284.6eV 和286.0 eV 处有两个峰,分别与C-C/C-H 和C-O/C-O-C/C-OH 键有关[34]。然而,高压交联多孔淀粉中的C1s 在284.6,286.0,287.3 eV处有3个峰(图4D),在287.3 eV 处有1 个新峰,对应于化学状态为C-O-P 键。这些结果表明,磷酸基团通过共价键在高压交联多孔淀粉上与-OH 形成C-O-P,即发生交联反应。

图4 多孔淀粉的X 射线光电子能谱Fig.4 X-ray photoelectron spectroscopy of porous starch
2.6 吸油率与吸水率
吸油率和吸水率反映多孔淀粉对负载物的吸附能力。原淀粉的吸油率是39.33%。由图5 可看出高压和交联处理后淀粉的吸油率均提高了,交联后的多孔淀粉吸油率提高更多,在200 MPa 压强下两种淀粉的吸油率达到最大值。吸油率的变化可能与孔道结构、孔径、孔容积有关,交联反应因可以加强淀粉颗粒的力学性能而使其结构更加稳定,使高压交联多孔淀粉的吸油率更高[35]。

图5 多孔淀粉的吸油率Fig.5 Oil absorption rate of porous starch

图6 可看出,不同压强处理后,高压交联多孔淀粉的吸水率均高于高压多孔淀粉。这主要是因为交联反应是引入磷酸盐基团与淀粉颗粒中的羟基形成氢键,磷酸基团具有亲水性,使水分子更容易被吸收[36]。

图6 淀粉样品的吸水率Fig.6 Water absorption of starch sample
2.7 多孔淀粉最佳制备工艺
2.7.1 高压交联多孔淀粉制备的单因素实验 由图7 可看出,反应温度升高,高压交联多孔淀粉的沉降积呈先降低后升高的趋势,反应活化能增加,淀粉样品与三偏磷酸钠分子获得能量,增加活化分子的占比,使有效碰撞次数增多。其次,由于温度升高,单位时间内反应物分子碰撞次数增多,因此高压交联多孔淀粉的交联度随温度的升高而增大。反应温度继续升高,淀粉发生局部糊化,阻碍了交联反应的进行,交联度有所下降。40 ℃时沉降积达到最低值,高压交联多孔淀粉的交联度最大。随着反应pH 值的增加,反应物的沉降积呈先下降后升高的趋势。适度提高pH 值,可促进三偏磷酸钠中磷酸集团与淀粉发生交联反应,生成磷酸二脂键。pH 值的升高使淀粉颗粒的膨胀程度增大,三偏磷酸钠更易进入淀粉颗粒中扩散及反应。当pH 过大时,引起部分淀粉颗粒发生糊化反应,从而抑制交联反应。pH 11 时沉降积达到最小值,此时交联度达到最大值。随着压强的增加,沉降积呈先增加后降低的趋势,淀粉颗粒表面及结晶结构都受到破坏,团粒结构发生解体,冷水溶解度提高,与三偏磷酸钠中的磷酸基团相容性提高。同时,颗粒表面孔径变大,磷酸基团更易扩散到淀粉分子内部。压力超过200 MPa 后,高压使玉米淀粉分子链变短,淀粉分子运动速度加快,阻止了交联反应的发生。随着交联剂用量的增加,高压交联多孔淀粉的交联度呈逐渐增加并趋于稳定的趋势。主要原因是交联剂用量增加,增大了分子间的有效碰撞几率,促进反应的进行。而当交联剂增到一定值时,这种促进作用基本可以忽略。三偏磷酸钠用量为3%时,达到最佳反应效果。
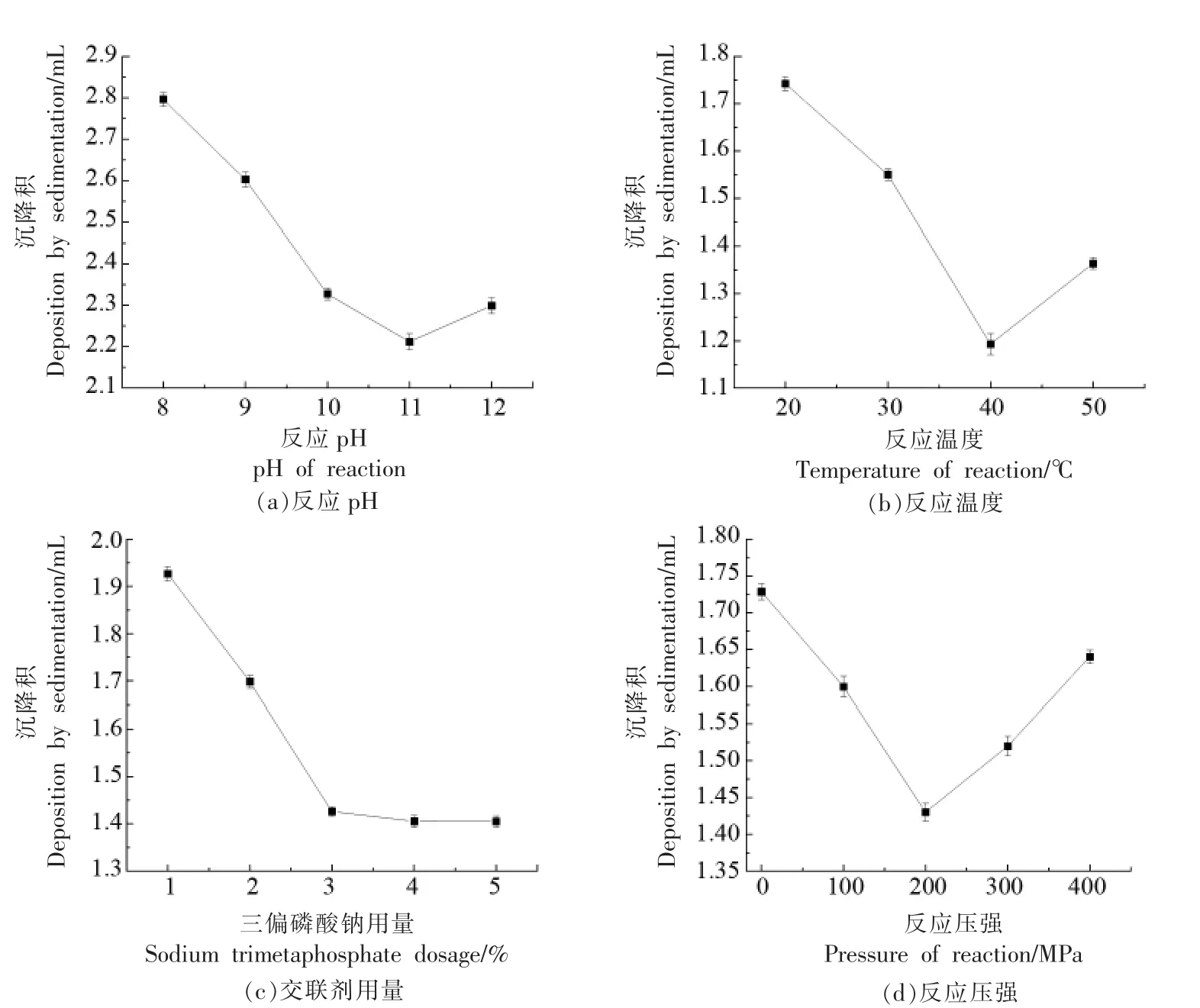
图7 单因素实验图Fig.7 Single factor test diagram
2.7.2 高压交联多孔淀粉正交试验 根据单因素实验结果,固定反应时间4 h。选取反应温度(A)、反应pH(B)、三偏磷酸钠用量(C)、反应压强(D)4个因素,用SPSS 软件设计L9(34)正交试验,以沉降积为指标,确定最佳试验条件。因素水平见表4,结果见表5。
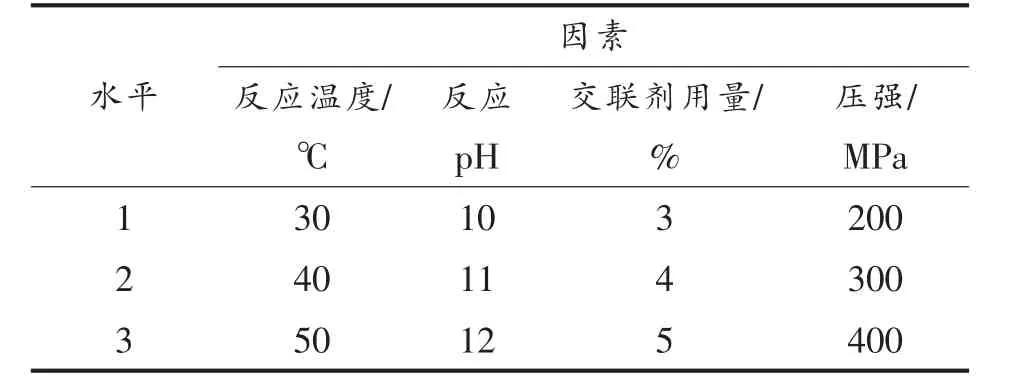
表4 高压交联多孔淀粉试验因素水平Table 4 factor and level about high pressure cross-linked porous starch experimental
由表5 中极差(R)可以看出:4 个因素对高压交联多孔淀粉交联度影响的主次因素排序为D>B>C>A,即反应压强>反应pH>反应温度>三偏磷酸钠用量。由均值(K)可以看出高压交联多孔淀粉的优水平是A2B2C1D1。最佳制备工艺为:反应温度40 ℃,反应pH 11,交联剂用量为淀粉基的3%,压强200 MPa。
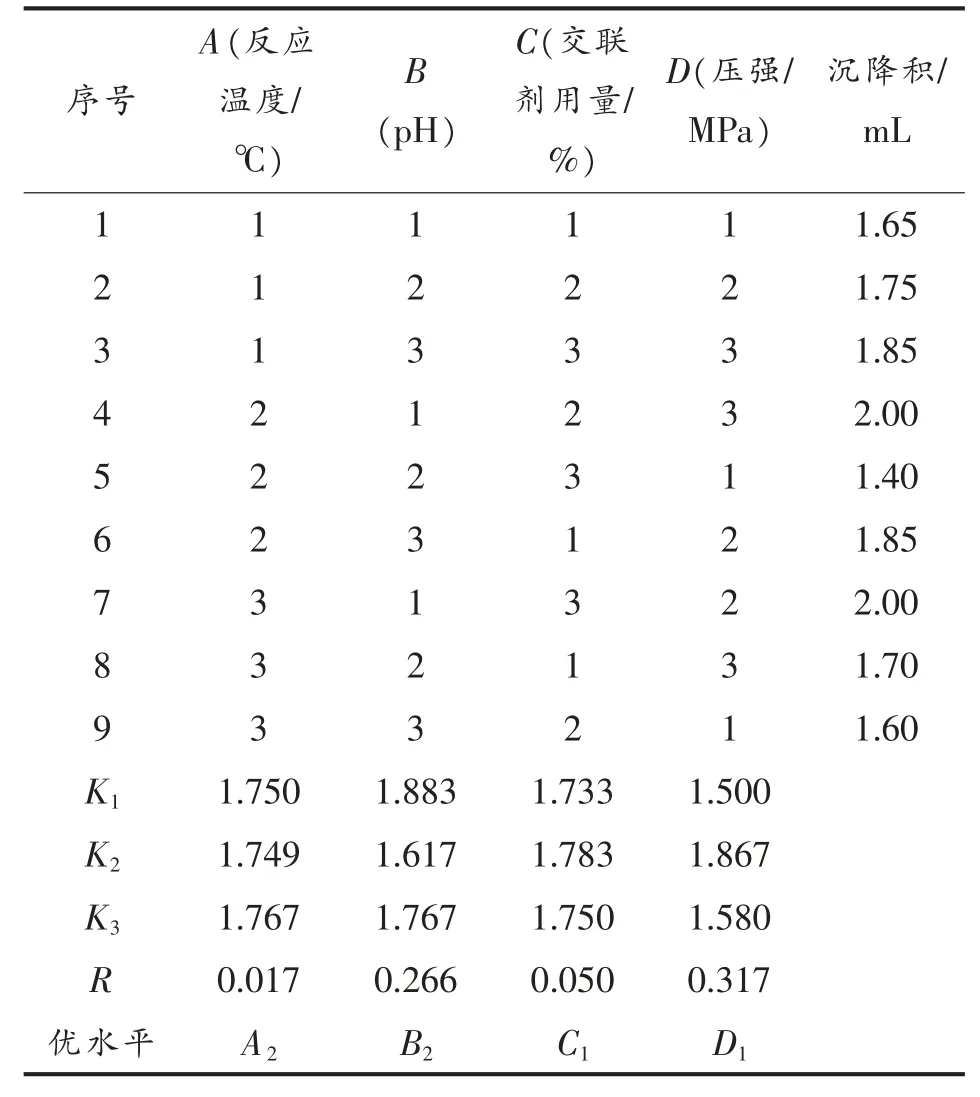
表5 正交试验设计与结果Table 5 Orthogonal test results
2.8 高压交联多孔淀粉的理化性质
高压多孔淀粉透光率较原淀粉增加了4.94%,而高压交联多孔淀粉的透光率有所下降。高压使淀粉的分子链变短,平均分子质量变小,羟基暴露的更多,更易形成均匀的水合体系,因此透明度升高,而交联反应会抑制淀粉颗粒的膨胀,使其结构更稳定,不容易形成水合体系,并且团聚使其平均分子质量增大,透光率降低[38]。冻融稳定性与析水率呈负相关,析水率越小,冻融稳定性越好。高压交联多孔淀粉与多孔淀粉和高压多孔淀粉相比具有较好的冻融稳定性,高压多孔淀粉的冻融稳定性最差。这主要是由于压强200 MPa 时淀粉颗粒更容易酶解,淀粉颗粒稳定性降低。而交联反应使分子间形成交联网状结构,增加了分子重排的难度,导致其分子结构更加牢固、稳定,从而使冻融稳定性提高。
与原淀粉相比,不同处理条件的多孔淀粉的溶解度和膨胀度均有增加。高压使淀粉分子的分子链变短,露出更多羟基,淀粉水溶性变强,而交联反应通过磷酸基团的附加共价键加强淀粉分子间的键合,使淀粉颗粒紧密结合在一起。此外,高压交联多孔淀粉的膨胀度明显低于多孔淀粉和高压多孔淀粉,表明淀粉分子间的交联反应加强了淀粉链间的结合,提高了淀粉颗粒的抗剪切力,从而抑制淀粉颗粒的膨胀。
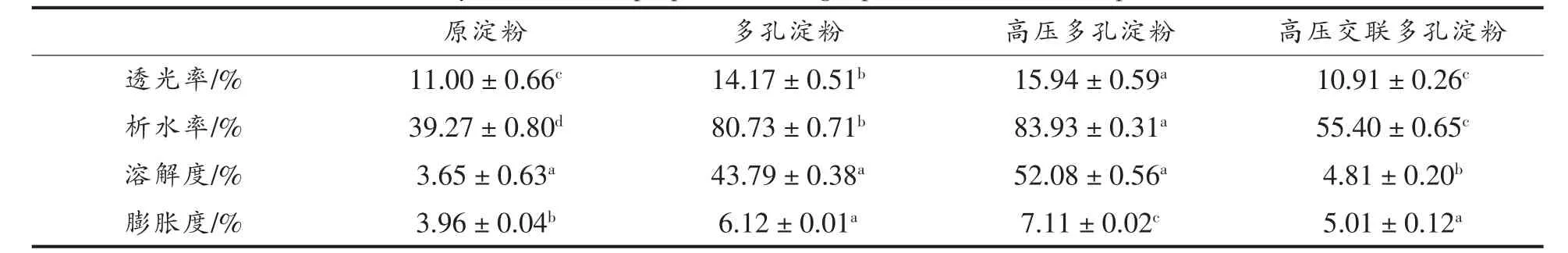
表6 高压交联多孔淀粉的理化性质Table 6 Physicochemical properties of high pressure crosslinked porous starch
3 结论
采用不同压强处理多孔淀粉,当压强200 MPa 时,高压多孔淀粉和高压交联多孔淀粉都表现出良好的多孔淀粉形态和性质。高压交联后的多孔淀粉颗粒的孔道结构也更均匀,比表面积、孔径均变大,形成结晶度降低的疏松结构,吸附性明显增加,吸油率及吸水率分别从68%和120%提高到75%和124%。
高压交联多孔淀粉的最佳制备条件是:反应温度40 ℃,反应pH 11,压强200 MPa,交联剂用量为淀粉基的3%。4 因素对高压交联多孔淀粉交联度影响的排序为反应压强>反应pH>反应温度>三偏磷酸钠用量。此工艺上制备的高压交联多孔淀粉透光率较多孔淀粉和高压多孔淀粉分别下降了3.26%和5.06%;析水率分别下降了24.7%和28.5%;不同处理条件下形成的多孔淀粉溶解度和膨胀度都较原淀粉明显提高,利于其的应用。

