衰弱评估工具在不同老年人群中的应用现状
陈雨朦,刘青青,钱媛
人口老龄化给老年人自身和家庭、卫生服务系统以及社会经济发展均带来诸多挑战,其中衰弱也是严重挑战之一,亟待解决[1]。研究显示,衰弱患者经历外界较小应激即更易发生跌倒、失能、谵妄、认知损害、急诊入院,甚至死亡等不良事件[2-3]。且衰弱患者自我健康报告水平低、主观幸福感低,生存质量受到严重影响[4]。确定衰弱人群是衰弱治疗和管理的第一步,目前国内外已开发出60余种衰弱评估工具,但对工具的选择国内外尚无统一标准[5],对衰弱的评估结果亦无法进行统一判断。本文对不同疾病、不同医疗环境老年人群衰弱评估进行梳理,帮助医护人员根据不同人群的特点和评估目的选择衰弱评估工具,以更好地预测不良健康结局,促进衰弱患者个性化的治疗和管理。
1 衰弱的概念
衰弱是因多系统储备能力下降导致机体易损性增加、抗应激能力减退和功能障碍增加的非特异性状态,与年龄增长密切相关[5],常由多种慢性疾病、某次急性事件或严重疾病引起[6]。虽然衰弱的概念在文献中不断演变,但有3个特点得到一致认可,首先,衰弱是多维度的,生理和心理社会因素在其发展中发挥作用;第二,尽管其患病率随着年龄的增长而增加,但衰弱是正常老化过程的极端后果;第三,衰弱是动态发展的,即个人的衰弱状态可在不同程度之间波动[7]。
2 常用的普适性衰弱评估工具
检索并综合国内外文献及相关指南共识提供的常用衰弱评估工具,见表1。
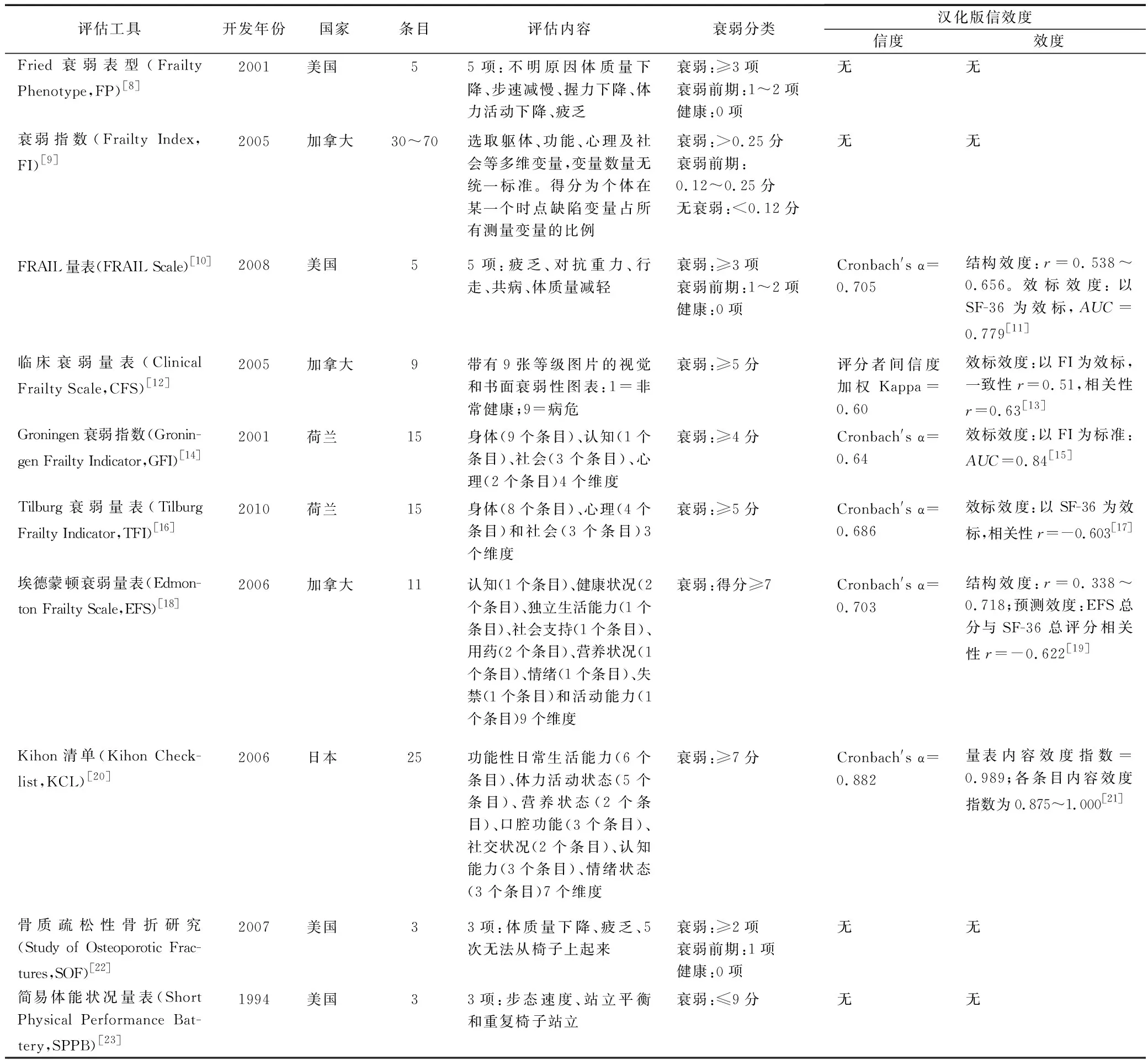
表1 常用的普适性衰弱评估工具
3 不同疾病患者衰弱评估工具应用现状
3.1心血管系统疾病 衰弱与心血管疾病存在多种关联机制,是预测心血管疾病不良结局的重要风险因子,通过评估衰弱可帮助确定心血管疾病中常用于诊断和治疗的多种医疗操作的适宜性,帮助制订个体化治疗方案,改善衰弱和患者结局[24]。2021年欧洲心脏病与衰弱专家共识推荐对≥70岁的急或慢性心血管疾病患者均须进行衰弱筛查和评估[24]。基于表型模型的FP[8]和基于累积缺陷模型的FI[9]是近年研究中应用最广泛的衰弱评估工具,但注重躯体衰弱的指标(如FP、SPPB和步速)等难以反映心力衰竭或病情复杂的老年心脑血管疾病患者的整体衰弱情况,且需要体能测试,在临床实践中比较耗时[25]。故欧洲心脏病学会、心力衰竭协会提出对此类患者建议采用多维度的评估方法如FI和老年综合评估(Comprehensive Geriatric Assessment,CGA)[25]。一项横断面研究采用CFS、FRAIL量表、FP、EFS以及FI对我国某三级医院心血管病房542例老年住院患者的衰弱情况进行了评价。结果显示,FI作为心血管衰弱评估工具灵敏度最高,CFS作为筛查工具灵敏度最高,故推荐CFS为首选筛查工具,FI为最佳评估工具[26]。由于目前尚无针对心血管疾病衰弱的最佳评估方法,故2019年HFA首次提出了心衰衰弱评分(HFA Frailty Score)模型,主要包括4个领域,即临床(共病、体质量减轻、跌倒)、身体功能(失能、平衡力下降、日常生活活动能力下降)、认知心理(认知障碍、痴呆、抑郁)和社会(独居、无社会支持),但目前该评分的具体细则及评分标准尚未公布[25]。
3.2慢性阻塞性肺疾病(Chronic Obstructive Pulmonary Disease,COPD) 据报道,COPD患者衰弱风险显著高于其他慢性疾病,其衰弱和衰弱前期发生率分别为20%和56%[27]。目前认为,炎性反应和肌肉功能障碍是COPD与衰弱的共同发病机制[28],而高龄、因食欲减退所致的营养不良、因气促及呼吸困难等原因引起的活动能力下降的共同作用促使COPD及衰弱的进一步发展[29],故尽早识别与管理COPD患者的衰弱状况尤为重要。常用的评估工具包括FP、FRAIL量表和FI等,均得到较好的验证及应用。Zhang等[30]使用FP、CFS、FI和SPPB评估了302例老年COPD患者的衰弱状态,结果显示这4种评估工具均与患者一年病死率相关,同时衰弱与病情急性加重(使用FFP)和住院(使用FFP、CFS和FI)有关,显示出中等的预测能力。然而以上均为普适性衰弱评估工具,尚未能与COPD特征相结合。杨婧[31]在2020年编制了针对COPD患者的衰弱评估量表,该量表由疾病症状、生理状态、健康信息、心理情绪及社会适应5个维度,共24个条目组成,量表的Cronbach′s α为0.742,重测信度为0.802,信效度较好。目前该量表应用尚未检索到,还有待更进一步探索。
3.3髋部骨折 髋部骨折是常见的老年脆性骨折,患者术后受到骨折与手术带来的双重创伤,机体维持稳态能力下降,脆弱性增加,易导致衰弱的发生。研究显示,老年股骨颈骨折患者手术前后衰弱的患病率显著高于一般老年人群(分别为41.6%和27.7%)[32]。衰弱增加了患者术后失能和并发症的患病率、病死率,延长了住院时间,是患者短期预后的独立危险因素。因此,早期识别和管理衰弱对制订临床治疗方案及术后并发症的风险预防均有重要意义。常用的髋部骨折衰弱评估工具包括衰弱指数FI、FP、FRAIL量表和CGA。其中CGA是确定衰弱程度的金标准,但它耗时且专业知识要求高,不适合常规临床实践[33]。FI可通过病历进行评估,能预测各种不良结局,但因项目繁多、用时较长,不适于快速评估[32]。FP和FRAIL量表在评估老年髋部骨折患者术前衰弱时一致性中等,但FP需评估患者在自然状态下的行走速度,故不适用于髋部脆性骨折患者的衰弱评估,而FRAIL量表操作便捷、适合在临床中快速筛查,且在预测术后转归方面更具优势[34]。近年来有学者提出用改良衰弱指数(Modified Frailty Index,mFI)量化手术老年患者的衰弱程度。mFI是一种多维度的综合评估方法,是基于加拿大健康和衰老衰弱指数研究(Canadian Study of Health and Aging Frailty Index,CSHA-FI)中70项潜在临床缺陷中的19项,经Patel等[35]在697例老年股骨颈骨折患者中应用并验证,可更全面、系统地了解髋部骨折患者状况,并能预测住院时间及预后,对临床治疗方案的决策有重要意义。
3.4老年肿瘤 老年肿瘤患者因身体、心理、疾病及相关治疗等原因,对不良结局的易感性增加,常合并衰弱,衰弱患病率超过50%[36]。衰弱可导致肿瘤患者化疗毒性、术后并发症和死亡等风险增加,严重影响生活质量,逐渐成为老年肿瘤患者治疗前评估的重要组成部分[37]。由于老年肿瘤患者疾病复杂,故最好选用在老年肿瘤患者中经过验证的衰弱评估工具,如脆弱老年人问卷-13(Vulnerable Elders Survey-13,VES-13)[38]、老年筛查工具-8(Geriatric-8,G-8)[39]、GFI、FP和CGA,其中GFI和FP在老年肿瘤患者中的应用研究较少[36],CGA虽能有效发现并针对性改善健康问题,但使用过程非常耗时,推广应用受限[37]。VES-13是由Saliba等[38]于2001年开发的简易自评筛查工具,从年龄、自评健康状况、活动情况(6个条目)、功能状态(5个条目)4个方面识别社区中存在健康恶化风险的衰弱老年人,VES-13在老年肿瘤患者中应用最广且具有较高的特异度和诊断价值,可作为自评工具或通过电话访谈进行使用,是美国综合癌症网络指南推荐使用的筛查工具,但该工具缺乏对老年人情绪状态和客观疾病等方面的评估[36]。汉化版VES-13由吴军等[40]于2019年翻译并验证,具有较好的信效度,Cronbach′s α为0.813。G-8是Bellera等[39]于2012年基于老年肿瘤患者开发的CGA简易版本,包括年龄和微型营养评定(MNA)中的7个条目,用于快速识别能从CGA获益的衰弱老年肿瘤患者,灵敏度高,是常规鉴定老年肿瘤患者的最简单工具。一项系统评价比较了FP、GFI、VES-13和G-8在老年肿瘤患者行CGA前的初筛效果,结果显示VES-13特异性最高(78%),G-8灵敏度最高(87%)[41]。然而G-8在国内尚无汉化与应用,在我国老年肿瘤患者中应用的准确性和有效性尚不可知,有待进一步研究。
4 不同机构衰弱评估工具应用现状
4.1社区卫生服务机构 社区老年人衰弱患病率为2.3%~24%[42-43]。由于健康轨迹会随着衰弱的进展而加速下降,逐渐难以减缓或扭转,最终导致死亡。而社区卫生服务机构老年专科医生相对缺乏,社区老年人对衰弱筛查重视不足,社区衰弱老年人常进展为失能,影响躯体功能和生活质量[44]。故需在充分考虑时间、人力和技术的前提下使用简便快捷的评估工具尽早识别社区衰弱及衰弱前期老年人,采取有效措施提前改善其现存的健康问题,预防衰弱进展,维持躯体功能。常用于社区的衰弱评估工具包括FRAIL量表、FP、EFS、VES-13和KCL。其中FRAIL量表简便,预测效度强,可作为社区老年人初步筛查衰弱的有效工具[44];FP能识别身体缺陷和潜在营养缺陷,无需初步临床评估,在临床研究中应用最多[45];EFS内容简便,无须具备老年医学的专业知识即可使用。KCL是2006年日本政府为预防老年人衰弱和失能而提出的衰弱评估工具[20],王志燕等[21]对其进行汉化并对458名社区老年人进行了调查,结果显示中文版KCL信效度良好,Cronbach′s α系数为0.882,可有效识别社区老年人的衰弱。韩君等[46]采用FP、FRAIL量表和EFS评估了上海1 625名社区高龄老年人,发现三者对社区高龄老年人衰弱筛查结果存在差异,FP比FRAIL量表更适合筛查社区高龄老年人的身体衰弱,EFS更适合筛查社区高龄老年人的综合衰弱。但FP需要测量握力和步速,无法做到快速便捷;VES-13实用、简洁,可在5 min内完成,能有效预测老年人功能下降和死亡风险。Bongue等[47]比较了FP、GFI和VES-13在预测1 643名社区老年人残疾、住院和病死率等方面的效果,发现VES-13是预测社区老年人失能、死亡和住院发生率最有效的工具,其灵敏度分别为91.0%、89.7%和92.3%。中文版VES-13亦具有较好的信效度,可用于初级保健机构进行快速衰弱筛查[39],但该问卷缺乏对老年人情绪状态的评估和客观疾病等方面的描述,故亦存在一定局限性。
4.2医院 衰弱老人适应急性疾病或创伤以及社会环境变化的能力较差,在其入院后,疾病和环境的双重变化可能导致症状和功能进一步恶化。研究显示,住院老年患者衰弱患病率高达25.1%~47.4%[48-49]。故需尽早尽快识别患者衰弱状态,帮助启动更为全面的CGA,以促进住院患者的衰弱管理和出院后的延续性护理。考虑到医院复杂的环境特点,其衰弱评估工具须做到多维度、能快速完成、由护士主导、不需要复杂的训练。基于衰弱表型和累积缺陷方法的衰弱评估工具已被证明可以预测住院患者病死率、急诊住院时间、住院需求和出院后的功能衰退[7],应用较广,但表型工具侧重于躯体功能而忽视了患者的心理和社会维度,且无法准确采集行动不便住院患者的数据,如握力或步速;FI虽具有多维度的特点,且可重复性和反应特性更佳,但执行起来较为费时,适于流行病学研究。CFS亦常用于评估住院老年衰弱患者,尤其适用于插管或认知障碍的住院老年重症患者,对病死率的预测效果优于FP、FRAIL量表和FI[50],但在评估衰弱和失能患者过程中可能部分受评估者主观判断的影响[50]。
2018年,Gilbert等[51]以疾病和相关健康问题国际统计分类第10版(ICD-10)为基础,研发了医院衰弱风险评分(Hospital Frailty Risk Score,HFRS),其对每个诊断赋予风险评分并计算总得分,总分<5分为低危,5~15分为中危,>15分为高危。HFRS与FP和FI具有较好的一致性,可帮助识别住院时间延长和死亡风险增加的老年衰弱患者,目前已在国外多个研究中得到验证[50,52]。因HFRS可从患者的常规数据中随时获得,以低成本的方式系统地筛查衰弱,故不会产生与手动评估相关的主观问题和潜在错误。目前暂未见HFRS在国内的应用研究,故其在国内住院老年患者中的应用价值还有待验证。牛娟娟等[53]在2022年发布了老年住院患者衰弱评估量表,包括生活活动能力(6条目)、一般健康状况(5条目)、营养状况(3条目)和精神心理状态(5条目)4个维度,19个条目,总量表的Cronbach′s α为0.934,重测信度为0.809,信效度良好,可作为评估老年住院患者衰弱的工具。但目前暂无应用研究报道,因此还有待进一步验证。
4.3养老机构 养老机构中高龄、多病老年人聚集,衰弱患病率达19%~75.6%[54-55]。司华新[56]以309名养老机构老年人为研究对象,以CGA为金标准比较了FP、FRAIL量表、SOF、TFI,GFI和FI对养老机构老年人不良健康结局的预测效果,发现衰弱患病率因评估工具不同变化范围较大(20.1%~79.6%),多维工具评估的衰弱患病率高于单维。各评估工具对衰弱均具有良好的诊断性能,其中以FI灵敏度最高。FRAIL、FP、SOF及FI均可识别出跌倒高风险老年人。考虑到其他衰弱评估工具多是为社区或住院人群开发而非针对养老机构老年人,Kaehr等[57]于2015年在FRAIL量表的基础上研制了专门适用于养老机构老年人的养老机构衰弱量表(FRAIL-NH),该量表包含了FP和FI的核心元素,由疲乏、转移、步行、失禁、体质量下降、营养摄入、穿衣7个条目组成。得分0~14分,≥7分为衰弱;分数越高,衰弱程度越严重。该量表对多种不良健康结局均具有良好的预测效度,同时克服了二者的局限性,通俗易懂,简单可行,并在包括中国在内的多个国家种族人群中得到验证[58-59]。中文版FRAIL-NH的Cronbach′s α为0.67,重测信度为0.84[56]。葛凤等[60]以302名养老机构老年人为研究对象,以FI判断的衰弱状态为参考,比较了FRAIL-NH量表和TFI对养老机构老年人衰弱的评估能力及评估效果,发现FRAIL-NH量表比TFI更适用于养老机构老年人衰弱评估,是养老机构老年人衰弱评估较理想的工具,值得在未来的研究和实践中进一步推广和应用。
5 小结
衰弱严重影响老年人的生存质量,对老年人的健康结局产生重要影响,因此早期识别、评估老年人的衰弱状态对干预措施的制订具有重要意义。目前已有大量的研究致力于开发客观量化的衰弱评估工具,其评估方式不限于问卷调查,且评估工具的一致性、应用范围、场所和评估的维度存在差异,故对衰弱的评估结果尚不能进行统一判断。在今后的衰弱调查中,调查者应在充分考虑评估目的、资源、优先级、调查对象特点以及可行性的前提下,选择合适的衰弱评估工具,以采取有效措施提前改善老年人现存的健康问题,预防衰弱进展,提高生存质量。

