尼洛替尼一线治疗CML获得临床深度EMR疗效的相关因素分析*
江慧 汪安友
慢性粒细胞白血病(CML)是一种克隆造血干细胞增殖性疾病,该病以骨髓造血干细胞无限制性增生为特征,全球报道年发病率约为1.6/100 000~2/100 000,约占成人白血病比例的15%[1-2]。酪氨酸激酶抑制剂(TKI)作为CML靶向基因治疗的一线用药,其中一代TKI治疗CML患者的十年生存率达85%以上,可显著延长CML患者的生存期[3]。尼洛替尼为第二代TKI靶向药物,与伊马替尼等一代TKI药物相比,其与ABL激酶域结合的亲和力更强,且不易受ABL激酶域突变影响,在CML治疗中能够获得更快和更深的分子学反应,已逐渐用于CML的一线治疗[4]。近年来,针对CML患者的治疗已经进入追求无治疗缓解(treatment free remission,TFR)时代,早期获得临床早期分子学反应(early molecular response, EMR)或者深度的EMR状态是CML患者预后关键指标,国内关于尼洛替尼一线治疗CML的早期深度EMR疗效研究,以及相关影响因素探讨的研究较少,为此本研究选取本院45例CML慢性期初治患者,观察尼洛替尼一线治疗的早期深度分子学反应疗效情况,并分析其潜在的相关影响因素,报道如下。
资料与方法
1 一般资料 回顾性选取分析2016年12月~2020年12月本院血液科收治的CML慢性期患者,纳入标准:符合《慢性髓性白血病中国诊断与治疗指南》中CML诊断标准[5];年龄14~70周岁;外周血或骨髓中原始细胞<10%;ECOG评分0~1;既往未曾使用过伊马替尼、尼洛替尼、达沙替尼等酪氨酸激酶抑制剂药物治疗;患者治疗依从性好,能配合完成相关检查;排除标准:BCR/ABL激酶区域突变;控制不佳的糖尿病、高血压者;甲状腺功能异常者;合并免疫缺陷病、严重器质性器官病变、其他恶性肿瘤;活跃的、不可控制的精神疾病。最终纳入51例病例,其中男23例,女28例,年龄14~70(37.61±5.34)岁,病程3~9(5.26±1.37)个月,Sokal风险:低危17例、中危19例、高危15例。
2 治疗方法 本研究药物尼洛替尼(达希纳)由瑞士Novartis公司生产,初诊CML慢性期者给予300 mg/次,2次/d,于进食前1 h或进食2 h后以水完整吞服,2次服药间隔12 h,治疗期间不联合干扰素等其他治疗抗CML药物治疗,治疗过程中根据个体耐受情况及血液检测指标及时调整剂量,最大治疗剂量应不高于800 mg/d。
3 观察指标 (1)分子学反应:治疗初期每周行血常规检查,待血象稳定后隔周复查血液生化指标;于治疗3、6、12个月采集外周血标本检测BCR/ABLIS水平评价分子学反应(BCR/ABLIS检测计算方法,采用本中心实验室定量PCR检测BCR/ABL分子水平基础数值×国际中心标准实验室比值系数CF值,本中心CF值为0.71)。根据国内外共识,EMR是指治疗3个月BCR/ABLIS≤10%;6个月时BCR/ABLIS≤1%;本研究我们定义早期深度分子学反应(深度EMR):3个月时BCR/ABLIS水平≤1%,6个月时BCR/ABLIS水平≤0.1%;(2)不良反应及预后:治疗过程中监测药物不良反应,包括血液学不良反应与非血液学不良反应,并参照CTCAE4.0版对相关不良反应进行分级;随访截止时间为2021年12月,中位随访时间26(12~60)个月,无进展生存(PFS)指尼洛替尼治疗开始至疾病加速期或急变期区间的时间。(3)收集患者临床资料,分析深度EMR的影响因素。
4 统计学方法 采用SPSS 20.00软件进行统计分析,计量资料以()表示 ,符合正态分布的资料比较采用独立样本t检验或方差分析,不符合正态分布资料采用秩和检验;计数资料用频数表示,组间比较采用χ2检验;多因素分析采用多变量二分类Logistic回归分析模型,P<0.05表示差异具有统计学意义。
结 果
1 分子学反应 尼洛替尼一线治疗3、6、12个月获得的早期最佳分子学反应率为82.3%、92.1%、86.2%,3个月时获得深度EMR为35例(68.6%),未获得深度EMR为16例(31.4%);6个月时获得深度EMR为26例(50.9%),未获得深度EMR为25例(49.1%);在治疗12个月时获得主要分子生物学反应(MMR)率为44例(86.2%);达MMR的中位时间为4(3~17)个月。
2 不良反应及预后情况 不良反应:主要出现中性粒细胞减少(4.4%)、血小板减少(6.7%)、贫血(2.2%),均为1~2级,可在短期内恢复,未出现3~4级血液学不良反应。非血液学不良反应为皮疹(4.4%)、瘙痒(4.4%)、恶心(2.2%),可耐受且经对症治疗后可缓解,未出现剂量调整情况;生存情况:无进展生存期率为98%(50/51)。
3 影响深度EMR的影响因素分析 单因素分析结果显示,尼洛替尼服用前病程、血小板计数、血红蛋白、外周血原始细胞及肋下脾长度均与CML患者获得深度EMR有关,差异有统计学意义(P<0.05),见表1;将上述临床参数引入多因素Logistic 回归分析模型,结果显示仅外周血有原始细胞、巨脾(脾肋下≥7 cm)为影响患者获得深度EMR的独立危险因素(P<0.05),见表2。

表1 影响CML患者获得深度EMR的单因素分析
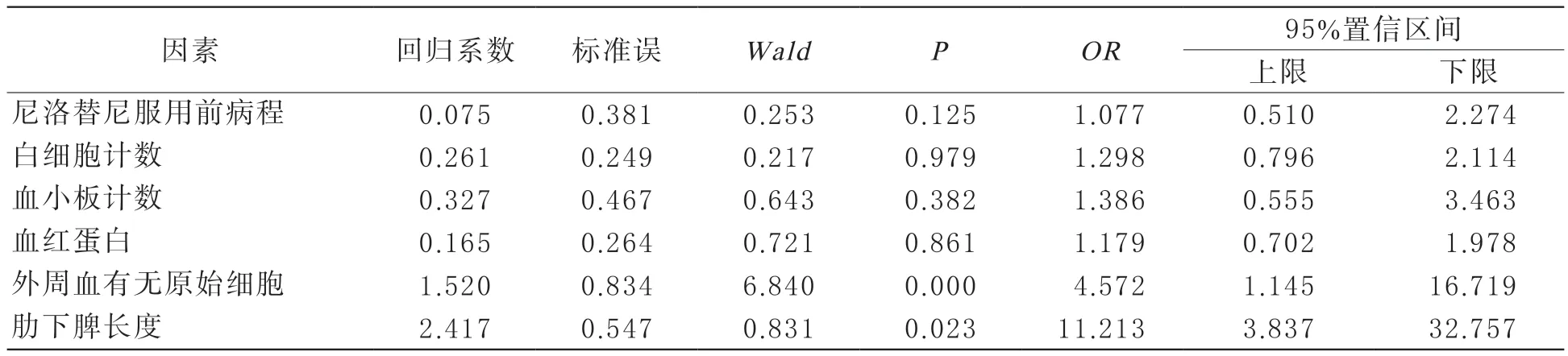
表2 CML患者获得深度EMR的多因素Logistic回归分析
讨 论
9和22号染色体易位形成BCR-ABL融合基因导致恶性骨髓增殖,也是CML发病的重要机制[6]。传统CML患者治疗主要采用干扰素、羟基脲及造血干细胞移植等方法,治疗效果并不显著,CML患者3年生存率仅约50%,且存在骨髓抑制、胃肠道反应、发热等毒副作用较多,同时并未能彻底消除BCR-ABL融合基因[7]。TKI药物可靶向抑制BCR-ABL蛋白的酪氨酸激酶活性,极大地提升了CML患者的生存率,成为CML患者治疗的首选药物。然而,仍有约30%的一代TKI制剂(伊马替尼)治疗患者会出现耐药、不耐受而终止治疗。与一代TKI相比,二代TKI尼洛替尼可获得更快更深的分子学反应[8]。而有研究表明[9-10],CML患者一线TKI治疗后能够实现早期分子学反应对患者良好预后具有积极的意义。近年来随着二代TKI制剂一线用于CML患者的治疗以及分子生物学深度检测能力的提升,尼洛替尼为CML患者带来TFR的治疗疗效,总体预后良好,患者不仅从早期的获得缓解到获得MMR,再到获得深度的分子生物学反应(DMR)和持续的DMR,这些是实现TFR的根本保障,更有部分CML患者已经达到TFR治疗标准。目前临床一线治疗在TFR治疗目标时代,以获得更快、更深、更持久的DMR是部分CML患者的治疗目标,有研究指出早期深度的分子学反应与后期患者TFR治疗目标的触及存在显著相关性[11-12],因此指导治疗方案的调整尤其是一线治疗的选择或对于早期疗效不佳患者的治疗方案选择尤为关键,EMR可预测CML患者的总体治疗反应、对患者后期获得DMR的累积率存在一定影响。既往临床研究多以观察CML患者EMR疗效指标,以及影响EMR相关因素的临床特征为主。近年来随着持续的DMR是TFR触及和成功的保障,更早更快更深获得DMR日益受到临床研究者的关注,因此本研究重点观察CML患者早期深度的分子生物学反应(即深度EMR)及其相关影响因素。
本研究发现,尼洛替尼一线治疗3、6、12个月获得的最佳分子学反应率为82.3%、92.1%和86.2%,3个月时获得深度EMR为35例(68.6%),6个月时获得深度EMR为26例(50.9%);在治疗12个月时获得主要分子学反应(MMR,BCR/ABLIS水平≤0.1%)率分别为44例(86.2%);达MMR的中位时间为4(3~17)个月。提示尼洛替尼一线治疗CML不仅可获得EMR,而且可获得深度EMR。薛磊等[13]报道提示尼洛替尼一线治疗CML获得EMR率可达94.44% ;殷华等[14]提出尼洛替尼一线治疗CML的累积MMR发生率为72.22%,这些与本研究结果基本相符。我们同时对比分析了一代TKI伊马替尼和二代TKI尼洛替尼一线治疗CML患者早期获得深度EMR的差异,期间我们与本中心既往193例采用伊马替尼一线治疗CML患者数据作了统计分析,结果显示伊马替尼vs. 尼洛替尼治疗获得深度EMR:3个月24%vs.68.6%;6个月25.2%vs. 50.9%。尼洛替尼与ABL激酶结合的亲和力较伊马替尼高出30倍[15-17],从而能获得早期更深的分子学反应。此外,尼洛替尼治疗CML具有较高的安全性,本研究中CML患者主要出现的不良反应有中性粒细胞减少、血小板减少、贫血,均为1~2级,可在短期内恢复,未出现3~4级血液学及非血液学不良反应;患者耐受较好,与相关报道结果一致[18]。
早期分子学反应与CML预后长期缓解关系密切,3个月BCR/ABLIS≤10%能够预测良好的预后[19],但这种预测是重点关注CML患者后期长期的MMR缓解状态。近年来,随着CML患者对TFR治疗效果的追求,患者疾病的深度缓解逐步受到临床研究者的重视,尤其CML患者早期分子生物学缓解的深度。早期3个月、6个月获得深度EMR的患者后期触及TFR的概率更高。本研究重点探讨分析影响深度EMR的潜在临床相关因素:尼洛替尼前病程、血小板计数、血红蛋白、外周血原始细胞及肋下脾长度,这些因素均与CML患者获得深度EMR有关,经多因素Logistic回归分析显示仅外周血原始细胞、巨脾为影响患者获得深度EMR的独立危险因素,P<0.05。外周血原始细胞分布是CML分期的重要参数,CML慢性期患者外周血原始细胞低于10%,同时原始细胞也是Sokal积分评估的重要依据,原始细胞越高,Sokal风险等级越高,而中高风险的 CML患者获得早期分子学反应难度较大,预后较差[20]。同时,巨脾为公认的CML预后不良的高危因素,常用的预后评分系统Sokal、EURO及EUTOS均将巨脾归为参考因素。脾脏是最重要的髓外造血器官,也是CML最常累及的脏器,CML所致的幼稚细胞大量淤积于循环中,脾脏会反复吞噬不成熟的细胞,引起脾脏功能的亢进而出现代偿性的增大,尤其在加速期,可见脾脏明显增大。因此,外周血有原始细胞、巨脾对于CML患者早期获得深度EMR可能是密切相关因素。在TFR治疗时代,这些因素对于临床部分以TFR为治疗目标的CML患者早期治疗的选择尤为重要,也值得临床深入研究探讨。
综上所述,尼洛替尼一线治疗慢性粒细胞白血病可有助于获得更加深度的早期分子学反应,具有较高的安全性;但在部分追求TFR为治疗目标的患者,即使采用尼罗替尼一线治疗,患者早期外周血伴有原始细胞、巨脾可能影响早期获得深度EMR,不利于患者尽早触及TFR,故这部分CML患者的初始治疗仍值得临床进一步探讨。
利益冲突所有作者均声明不存在利益冲突

