纳米生物炭对铵态氮的吸附-解吸效果研究
纪文婕,孙一迪,韩正砥,谢基淦,周明耀
(扬州大学水利科学与工程学院,江苏 扬州 225009)
0 引 言
氮是植物生长过程中必不可少的营养元素。目前国内主要粮食作物的氮肥利用率约为39.2%,与西方国家仍存在较大差距[1]。大量溶解氮通过淋溶损失、地表径流流失以及氨挥发等途径流失到土壤、水体和大气中,引起水体富营养化和铵态氮含量超标等环境问题[2,3]。因此如何有效降低氮素对环境的污染一直是农业生产中的研究重点。
生物炭是将生物质在缺氧或绝氧条件下经过高温裂解获得的高含碳固体产物,其理化性质稳定,比表面积大,表面孔隙结构和官能团丰富,这些特性使得生物炭具有良好的吸附性能[4]。近年来,生物炭在减少农业土壤氮肥损失和提高作物对氮素的利用效率方面获得了较多研究成果[5]。Jassal 等研究发现生物炭表面存在的离子交换量远小于其对离子的吸附量,认为生物炭主要依靠表面孔隙来吸附各种离子[6]。李帅霖等人研究发现存在大量含氧官能团的生物炭表面具有高密度的负电荷,能将带正电荷的铵根离子吸附在其表面[7]。以上研究可知,生物炭降低氮素流失与其对氮素的高吸附性能密切相关。尽管如此,本体生物炭的吸附能力有限,且在应用上存在用量大的问题。近年来许多研究采用各种改性方法对生物炭进行改性[8],常用的改性方法有氧化改性、还原改性、酸碱改性、金属负载改性等化学方法和高温热处理改性、微波改性等物理方法以及混合改性等改性方法[9,10],但是这些改性方式在规模化的实际生产中均存在生产成本高,工艺复杂,甚至产生有害废弃物的问题,缺乏易操作和无溶剂/无化学改性方法。
纳米材料及其相关产品在农业和环境领域的应用为生物炭改良提供了新途径。与本体生物炭相比,低能耗、操作性强和绿色环保的物理改性方法(球磨法)制备的纳米生物炭材料兼具生物炭和纳米材料的优点,其具有更小的孔径、更高的比表面积、更丰富的含氧官能团[11],吸附和离子交换性能更强。Ramezanzadeh 等人采用球磨法制备的纳米生物炭相对本体生物炭比表面积提高了210%,对镉的吸附量提高了412.2%[12]。Xiao 等人开展的室内模拟试验发现与本体生物炭相比,纳米生物炭对重金属镉、铜和铅的吸附量分别增加了93.9%、75.6%和64.6%[13]。Yue 等人进行的室内培养试验研究表明,纳米生物炭对土壤中镉的高吸附性能抑制了水稻对镉的吸收[14]。纵观国内外研究成果,有关纳米生物炭对铵态氮吸附-解吸性能的研究鲜有报道。因此本研究拟采用球磨法制备纳米生物炭,探究其对铵态氮的吸附-解吸效果,以期为农田施用纳米生物炭减少氮素损失、提高氮肥利用率以及和绿色开发高效生物质资源提供理论依据和技术支撑。
1 材料与方法
1.1 试验材料
本体生物炭购于豪派环保公司,以稻草秸秆为原料,在450 ℃下的马弗炉中限氧热解2 h 而成。纳米生物炭采用球磨法制备。使用行星球磨仪,将本体生物炭在540 r/min 条件下研磨6 h,获得纳米生物炭。研磨过程中球磨仪每正转研磨30 min 停止10 min 后反转研磨30 min,防止由于温度升高或长时间同方向研磨引起的生物炭聚积,研磨球直径为3、5、8 mm,球粉比为5∶1[4]。本体生物炭和纳米生物炭的基本理化性质见表1。

表1 本体生物炭和纳米生物炭的基本理化性质Tab.1 Basic physical and chemical properties of bulk biochar and nano-biochar
1.2 试验方法
1.2.1 纳米生物炭对铵态氮吸附过程影响的试验
试验采取完全随机试验设计,所有处理以不添加生物炭为对照,重复3次。
(1)不同生物炭投加量吸附试验。取初始浓度1.0 g/L,初始 pH 为 5.5 的 NH4Cl 溶液 50 mL,分别加入 0.2、0.4、0.6、0.8、1.0、2、3 g 本体生物炭和纳米生物炭。置于恒温水浴(25℃)振荡器中振荡,振荡频率200 r/min,振荡时间4 h,反应结束后测定上清液中NH4+-N浓度。
(2)不同初始溶液氮浓度吸附试验。取初始浓度为0.1、0.3、0.6、0.9、1.2、2.0、3.0 g/L,初始 pH 为 5.5 的 NH4Cl 溶液50 mL,分别加入1.0 g本体生物炭和纳米生物炭。置于恒温水浴(25℃)振荡器中振荡,振荡频率200 r/min,振荡时间4 h,反应结束后测定上清液中NH4+-N浓度。
(3)不同初始溶液pH 吸附试验。取初始浓度1.0 g/L 的NH4Cl 溶液50 mL,分别加入1.0 g 本体生物炭和纳米生物炭,利用 NaOH 和 HCL 调节溶液 pH 值分别为 5、6、7、8、9、10。置于恒温水浴(25℃)振荡器中振荡,振荡频率200 r/min,振荡时间4 h,反应结束后测定上清液中NH4+-N浓度。
(4)不同吸附时间吸附试验。取初始浓度1.0 g/L,初始pH 为5.5 的NH4Cl 溶液50 mL,分别加入1.0 g 本体生物炭和纳米生物炭,置于恒温水浴(25 ℃)振荡器中振荡,振荡频率200 r/min,分别振荡 10、20、40、60、90、120、150、180、210、240 min。反应结束后测定上清液中NH4+-N浓度。
吸附量按下式计算:

式中:qe为吸附平衡时的单位吸附量,mg/g;C0为初始溶液浓度,mg/L;Ce为吸附平衡后浓度,mg/L;V为溶液的体积,L;M为生物炭质量,g。
1.2.2 纳米生物炭对铵态氮解吸过程影响的试验
将1.2.1(2)中经过3.0 g/L 反应的本体生物炭和纳米生物炭进行解吸,采用1 mol/L 的KCl溶液50 mL 浸提1 次。置于恒温水浴(25 ℃)振荡器中振荡,振荡频率200 r/min,分别振荡10、20、40、60、90、120、150、180、210、240 min。反应结束后测定上清液中NH4+-N浓度。解吸量和解吸率按下式计算:
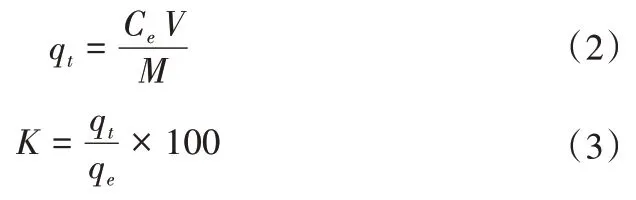
式中:qt为解吸平衡时的单位解吸量,mg/g;qe为解吸平衡时的单位吸附量,mg/g;Ce为解吸平衡后浓度,mg/L;V为解吸溶液的体积,L;M为生物炭质量,g。
1.2.3 吸附等温线模型
采用吸附等温线模型模拟1.2.1 (2) 试验所得数据,Langmuir模型和Freundlich模型方程形式如下[15]:
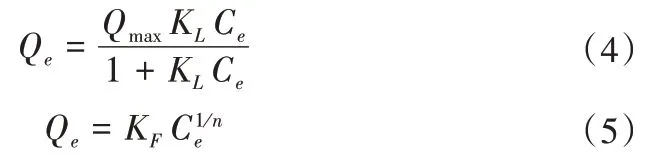
式中:Qe为吸附平衡时的单位吸附量,mg/g;Qmax为最大吸附量,mg/g;Ce为初始溶液浓度,mg/L;KL为Langmuir 模型参数;KF为Freundlich模型吸附常数,L/mg;n为Freundlich模型参数。
1.2.4 吸附动力学模型
采用吸附动力学模型模拟1.2.1(4)试验所得数据,准一级动力学模型和准二级动力学模型方程形式如下:
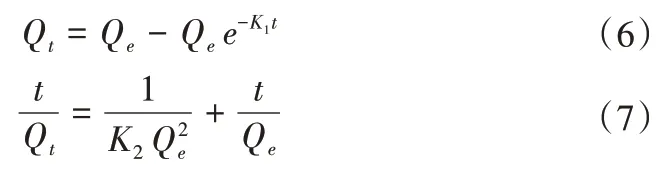
式中:Qt表示t时刻的单位吸附量,mg/g;t表示吸附时间,min;Qe表示反应平衡时的单位吸附量,mg/g;K1表示准一级吸附速率常数,g/(mg·min);K2表示准二级吸附速率常数,g/(mg·min)。
1.2.5 解吸动力学模型
采用解吸动力学模型模拟解吸实验所得数据,准一级动力学模型和准二级动力学模型方程形式同1.2.4。
1.3 测定项目及方法
本体生物炭和纳米生物炭的颗粒直径分布使用动态光散射仪(Malvern,ZEN3600,英国)测定,比表面积使用全自动比表面积及孔隙度分析仪(Autosorb-IQ2-MP-XR-VP,美国)进行测定,元素含量采用元素分析仪(Elementar,Vario EL III,德国)进行测定。表面酸性/碱性含氧官能团数量的测定采用Boehm 滴定法。水样中铵态氮(NH4+-N)的平衡浓度采用氯化钾溶液提取-分光光度法法测定,测试仪器为紫外分光光度计。
1.4 数据分析
数据处理采用Microsoft Excel 2010,采用Origin(ver.9.1)进行模型模拟分析及作图。
2 结果与讨论
2.1 纳米生物炭对铵态氮的吸附效果研究
2.1.1 生物炭投加量对纳米生物炭吸附NH4+-N的影响
不同生物炭投加量条件下本体生物炭和纳米生物炭吸附NH4+-N 的变化特征如图1 所示。投加量小于1 g 时,两种生物炭对铵态氮的吸附量随投加量的增加均呈现明显的上升趋势;投加量达到1 g 后,吸附上升趋势变缓,但纳米生物炭的上升幅度大于本体生物炭,主要因为纳米生物炭表面孔隙增多,比表面积增大,酸性官能团增加;投加量达到2 g 后,吸附反应达到动态平衡。纳米生物炭的最大吸附量为6.910 mg/g,是相同条件下本体生物炭吸附量的2倍。

图1 生物炭投加量对吸附NH4+-N的影响Fig.1 The effect of the biochar dosage on the adsorption of NH4+-N
2.1.2 溶液氮浓度对纳米生物炭吸附NH4+-N的影响
不同初始溶液氮浓度条件下本体生物炭和纳米生物炭吸附NH4+-N 的变化特征如图2所示。初始氮浓度小于1.2 g/L时,随着氮浓度的增加,本体和纳米生物炭对铵态氮的吸附量呈现明显的上升趋势;溶液氮浓度达到1.2 g/L 后,吸附上升趋势变缓,但纳米生物炭的上升幅度大于本体生物炭;溶液氮浓度达到2 g/L 后,吸附反应达到动态平衡。生物炭表面的吸附位点数量有限,当其表面离子的相互作用达到饱和时,即使溶液氮浓度升高,生物炭也无法继续进行吸附行为[16]。纳米生物炭表面存在更多的孔隙和含氧官能团,吸附位点更多,其对铵态氮的吸附性能优于本体生物炭。纳米生物炭的最大吸附量为6.880 mg/g,是相同条件下本体生物炭吸附量的1.9倍。
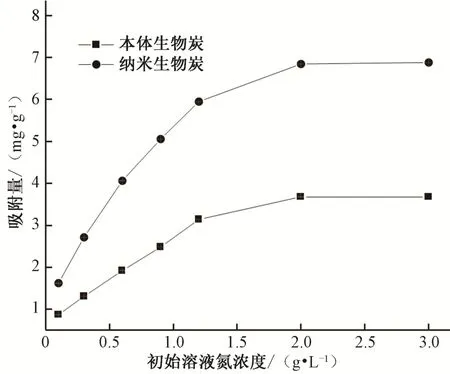
图2 初始溶液氮浓度对吸附NH4+-N的影响Fig.2 The effect of initial nitrogen concentration on the adsorption of NH4+-N
本体生物炭和纳米生物炭吸附铵态氮的等温线模型模拟结果如图3 所示,两种吸附等温线模型拟合参数如表2 所示。纳米生物炭综合吸附能力较强,两种模型拟合后方程R2均达0.9 以上,这是因为纳米生物炭比表面积较大,孔隙多而不均[17]。Langmuir 方程中,两种生物炭的R2均大于Freundlich 方程中的R2,说明Langmuir 方程能更好地模拟本体生物炭和纳米生物炭对铵态氮的动态吸附过程,两种生物炭对铵态氮的吸附主要是单分子层吸附[18],这与Thi 等[19]和宋婷婷等[20]的研究结果一致。两种生物炭的KL值大小顺序为纳米生物炭>本体生物炭,表明纳米生物炭与铵态氮的结合稳定性更强。Langmuir 方程中,纳米生物炭对铵态氮的最大吸附量可达8.512 mg/g,约为本体生物炭的1.8 倍。Freundlich 方程中,n值介于1~10 之间,说明两种生物炭对铵态氮的吸附均较容易进行[21]。
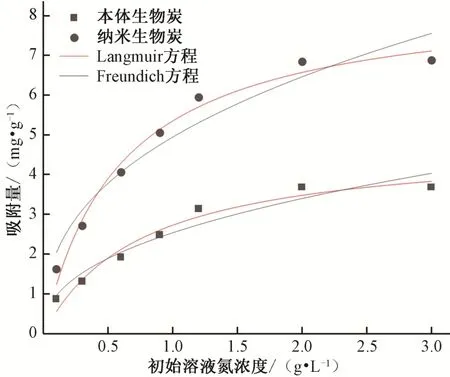
图3 生物炭对铵态氮的吸附等温线模型Fig.3 Isothermal adsorption model of biochars for ammonium nitrogen

表2 吸附等温线模型参数Tab.2 Isothermal adsorption model parameters
2.1.3 溶液pH值对纳米生物炭吸附NH4+-N的影响
不同溶液pH 值条件下本体生物炭和纳米生物炭吸附的变化特征如图4 所示。两种生物炭对铵态氮的吸附量随pH 的升高先增加后又减少。pH 为7 时,本体生物炭和纳米生物炭对铵态氮的吸附效果最好,吸附量分别为4.066 mg/g和6.825 mg/g。pH 较低时,纳米生物炭表面呈正电荷,与NH4+-N 产生静电斥力,不易于吸附[22];pH 过高时,溶液中铵态氮的主要存在形式为游离的铵态氮,影响纳米生物炭对NH4+-N 的吸附效果[23]。相比本体生物炭,纳米生物炭对铵态氮的吸附量在不同溶液PH下均有明显的提高,最大可达2.2倍。

图4 溶液pH值对吸附NH4+-N的影响Fig.4 The effect of solution pH on the adsorption of NH4+-N
2.1.4 吸附时间对纳米生物炭吸附NH4+-N的影响
本体生物炭和纳米生物炭吸附NH4+-N 随时间的变化特征如图5所示。反应初期,生物炭表面的孔隙及含氧官能团可与铵态氮进行最大面积的接触,同时溶液中铵态氮浓度较高,两种生物炭对铵态氮的吸附量快速增长[24]。宋婷婷等[20]研究竹炭与玉米秸秆炭等对铵态氮吸附效果,本实验结果与其类似。随着时间的延长,两种生物炭对铵态氮的吸附量的增长趋于平缓并达到吸附饱和的状态。本体生物炭在吸附时间为180 min 时,吸附反应达到动态平衡;纳米生物炭在吸附时间为210 min 时,吸附反应达到动态平衡。这是因为纳米生物炭表面有更多的空隙和含氧官能团,纳米生物炭到达吸附平衡状态需要更长时间。纳米生物炭对铵态氮的吸附量的最大吸附量为5.405 mg/g,是相同条件下本体生物炭吸附量的2.1倍。

图5 吸附时间对吸附NH4+-N的影响Fig.5 The effect of adsorption time on the adsorption of NH4+-N
本体生物炭和纳米生物炭吸附铵态氮的动力学模型模拟结果如图6 所示,两种吸附动力学模型拟合参数如表3 所示。准二级动力学吸附方程的R2分别为0.947、0.982,均大于准一级动力学吸附方程的R2,说明准二级动力学方程能更好地模拟本体生物炭和纳米生物炭对铵态氮的动态吸附数据,两种生物炭对铵态氮的吸附主要是化学吸附,这与由Langmuir 等温线方程推断出两种生物炭对铵态氮主要是单分子层吸附的结果相一致[9]。这是因为准一级动力学方程通常只适合描述初级阶段的动力学,而不能准确概括吸附的全过程。准二级动力学模型包含了外部液膜扩散、表面吸附和颗粒内扩散等吸附的全部过程,更全面准确的反应了铵态氮在生物炭表面的吸附过程[25]。准二级动力学方程中,平衡时纳米生物炭对铵态氮的单位吸附量可达6.451 mg/g,约为本体生物炭的2.2倍。

图6 生物炭对铵态氮的吸附动力学模型Fig.6 Dynamic adsorption model of biochars for ammonium nitrogen

表3 吸附动力学模型参数Tab.3 Dynamic adsorption model parameters
2.2 纳米生物炭对铵态氮的解吸效果研究
解吸试验主要考虑吸附量饱和时,解吸时间对两种生物炭解吸铵态氮的效果影响。本体生物炭和纳米生物炭解吸NH4+-N 随时间的变化特征如图7 所示。反应初期,吸附在生物炭表面或者孔隙的近外部的铵态氮易被解吸,生物炭对铵态氮的解吸量快速增长。随着时间的延长,两种生物炭对铵态氮的解吸量增长的趋势变得缓慢并达到饱和状态,这是因为NH4+-N 不断向生物炭孔隙内部和深处扩散而不易被解吸。解吸时间为210 min 时,本体生物炭的解吸反应达到动态平衡;解吸时间为240 min 时,纳米生物炭的解吸反应达到动态平衡。纳米生物炭对铵态氮的最大解吸量为6.051 mg/g,是相同条件下本体生物炭解吸量的1.9 倍。经过球磨后的纳米生物炭孔隙更为畅通,有利于其他阳离子与NH4+-N 的交换,纳米生物炭对铵态氮的解吸量显著高于本体生物炭,纳米生物炭到达解吸平衡状态也需要更长时间。田雨等[26]研究改性材料对铵态氮的吸附解吸效果,本实验结果与其类似。本体生物炭对铵态氮的最大解吸率为83.72%,纳米生物炭对铵态氮的最大解吸率为90.71%,显著高于本体生物炭。
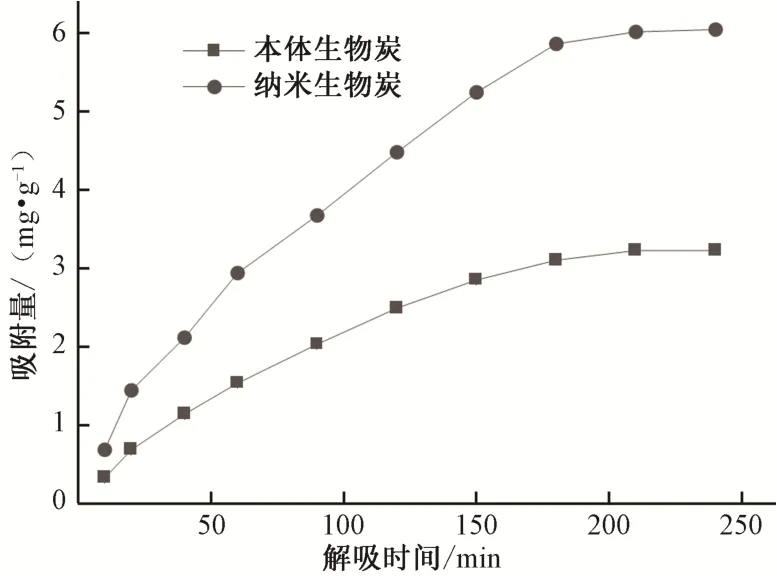
图7 解吸时间对解吸NH4+-N的影响Fig.7 The effect of desorption time on the desorption of NH4+-N
本体生物炭和纳米生物炭解吸铵态氮的动力学模型模拟结果如图8 所示,两种解吸动力学模型拟合参数如表4 所示。准二级动力学解吸方程的R2分别为0.997、0.993,均大于准一级动力学解吸方程的R2,说明准二级动力学方程能更好地模拟本体生物炭和纳米生物炭对铵态氮的动态解吸过程,两种生物炭对铵态氮的解吸主要是化学解吸,这与准二级动力学方程推断出两种生物炭对铵态氮主要是化学吸附的结果相一致,说明两种生物炭对铵态氮的解吸过程可以看作是吸附过程的逆向反应。
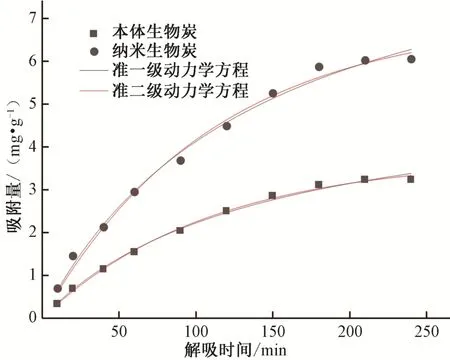
图8 生物炭对铵态氮的解吸动力学模型Fig.8 Dynamic desorption model of biochars for ammonium nitrogen
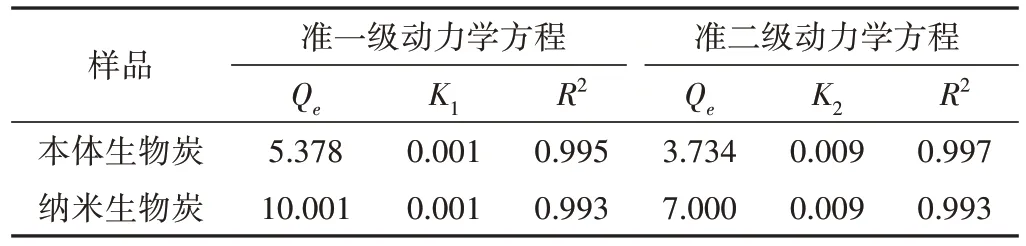
表4 解吸动力学模型参数Tab.4 Dynamic desorption model parameters
本研究结合材料本身的理化性质、模拟动态吸附-解吸过程以及吸附等温线模型和吸附-解吸动力学模型研究了本体生物炭和纳米生物炭对铵态氮的吸附-解吸效果以及引起差异的内在机理。以往研究表明生物炭施入土壤后可对土壤中的养分和肥料具有一定束缚和持留作用[27],本试验中纳米生物炭对铵态氮的吸附-解吸能力相对于本体生物炭都表现出明显的优势,由此推测化肥配施纳米生物炭对氮素的持留和缓释效果更好,可以更有效的减少氮素流失,促进作物对氮素的吸收利用,进而提高氮肥利用率。该研究结果是基于室内吸附-解吸模拟试验,方法存在一定的局限性。因此纳米生物炭应用于实际生产中对氮素的阻控能力或者与肥料混施于田间对氮素的固持和缓释效果有待进一步的试验研究。
3 结 论
(1)本体生物炭和纳米生物炭对铵态氮的吸附量随其投加量的增加和初始溶液氮浓度的增大呈“快速增加,缓慢平衡”的趋势,且纳米生物炭对铵态氮吸附量的增加幅度大于本体生物炭。溶液pH 会对生物炭吸附铵态氮的效果产生影响,溶液pH 为7 时,两种生物炭对铵态氮的吸附效果最好。相对于本体生物炭,纳米生物炭吸附铵态氮的平衡时间更长且吸附量显著增大。纳米生物炭的最大吸附量为6.91 mg/g,是相同条件下本体生物炭吸附量的2倍。
(2)相对于本体生物炭,纳米生物炭解吸铵态氮的平衡时间更长,且解吸量和解吸率显著增大。纳米生物炭最大解吸量为6.051 mg/g,是相同条件下本体生物炭解吸量的1.9 倍。本体生物炭对铵态氮的最大解吸率为83.72%,纳米生物炭对铵态氮的最大解吸率为90.71%。
(3)纳米生物炭对铵态氮的吸附方式主要是单分子层吸附和化学吸附,由外部液膜扩散、表面吸附和颗粒内扩散等多种机理共同作用。纳米生物炭对铵态氮的解吸过程可以看作是吸附过程的逆向反应。

