肠道综合物理疗法对不完全性脊髓损伤患者便秘的影响
李亚楠,吴娟,栗亮,陈聪,靖华芳,高轶,韩向华,王越,廖利民
脊髓损伤后中枢神经受损,造成损伤平面以下的运动、感觉及自主神经障碍,超过80%的患者出现排便困难、便秘、便失禁、排空不全、排便时间延长、腹胀等神经源性肠道功能障碍(Neurogenic bowel dysfunction,NBD)的症状[1-2],其中以便秘、排便困难及排便时间延长最常见(患病率56%~80%),症状可随时间推移而加重[3],并可伴随痔疮、出血、直肠脱垂、肛裂、电解质紊乱等多种并发症,给患者带来极大痛苦,严重影响了患者的身心健康和生活质量。目前,针对NBD的治疗包括行为及饮食干预、药物、物理疗法、灌肠、手术等[4-5],治疗方法和效果有限,其中对NBD中便秘症状的针对性研究较少。本研究观察生物反馈电刺激、肠道运动疗法及两者结合的肠道综合物理疗法对不完全性脊髓损伤患者便秘的影响,探寻脊髓损伤后便秘治疗的新方法。
1 资料与方法
1.1 一般资料 选取2020年10月~2021年10月在中国康复研究中心住院,存在神经源性便秘的不完全性脊髓损伤患者30例。纳入标准:年龄20~60岁;颈、胸段不完全性脊髓损伤,诊断符合美国脊髓损伤学会《脊髓损伤神经学分类国际标准(2019年修订)》诊断标准[6],脊髓损伤等级为C级或D级;存在神经源性肠道症状,便秘诊断标准参照罗马Ⅲ和国际胃肠病学组织的指南标准:排便困难、自主排便次数小于3次/周、排便不尽感等;生命体征平稳,病程≥3个月;腹直肌、竖脊肌及双下肢关键肌肌张力,改良Ashworth分级≤2级;自愿参加,签署知情同意书者。排除标准:有开放性损伤或生命体征不稳定等;有严重胃肠道疾患等;有直肠肛门外伤手术史等;先天性及进展性脊髓损伤患者等;研究者认为不适合的患者。本研究经中国康复研究中心医学伦理委员会批准(NO.2020-139-1)。将30例患者随机分为生物反馈电刺激组(A组,n=10)、肠道运动疗法组(B组,n=10),肠道综合物理疗法组(即生物反馈电刺激结合肠道运动疗法,C组,n=10)。3组一般资料比较差异无统计学意义。见表1。

表1 3组患者一般资料比较
1.2 方法 3组均进行常规干预,包括:饮食管理:多饮水及蔬菜水果,水按40ml/kg+500ml/d计算摄入量;定时排便,按既往规律或早餐后1h排便;排便体位尽量采用坐位;药物:研究开始后停用辅助排便药物,如有必要,泻药使用乳果糖,栓剂采用开塞露,记录用量;运动治疗:住院患者每日进行常规康复训练,运动量在3~3.5h/d。①A组在常规干预的同时,进行生物反馈电刺激治疗:使用PRB055型生物反馈治疗仪训练,治疗前嘱患者排空膀胱,仰卧位,放置皮肤电极(一片贴在髂前上棘,两片贴在脐周腹肌表面)及肛管刺激电极(经肛门置入,深度5cm),刺激频率25~75Hz,带宽500us,刺激强度以患者盆底肌肉出现明显收缩且可耐受为度,治疗30min/次,1次/d。②B组在常规干预的同时,进行肠道运动疗法干预,患者排空膀胱,仰卧位,屈髋屈膝,按以下顺序进行训练:腹式呼吸训练:呼气时收紧腹部,腹部向脊柱方向贴,维持5s,吸气放松,放松5s,交替进行,15次/组×2组;腹部肠道按摩:操作者将手掌叠加,用除拇指外的4指从右向左,沿结肠的走形做顺时针按摩。在乙状结肠处,加强手指的压力,之后再从右向左按摩,15次/组×2组;盆底肌训练:采用凯格尔运动,指导患者收缩阴道周围肌肉和肛门周围肌肉,维持5s后放松,放松5s后再进行以上运动,10次/组×5组;腹肌增强训练:包括仰卧起坐和直腿抬高运动,均为15次/组×2组;桥式运动:患者做搭桥运动,将臀部抬起,与肩部,膝盖成一条直线,保持5s,放松,15次/组×2组;腹式呼吸,同上。以上训练每节间休息1min,治疗共30min/次,1次/d。③C组在常规干预的同时,进行肠道综合物理疗法训练:先后进行生物反馈电刺激和肠道运动疗法的干预,1次/d。3组治疗均为每周5d,为期4周。
1.3 评定标准 3组治疗前后进行以下评定:
1.3.1 NBD评分 用于评估脊髓损伤患者结肠、直肠及肛门的功能障碍程度。包括最近4周内平均排便时间、排便次数、是否需要手指协助、失禁频率、有无排气失禁、是否需要尿布、是否需要口服泻药或止泻剂、肛周问题、腹痛或不适等,总分0~47分,得分越高,障碍程度越重[7]。
1.3.2 Wexner便秘评分 包括排便次数、是否排空、有无腹痛、排便时间、是否需要协助、排便失败的次数、便秘病史等指标,总分0~30分,得分越高,便秘越严重[8]。
1.3.3 便秘患者生活质量量表评分(Patient Assessment of Constipation Quality Of Life, PAC-QOL) 便秘患者生活质量量表。包括生理不适、社会心理不适、担忧和满意度等。总分0~112分,得分越高,病情越严重[9]。
1.3.4 便秘患者症状自评量表评分(Patient Assessmentof Constipation Symptom, PAC-SYM) 便秘患者症状自评量表,包括粪便性状、直肠症状和腹部症状等。总分0~48分,得分越高,便秘症状越重[9]。
1.3.5 排便日记 记录患者每天乳果糖的用量及每次排便开塞露的用量,计算治疗开始第一周(记为治疗前)及最后一周(记为治疗后)的平均用量。
1.3.6 肛门直肠测压 用于量化肛门直肠机械性能的诊断性检测。测试前患者排空肠道,采用左侧位,屈膝屈髋,将顶端带有球囊的四通道压力传感器润滑,放入肛门,测定肛门静息压、肛门收缩压、直肠容量感觉阈值(初始感觉阈值,急迫感觉阈值,最大感觉阈值)[1]。
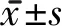
2 结果
2.1 3组 NBD、Wexner便秘、PAC-QOL及PAC-SYM评分量表比较 治疗前,3组的NBD、Wexner便秘、PAC-QOL及PAC-SYM评分比较差异无统计学意义。治疗4周后,3组的NBD、Wexner便秘,PAC-QOL及PAC-SYM评分均较治疗前有明显减少(P<0.01)。治疗后组间比较:C组与A、B组间对比,NBD、Wexner便秘、PAC-QOL及PAC-SYM评分有明显减少(P<0.05),A、B组间比较差异无统计学意义。见表2~4。
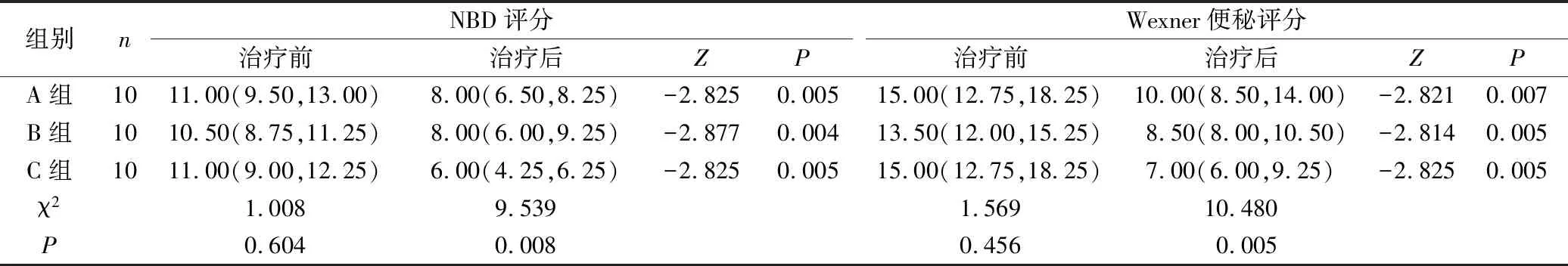
表2 3组NBD及Wexner便秘评分治疗前后比较 分,M(QL, QU)
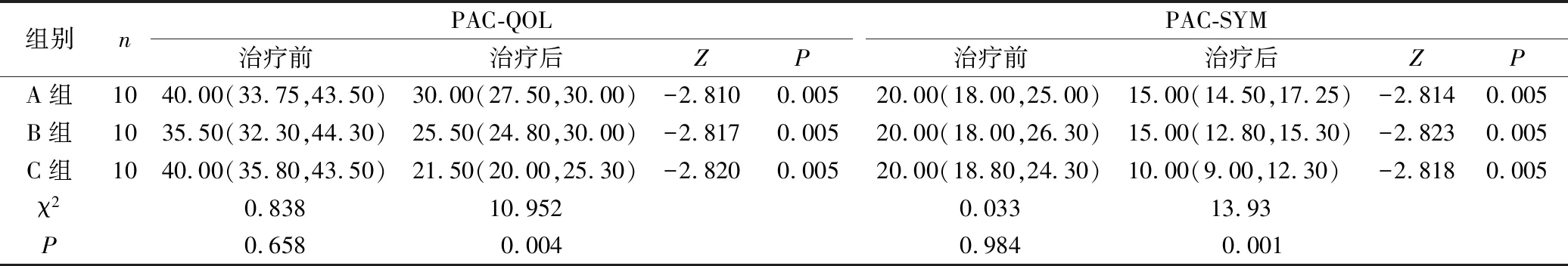
表3 3组PAC-QOL及PAC-SYM评分治疗前后比较 分,M(QL, QU)

表4 3组间NBD、Wexner便秘、PAC-QOL及PAC-SYM评分比较
2.2 3组药物用量比较 治疗前,3组的乳果糖及开塞露用量差异无统计学意义,治疗后,3组的乳果糖及开塞露用量均较治疗前有明显减少(P<0.01);治疗后组间比较:C组与A、B组间对比,乳果糖及开塞露用量有明显减少(P<0.05),A、B组间比较差异无统计学意义。见表5,6。
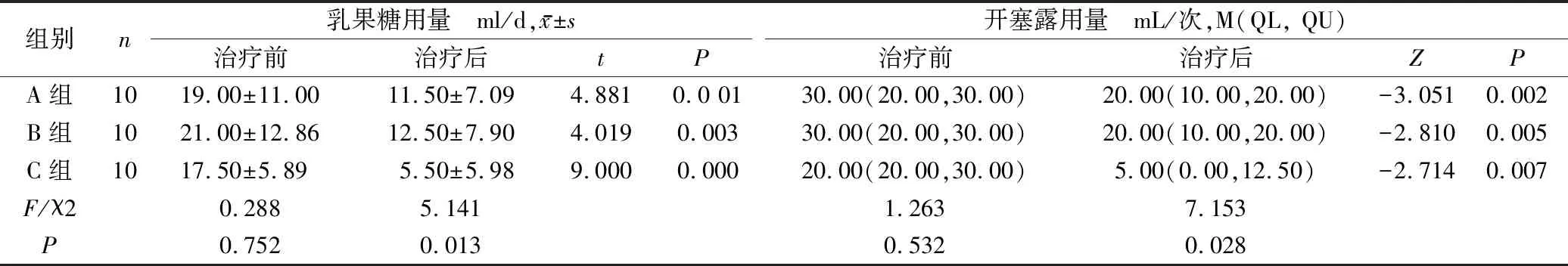
表5 3组治疗前后乳果糖用量和开塞露用量比较
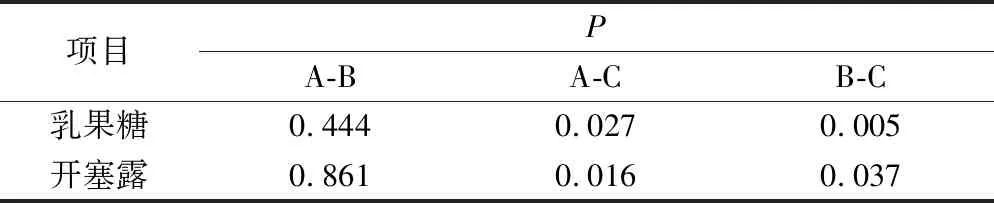
表6 3组间药物用量比较
2.3 3组肛门直肠测压比较 治疗前,3组的肛肠动力数值差异无统计学意义,治疗后,3组的收缩压较治疗前有明显增加(P<0.05),直肠感觉阈值均较治疗前有明显减少(P<0.05),静息压治疗前后比较差异无统计学意义。治疗后,3组间的肛肠动力学数据差异无统计学意义。见表7~8。
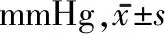
表7 3组静息压和收缩压治疗前后比较
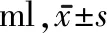
表8 3组初始感觉阈值、急迫感觉阈值以及最大耐受感觉阈值治疗前后比较
3 讨论
完整的排便过程依赖于中枢神经、周围神经及自主神经的协调控制。脊髓损伤后,神经完整性被破坏,排便功能受影响,出现一系列神经源性肠道功能障碍(NBD)的症状[1]。它的严重程度取决于脊髓损伤的水平、程度、病程、患者的年龄、用药等。便秘作为其常见症状,严重影响患者的日常生活,给患者造成极大的心理负担。
目前针对脊髓损伤后NBD的治疗主要包括:饮食调整[10]、行为干预、药物、直肠肛门刺激、灌洗、神经电刺激、骶前根刺激、手术等[11]。但这些方法通常证据水平较低[1],治疗效果有限。近几年生物反馈也被用在脊髓损伤后NBD的治疗中[12],研究表明,生物反馈可运用视觉反馈指导盆底肌进行正确的收缩与放松[13],增强盆底肌肌力,改善盆底肌与腹肌、肛门肌肉的协调运动,同时适当放松盆底肌肉可促进大便向前推进[14-15],从而改善便秘症状。此外,直肠内电刺激可对盆底肌肉及神经产生直接刺激,也可改善局部血流,促进神经再生,同时可以调节骶神经、局部皮肤神经、自主神经对肠道、盆底肌、肛门外括约肌的控制,缩短肠道管理时间,改善肠道功能[16-17]。本研究中,生物反馈电刺激结合了生物反馈和电刺激的功能优势,对患者的排便功能产生了积极的影响,患者NBD评分、Wexner便秘评分、PAC-QOL评分、PAC-SYM评分、乳果糖及开塞露用量较治疗前均有明显减少,提示生物反馈电刺激治疗能改善患者的便秘症状及生活质量。
本研究观察到肠道综合运动疗法也产生了积极的实验效果,这可能是因为:①腹式呼吸可增强膈肌、腹肌力量,增加腹内压,也可促进盆底肌的收缩与放松[18],协调腹肌和盆底肌运动,同时可刺激副交感神经活动,增加结肠运动并改善排便频率[19];②腹部按摩可以沿着结肠走向推动粪便前行,刺激并调整肠道自主神经,使肠道平滑肌紧张度增强,促进胃、肠节奏性收缩与蠕动,促进食物残渣运行,有效缩短结肠转运时间,提高排便频率,改善便秘症状[19-20];③腹肌增强及桥式运动可以增强腹肌肌力,增加腹内压,促进直肠排空,同时也能提高躯干、臀肌及盆底肌力量[18],改善机体运动功能,从而对粪便运输产生积极影响[1];④凯格尔运动可以增强并协调盆底肌的收缩与放松,还可以增强神经对耻直肌的控制,提高肛提肌的力量,改变直肠肛管角来促进排便[17]。通过整体运动疗法的干预,患者各项量表评分、乳果糖及开塞露用量均有明显减少,提示肠道运动疗法对患者排便功能及便秘症状有显著的改善作用。
肠道综合物理疗法结合了生物反馈电刺激和肠道运动疗法的优势,表现出更好的治疗效果。本研究显示,肠道综合物理疗法在NBD评分、Wexner便秘评分、PAC-QOL评分、PAC-SYM评分、乳果糖及开塞露用量方面均较单一的疗法有明显的减小,表明肠道综合物理疗法组比生物反馈电刺激及肠道运动疗法组有更好的改善效果。
本研究也运用肛门直肠压力测试进行评估,肛肠压力测试是在直肠及肛门括约肌处使用压力传感器进行肛门直肠压力评估的检查方法,可以反映肛门括约肌的功能以及肛门与直肠的协调运动[21]。其中静息压力反映了肛门内括约肌张力,主要用于维持静息状态下肛门控制,收缩压反映了肛门外括约肌张力,主要用于维持应激状态下肛门控制。排便阈值反映了直肠肛管对直肠内容量的感知能力,以此判断患者的肠道感觉功能[22]。本研究发现,与治疗前相比,治疗后3组患者的收缩压均有所增加,而直肠感觉阈值明显降低,其原因可能是因为随着治疗,盆底肌及肛门外括约肌、腹肌的肌力及控制力增强,排便协调性增强,排便频率及便秘症状有改善,患者肠道粪便滞留减少,对肠壁的过度牵张减少,肠道感受器敏感性增强。但3组静息压、收缩压、直肠容量感觉阈值的组间比较无明显差异,分析可能与受试者人数少,试验时间较短有关,也可能与脊髓损伤后神经完整性被破坏、排便模式发生变化有关,未来可加大样本量,延长实验周期,进行深入研究。
综上所述,三种方法都对不完全性脊髓损伤患者的便秘症状有改善作用,但肠道综合物理疗法与生物反馈电刺激及肠道运动疗法相比,对脊髓损伤患者便秘的改善作用更明显,可作为不完全性脊髓损伤后便秘的优选治疗方法。

