药物涂层球囊、药物洗脱支架在冠状动脉原位弥漫性长病变治疗中的应用对比观察
周世龙,王喜甲,白雪洋,韩旭飞,李中根,李凌
药物涂层球囊、药物洗脱支架在冠状动脉原位弥漫性长病变治疗中的应用对比观察
周世龙,王喜甲,白雪洋,韩旭飞,李中根,李凌
郑州大学第一附属医院心内科,郑州 450052
对比观察药物涂层球囊(DCB)、药物洗脱支架(DES)在冠状动脉原位弥漫性长病变治疗中的应用效果。接受PCI术治疗的冠状动脉原位弥漫性长病变患者202例,依据介入策略的不同,分为DCB组(68例患者,共72处病变)和DES组(134例患者,共142处病变)。DCB组患者在PCI术中应用DCB治疗,DES组患者在PCI术中应用DES治疗,观察两组术后即刻最小管腔直径(MLD)、术后即刻狭窄程度、术后即刻管腔获得。术后6~12个月内进行冠状动脉造影随访,观察随访时MLD、随访时狭窄程度、晚期管腔丢失、净管腔获得。观察两组术后12个月时并发症发生情况,包括靶病变再狭窄、靶病变血运重建(TLR)、非致死性心肌梗死、全因死亡等。DCB组术后即刻MLD、术后即刻管腔获得均低于DES组(均<0.05),DCB组术后即刻狭窄程度高于DES组(<0.05)。DCB组术后冠状动脉造影随访时晚期管腔丢失低于DES组(<0.05)。两组术后12个月时靶病变再狭窄、TLR、非致死性心肌梗死、全因死亡等并发症相比,均>0.05。PCI术中应用DCB、DES治疗冠状动脉原位弥漫性长病变,DES术后即刻疗效优于DCB,但DCB术后晚期管腔丢失更少。
经皮冠状动脉介入治疗;药物涂层球囊;药物洗脱支架;冠状动脉原位弥漫性长病变
药物洗脱支架(drug eluting stent,DES)在经皮冠状动脉介入治疗(percutaneous coronary intervention, PCI)中的安全性和有效性已经得到广泛的认可,其相较于既往的裸金属支架,可大大降低支架内再狭窄和再次血运重建的风险。但DES被置入到血管壁后也带来了一些新问题,如动脉血管壁的延迟愈合、持续的内膜慢性炎症、损伤支架植入节段的血管舒缩功能、促进新生动脉粥样硬化、延长双联抗血小板治疗的持续时间。药物涂层球囊(drug-coated balloon,DCB)是一种表面涂布有抗增殖药物的半顺应性球囊,当球囊扩张与血管壁接触时,可将涂层的抗内膜增殖药物快速、均匀地释放到局部血管病变处,且不在血管壁内遗留任何金属支撑,有着“介入无植入”的独特优势。目前DCB在支架内再狭窄病变、小血管病变、分叉病变中治疗的有效性和安全性已得到广泛验证及认可[1-4],DCB处理支架内再狭窄病变更是作为I类级别证据被推荐[5]。随着DCB临床应用数量的日趋增多,其在冠状动脉原位病变(指先前未经过介入治疗的血管病变)中的应用指征亦在不断扩展。冠状动脉弥漫性长病变具有血管直径小、累及范围长的特点,常需要多个DES的植入,而支架的长度、数量及多个支架同时串联使用是明确的支架内血栓形成及支架内再狭窄的危险因素[6-8];且当支架的拼接使用长度超过60 mm时,更是与较高的靶病变血运重建(target-lesion revascularization,TLR)率有关[9]。而单纯DCB治疗冠状动脉弥漫性长病变,理论上可以较DES降低靶病变再狭窄及血运重建的风险,且不在血管内遗留金属支撑。目前国内外关于单纯DCB在冠状动脉原位弥漫性长病变中应用的研究报道较少。因此,我们对比观察了DCB、DES在冠状动脉原位弥漫性长病变治疗中的应用效果,现报告如下。
1 资料与方法
1.1临床资料选取2019年5月—2020年5月于郑州大学第一附属医院接受PCI治疗的冠状动脉原位弥漫性长病变患者202例。纳入标准:①经冠状动脉造影检查诊断为冠状动脉原位弥漫性长病变,其诊断根据美国1988年ACC/AHA冠状动脉形态学分类标准:靶血管病变长度>20 mm;②介入策略采用单纯DCB扩张术或单纯DES置入术;③术后成功完成冠状动脉造影复查。排除标准:①支架内再狭窄病变;②急性或慢性完全闭塞病变;③桥血管病变;④严重钙化或扭曲病变;⑤严重肾功能不全(估算的肾小球滤过率<30 mL/min)或严重左心功能不全者(LVEF<30%);⑥有其他严重疾病,预期寿命小于1年者;⑦不能接受阿司匹林和(或)氯吡格雷及替格瑞洛等抗血小板治疗者。所有患者在术前均签署PCI治疗知情同意书。依据所采取介入策略的不同,分为DCB组和DES组。DCB组68例患者,共72处病变,男44例,年龄(58.25 ± 7.21)岁,既往有心肌梗死病史者5例、PCI术史者4例,有吸烟史者25例、饮酒史者12例,合并高血压病者36例、糖尿病者25例,LVEF为60.26% ± 6.89%,三支血管病变者30例,SYNTAX评分为(15.78 ± 5.72)分,参考血管直径为2.70(2.55,3.08)mm,病变长度27.35(23.09,36.07)mm,术前基线最小管腔直径(minimal lumen diameter,MLD)(0.49 ± 0.16)mm,术前直径狭窄程度81.53%(78.94%,84.80%);DES组134例患者,共142处病变,男83例,年龄(59.46 ± 8.95)岁,既往有心肌梗死病史者15例、PCI术史者13例,有吸烟史者52例、饮酒史者18例,合并高血压病者79例、糖尿病者52例,LVEF为60.09% ± 6.69%,三支血管病变者62例,SYNTAX评分为(15.72 ± 4.21)分,参考血管直径为2.75(2.47,2.98)mm,病变长度29.64(25.28,41.85)mm、术前基线MLD(0.47 ± 0.14)mm、术前直径狭窄程度82.44%(78.92%,86.32%);两组患者术前基线资料具有可比性(均>0.05)。
1.2DCB、DES应用方法采用桡动脉或股动脉入路途径,依据病变的特征,由术者选择合适的预扩张球囊,如普通顺应性球囊、半顺应性球囊、棘突球囊、切割球囊等,对靶病变进行预先扩张。DCB组:选用紫杉醇药物涂层球囊,球囊/血管直径比率为0.8~1.0,长度超过预处理区域2 mm以上。将DCB准确定位至靶病变处,使用命名压维持扩张30~60 s,以避免夹层。当残余狭窄过重或出现血流限制型夹层时,则行补救性DES置入。DES组:选用支架/血管直径比率为1.1~1.2的DES,长度超过靶病变3~5 mm。将DES球囊输送至靶血管病变处,准确定位后释放支架,然后使用非顺应性高压球囊后扩张使支架完全贴壁。患者在术前均接受标准的双联抗血小板治疗(dual antiplatelet therapy, DAPT),术后如无禁忌症均终身服用阿司匹林。行DCB扩张术后继续维持DAPT治疗至少6个月,如果患者接受了补救性DES置入,则术后继续维持DAPT治疗至少12个月;行DES置入术后继续维持DAPT至少12个月。
1.3疗效评价
1.3.1术后即刻疗效评价术后即刻应用Allura Xper FD系列定量分析软件进行定量冠状动脉造影(quantitative coronary angiography,QCA)参数测量,包括术后即刻MLD、术后即刻狭窄程度,计算术后即刻管腔获得。术后即刻管腔获得=术后即刻MLD-基线MLD。
1.3.2术后冠状动脉造影随访时疗效评价患者在术后6~12个月的时间内或作为计划内分次血运重建的一部分完成冠状动脉造影随访,测量随访时MLD、随访时狭窄程度,计算晚期管腔丢失、净管腔获得。晚期管腔丢失=术后即刻MLD-随访时MLD,净管腔获得=随访时MLD-基线MLD。
1.4术后并发症观察通过门诊、电话采访、查阅病历的方式对两组患者完成术后为期12个月的临床随访,观察术后12个月时并发症发生情况,包括靶病变再狭窄、TLR、非致死性心肌梗死、全因死亡等。靶病变再狭窄定义为复查造影时靶病变血管直径狭窄程度>50%。

2 结果
2.1两组术后即刻疗效比较两组术后即刻疗效比较见表1。由表1可知,DCB组术后即刻MLD、术后即刻管腔获得均低于DES组(均<0.05),DCB组术后即刻狭窄程度高于DES组(<0.05)。
表1 两组术后即刻疗效比较( ± s)
注:与DES组相比,*<0.05。
2.2两组术后冠状动脉造影随访时疗效比较两组术后冠状动脉造影随访时疗效比较见表2。由表2可知,DCB组术后冠状动脉造影随访时晚期管腔丢失低于DES组(<0.05)。
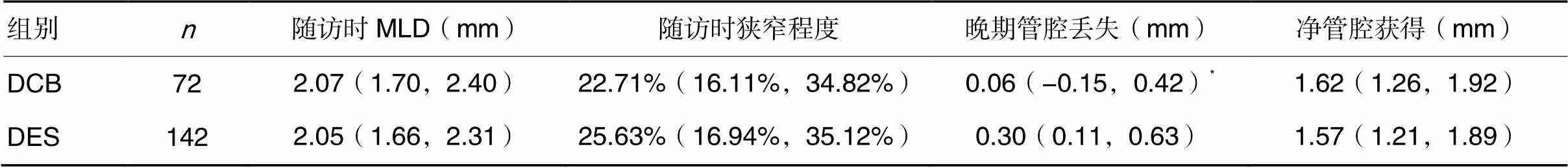
表2 两组术后冠状动脉造影随访时疗效比较[M(P25,P75)]
注:与DES组相比,*<0.05。
2.3两组术后并发症比较两组患者随访期间均无全因死亡发生。DCB组有10例患者共10处病变发生了靶病变再狭窄,其中6例患者共6处病变进行了TLR,无患者出现非致死性心肌梗死;DES组有21例患者共21处病变发生了靶病变再狭窄,其中11例患者共11处病变进行了TLR,1例患者发生了非致死性心肌梗死,两组术后并发症相比,均>0.05。
3 讨论
本研究证实单纯DCB治疗冠状动脉原位弥漫性长病变是一种可选择的相对有效的冠脉介入方式,有着更少的血管晚期管腔丢失和与DES组相似的造影再狭窄率和靶病变血运重建率。DCB治疗冠状动脉原位弥漫性长病变,展示出了良好的术后即刻效果,这与既往研究中DCB处理冠脉原位病变的术后即刻有效性相当[4, 10, 11]。至于DCB组与DES组在术后即刻MLD、术后即刻管腔获得之间的差异,可能与DCB术后靶病变处血管缺乏金属钢梁支撑、血管的急性弹性回缩有关。既往关于对比普通球囊扩张和金属裸支架植入疗效的研究也观察到了这一现象[12]。
在完成造影随访时,我们观察到对于处理冠状动脉原位弥漫性长病变,DCB组相较于DES组有着更少的晚期管腔丢失,表现出DCB在抗内膜增殖方面相较于DES有着更好的优势。DES治疗冠状动脉弥漫性长病变时,为了避免地理缺失所造成的边缘再狭窄,往往要求支架对病变的全覆盖,即“the longer, the better”。然而目前已知支架长度、数量及多支架拼接是明确的支架内血栓形成及支架内再狭窄的危险因素。病变长度越长,所需要置入的支架长度也越长,这往往会导致欠佳的支架置入结果,如支架贴壁不良和支架异位[13]。尽管新一代的DES采用生物相容性更好的聚合物材料、更薄的支架梁和更优的支架结构设计,但仍被观察到支架长度与TLR及支架内血栓形成的风险增加有关[14]。而支架拼接也可导致PCI后相关不良临床事件的风险的增加[8],原因是支架重叠区域会导致更加明显的内膜延迟愈合和持续的炎症反应。而DCB不同于DES,其可快速且均匀地释放抗内膜增殖的药物、保持血管壁原有的自然结构、不损伤血管壁对舒缩刺激的反应、减少新生动脉粥样硬化的风险、缩短DAPT治疗的时间;DCB与既往的普通球囊相似,不在血管内遗留任何金属支撑,不存在支架所固有的血栓形成风险,但较其可进一步降低靶病变再狭窄的风险[15]。
与既往DCB处理冠状动脉原位病变研究一致[16],本研究中DCB组也观察到部分病变存在负性的晚期管腔丢失,即血管的晚期管腔增大。既往已有研究[17]观察到DCB治疗冠状动脉原位病变,由于没有金属结构对血管壁的限制,在晚期可观察到约10%的管腔直径的增加。我们认为可能的机制是,DCB通过其所携带的紫杉醇可以抑制病变部位平滑肌细胞以及内皮细胞的增殖。最近也有研究观察到新一代的西罗莫司药物涂层球囊,虽然在靶病变的晚期管腔丢失方面不劣于紫衫醇药物涂层球囊,但并未观察到有着更多的晚期管腔增大[18],这提示我们在选取药物球囊表面所涂层的药物时要有一定的考量,本研究均选用的是紫杉醇药物涂层球囊。
尽管DCB组有着更少的晚期管腔丢失,但在术后12个月时两组所观察到的靶病变再狭窄率和TLR率相似。原因可能是DCB组更少晚期管腔丢失与欠佳的术后即刻管腔获得相平衡的缘故,从而导致两组间的净管腔获得相当。既往在BELLO等[1]的研究里也观察到在随访6个月时,DCB组虽有着更少的晚期管腔丢失,但DCB组与DES组的MACE发生风险相当;但在随后3年的随访结果表明,DCB组有着更低的MACE发生率[19]。UNVERDORBEN等[20]在比较DCB和DES处理支架内再狭窄病变的研究中也观察到,在6个月的随访时支架内再狭窄发生率差异比较无统计学意义,但在12个月的随访时DCB组MACE发生率更低,且在随后3年的随访时间内,DCB组的优势持续存在。这提示我们在术后的短期内,DCB可有着与DES相媲美的术后效果;而随着更加长期的随访,DCB介入无植入的独特优势则可能被突显出来,更有助于患者的长期临床获益。
本研究为单中心、回顾性、非随机对照的观察性研究,且样本量有限,会产生一定的偏差以及混杂因素的干扰。本研究为排除无症状性冠脉再狭窄的影响及探索组间晚期管腔丢失的差异,严格入选了仅术后接受冠脉造影复查的弥漫性长病变患者;而在临床实践中,实际造影复查人群比例较低,患者往往因经济及依从性原因而未遵医嘱行造影复查,这会产生一定的选择偏倚。因此,将来需要多中心、更大样本的随机对照临床试验去进一步探讨单纯DCB在冠状动脉原位弥漫性长病变中的有效性和安全性。
综上所述,本研究证实单纯DCB治疗冠状动脉原位弥漫性长病变,是一种可供选择的有效的治疗方式,与DES相比有着更少的晚期管腔丢失和相似的靶病变再狭窄率和TLR率。但我们仍然需要进一步的研究去充分评估DCB在此临床情景下的应用。
[1] LATIB A, COLOMBO A, CASTRIOTA F, et al. A randomized multicenter study comparing a paclitaxel drug-eluting balloon with a paclitaxel-eluting stent in small coronary vessels the BELLO (balloon elution and late loss optimization) study[J]. J Am Coll Cardiol, 2012,60(24):2473-2480.
[2] CUI K Y, LYU S Z, ZHANG M, et al. Drug-eluting balloon versus new-generation drug-eluting stent for the treatment of in-stent restenosis: an updated systematic review and meta-analysis[J]. Chin Med J, 2018,131(5):600-607.
[3] BERLAND J, LEFEVRE T, BRENOT P, et al. DANUBIO - a new drug-eluting balloon for the treatment of side branches in bifurcation lesions: six-month angiographic follow-up results of the DEBSIDE trial[J]. Eurointervention, 2015,11(8):868-876.
[4] JEGER R V, FARAH A, OHLOW M A, et al. Drug-coated balloons for small coronary artery disease (BASKET-SMALL 2): an open-label randomised non-inferiority trial[J]. Lancet, 2018,392(10150):849-856.
[5] 韩雅玲.中国经皮冠状动脉介入治疗指南(2016)[J].中华心血管病杂志,2016,44(5):382-400.
[6] D'ASCENZO F, BOLLATI M, CLEMENTI F, et al. Incidence and predictors of coronary stent thrombosis: Evidence from an international collaborative meta-analysis including 30 studies, 221,066 patients, and 4276 thromboses[J]. Int J Cardiol, 2013,167(2):575-584.
[7] LEE C W, PARK D W, LEE B K, et al. Predictors of restenosis after placement of drug-eluting stents in one or more coronary arteries[J]. Am J Cardiol, 2006,97(4):506-511.
[8] RABER L, JUNI P, LOFFEL L, et al. Impact of stent overlap on angiographic and long-term clinical outcome in patients undergoing drug-eluting stent implantation[J]. J Am Coll Cardiol, 2010,55(12):1178-1188.
[9] SHARP A S P, LATIB A, IELASI A, et al. Long-term follow-up on a large cohort of “full-metal jacket” percutaneous coronary intervention procedures[J]. Circ-Cardiovasc Interv, 2009,2(5):416-422.
[10] LATIB A, COLOMBO A, CASTRIOTA F, et al. A randomized multicenter study comparing a paclitaxel drug-eluting balloon with a paclitaxel-eluting stent in small coronary vessels: the BELLO (Balloon Elution and Late Loss Optimization) study[J]. J Am Coll Cardiol, 2012,60(24):2473-2480.
[11] YU X, JI F S, XU F, et al. Treatment of large de novo coronary lesions with paclitaxel-coated balloon only: results from a Chinese institute[J]. Clin Res Cardiol, 2019,108(3):234-243.
[12] BETRIU A, MASOTTI M, SERRA A, et al. Randomized comparison of coronary stent implantation and balloon angioplasty in the treatment of de novo coronary artery lesions (START): a four-year follow-up[J]. J Am Coll Cardiol, 1999,34(5):1498-1506.
[13] KIM B G, CHO S W, KIM D H, et al. Stent length is a contributing factor of suboptimal stent expansion in drug-eluting stents[J]. Kardiol Pol, 2015,73(8):598-605.
[14] KONG M G, HAN J K, KANG J H, et al. Clinical outcomes of long stenting in the drug-eluting stent era: patient-level pooled analysis from the GRAND-DES registry [J]. EuroIntervention, 2021,16(16):1318-1325.
[15] HER A Y, ANN S H, SINGH G B, et al. Comparison of paclitaxel-coated balloon treatment and plain old balloon angioplasty for de novo coronary lesions[J]. Yonsei Med J, 2016,57(2):337-341.
[16] SOGABE K, KOIDE M, FUKUI K, et al. Optical coherence tomography analysis of late lumen enlargement after paclitaxel-coated balloon angioplasty for de-novo coronary artery disease[J]. Catheter Cardiovasc Interv, 2021,98(1):35-42.
[17] KLEBER F X, SCHULZ A, WALISZEWSKI M, et al. Local paclitaxel induces late lumen enlargement in coronary arteries after balloon angioplasty[J]. Clin Res Cardiol, 2015,104(3):217-225.
[18] ALI R M, ABDUL KADER M, WAN AHMAD W A, et al. Treatment of coronary drug-eluting stent restenosis by a sirolimus- or paclitaxel-coated balloon[J]. JACC Cardiovasc Interv, 2019,12(6):558-566.
[19] LATIB A, RUPARELIA N, MENOZZI A, et al. 3-year follow-up of the balloon elution and late loss optimization study (BELLO)[J]. JACC-Cardiovasc Interv, 2015,8(8):1132-1134.
[20] UNVERDORBEN M, VALLBRACHT C, CREMERS B, et al. Paclitaxel-coated balloon catheter versus paclitaxel-coated stent for the treatment of coronary in-stent restenosis: the three-year results of the PEPCAD II ISR study[J]. EuroIntervention, 2015,11(8):926-934.
Comparative observation of drug-coated balloon and drug-eluting stent in the treatment of de-novo diffuse long coronary lesions
,,,,,
,,450052,
To compare and observe the effects of drug-coated balloon (DCB) and drug-eluting stent (DES) in the treatment of de-novo diffuse long coronary lesions.Totally 202 patients with de-novo diffuse long coronary lesions who underwent PCI were divided into the DCB group (68 patients with 72 lesions) and DES group (134 patients with 142 lesions) according to interventional strategy. Patients in the DCB group were treated with DCB only and patients in the DES group were treated with DES only. The differences between the two groups in terms of the immediate postoperative minimum lumen diameter (MLD), stenosis degree and lumen gain were observed. Coronary angiography follow-up was performed within 6 to 12 months after PCI. We observed MLD, stenosis degree, late lumen loss, and net lumen gain at follow-up. The complications of the two groups at 12 months after PCI were also observed, including target lesion restenosis, target lesion revascularization (TLR), nonfatal myocardial infarction, and all-cause death.The immediate postoperative MLD and lumen gain in the DCB group were lower than those in the DES group (all<0.05), and the immediate postoperative stenosis degree was higher in the DCB group (<0.05). The late lumen loss at follow-up in the DCB group was lower than in the DES group (<0.05). No significant differences were found in the rates of target lesion restenosis, TLR, nonfatal myocardial infarction, and all-cause death between two groups (all>0.05).The immediate postoperative efficacy of DES was better than that of DCB in the treatment of de-novo diffuse long coronary lesions, but the late lumen loss of DCB was less.
percutaneous coronary intervention; drug-coated balloon; drug-eluting stent; de-novo diffuse long coronary lesions

10.3969/j.issn.1002-266X.2022.33.004
R541.4
A
1002-266X(2022)33-0013-05
周世龙(1997-),男,在读硕士研究生,主要研究方向为冠脉介入治疗。E-mail: 806007872@qq.com
李凌(1960-),女,硕士,主任医师,主要研究方向为冠脉介入治疗。E-mail: liling63035@sina.com
(2022-06-14)

