低电流密度下不同材质阳极电解生成过硫酸盐研究
张 瑞,张 峰,李红艳,王朝旭,崔佳丽,崔建国
(太原理工大学环境科学与工程学院,山西 太原 030024)
过硫酸盐也称过二硫酸盐(Peroxydisulfate,PDS),其标准氧化还原电位为2.01 V〔1〕,属于强氧化剂〔2-3〕,目前被广泛应用于化工、轻工、环保等领域〔4〕。国内普遍采用电解法,以铂(Pt)或钛基镀铂(Ti/Pt)电极为阳极,在0.8~1.2 A/cm2高电流密度下,电解氧化硫酸盐生产PDS〔5〕,有 时 也 在 阳 极 液 中 添 加PDS 和 硫 氰 酸 铵(NH4SCN),或在阴极液中添加硫酸(H2SO4)以改善PDS的生成,各种电解质浓度总和可达4.0 mol/L〔6-7〕。
研究人员对电解法生成PDS 的机理已有一定研究。W. SMIT 等〔8-9〕认为硫酸根()在Pt 电 极 上被直接氧化从而生成PDS,也有学者提出溶液中的水被电解产生羟基自由基(·OH)氧化是生成PDS 的 重 要 途 径〔10〕。J. KIM 等〔11〕发 现PDS 在BDD(Boron-doped diamond)电极上的生成途径包含2 种,即硫酸氢根()被·OH 氧化〔式(1)、式(2)、式(4)〕和HSO4-在电极上被直接氧化〔式(3)、式(4)〕。

采用电解法制备PDS 时,电极材料对其制备工艺有重要影响〔12〕。Pt氧化能力较强,是较好的阳极材料〔5〕,但工业中使用Pt 电极制备PDS 所需电流密度较高,一般都大于500 mA/cm2,致使Pt 腐蚀速率过快,且电极磨损明显〔13〕,另外,因析氧反应竞争,其电流效率也较低(<75%)〔1,7〕。为改善PDS生成条件,减少电极损耗,研究人员对具有较高析氧电位和·OH 产率的典型阳极在低电流条件下(电流密度<100 mA/cm2)制备PDS的表现进行了考察,结果显示:BDD 阳极氧化H2SO4(>2 mol/L)生成的反应在低电流密度下可达到较高电流效率〔14〕;Ti/PbO2电极析氧电位1.6 V〔15〕,能产生较高浓度的·OH,是氧化常用阳极〔16〕;Ti/SnO2电极氧化还原电位为1.9 V〔17〕,平均氧化效率比Pt电极高5倍〔18〕。
本研究采用H 型反应器,分别以Si/BDD、Ti/SnO2、Ti/PbO2、Ti/Pt 电极为阳极,结合电化学行为分析,针对Na2SO4浓度、电流密度及添加物质等因素,考察4 种阳极在低电流条件下电解生成PDS 的情况,以期为电化学制备PDS 的工业应用提供参考。
1 材料与方法
1.1 试剂
Na2SO4、碘化钾(KI),购自科密欧化学试剂有限公司;NH4SCN、叔丁醇(TBA)、H2SO4,购自天津大茂化学试剂厂;N,N-二甲基-4-亚硝基苯胺(RNO),购自MACKLIN 生化科技有限公司;过硫酸钠(Na2S2O8),购自Aladdin 试剂有限公司。以上试剂均为分析纯,购买后直接使用。实验所用溶液均由超纯水(电阻率为18.2 MΩ·cm)配制。
1.2 实验装置和实验方法
实验在H 型分槽反应器中进行。有效容积均为150 mL 的阳、阴极室间以杜邦质子交换膜Nafion-117隔开。阳极板(25 mm×50 mm)和相同尺寸的阴极板竖直平行分置于阳、阴极室内,浸没高度均为45 mm,极板间距为7 cm。分别选用Si/BDD、Ti/SnO2、Ti/PbO2、Ti/Pt电极为阳极,石墨电极为阴极,其中,Si/BDD 电极购自瑞士Neocoat,Ti/SnO2、Ti/PbO2、Ti/Pt、石墨电极购自合肥正影豪金属材料商行。直流稳压电源MS603D(迈盛,电流0~3 A,电压0~60 V)通过铜制导线和铂制电极夹与电极板连接,以恒定电流密度为电极供电。实验中,H 型反应器置于恒温磁力搅拌器上,连续搅拌确保溶液混合均匀。
采用单因素方法,考察电流密度和电解质浓度对不同阳极电生PDS 的影响;通过向电解液中分别投 加PDS、H2SO4或NH4SCN,考 察PDS、H2SO4以 及NH4SCN 对不同阳极电生PDS 的影响。实验时,每隔10 min 从阳极室取样并对PDS 浓度进行测定,每组实验重复3 次。
1.3 分析方法
使用电化学工作站CHI600E(上海辰华)在三电极体系下测定循环伏安(CV)曲线。测试中分别采用4 种阳极为工作电极,石墨电极为对电极,饱和甘汞电极(SCE)为参比电极,分别以Na2SO4、Na2SO4+Na2S2O8、Na2SO4+NH4SCN 溶液作为电解质溶液,考察4 种阳极在不同电解质条件下的析氧电位和对的氧化能力。测试在20 ℃下进行,扫描速率10 mV/s。测试开始前通入高纯氮气20 min 以去除溶解氧。
通过RNO脱色反应考察4种阳极产生·OH的能力。实验在恒流模式下电解50µmol/LRNO溶液,RNO浓度采用紫外-可见分光光度法测定,检测波长为440 nm。
在考察电生PDS 的影响因素时,以电生PDS 浓度和电流效率(CE)为考察指标,其中电生PDS 浓度采用紫外-可见分光光度法测定,显色剂为KI,检测波长为352 nm〔19〕,电流效率依照式(5)进行计算。

式中:CE——电流效率,%;
n——反应所转移的电子数,取值为2;
C——的浓度,mol/L;
V——电解液体积,L;
F——法拉第常数,取值为96 485 C/mol;
I——电流,A;
t——电解时间,s。
2 结果与讨论
2.1 电化学行为
分别以1.0 mol/L Na2SO4、1.0 mol/L Na2SO4+0.5 mol/L Na2S2O8、1.0 mol/L Na2SO4+2.3 mmol/L NH4SCN溶液作为电解质溶液,测定4 种电极的CV 曲线。考虑到4 种电极自身电位窗口相差较大,设定不同的扫描范围,所得扫描结果见图1。

图1 4 种阳极的CV 曲线Fig.1 CV curves of four anodes
图1(a)中,Si/BDD 电极在2.0 V 左右出现一个微弱氧化峰,该峰可能对应于的直接氧化,这与Mingming ZHOU 等〔20〕发 现 的在Si/BDD 电极 上的氧化反应先于析氧反应发生相吻合,较低的峰电流表明Si/BDD 电极对的直接氧化能力较弱;Ti/PbO2电极在1.3 V 左右出现一个氧化峰,并且在负向扫描的1.0 V 左右出现一个还原峰,这一对氧化/还原峰可能对应于PbO2/PbSO4之间的转化〔21〕,表明无元素掺杂的Ti/PbO2电极稳定性较差,刘元〔22〕也发现了与此类似的现象;Ti/SnO2和Ti/Pt 电极扫描中未见氧化峰。此外,4 种电极析氧电位差异明显,Si/BDD、Ti/SnO2、Ti/PbO2、Ti/Pt 电极析氧电位依次降低,分别为2.3、1.7、1.5、1.4 V。较高的析氧电位有利于减小析氧副反应的发生,提高电催化氧化性能。根据现有PDS 生成机理,·OH 间接氧化SO42-是PDS 生成途径之一。而从CV 测试结果来看,实验所选4 种电极对的直接氧化能力均较弱,电生·OH 的介导氧化可能是发生转化的主要途径。
对比图1(a)、1(b)发现,PDS 的添加使4 种电极的析氧电位均有所提高,Si/BDD 电极的析氧电位增幅最大。析氧电位的提高可能对PDS 的生成效率产生正向促进作用。当采用Si/BDD 和Ti/PbO2电极为工作电极时,观察到响应电流降低的现象,这可能是因为PDS 对·OH 生成的促进作用大于对氧气(O2)生成的抑制作用〔23〕。
由图1(c)可知,添加NH4SCN 后,4 种阳极的电流响应值均有不同程度的增加。作为工业生产PDS常用的去极化剂,NH4SCN 的投加可使电流效率提高10%左右〔24〕。去极化剂可在阳极上优先被氧化以稳定电极电位,其添加仅对O2的生成产生影响,而不影响和的放电〔5〕。但NH4SCN 在减缓O2生成的同时,其SCN-也会被氧化成CN-,造成环境污染〔16〕。
2.2 电解制备PDS 的性能比较
在Na2SO4浓度0.9 mol/L、电流密度60 mA/cm2条件下,4 种阳极电解体系生成PDS 的性能见图2。
由图2 可知,反应期间各体系均有PDS 生成,且生成PDS 的速率均较为稳定。在反应时间为60 min时,Si/BDD 阳极电解体系生成的PDS 浓度可达24.12 mmol/L,远高于其他3 种体系;Ti/SnO2阳极电解体系生成的PDS 浓度为1.40 mol/L,Ti/PbO2和Ti/Pt阳极仅产生微量PDS。值得注意的是,在工业中广泛使用的Ti/Pt 阳极,在600 mA/cm2的电流密度下制备PDS 的电极效率可达90%〔6〕,而在本实验的低电流密度条件下,PDS 生成量极低,远逊于Si/BDD 和Ti/SnO2阳极电解体系的表现。

图2 4 种阳极电解体系生成PDS 的性能比较Fig.2 Performance comparison of PDS generation by four kinds of anode electrolysis systerm
采用RNO脱色实验,在Na2SO4浓度0.9 mol/L、RNO浓度50µmol/L、电流密度60 mA/cm2条件下,通过对比添加TBA 前后RNO 的脱色情况,考察4 种阳极电解体系中·OH 的产率,实验所得RNO 的降解结果见图3。
图3(a)显示,未添加TBA、反应10 min 时,Si/BDD、Ti/PbO2、Ti/Pt、Ti/SnO2阳极反应体系的RNO 降解率分别为96.7%、92.8%、92.5%、91.2%。图3(b)显示,添加1 mol/LTBA对·OH进行猝灭,4种阳极在10 min内对RNO降解率不同程度减少,其中Si/BDD 阳极受到的影响最大,其次是Ti/SnO2、Ti/PbO2和Pt 阳极。RNO 脱色实验中效果较好的Ti/PbO2阳极在电生PDS 中却表现十分逊色,这表明·OH 的产率与PDS 生成量并非正相关。因TBA 主要猝灭电极表面的·OH,对于物理吸附态的·OH 无法深度猝灭,故而TBA 对4 种阳极影响效果不同反映出的可能是·OH 存在形态和反应活性的不同。在经典电催化产生·OH 的理论中,水在电极上放电产生的吸附态·OH 是O2析出反应的主要中间体〔式(6)、式(7)〕,电生·OH 的活性与其和电极材质M 的相互作用密切相关〔式(8)〕,强氧化能力阳极表面M-·OH 相互作用较弱,表面·OH 的吸附焓低,导致析氧反应电化学活性低(即高氧过电位)、反应物氧化活性高(即高反应物氧化电流效率)。一些研究者认为,电极对·OH的吸附性能影响·OH 的氧化能力,电极吸附性由弱至强依次为Si/BDD、Ti/SnO2、Ti/PbO2、Ti/Pt 阳极〔25-27〕,与电解生成PDS 的性能顺序一致。的氧化电位高于析氧电位,在低电流密度条件下,阳极直接氧化的作用较弱,主要被逸散至表面的·OH 所氧化。故对·OH 吸附较弱的Si/BDD 和Ti/SnO2阳极的PDS 生成量高于Ti/PbO2和Ti/Pt阳极PDS 生成量。综上,低电流密度条件下,自由基的形态对于PDS 的生成可能更为重要。

图3 各阳极体系RNO 的降解Fig.3 Degradation of RNO in each anode system

考虑到Ti/PbO2、Ti/Pt 阳极与Si/BDD、Ti/SnO2阳极相比,体系PDS 产量较低,故后续章节着重对Si/BDD 和Ti/SnO2阳极进行研究。
2.3 影响因素研究
2.3.1 Na2SO4浓度
在40 mA/cm2电流密度下,分别以0.3、0.6、0.9 mol/L Na2SO4溶液为电解液,考察Na2SO4浓度对Si/BDD和Ti/SnO2阳极电解体系PDS 生成量和电流效率的影响,结果见图4。

图4 电解质浓度对电解法制备PDS 的影响Fig.4 Effect of electrolyte concentration onthe preparation of PDS by electrolysis
由图4 可知,总体上看,在40 mA/cm2电流密度下,使用Si/BDD 和Ti/SnO2阳极,在实验所选Na2SO4浓度范围内,PDS 生成量和CE 均随Na2SO4浓度的增加而增加,但二者变化规律略有不同。
Si/BDD 为阳极时,当Na2SO4浓度由0.3 mol/L 逐步提高到0.6、0.9 mol/L,反应60 min 时体系生成的PDS 浓 度 由3.33 mmol/L 提 高 到6.99、9.58 mmol/L。在Na2SO4浓度为较低的0.3 mol/L 时,CE 随反应时间延长从8.25%降至5.95%,当Na2SO4浓度增加至0.6、0.9 mol/L,CE 随时间延长表现为先略有下降后逐渐升高,其低点分别出现在反应30 min 和反应20 min时,相应的CE 分别为7.58%和13.24%。
Ti/SnO2为阳极时,当Na2SO4浓度由0.3 mol/L 逐步提高到0.6、0.9 mol/L,反应60 min时体系生成的PDS浓度由0.15 mmol/L 提高到1.14、1.36 mmol/L。在Na2SO4浓度为0.3 mol/L 时,体系CE 随反应时间延长的变化规律与Si/BDD 作为阳极时类似,从0.75%降至0.27%,随着Na2SO4浓度增加,体系CE 逐步升高,且CE 变化幅度较Si/BDD 更小。
从热力学角度分析,Na2SO4浓度的增加使得电解反应向更有利于PDS生成的方向进行,此外电解液中更高Na2SO4浓度带来的浓度差可使向阳极的扩散速率更快,从而使体系PDS生成量和CE更高,且CE更稳定。实际应用中综合考虑经济及能耗等因素,选择在较高浓度0.9 mol/L 的Na2SO4溶液中进行PDS 的制备。
2.3.2 电流密度
电流密度直接影响电化学体系中的电子传递效率。在0.9 mol/L Na2SO4溶液中,分别以Si/BDD 和Ti/SnO2电极为阳极,在较低电流密度范围内考察电流密度对PDS 生成的影响,结果见图5。
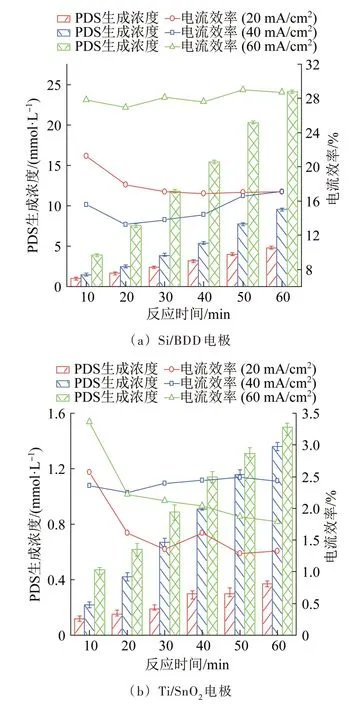
图5 电流密度对电解法制备PDS 的影响Fig.5 Effect of current density on the preparation of PDS by electrolysis
由图5可知,在同一电流密度下,2种电极在60 min的电解过程中,生成的PDS 浓度均随反应时间增加而升高;对于同一电极,电流密度越大,相同反应时间内PDS生成量越多。当电流密度从20 mA/cm2逐步升至40、60 mA/cm2时,反应60 min,Si/BDD 阳极体系生成的PDS浓度由4.78 mmol/L 分别提升至9.58、24.12 mmol/L,Ti/SnO2阳极体系的PDS 浓度则由0.37 mmol/L 提升至1.36、1.5 mmol/L。相较于Si/BDD 阳极体系,Ti/SnO2阳极体系的PDS 生成量增幅明显较低。
由图5 还可以看出,Si/BDD 阳极体系在电流密度为60 mA/cm2时的CE 稳定在27.6%~29.0%,显著高于电流密度为20、40 mA/cm2时的值。这可能源于,电流密度不同导致过硫酸盐合成的主要途径不同,在电流密度低至20、40 mA/cm2时,所施加的电流可能没有越过反应的极限电流,导致某些与过硫酸盐合成直接相关的反应不能发生,致使其电流效率较低〔28〕。此外,随着电流密度从20 mA/cm2升至40 mA/cm2,析氧副反应增强,产生的O2部分附着于电 极 表 面,也 会 使氧 化 受 到 抑 制〔29〕。相 较 于Si/BDD 阳极,Ti/SnO2阳极电解过程中的CE 较低,且随着电解的进行,CE 持续下降,这可能是由于随着电解的进行,Ti/SnO2阳极活性逐渐降低。
一般而言,氧过电位与电流密度正相关。电流密度越高,氧过电位越高,越有利于PDS 的生成和对O2析出反应的抑制,表现出更高的电流效率;而在低电流密度时,析氧反应所需的氧化还原电位较PDS生成反应所需更低〔30〕,导致了较低的电流效率。
实验中还观察到,当Si/BDD 阳极电解体系的电流密度从20 mA/cm2增至40 mA/cm2时,反应60 min时PDS 生成浓度仅增加了4.8 mmol/L,且此时的电流效率总体也略低于电流密度为20 mA/cm2时。除了随电流密度增大,析氧副反应增强外,电解池温度升高导致部分生成的PDS 分解也是可能造成这一现象的原因[14]。Jingju CAI 等〔31〕发现,在20 ℃和30 ℃下电解2 h,PDS 的生成量较9 ℃下分别降低12%和23%。尽管电流密度从40 mA/cm2增至60 mA/cm2时欧姆热效应增强,但较高电流密度下通过电子转移被直接氧化的速率也增强〔32〕,导致欧姆热效应对不同电流密度下生成PDS 的影响不同。因此,实际工业应用中,为获得更高的电流效率和PDS 产量而选择在较高电流密度下进行电解时,应对电解液热稳定性进行控制。
2.3.3 PDS 和H2SO4的添加
为提升电解液电导率,PDS 的工业生产中常在电解液中添加PDS 和H2SO4,二者不引入新的杂质,便于后续生产中的提纯。在电流密度为60 mA/cm2,电解质为0.9 mol/L Na2SO4溶液条件下,分别以Si/BDD、Ti/SnO2为阳极,仅向阳极液中添加不同浓度PDS,或仅向阴极液中添加500 mmol/L H2SO4,考察PDS 和H2SO4对PDS 生成的影响,结果见图6。

图6 阳极/阴极电解液中投加PDS/H2SO4对电解法制备PDS 的影响Fig.6 Effect of adding PDS/H2SO4 to anode/cathode electrolyte on the preparation of PDS by electrolysis
由图6 可知,仅向阳极液中添加400 mmol/L PDS时,电解60 min 后,Si/BDD 和Ti/SnO2阳极电解反应的PDS 生成量较未添加时分别提高了20.2% 和5.3%。结合CV 测定结果,阳极液中PDS 的添加可使电极析氧电位升高,有利于减少析氧副反应的发生,同时Si/BDD 阳极可将吸附在其表面的PDS 转化为PDS*进而促进·OH 的生成〔23〕,这可能是PDS 生成量提高的原因。同时,实验中也观察到,与未添加PDS 相比,2 种阳极反应所需的槽电压随PDS 的增加而略有下降,最高降幅达1 V。
由图6 还可知,仅向阴极液中添加0.5 mol/L H2SO4对于2 种阳极体系PDS 的生成量均没有明显改善,但其有助于降低电解时的槽电压。H2SO4的加入增加了电解液的离子强度,实验过程中观察到,与未添加H2SO4相比,2 种阳极起始电压下降值均达4 V,反应60 min 时的电压降低幅度也有2 V 左右。M. DOYLE 等〔33〕也 发 现H+在 水 中 和 穿 过Nafion117阳离子选择渗透膜时电导率都优于Na+。
综上可知,在选用Si/BDD 和Ti/SnO2电极作为阳极的工业应用中,可以通过向阴极液中添加H2SO4和向阳极液中添加PDS 来减小电解所需槽电压,以此节约能耗,提高产量。
2.3.4 NH4SCN 的添加
在电解制备PDS 的反应中,阳极发生的析氧副反应是限制Na2SO4氧化的重要因素,为抑制O2的生成,一般采取在阳极液中添加析氧抑制剂的措施。已有研究表明,析氧抑制剂可降低析氧速率,抑制O2生成,且对PDS 的生成无负面影响〔5〕。
在电流密度为60 mA/cm2,电解质为0.9 mol/L Na2SO4溶液条件下,向阳极液中添加2.3 mmol/L NH4SCN,考察NH4SCN 的投加对阳极电生PDS 的影响,结果见图7。
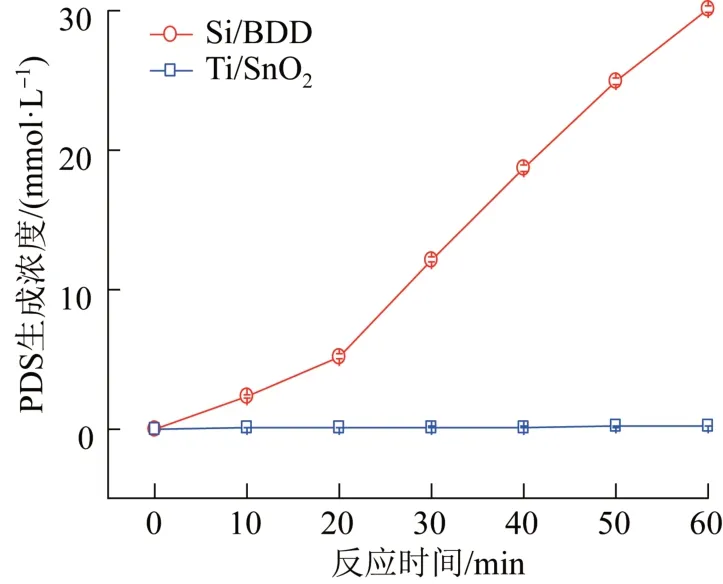
图7 阳极电解液中投加NH4SCN 对电解法制备PDS 的影响Fig.7 Effect of adding NH4SCN into the anode electrolyte on the preparation of PDS by electrolysis
由图7 可知,在选用Si/BDD 电极作为阳极时,在60 min 的电解过程中,体系所生成的PDS 的浓度逐渐增加至30.17 mmol/L,与不添加NH4SCN 时相比增加了6.05 mmol/L,与此同时,经测定体系的电流效率提高了25.10%。这表明NH4SCN 的添加对于Si/BDD 阳极电生PDS 有促进作用。结合图1(c)的CV 测定结果,分析得到NH4SCN 对析氧电位的提升和对析氧副反应的抑制可能是Si/BDD 阳极电解体系PDS 生成量增加的原因。而对于Ti/SnO2阳极,在添加NH4SCN 后,虽然观察到反应时阳极表面气泡生成明显减少,但实际得到的PDS 产量却略有下降。此外,在相同反应条件下,以Ti/PbO2和Ti/Pt 电极作为阳极进行实验时也观察到阳极气泡生成减少以及PDS 生成量增加不显著的现象。这表明对于Ti/SnO2、Ti/PbO2和Ti/Pt 阳 极 来 讲,在 较 低 的 电 流 密 度和电解质浓度下,析氧副反应不是限制PDS 生成的主要因素,且NH4SCN 在电极表面的吸附还可能减少电极活性位点,使得NH4SCN 的添加对于提升PDS 生成量的效果较差。因此,工业上在低电流密度条件下制备PDS 时,当选用Si/BDD 电极作为阳极且在对生成的PDS 纯度要求不高的情况下,可以考虑通过添加NH4SCN 来增加PDS 产量,而对于其他3 种阳极则应慎重考虑NH4SCN 的使用。
2.4 实验条件优化研究
为了探究电解过程中主要的实验因素对生成PDS 的影响程度,选择前期实验效果最佳的Si/BDD电极作为阳极,以Na2SO4浓度(A)、电流密度(B)、外加PDS 浓度(C)3 个主要影响因素设计正交实验,实验因素和水平见表1。
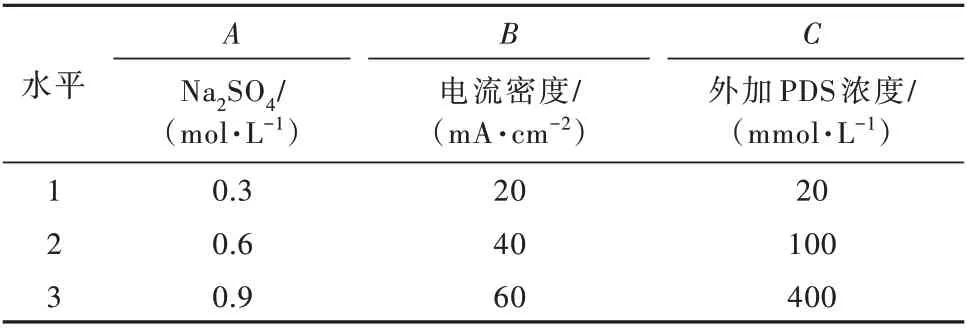
表1 正交实验因素水平表Table 1 Orthogonal test factor level table
表2 为正交实验结果。由表2 可得,各因素对电解生成PDS 的影响的显著性顺序为:电流密度>Na2SO4浓度>外加PDS 浓度,最佳PDS 生成量条件是B3A3C3,在该实验条件下,PDS 生成浓度可达29.95 mmol/L。

表2 正交实验结果Table 2 Orthogonal test results
3 结论
研究采用H 型反应器在恒流电解反应模式下探究了Si/BDD、Ti/SnO2、Ti/PbO2、Ti/Pt 4 种阳极在中性条件下的电化学行为,以及低电流密度条件下电解生成PDS 过程中电解质浓度,电流密度,PDS、H2SO4及NH4SCN 的投加对PDS 生成的影响,得到如下结论:
(1)CV 曲线中,Si/BDD 阳极的电势窗口最宽,之后依次是Ti/SnO2、Ti/Pt 和Ti/PbO2阳极。Si/BDD 阳极可以直接氧化,但氧化能力较弱,而其余3 种阳极均未见的氧化峰。在低电流密度条件下,4 种阳极生成PDS 的主要途径可能是通过电解水产生的·OH介导了的氧化。(2)在低电流密度的电解条件下,Si/BDD 阳极制备PDS 的效果明显优于Ti/SnO2、Ti/Pt 和Ti/PbO2阳极。对于Si/BDD 阳极,Na2SO4浓度的增加有利于PDS 的生成,同时PDS 的生成量也随电流密度的增加而增加;在低电流密度范围内,适度提升电流密度可获得更高且更稳定的电流效率。阴极液中添加H2SO4有利于降低外加电压,阳极液中添加PDS 有利于提升PDS 生成量。NH4SCN 的加入可以抑制析氧副反应,促进的氧化。

