g-C3N4的制备及其光催化降解诺氟沙星的机理及产物毒性研究
田 倩,吕 勇,李晨光,张延蕾,李锋民,4
(1.中国海洋大学环境科学与工程学院,近海环境污染控制研究所,山东 青岛 266100;2.中国海洋大学海洋环境与生态教育部重点实验室,山东 青岛 266100;3.中海油天津化工研究设计院有限公司,天津 300131;4.青岛海洋科学与技术试点国家实验室,海洋生态与环境科学功能实验室,山东 青岛 266071)
诺氟沙星(Norfloxacin,NOR)是第三代氟喹诺酮类抗生素,已被广泛用于人类医疗、畜牧业及水产养殖等〔1〕。NOR 通常在生物体内代谢不完全,60%~90%的NOR 以原药或代谢物的形式经排泄进入环境,并随自然水循环迁移到地表水、地下水甚至饮用水中〔2-3〕。长期存在的抗生素污染会导致细菌耐药性的形成和耐药基因的传播,威胁人类健康和生态平衡。光催化氧化技术具有绿色、高效且成本较低的优势〔4-6〕,在抗生素的处理方面展现出良好应用前景。在光催化剂的选择方面,类石墨相氮化碳(g-C3N4)较传统的TiO2、ZnO 等光催化剂具有更高的太阳能利用率且化学性质稳定、易于合成,受到研究者的广泛关注〔7-8〕。
光催化氧化通常难以完全矿化有机污染物,母体化合物经光催化降解后会生成多种降解产物〔1〕,甚至可能生成有毒副产物危害环境。Han GONG等〔9〕发现使用CoFe2O4/TiO2作催化剂在紫外光下催化降解磺胺甲唑会生成有毒中间产物磺胺,其会显著抑制藻类生长。此外,光源类型会影响光催化反应机制〔10〕,可能导致抗生素的降解途径和产物种类不同,从而引发不同的毒性效应。然而,目前有关g-C3N4基光催化剂去除水中抗生素的研究多致力于通过形貌调控、元素掺杂、异质结构建等方法改性催化材料以提高对污染物的去除能力,侧重于对合成材料进行理化性质表征分析及催化性能比较〔11-13〕,而对于抗生素的降解途径及产物毒性等研究相对较少。基于以上问题,本研究通过热聚合法合成g-C3N4纳米片,探究其分别在模拟阳光和可见光下光催化降解典型抗生素NOR 的性能和机理,并采用毒性预测软件(T. E. S. T)评估NOR 降解过程中中间产物的毒性,为光催化技术应用于NOR 的污染治理提供参考。
1 材料与方法
1.1 主要试剂和仪器
试剂:诺氟沙星(C16H18FN3O3,纯度≥98%),购于美国Sigma-Aldrich 公司;甲醇、乙腈均为色谱纯,购于德国Merck 公司;甲酸,色谱纯,购于美国Thermo Fisher 公司;5,5-二甲基-1-吡咯啉氮氧化物(DMPO,纯度≥97%),2,2,6,6-四甲基哌啶氧化物(TEMPO,纯度≥97%),均购于上海阿拉丁;其他试剂如尿素、无水乙醇、异丙醇、草酸铵、L-抗坏血酸等均为分析纯,购于国药集团;实验用水为超纯水(18.2 MΩ·cm)。
仪器:XPA-7 型光化学反应仪,南京胥江机电厂;TOC-Vpcn 总有机碳分析仪、UV-3600 紫外-可见漫反射光谱仪,日本岛津;1260 型高效液相色谱、1290-6430 型高效液相色谱-质谱联用仪,美国安捷伦;SU8010 扫描电子显微镜、H-7650 透射电子显微镜,日本日立;D8 X 射线衍射仪,德国布鲁克;JES FA200 电子顺磁共振波谱仪,日本电子株式会社。
1.2 g-C3N4纳米片的制备及表征
以尿素为前驱体,通过热聚合法合成g-C3N4纳米片。称取10 g 尿素于氧化铝坩埚中,将其置于管式炉,在N2氛围下以5 ℃/min的速率升温至550 ℃并保持4 h,降温后取出,经研磨、无水乙醇洗涤、离心分离并在80 ℃下烘干后得到g-C3N4纳米片。
采用X 射线衍射仪(XRD)对所制备的g-C3N4纳米片的晶体结构进行分析;采用扫描电镜(SEM)和透射电镜(TEM)观察g-C3N4纳米片的表面形貌;采用紫外-可见漫反射光谱测试g-C3N4纳米片的光学性能。
1.3 g-C3N4纳米片光催化降解NOR 的研究
选用350 W 长弧氙灯作为模拟阳光辐照源(λ≥290 nm),添加420 nm 滤光片后作为可见光辐照源(λ≥420 nm)。溶液中NOR 的初始质量浓度为10 mg/L,用0.1 mol/L 的盐酸和氢氧化钠溶液调节溶液pH 至7 左右。根据预实验结果,设置催化剂g-C3N4纳米片在模拟阳光下投加质量浓度为0.2 g/L,可见光下投加质量浓度为0.4 g/L,设置未添加g-C3N4纳米片的NOR 溶液作为空白对照,与实验组同步在光照下反应。光催化反应前,在黑暗条件下磁力搅拌30 min 以达到吸附平衡,随后打开光源开始反应并定时取样。所取样品在13 000 r/min 的转速下离心10 min 后过0.22 µm 聚四氟乙烯滤膜,用于后续检测。采用猝灭实验和电子顺磁共振技术(EPR)鉴定活性物种用于分析降解机理。
1.4 分析测试方法
采用HPLC 测定NOR 浓度。色谱柱为Zorbax Eclipse Plus C18 柱(D4.6 mm×100 mm,3.5 µm),柱温30 ℃;流动相由甲醇、乙腈和0.01 mol/L 草酸溶液(体积比17∶8∶75)组成,流速1 mL/min;进样体积为5 µL;紫外检测器波长为280 nm。
采用HPLC-MS测定NOR 经光催化降解后产物的种类。液相色谱柱为Waters Symmetry C18柱(D2.1 mm×150 mm,5µm),柱温25 ℃;进样体积10µL;流速恒定为0.2 mL/min;使用体积分数为0.1%的甲酸水溶液作为流动相A,乙腈作为流动相B;采用梯度洗脱模式对降解产物进行分离,20 min 内流动相B 由5%(体积分数,以下同)升至100%,保持3 min后在1 min内降回5%,并平衡6 min。MS 采用ESI 正离子模式,毛细管电压4 000 V,雾化器压力241.3 kPa,离子源温度350 ℃,干燥气(N2)流量9.0 L/min,在质荷比(m/z)为50~600 范围内全扫描;确定产物离子后,在MS/MS 模式下进样得到产物的二级质谱图;碰撞能参数根据需求调节。
采用TOC-Vpcn 总有机碳分析仪在NPOC 模式下测定光催化降解过程中反应液的总有机碳(TOC)。
2 结果与分析
2.1 g-C3N4纳米片的表征
2.1.1 g-C3N4纳米片的XRD 分析
XRD 用于明确材料的晶型结构,从图1 所示的g-C3N4纳米片的XRD 中可以观察到材料分别在2θ为13.1°和27.6°处有2 个主要衍射峰,其中2θ=13.1°对应g-C3N4的(100)晶面,表示3-s-三嗪结构在层内重复排列〔14〕;2θ=27.6°对应g-C3N4的(002)晶面,表示类石墨结构以0.33 nm 的层间距堆叠〔15〕。该结果表明实验成功制备得到了g-C3N4材料。

图1 g-C3N4纳米片的XRDFig.1 XRD patterns of g-C3N4 nanosheets
2.1.2 g-C3N4纳米片的表面形貌分析
采用SEM 和TEM 观察g-C3N4纳米片的表面形貌,结果见图2。

图2 g-C3N4纳米片的SEM(a)和TEM(b)Fig.2 SEM(a)and TEM(b)of g-C3N4 nanosheets
由图2(a)可知,g-C3N4由大量不规则的弯曲层状结构堆积而成,其表面分散有细小孔道,这是由于尿素在高温煅烧下释放出部分氨气造成的。材料蓬松多孔的结构会增加光催化剂与污染物的接触机会,并提供更多的光催化活性位点,一定程度上可促进光催化反应进程〔16〕。图2(b)的TEM 图像清晰显示出材料边缘的微观薄片结构,证实了g-C3N4纳米片的存在。
2.1.3 g-C3N4纳米片的光吸收性能
采用紫外-可见漫反射光谱测试g-C3N4纳米片的光学性能,结果见图3。

图3 g-C3N4纳米片的紫外-可见漫反射光谱及(αhν)1/2-hν曲线Fig.3 UV-Vis spectra and corresponding(αhν)1/2-hν plot ofg-C3N4 nanosheets
由图3 可知,g-C3N4纳米片的最大光吸收边缘可延伸至可见光,表明其具有可见光响应能力。通过Tauc 公式〔式(1)〕〔17〕估算g-C3N4纳米片的带隙宽度,约为2.52 eV,显著低于块状g-C3N4的带隙宽度2.75 eV〔18〕,并接近苏跃涵等〔19〕所制备的二维超薄g-C3N4的带隙宽度,表明该材料具有优异的光吸收能力及较高的光催化潜力。通过式(2)和式(3)〔20〕可得所制备的g-C3N4纳米片的价带和导带电势分别为1.48 eV 和-1.04 eV,此数据用于后续降解机理分析。
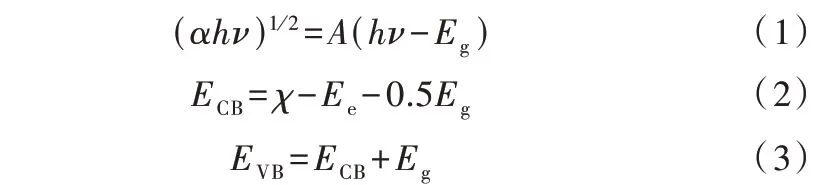
式中:α——吸光系数;
h——普朗克常数,取4.135 667 696 9×10-15eV·s;
ν——光的频率,s-1;
A——材料特征常数;
Eg——半导体材料的禁带宽度,eV;
EVB——价带的边缘电势,eV;
ECB——导带的边缘电势,eV;
Ee——氢原子自由电子的能量,约为4.5 eV;
χ——半导体的电负性,对于g-C3N4材料取值为4.72 eV。
2.2 g-C3N4 纳米片在不同光源下催化降解NOR 的性能
分别在模拟阳光和可见光下考察g-C3N4纳米片对NOR 的光催化降解性能,并对其动力学进行探究,结果见图4。
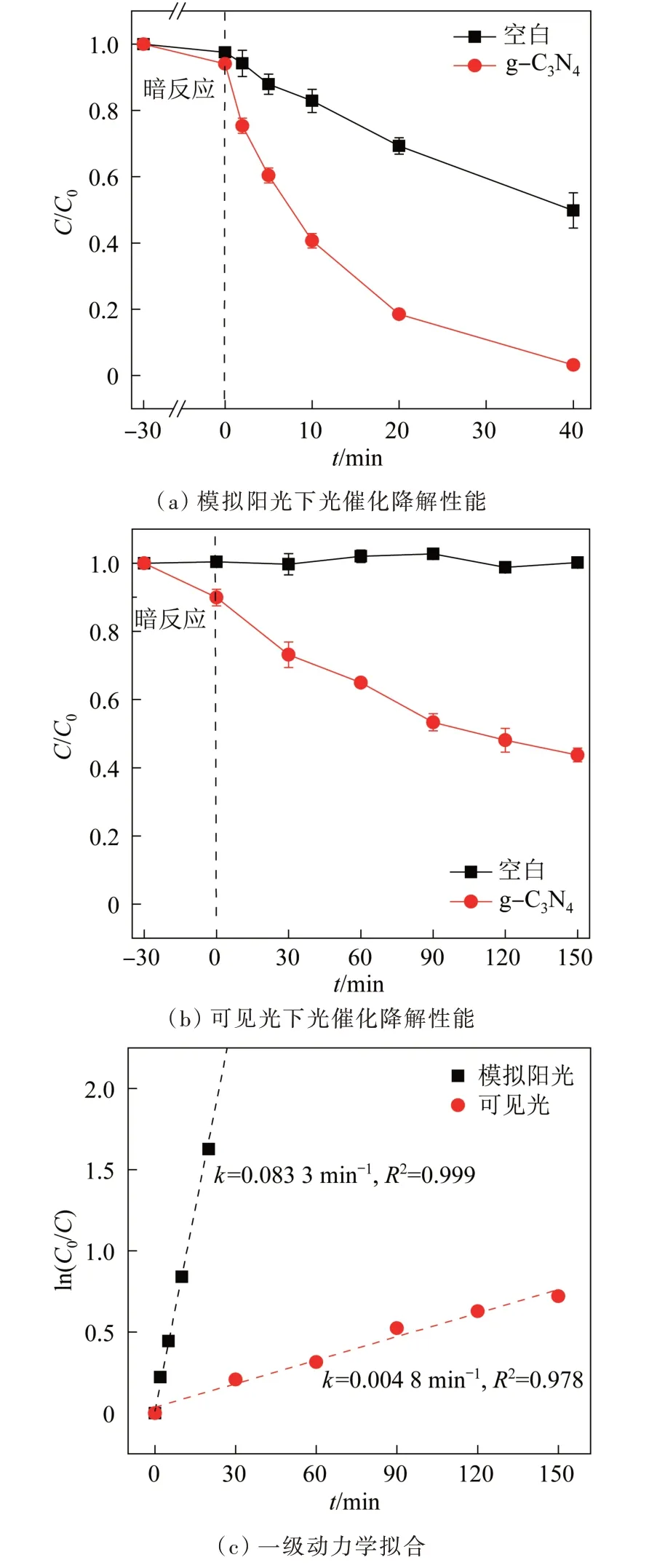
图4 g-C3N4纳米片对NOR 的光催化降解性能Fig.4 Photocatalytic degradation of NOR by g-C3N4 nanosheets
实验开始前,进行30 min 的暗吸附,g-C3N4与NOR 可在该时间内达到吸附平衡,之后在光源辐照下对NOR 进行降解。由图4(a)可知,未加g-C3N4时,NOR 在模拟阳光辐照下可发生降解,反应40 min 后其降解率为52%,添加g-C3N4后,NOR 被迅速降解,反应40 min 后NOR 去除率可达97%。由图4(b)可知,未加g-C3N4时,NOR 在可见光下较为稳定,基本不发生降解,添加g-C3N4后,NOR 发生降解,反应150 min 后NOR 去除率为57%。
图4(c)显示了NOR 在2 种光源下降解的准一级动力学模型拟合结果。如图4(c)所示,2 种光源下拟合模型R2均大于0.97,拟合结果良好;模拟阳光下,NOR 的反应速率常数k=0.083 3 min-1,约为可见光下的17 倍,表明g-C3N4在模拟阳光下对NOR 降解的光催化效率远高于可见光下。
为了解NOR 的矿化情况,实验测定了降解过程中溶液TOC 的变化,结果如图5 所示,在NOR 溶液中添加g-C3N4并分别经模拟阳光和可见光照射后,TOC 皆呈缓慢降低趋势,180 min 后TOC 去除率分别为15.5%和12.8%,表明光催化体系对于NOR 的矿化能力较弱,溶液中仍存在较多未矿化的有机产物。

图5 光催化体系降解NOR 过程中TOC 的变化Fig.5 Changes of TOC during the degradation of NOR by photocatalytic system
2.3 g-C3N4在不同光源下催化降解NOR 的机理
采用异丙醇、L-抗坏血酸和草酸铵分别作为羟基自由基(·OH)、超氧自由基(O2·-)和光生空穴(h+)的猝灭剂进行猝灭实验以探究g-C3N4光催化降解NOR 过程中的主要活性物种及其对NOR 降解的贡献〔21〕。图6(a)、6(b)分别显示了添加不同猝灭剂对g-C3N4在模拟阳光和可见光下催化降解NOR 的影响,之后通过准一级动力学方程拟合,得到了各实验组的反应速率常数,结果见图6(c)。

图6 猝灭剂对光催化降解NOR 的影响Fig.6 Effect of quencher on photocatalytic degradation of NOR
由图6(a)可知,在模拟阳光下各猝灭剂的加入导致NOR 的光催化反应速率呈现不同程度降低。光照40 min 后,添加异丙醇、草酸铵和L-抗坏血酸的实验组相比于未添加猝灭剂的对照组,NOR 降解率分别降低了2.9%、14.7%和41.7%。这说明模拟阳光下,·OH、、h+均参与反应,且其对NOR 降解的贡献率排序为>h+>·OH。由图6(b)可知,在可见光下,L-抗坏血酸的添加基本抑制了NOR 的降解,而其他猝灭剂的添加对降解反应影响甚微,表明是g-C3N4在可见 光 下催化降解NOR 的主要活性物种。
为进一步探究反应机理,实验采用EPR 技术测定了g-C3N4在不同光源下所产生的活性物种。DMPO 用于在水和甲醇中分别捕获·OH 和,TEMPO 作为自旋标记物在乙腈中表征h+的产生〔22-23〕,实验结果见图7。

图7 模拟阳光(a~c)和可见光(d~f)下活性物种加合物的EPRFig.7 EPR spectra of active adducts under simulated sunlight(a-c)and visible light(d-f)
由图7(a)~7(c)可知,g-C3N4在模拟阳光辐照下产生了典型的·OH 四重信号峰和六重信号峰,且信号强度随光照时间延长而增强,表明模拟阳光辐照下体系中·OH 和不断生成。TEMPO 的信号强度随光照时间延长而减弱,证明体系中也在不断产生h+。
图7(d)~7(f)显示,在可见光辐照下,仅有相对较弱的和h+信号,无明显的DMPO-·OH 加合物信号,表明体系中产生了较少的和h+,且·OH 没有检出。
结合g-C3N4纳米片的光学性质和能带结构分析光催化体系对NOR的降解机理。当g-C3N4受到波长小于492 nm 的光辐照时,电子发生跃迁产生光生电子空穴对,氧化性空穴可直接氧化污染物,且氧化能力与催化剂价带边位置有关,同样导带边位置决定了电子的还原能力大小〔10,24〕。由2.1.3 节可知,g-C3N4的导带电势为-1.04 eV,比O2/(-0.33 eV)的还原电势更负〔25〕,故其可以捕获氧分子生成以发挥氧化作用;g-C3N4的价带电势为1.48 eV,低于·OH/H2O(+2.73 eV)和·OH/OH-(+1.99 eV)的还原电势〔26〕,故空穴不能直接氧化H2O或OH-生成·OH。与此分析不同的是,从EPR 图谱上可观察到g-C3N4在模拟阳光辐照下产生了明显的·OH四重信号峰,所以·OH 生成的可能路径为:

即光生电子(e-)还原氧气分子产生过量的,再通过质子化反应生成·OH,从而参与氧化还原反应〔27〕,此过程在王盈霏等〔28〕的研究中也有报道。在可见光辐照下,g-C3N4没有明显的·OH 信号峰,且EPR 结果显示h+和O2·-的特征峰信号也较弱,推断在可见光下可能没有足够的生成并与H+、e-反应,以至于无法生成·OH,或者在10 min 的辐照时间内·OH 的生成量较少而不足以被捕获。对比不同光源下NOR 的光催化降解性能可知,g-C3N4在模拟阳光及可见光下对NOR 的光催化降解效率有所差别的原因可能在于体系所产生的活性物种种类和数量有所差异。
2.4 g-C3N4光催化NOR 的降解途径分析
该研究通过HPLC-MS/MS 测定了g-C3N4纳米片在2 种光源下光催化降解NOR 的中间产物。依据产物质荷比,在可见光下鉴定出11 种产物,在模拟阳光下共鉴定出20 种产物(含可见光下的11 种),以各产物质荷比对其命名,如质荷比为318,则命名为P318。依据产物结构,推测NOR 在模拟阳光和可见光下的降解途径,结果分别见图8 和图9。

图8 模拟阳光下g-C3N4光催化NOR 的降解产物及途径Fig.8 The photocatalytic degradation products and pathways of NOR by g-C3N4 under simulated sunlight
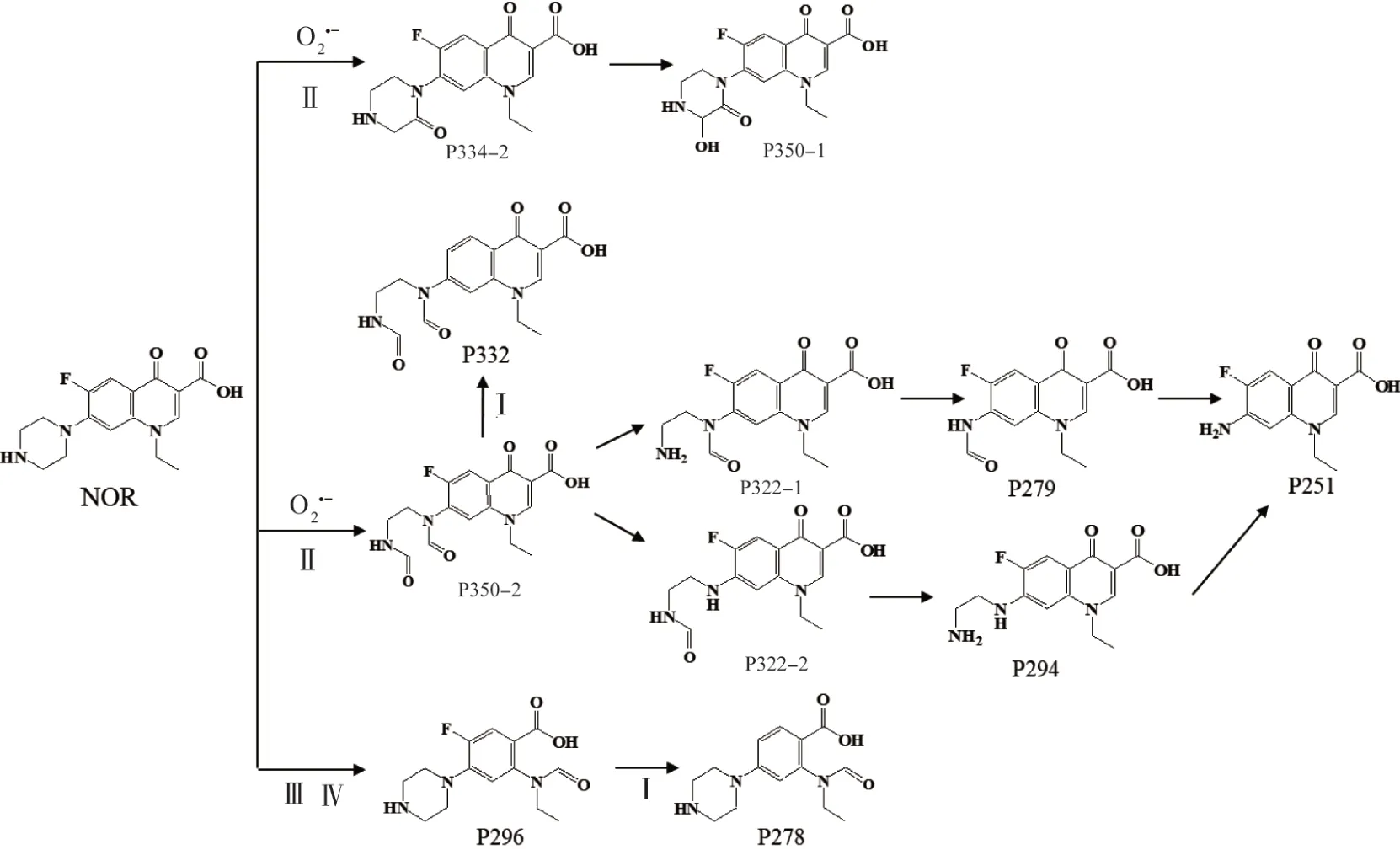
图9 可见光下g-C3N4光催化NOR 的降解产物和途径Fig.9 The photocatalytic degradation products and pathways of NOR by g-C3N4 under visible light
依据降解途径将NOR的降解总结为4种反应机理。
机理Ⅰ:脱氟反应。如模拟阳光下NOR→P318,是通过NOR 苯环上的氟被羟基基团所取代而进行,P350-2→P332,P251→P233,P350-1→P334-3 则是通过C—F键的直接断裂而进行;而可见光下无羟基取代脱氟反应发生,仅P350-2→P332和P296→P278 是通过C—F 键的直接断裂进行,这可能是由于g-C3N4在可见光下不能生成·OH,从而不能通过间接加成或取代反应降解NOR。
机理Ⅱ:哌嗪环转化。在模拟阳光下该机理的反应类型较为丰富,如NOR→P334-2→P350-1 是通过哌嗪环的羰基化、羟基化进行的,之后产物可再一步分解,同时NOR 也可以通过开环、结构重组及脱羧等反应生成各种哌嗪环氧化中间体〔29-30〕,如NOR→P350-2→P322-1→P293→P279→P251,而P251脱氨基后又转化为P236,完全脱除哌嗪环;在可见光下,该机理下的反应类型及产物种类明显减少,NOR经哌嗪环转化最终生成了产物P350-1和P251,未能生成完全脱去哌嗪环的转化产物。
机理Ⅲ和Ⅳ分别为脱羧反应和喹诺酮环裂解,在2 种光源下这2 个机理的反应路径一致,皆由NOR→P296 体现。
以上4 种机理中,哌嗪环转化是NOR 降解的主要机理,通过产物结构和降解机理判断NOR 主要受攻击;同时大多数降解产物保留了NOR 的核心苯环结构,反映出该苯环结构较为稳定,难以被破坏〔31〕。
虽然g-C3N4在可见光下光催化降解NOR 的效率相对较低,但其生成的次级产物较少;而在模拟阳光下NOR 降解效率提高的同时,涉及到的反应类型也趋于多元化,降解过程中生成了更多种类的反应中间体。这些中间体的毒性如何、是否存在环境风险仍需进一步探究。
2.5 g-C3N4光催化NOR 的降解产物毒性评估
采用美国EPA开发的毒性评估软件工具(T.E.S.T),并选取急性毒性(Acute toxicity)、生物蓄积因子(Bio⁃accumulation factor,BCF)、发育毒性(Developmental toxicity)、Ames致突变性(Mutagenicity)作为毒理学指标对NOR降解产物进行毒性评估预测〔32〕,评估结果见图10。
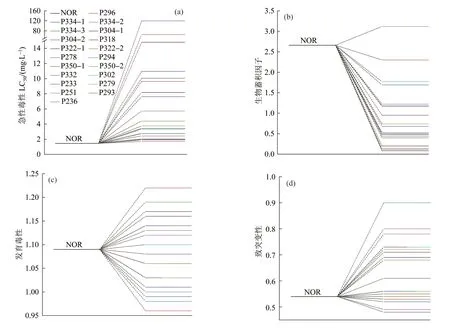
图10 NOR 及其光催化降解产物的急性毒性(a)、生物蓄积因子(b)、发育毒性(c)和致突变性(d)Fig.10 Acute toxicity(a),bioaccumulation factor(b),developmental toxicity(c)and mutagenicity(d)of NOR and its photocatalytic degradation products
对于急性毒性,以96 h带鲦鱼(Fathead minnow)50%致死浓度(LC50-96 h)来进行表征,使带鲦鱼的LC50-96 h<1 mg/L、=(1~10)mg/L、>10 mg/L、>100 mg/L的物质的毒性,被分别定义为“高毒”、“有毒”、“有害”和“无害”〔33〕,实际预测结果如图10(a)所示,NOR属于“有毒”物质,经光催化后75%的降解产物也属于“有毒”物质,少部分降解产物如P296、P304-1、P233的毒性降为“有害”,P278为“无害”降解产物。
由图10(b)可知,与NOR 的生物蓄积因子(BCF=2.66)相比,大多数降解产物的生物蓄积因子显著下降,只有P236 显示出轻微的蓄积因子上升,故NOR经降解后,生物蓄积性明显降低。
图10(c)的发育毒性预测结果表明,NOR 是一种发育性毒物(发育毒性>0.6),会在胚胎期干扰生物发育。经光催化降解后有11 种降解产物的发育毒性下降,其余9 种表现为轻微升高。
此外如图10(d)所示,NOR 呈致突变阳性,降解产物除P332 和P233 外,其余也均具有致突变性(致突变毒性>0.5)。且除P296、P334-2、P322-2、P278以及无致突变性的P332 和P233 外,其余产物的致突变毒性均有不同程度增加。
整体而言,NOR 经g-C3N4光催化降解后,降解产物的急性毒性有所降低,但仍保留了部分毒性,而生物蓄积毒性降低的同时发育毒性和致突变毒性有所升高,表明NOR 经光催化降解后仍存在一定的环境风险,需引起关注。
3 结论
(1)以尿素为前驱体,通过热聚合法合成了g-C3N4纳米片,并考察了其在不同光源下催化降解NOR 的性能,结果表明,在溶液NOR 的初始质量浓度为10 mg/L、pH=7 条件下,在模拟阳光下投加质量浓度为0.2 g/L 的g-C3N4纳米片时,可在反应40 min时去除97%的NOR,在可见光照射下投加质量浓度为0.4 g/L 的g-C3N4纳米片时,可在反应150 min 时去除57%的NOR。
(3)毒性预测结果显示,NOR 经光催化后的降解产物对带鲦鱼的急性毒性相比于母体化合物有所降低,同时大部分产物的生物蓄积性降低,但部分产物的发育毒性和致突变性等慢性毒性有所升高,存在一定环境风险。

