CT纹理分析联合临床病理信息预测进展期胃癌术后复发的价值
黄列彬,刘昱,黄文斯,陈钦贤,薛慧敏,冯宝,龙晚生,李荣岗
据统计,胃癌于2015年成为我国第二大常见癌症,其死亡率在所有癌症中排第三[1]。目前,手术仍是胃癌的主要治疗手段,然而术后复发率居高不下。据文献报道,胃癌术后复发率从20.1%到50.7%不等[2,3],严重影响患者预后,如何降低胃癌患者术后复发率成为改善预后的关键。目前主要依据TNM分期系统来制定治疗方案及评估预后,Ⅱ期以上的胃癌患者均建议接受术后化疗[4],然而即使是同一TNM分期的患者,其临床结果也常常不同[5]。准确筛选出高复发风险的患者对实现精准个体化治疗、降低复发率及改善预后很有帮助。CT纹理分析是影像组学中的一个领域,可从CT图像中提取肉眼无法辨别的定量特征,进而反映肿瘤异质性等情况[6],在肿瘤分期及预后评估等方面应用较广[7-10]。本研究旨在探讨CT纹理分析联合临床病理信息在预测进展期胃癌术后复发中的价值。
材料与方法
1.研究对象
回顾性搜集2009年9月-2014年8月间于本院住院,并经手术病理证实为进展期胃癌的患者。病例纳入标准:①有完整的术前腹部增强CT图像;②术前CT检查与手术时间的间隔小于两周;③经手术病理证实为胃腺癌,且肿瘤浸润深度分期为T2及以上分期;④临床资料完整;⑤除外复发的病例,其余病例随访时间≥5年。病例排除标准:①CT图像质量差,病灶显示不清;②同时合并其他恶性肿瘤。
2.检查方法
所有病例均采用东芝Aquilion One-64 CT进行扫描,扫描参数:管电压120 kV,自动管电流,准直宽度64×0.625 mm,螺距0.7,距阵512×512,层厚3 mm,层间隔3 mm,重建层厚3 mm。先行平扫,后采用高压注射器注射对比剂碘普罗胺(拜耳先灵),剂量1.5 mL/kg,流率3.0~3.5 mL/s,分别于注射对比剂后30 s及60 s行动脉期及静脉期扫描。
3.病理评估
由1位具有丰富胃癌病理诊断经验的医生依据AJCC第八版癌症分期系统对所有入组病例的病理切片重新评估。评估内容包括病理分级、Lauren分型、Borrmann分型、脉管侵犯、T分期、N分期、TNM分期等。
4.复发定义及随访
复发包括局部复发、腹膜转移和远处转移。局部复发包括发生在吻合口、残胃、十二指肠残端和/或胃区域淋巴结的复发;腹膜转移包括发生在腹膜、网膜、肠系膜的转移灶;远处转移是发生在其他器官和非胃区域淋巴结的转移灶[11]。吻合口、残胃的复发通过胃镜活检病理证实。胃区域淋巴结、十二指肠残端的复发主要通过术后增强CT随访动态观察来确定。在术后增强CT随访中,出现胃区域淋巴结增大伴坏死,或动态随访时胃区域淋巴结逐渐增大,在除外结核等因素后,则认为区域淋巴结复发。术后CT检查发现腹膜、网膜、肠系膜结节状或肿块状增厚,且腹水检查癌细胞阳性或腹膜病灶活检发现癌细胞,则认为腹膜转移。远处转移通过术后增强CT检查确诊。
本研究的终点是复发,除外复发的病例,其余病例随访时间≥5年。患者前2年每3~6个月随访1次,以后3年每6~12个月随访1次,然后每年1次。主要随访检查手段有腹部增强CT、胃镜检查和肿瘤生物标志物检查等。
5.肿瘤分割及纹理特征提取
本研究采用静脉期图像进行肿瘤分割。由两位放射科医师采用基于Matlab2016(Mathworks,Natick,MA,USA)编写的程序对肿瘤边缘进行手动勾画,勾画时尽量避开胃腔气体、液体或胃周脂肪。医师1勾画全部病例,医师2在训练集随机勾画30例患者,随后利用勾画好的图像重建肿瘤立体图(图1),进而提取纹理特征。采用组间相关系数(Intraclass correlation coefficients,ICC)评估2位医师提取的纹理特征的可重复性和稳定性,ICC值大于0.75的纹理特征认为是可靠的。为提高特征的可重复性和鲁棒性,采用不同权重下的小波带通滤波[权重系数=(0.5,0.67,1,1.5,2)]、各向同性重采样[重采样系数=(0.9,1,1.2,1.5,2)]和灰度离散化[量化算法=(Equal,Lloyd),灰度级=(8,16,32,64)]。通过软件分析肿瘤3D图像,提取10320个纹理特征,包括720个全局纹理特征、2160个灰度共生矩阵特征(Gray Level Co-occurrence Matrix,GLCM)、3120个灰度游程矩阵特征(Gray Level Run Length Matrix,GLRLM)、3120个灰度区域尺寸矩阵(Gray Level Size Zone Matrix,GLSZM)和1200个邻域灰度差分矩阵(Neighbouring Gray Tone Difference Matrix,NGTDM)。

图1 胃癌手工分割结果。a)静脉期手动分割的病灶;b)三维重建的病灶体积。
6.特征筛选及模型构建
以术后5年复发为终点事件,采用(LASSO)logistic回归进行纹理特征选择,非零系数特征被认为是胃癌术后复发有价值的预测因子。随后,所选的非零系数纹理特征被用于构建纹理标签。
除外CT纹理标签,本研究亦对病例的临床、病理相关指标进行分析,构建临床预测模型。此外,通过结合对预测胃癌复发有统计学意义的独立预测因子和纹理标签构建组合模型,并通过放射列线图的形式直观展示,以便于应用。
7.统计学分析
采用SPSS 19.0软件及R语言统计分析软件进行统计学分析。分类变量(如性别)的组间比较采用卡方检验和费舍尔精确检验,而连续变量(如年龄)的组间比较采用秩和检验。采用受试者工作特征(receiver operating characteristic,ROC)曲线和决策曲线分析(decision curve analysis,DCA)评价不同模型的预测效果。以P<0.05为差异具有统计学意义。
结 果
1.复发组及未复发组患者的基本信息
本研究最终纳入162例患者,其中52例在随访过程发生复发(单纯原位复发14例,原位复发合并肺转移3例,肝、肺及其他远处转移35例)。本组病例以随机数字表法按5:3比例将患者分为训练集(n=100)和验证集(n=62),162例患者的基本信息见表1。
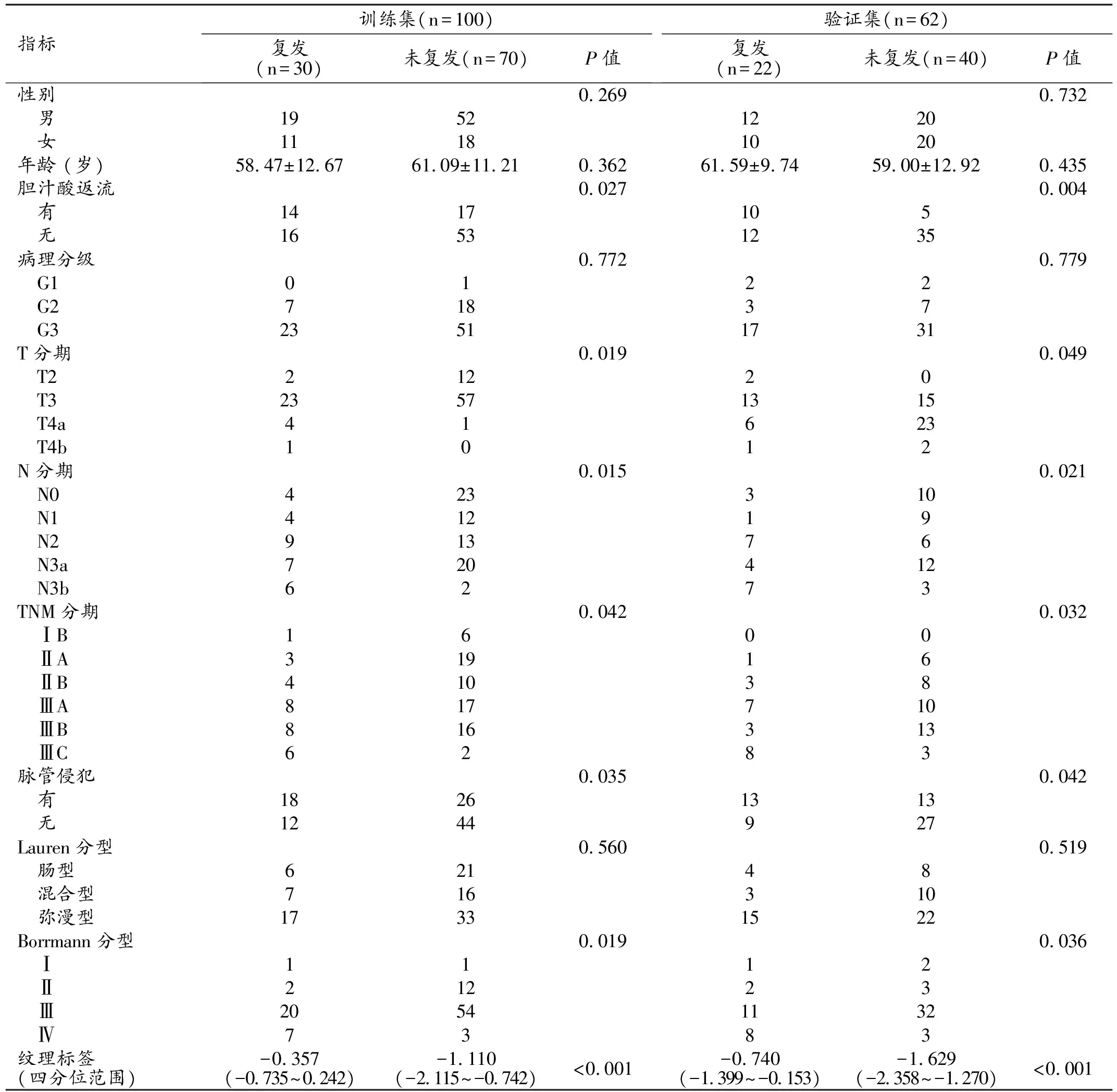
表1 复发组及未复发组患者的基本信息 (例)
2.纹理特征提取及纹理标签构建
对训练集和验证集数据进行U检验,再进行ICC检验,得到有统计学意义且有较好一致性的48个特征(P<0.05,ICC>0.750)。采用LASSO回归方法最终选出8个与复发相关的特征,分别为GLSZM-LGZE_0.5_0.9_Lloyd_64、GLRLM-SRHGE_0.67_1_Equal_64、GLRLM-LGRE_0.67_1.2_Lloyd_8、GLCM-Variance_0.67_2_Equal_32、NGTDM-Contrast_1.0_0.9_Lloyd_64、GLSZM-SZE_1.0_2_Lloyd_32、GLSZM-SZE_2.0_1_Equal_8和GLSZM-LGZE_2.0_1.2_Lloyd_64,进而构建纹理标签。
3.临床模型及组合模型的构建
对复发组及未复发组有统计学差异的临床病理指标进行多因素回归分析并构建临床模型,最终胆汁酸返流、TNM分期、脉管侵犯等3个指标经Logistic回归筛选出来并具备统计学差异(P<0.05,表2)。
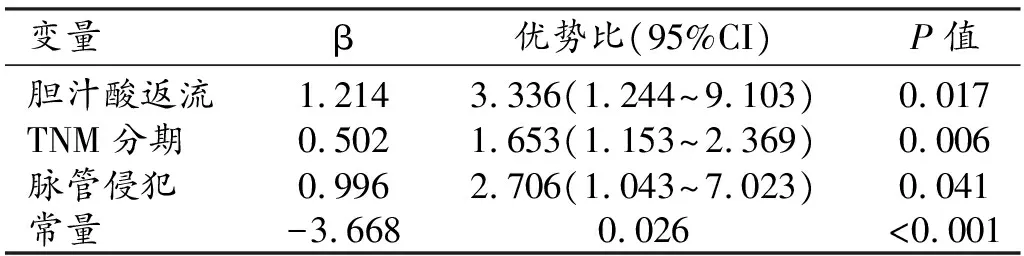
表2 临床病理指标多因素逻辑回归分析结果
将上述3个指标与纹理标签作为组合模型的输入特征,进行多因素分析并构建组合模型,其中胆汁酸返流和纹理标签被筛选出来且具有统计学意义(表3)。结合这2个独立因素,构建组合模型并以放射组学列线图形式表示(图2a)。使用校准曲线确定训练集和验证集中预测值与实际值之间的关系(图2b、2c)。
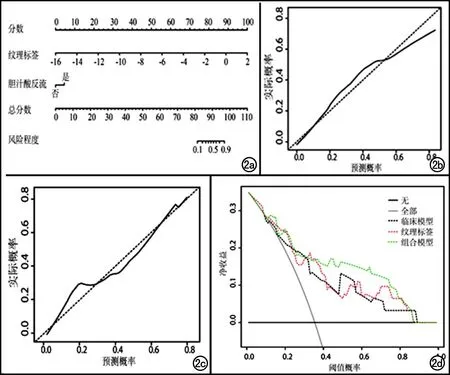
图2 放射组学列线图的性能和各模型决策曲线分析。a)结合纹理标签和临床因素的放射组学列线图;b)组合模型在训练集中的校准曲线;c)组合模型在验证集中的校准曲线;d)各种模型的决策曲线分析。
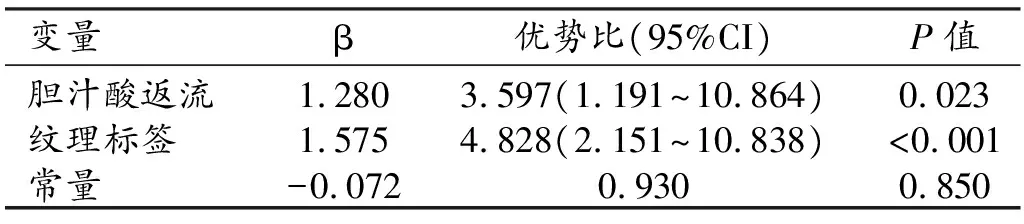
表3 多因素分析构建组合模型
4.评估模型的效能
临床模型、纹理标签和组合模型在训练集的曲线下面积(area under curve,AUC)分别为0.748、0.809及0.841,在验证集的AUC分别为0.786、0.799及0.840。
采用净重分类指数(net reclassification index,NRI)评估纹理标签是否优于临床模型,结果显示纹理标签的预测效果优于临床模型,在验证集中两模型比较时,NRI=0.325,P=0.011。DCA分析结果表明,组合模型在阈值概率为0.31~0.87时,预测胃癌复发效果更佳(图2d)。
5.基于纹理标签的无瘤生存率分析
以纹理特征标签中位数为界,分别对训练集与验证集的数据进行分组,再进行无瘤生存率分析,结果显示小于纹理特征标签中位数及大于中位数患者的5年DFS差异有统计意义(P<0.05,图3)
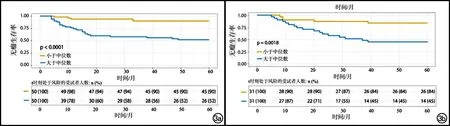
图3 a)训练集的生存曲线;b)验证集的生存曲线。
讨 论
对胃癌患者进行准确的预后评估及风险分层是实施个体化精准治疗的关键。目前临床上主要依据TNM分期系统对胃癌患者进行预后评估及制定治疗方案。Chu等[12]的研究结果显示TNM晚期的胃癌患者无病生存期较短,复发风险较高。Pan等[13]的研究结果显示,TNM分期是胃癌切除术后患者预后的独立预测因子,其预测胃癌患者术后5年生存期的AUC为0.721。本研究结果显示,TNM分期为胃癌患者术后复发的独立预测因子,与文献报道相仿。此外,本研究结果显示胆汁酸返流及脉管侵犯亦是胃癌术后复发的独立预测因子。胆汁酸可激活法尼醇X受体(FXR)/核因子κB(NF-κB)信号通路,诱导粘蛋白2(一种肠上皮化生标志物)及尾端相关同源盒转录因子2(一种肠道特异性转录因子)在正常胃上皮细胞中的异位表达,在诱导胃肠化生和胃癌发生中起着重要的作用[14]。既往研究显示,脉管侵犯是胃癌患者术后复发的独立预后因素,是淋巴结转移和远处转移的起始环节,对预后有着重要影响[15]。本研究对上述3个独立因素构建的临床预测模型进行评估,结果显示临床模型对预测胃癌患者术后复发有一定效能,但其效能仍相对较低。笔者结合文献分析认为,这或因TNM分期系统主要是依据肿瘤解剖特征进行评估,并未包含肿瘤异质性及患者相关个体化预测信息,难以做到个体化精准评估[5]。
CT纹理分析是影像组学的一个领域,它可以提取、分析和解释定量成像特征,客观评估病变和器官的异质性及反映有关组织微环境等信息,已广泛应用于肿瘤良恶性鉴别、疗效评估及预后评估等方面[6]。黄裕存等[16]的研究结果显示肿瘤最大径及体积特征可用于胃癌患者术后危险分层,构建的纹理特征标签预测胃癌患者3年总生存期(Overall Survival,OS)的AUC为0.72。Giganti等[9]研究发现能量、熵、偏度及平均绝对偏差等特征与预后相关,CT纹理分析可以提高胃癌危险分层多变量预后模型的性能。
本研究从静脉期CT图像中提取了10320个纹理特征,通过LASSO回归模型筛选出8个与复发相关的纹理特征,并构建纹理标签。结果显示该标签对预测胃癌术后复发具有较好的效果(AUC=0.799),其预测效果优于单纯临床模型。组合模型是通过结合纹理标签和临床病理信息综合诊断的一种方法,通过将纹理标签的预测值和临床模型筛选出来的临床病理指标作为特征,应用多因素LASSO逻辑回归进行特征筛选并构建组合模型,选出与复发相关联的特征(纹理标签和胆汁酸返流)。研究结果表明,组合模型预测胃癌术后复发的效果最佳(AUC=0.840)。这进一步说明胃癌术后复发是受多方面因素影响、复杂的进程,结合不同因素及手段对其进行预测可提高其预测效果。本研究在构建组合模型时,胆汁酸返流进入了模型,而TNM分期及脉管侵犯却没能进入模型;笔者分析其原因认为,纹理标签是由病灶的术前CT图像中提取特征组成,这些由完全分割肿瘤图像提取的特征或已包含有TNM分期及脉管侵犯等信息,故在筛选了纹理标签的情况下,TNM分期及脉管侵犯未能同时进入模型。另一方面,胆汁酸返流作为诱导胃肠化生和促进胃癌发生的重要因素[14],作用在吻合口及残胃,主要促进原位局部复发的发生。本组病例共有17例发生了原位复发,因而胆汁酸返流被筛选入模型作为相应信息补充。总而言之,基于CT的纹理分析作为一种非侵入性的肿瘤特征分析方法,可与临床病理相关信息相互补充,有助于提高胃癌术后复发的预后评估,为临床决策及个体化精准治疗提供一定帮助。
本研究存在以下局限性:首先,本研究样本量相对较小;其次,本研究为回顾性研究,且为单中心数据,数据偏倚难以完全避免。
综上所述,CT纹理分析对评估胃癌术后复发有一定价值。联合CT纹理标签及相应临床病理因子构建组合模型,可更好地对胃癌患者进行术后复发风险评估,为个体化精准治疗提供依据。

