CO2催化制备高附加值化学品研究进展
赵琳,刘庆岭,周伟,韩辉,代中元
1 前言
随着社会工业化程度的提高和CO2排放的增加,大气中的CO2浓度不断提高,增长较快,其产生的温室效应已导致全球气候变暖等一系列生态环境问题,如何降低大气中CO2的浓度,减缓大气中CO2浓度的上升速度,已成为一项世界范围内具有挑战性的重要研究课题。
CO2是C1化合物中最廉价、丰富且无毒的可再生资源,CO2的价格通常不足1 000 元/t,而由其合成的化学品价值每吨可达数千元甚至上万元。采用CO2制备高附加值化学品的过程基本不会产生二次污染,有毒有害物质排放较少。工业界和学术界对CO2资源化再利用和改善CO2对环境的影响有着广泛的研究。
CO2是非极性分子,利用CO2转化制备高附加值化学品的难点在于CO2中的碳元素处于最高价态,其具有良好的热力学稳定性和动力学惰性,不易被活化。目前,利用二氧化碳催化转化制备化学品通常包括如下几种方式:一是将CO2直接进行热分解,制备CO和O2;二是利用CO2与另一种温室气体甲烷发生干气重整、偶联反应或制乙酸;三是利用CO2与其他物质反应,制备甲烷、低碳烃、甲醇、甲酸及其衍生物,以及醚类、醛类、汽油、低碳醇等化学品;四是利用CO2与PO发生聚合反应,制备高分子可降解材料。
2 二氧化碳催化转化制备化学品
2.1 催化分解制CO
CO2热分解方程式为CO2=CO+O2,反应开始发生的温度在2 000K以上,完全转化温度更高,采用催化剂催化该反应,可在较大程度降低反应温度。近期也有通过光催化或电催化实现这一反应过程的研究报道。
康敏[1]等人使用共沉淀法制备了NiFe2O4和NiFe2O4/ZrO2催化剂,用于CO2催化分解制备CO。研究者表征了反应前后的催化剂,发现高温条件下两种催化剂均发生了不同程度的烧结,催化剂随反应进程的延长性能逐渐下降,且随催化循环次数的增多,CO的产量显著降低。研究者通过对比发现,二氧化锆的加入,起到了提高催化剂热稳定性和循环反应稳定性的作用。
由于热催化分解CO2,反应的温度太高,设计和合成可见光催化材料,提高光催化CO2分解反应效率的研究工作十分有意义。Jiang[2]等人提出了一种简单有效的方法,即通过合成杂原子掺杂的多孔处理油菜花粉(TRP)和NH2-功能化的TRP 来促进CO2转化。研究者发现,杂原子掺杂可以加速相邻碳原子之间的光致电荷转移。而NH2-基团的引入,为促进CO2的吸附提供了有效的位点,有利于CO2向CO 的转化。实验结果表明,在没有助催化剂和牺牲剂的气固反应体系中,TRP-NH2的可见光驱动 CO 生成速率为 1 165.3μmol/h/g,是 TRP(488.4μmol/h/g)和 g-C3N4(16.6μmol/h/g)的 2.4 倍和70.1倍。研究结果揭示了表面NH2-基团和光催化CO2还原性能之间的相关性,并可推广到其他CO2分解催化剂。
电化学CO2还原(ECR)技术作为一种新兴的CO2利用技术,因其环保、操作条件温和、反应过程易于控制等优点而受到广泛的关注。Jo[3]等人在聚吡咯修饰碳纸(CP/PPy)电极上构建了Zn 和Ag 双金属电催化剂,将CO2电化学还原为CO。在CP/PPy/Zn电极上,用Ag部分电偶置换Zn,制备了不同锌和银原子比的双金属催化剂。与单金属催化剂CP/PPy(Ag 或 Zn)相比,CP/PPy/Zn/Ag 双金属催化剂电化学还原CO2成CO的选择性明显提高(图1),而析氢反应(HER)受到抑制。在双金属催化剂中,Ag-Zn 原子的混合可以提高CO 的选择性和产出率。所开发的电化学催化剂在饱和的1M KHCO3水溶液中进行CO 还原反应,其最大法拉第效率约为70%,最大电流密度为8.6mA/cm2。

图1 CP/PPy/Zn/Ag双金属催化剂电化学还原CO2示意[3]
但总体来说,采用热催化、光催化和电催化分解制备CO的反应过程,能耗高且转化率较低,目前很难在工业中大规模应用。
2.2 与CH4发生反应
CO2和甲烷均为温室气体,可重整制备重要的化工合成原料气(CO,H2),又称甲烷干气重整,大部分过渡金属对于甲烷干气重整都有一定催化活性。CO2还可与CH4发生偶联反应制备乙烷,与甲烷反应合成乙酸。乙酸制备主要化学反应方程式和吸放热情况如表1所示。

表1 CO2与CH4反应方程式及吸放热情况
Park[4]等人研究了在高度有序的介孔SBA-15(NP/SBA-15)上,保持原始较小的镍纳米粒子(NP)的有效方法,其尺寸分布均匀(约为5nm),并用于高温(800℃)甲烷与CO2干气重整(DRM)。研究者发现,在SBA-15介孔孔道中,纳米镍颗粒的团聚可被抑制,结焦量减少,进而催化活性提高。特别是经乙酸酐两步表面预处理和H2O处理后,有机稳定的纳米镍颗粒具有较高的分散性,并优先沉积在有序的介孔SBA-15 孔道内,其聚集性不明显。Shavi[5]等人将ZnO-、CeO2-和MnO2-负载到蒙脱土(MMT)上制备了单组分和双组分催化剂(图2),并用于CO2和甲烷制乙酸反应。因为反应活化能较高,直接转化难度较大,所以动力学和反应机理信息对CH4与CO2的羰基化反应至关重要。研究者通过对反应机理的研究发现,ZnO和CeO2的双活性位点分别优先吸附CH4和CO2,避免了表面吸附竞争。在适当浓度(Ce:0.44wt%,Zn:2.20wt%)时,乙酸的生成速率最大。DFT计算结果表明,ZnO催化剂上吸附的CO2更容易从CeO2侧迁移到ZnO侧,有利于乙酸的生成。
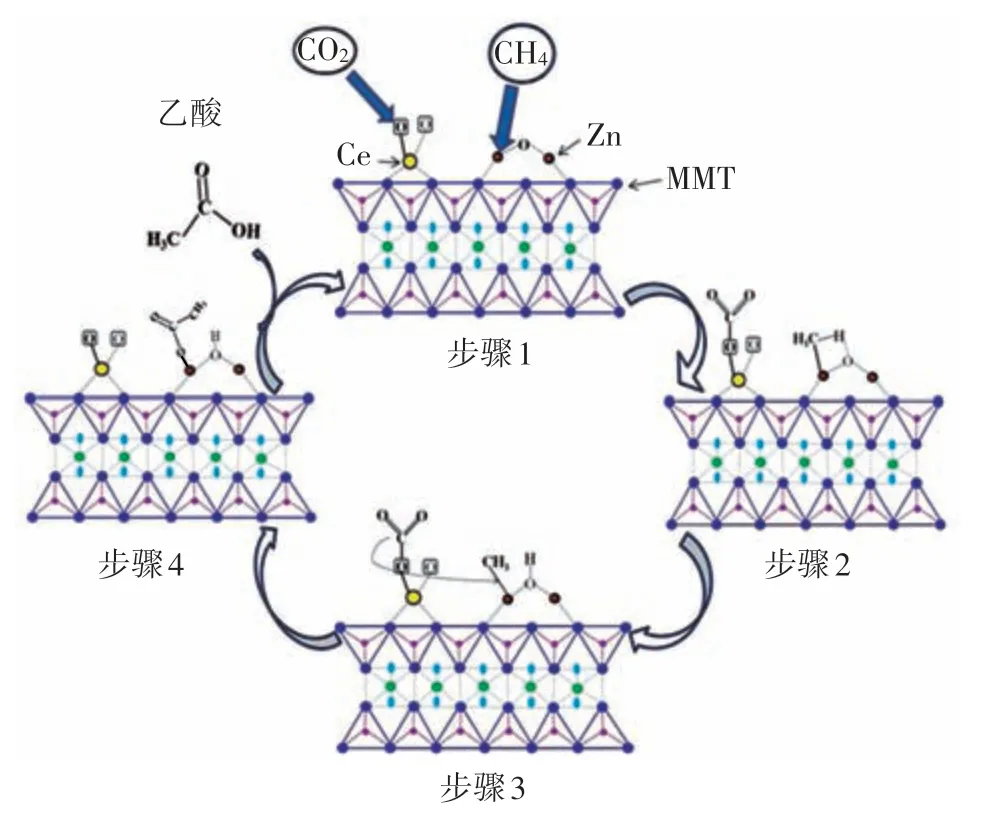
图2 在CeO2-ZnO/MMT催化剂上由CH4和CO2形成乙酸的机理步骤示意图[5]
甲烷干气重整与甲烷水蒸气重整相似,制备合成气可用于进一步合成化学品,但该技术也存在催化剂易积碳和活性组分易烧结问题,尚未有工业规模的应用实例,未来需要在反应机理方面进行深入研究,提高催化剂的分散度和热力学稳定性,同时对其活性组分进行调整,抑制积碳的生成。而对于制备乙酸的反应,则需要在控制催化剂表面酸性位数量及催化剂孔结构形状方面深入研究。
2.3 催化加氢反应
常见的一些CO2加氢催化还原等反应的吉布斯自由能均为正,表明反应不能自发进行,需要的反应温度和能耗较高,该技术被认为是21 世纪的巨大挑战,这也是阻碍该项技术大规模工业化应用的重要原因。Kumar[6]在2012年的物理化学年会中强调:“实际上,转化CO2的每种方法都需要催化剂来促进化学键的形成和分解”,CO2的转化都要经过在催化剂的作用下断键成键的过程。因此,研究CO2的催化转化制备化学品是一项对人类社会有着积极意义的课题。
2.3.1 甲烷化反应

CO2通过加氢制备甲烷已有一个多世纪的研究历史。甲烷有着广泛的用途,可直接作为燃料,还可用于合成甲醛和甲醇等。甲烷化反应多采用过渡金属作为催化剂,反应形式为气固反应。由于甲烷化反应过程中受热力学因素的限制,近年来鲜有其研究报道。
Rosid[7]等人通过湿法浸渍法制备了掺杂锰、钌的负载型氧化钕催化剂,并用于CO2甲烷化反应。研究者以400℃焙烧的Nd/Al2O3催化剂为基础开始进行催化剂筛选,对催化剂焙烧温度和不同Ru 负载量等进行优化。最终选用1 000℃焙烧的Ru/Mn/Nd(5:20:75)/Al2O3为潜在最优催化剂,其在400℃反应温度下,可使CO2完全转化,CH4选择性为40%。XRD表征结果显示,该材料存在无定形态的RuO2、MnO2和 Nd2O3等活性物质;EDX 表征结果显示,该催化剂Mn的质量比最高。
2.3.2 合成烃类
烯烃是化学工业中重要原材料,采用CO2制备烃类燃料,可缓解烃类生产对石油资源的依赖,同时也是一项有着重要战略意义的工业技术。尽管CO2加氢制备各种C1 化合物的研究取得了长足进展,但由于CO2具有极高的惰性和高碳-碳耦合势垒,因此直接从CO2中合成含两个或两个以上碳的高附加值产品(如汽油)仍是一个巨大的挑战。一般制备过程是,CO2和氢气经过逆水煤气变换(RWGS)反应,生成CO 和H2O,随后CO 继续加氢,通过费托合成(Fischer-Tropsch synthesis)生成烃类。最近也有一些其他合成路线报道。CO加氢与CO2加氢有较大区别,二者不仅活化方式不同,反应途径也不同,不能直接将CO 加氢催化剂用于该反应。目前,CO2加氢合成烃类使用的催化剂大多由CO 加氢催化剂经针对性优化得到,主要活性组分一般包括Fe、Co和Ni等元素。
CO2加氢制备烯烃的反应机理可分为两步:
第一步:逆水煤气反应,即CO2通过逆水煤气变换反应转化为CO。该反应方程式如下:

第二步:费托合成反应,即第一步生成的CO通过费托合成反应加氢转化为烃类。该反应方程式如下:
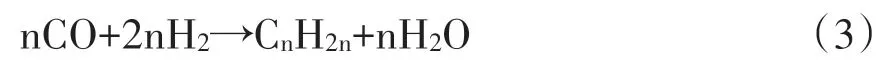
在使用氧化物/沸石双功能催化剂的CO2加氢生产燃料和化学品时,通常采用反应协同耦合策略,氧化物可促进对CO2的激活。Lu[8]等人将不同粒径的In2O3与SAPO-34 结合,作为CO2加氢的双功能催化剂。随着In2O3平均晶粒尺寸从29nm 减小到19nm,低碳烯烃的CO2转化率和选择性逐步增大。研究者认为,这一趋势主要是由CO2和H2活化的氧空位数量的增加引起。粒径<19nm的氧化铟比其他粒径尺寸的氧化铟更容易烧结,研究结果表明,19nm 是CO2加氢反应催化剂氧化铟的最佳粒径,氧化铟粒径大小对于设计高活性、高选择性和高稳定性的催化剂至关重要。
Sun[9]等人设计并制备了一系列不同含量Rb作为促进剂的Fe3O4微球催化剂,发现Rb 催化剂对CO2的转化和低碳烯烃的选择性有积极的影响。通过改变Rb催化剂相应活性组分的相对含量来调整RWGS 和后续FTS 反应非常重要。XPS 分析表明,适当的Rb 负载量可以调节催化剂表面的碳质物质含量和氧化铁含量,有利于催化剂的协同效应,产生低碳烯烃。实验和XPS 结果表明,高负载量的Rb具有较低的RWGS能力和较高的链生长能力,其较高的二氧化碳吸附能力和较低的H/C率进一步促进了C5+烃类的选择性。低负载量的Rb 具有较高的RWGS能力和高链生长能力,导致CH4的高选择性和低碳烯烃/链烷烃比。3wt%Rb 负载量是将表面含碳物质含量和三氧化二铁含量调整到更合理的比例的合适负载量,可通过协同作用促进串联反应,对低碳烯烃(C2-C4,47.4%)的选择性较高,烯烃/烷烃比高(10.7)。
Malhi[10]等人通过使用动力学和结构表征拉曼光谱、X射线衍射和CO程序升温还原技术,揭示Na修饰和/或ZnO 添加对Fe 基催化剂结构的影响,以及CO2加氢制烯烃的反应途径和速率与反应物组成和反应温度间的关系。铁基催化剂上的CO2加氢反应是初级逆向水煤气变换反应生成CO及随后CO加氢生成烯烃和链烷烃的两步连续反应。氧化锌的加入提高了CO2加氢生成所有含碳产物的速率,因为氧化锌促进了铁基催化剂中活性相铁碳化物的生成,初级RWGS反应、次级CO加氢生成烯烃和链烷烃之间的相对速率对Zn的添加不敏感。研究者还发现,在Fe 催化剂上添加Na 元素,显著改变了烯烃生成速率对反应物和反应温度的依赖性,这可能是Na 原子改变了Fe 催化剂的还原性和表面特性,从而改变了烷烃和烯烃比。通过添加Na和Zn 改性后的Fe 基催化剂,催化CO2加氢制烯烃性能最佳,CO2转化率为43%,对高烯烃的选择性为54.1%,高烯烃/烷烃比为7.3。
目前采用CO2制烃类存在的问题是催化剂活性较低且目标产物的选择性较低,如能在反应机理研究方面有重大突破,将会对该项技术的大规模工业化应用有重要推进作用。
2.3.3 制备甲醇和二甲醚
甲醇是一种清洁能源,也是重要的基础化工原料,以甲醇作中间体也可以制备一系列重要的化工产品。用二氧化碳制甲醇是一种有效的碳减排途径,在工业上也得到了一些应用,但在提高二氧化碳转化率和产物选择性方面还需要进一步努力。
甲醇合成反应,即CO2与H2反应生成甲醇和水。该反应方程式如下:

Cu/ZrO2/SiO2是CO2选择加氢制甲醇有效的催化剂。Lam[11]等人为了解混合氧化物基催化剂中ZrO2的作用,对 Cu 和 Zr 的 K-edge 进行了原位 X 射线吸收光谱分析。在反应条件下发现,Cu 保持金属性,而Zr 存在于三种配位环境中,与块状ZrO2、配位饱和和不饱和Zr(IV)表面位点相关。配位不饱和Zr表面位点的数量,可以通过参考X射线吸收近边缘结构(XANES)光谱的线性组合拟合来量化,其数量与CH3OH形成速率相关,表明Zr(IV)路易斯酸表面位点在提高对CH3OH的选择性方面的重要性。
In2O3负载的铑催化剂被证实对CO2加氢制备甲醇具有反应活性。在这项工作中,Lu[12]等人制备了In2O3-ZrO2固熔体,并将其用于负载铑催化剂。采用沉积-沉淀法,使Rh催化剂高度分散。催化剂表征证实,ZrO2的使用优化和稳定了In2O3的氧空位,从而增强了CO2的吸附和活化。高度分散的Rh催化剂显著提高了In2O3-ZrO2载体的加氢能力。与Rh/In2O3相比,In2O3-ZrO2负载的Rh催化剂表现出更高的活性和甲醇选择性。在300℃和5MPa 的反应条件下,Rh/In2O3-ZrO2催化剂的甲醇选择性达到 66.5%,时空产率(STY)为 0.684gMeOH/h/gcat,CO2转化率为18.1%。300℃时的甲醇选择性和甲醇STY分别比Rh/In2O3催化剂高19%和26%。
Han[13]等人采用离子交换法将单原子Pd 负载在Cu/ZrO2上,研究了Pd 元素在Cu/ZrO2催化剂中对CO2加氢制甲醇的作用。在相对温和的条件下(1.5MPa,260℃),Pd 的掺杂使Cu/ZrO2催化剂上甲醇的产率从223μmol/g/h 提高到512μmol/g/h,增加了Cu物质上的分裂H吸附,并加强了Cu物质与界面处氧空位之间的相互作用,从而促进了Cuδ+物质的形成,这对甲醇的形成至关重要。
铜基催化剂是CO2制甲醇反应中最具代表性的催化剂,但在反应过程中,Cu纳米颗粒面临易烧结失活等问题。通过优化催化剂结构,可以调整负载催化剂上的反应路径,有助于开发高效催化剂。Xiao[14]等人设计并制备了Co@Six催化剂(图3),可实现CO2高效制甲醇。研究者通过调节钴硅比进行催化剂优化,发现Co@Si0.95催化剂有着最佳的CO2转化率,可达8.6%,甲醇选择性70.5%。结果表明,Co@Si0.95上的CO2加氢过程可能与已知的Cu/ZnO 催化剂上的机理相似,其中,CH3O·的转化对甲醇的选择性生成至关重要。研究者推断Co@Si0.95上的钴氧化物占主导地位的相为阻碍副反应和促进甲醇生成提供了一个近乎最佳的结构。研究者认为,此类钴催化剂为优化CO2加氢的选择性和生产高级甲醇提供了机会。
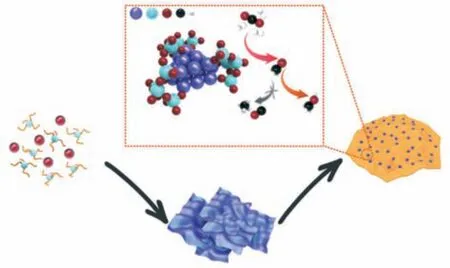
图3 Co@Six催化剂的合成及催化策略[16]
二甲醚是化工基础原料,可用于发泡剂、制冷剂、萃取剂的生产,在护发、护肤和药品等领域也有应用。在二氧化碳制二甲醚的过程中使甲醇合成反应和甲醇脱水反应同步发生,因此可以采用两种催化剂混合制成双功能催化剂作为CO2制二甲醚催化剂,其中,甲醇合成催化剂在前面已有介绍。甲醇脱水催化剂多为分子筛、氧化铝等,甲醇脱水反应方程式为:2nCH3OH→nCH3OCH3。
Fan[15]等人采用共沉淀法制备了一系列铁(Fe)改性的CuO-ZnO-ZrO2-Al2O3(CZZA)催化剂,研究了Fe改性CZZA和HZSM-5双功能催化剂用于CO2加氢合成二甲醚(DME)。研究者研究了Fe 负载量、反应温度、反应压力、空速和合成Fe改性CZZA催化剂的前驱体浓度对二甲醚合成催化活性的影响。长期稳定性测试表明,Fe改性提高了通过CO2加氢合成DME 的CZZA 催化剂稳定性。当Fe负载量为 0.5(Fe 与 Cu 的摩尔比)时,在 100h 的反应过程中,DME 收率从4.2%显著降低到1.4%。氢气程序升温还原的分析表明,由于H2在氧化铁上的辅助吸附,Fe 的引入提高了催化剂的还原性。Fe 改性CZZA 催化剂在DME 形成中的良好稳定性很可能归因于通过添加氧化铁引入的氧溢出,这可能抑制了铜表面的氧化并提高了铜在长期反应过程中的热稳定性。
2.3.4 制备低碳醇
低碳醇作为燃料在化工领域有着广泛的应用,近年来对低碳醇的研究也成了行业热点。低碳混合醇可与汽油良好混合,辛烷值高,可替代甲基叔丁基醚作为汽油添加剂或作为清洁燃料。在化学工业中,CO2合成低碳醇被认为是合成碳基燃料和原料的重要发展方向,其不仅可以减少碳排放,还能在一定程度上缓解能源危机,具有良好的发展前景。低碳醇的合成过程涉及碳链的增长和含氧官能团的生成两种类型的反应,因此可借鉴F-T合成催化剂和甲醇合成催化剂的研究经验。目前,制备低碳醇催化剂主要包括贵金属催化剂和过渡金属催化剂等,如Rh、Cu、Mo 和Co 基催化剂,一般可采用碱金属、碱土金属等作为助剂。但现有催化剂的低活性,是该类工艺达到工业化水平的一大障碍。
Witoon[16]等人合成了一种新型K-Co 促进的In2O3催化剂,用于CO2加氢制低碳醇。K和Co的最佳负载量分别为 2.5wt%和 5.0wt%时,可达到169.6g/kgcat/h 的高 C2+OH 时空产率,且在总醇中,C2+OH分布良好,为87.4%。在用负载量5wt%Co促进的In2O3催化剂上,只获得了非常低的时空产率,C2+OH 仅为 0.4g/kgcat/h。研究者认为,弱 H2吸附的减少和吸附H与催化剂表面相互作用的改善,延缓了加氢,使CO在被吸附的CxHy物质加氢之前插入,抑制其形成烃,从而显著降低了CH4和低碳烯烃的形成,促进了低碳醇量的提高。
由于铁催化剂的CO 非解离活化能力较差,通常不被认为是最理想的候选催化剂,且在上述过程中需要与其他金属(如Rh、Pd、Cu)结合进行催化反应。Yao[17]等人制备了一种Na 和S 共改性的铁催化剂(FeNaS-0.6),实现了醇的80.5mg/gcat/h时空产率,且其中>98%对应于C2+OH。研究者认为,Na和S的协同作用,使单金属铁催化剂能够同时提供低碳醇合成所需的分子吸附物质—CO 和烷基。DFT模型还证实了,在Na和S共改性铁催化剂上更容易形成醇。
2.4 制备甲酸及其衍生物
CO2加氢反应可合成甲酸及甲酸的衍生物(如甲酸盐、甲酸酯、酰胺)等。酰胺类化合物是一类重要的化工原料和溶剂,广泛应用于医药、农药、日用化学品及石油化工等众多领域且需求量巨大。此外,还可以二氧化碳为碳源,通过高效催化体系的建立,实现二氧化碳与胺反应,合成具有重要意义的甲酰胺。催化体系可分为贵金属催化剂(如Ir、Pd、Pt、Ru、Rh),非贵金属催化剂(如Ni、Mo、Cu、Fe、Co、Zn、Al),有机分子催化剂和无机催化剂体系,常用的还原剂为H2、硅烷和硼烷。
He[18]等人合成了一种无定形NiRu0.1B催化剂,用于CO2加氢制甲酸反应,并显示出足够的催化活性。该催化剂的无定形结构,提供了丰富的悬空键和不饱和原子,以增强对反应物气体分子的吸附。此外,B 元素的给电子效应,对于产生活性富电子金属中心至关重要,这有助于形成M-H单键,以激活CO2分子。由于非晶结构和给电子体的协同作用,非晶NiRu0.1B 催化剂在低温下,表现出比Ni-B和晶态Ni-B更高的活性和稳定性。这项工作不仅展示了一种制备无定形双金属催化剂的简便方法,还证明了无定形金属是用于将CO2加氢成甲酸的有前途的多相催化剂。
Dai[19]等人制备了凹凸棒石负载的Pd/PAL 催化剂,用于CO2和H2甲酰化反应(图4)。研究者发现,具有不同结构的仲胺和伯胺均可在<100℃转化为所需的甲酰胺,并获得良好至优异的收率,且催化剂可重复使用,稳定性好。通过BET、XRD 和XPS 表征发现,部分负载的金属Pd 进入到载体内部,与载体内部酸碱位点的协同作用,可能是催化剂Pd/PAL能够高效催化CO2/H2和胺反应合成甲酰胺的重要原因。

图4 Pd/PAL催化下胺与CO2和H2的N-甲酰化反应[23]
Mabena[20]的研究中,报告了新合成的S^N^S 和Se^N^Se三齿铂(II)和钯(II)钳形配合物。这些配合物可作为碱性条件下二氧化碳加氢生成甲酸盐的预催化剂。这些新的分子催化剂被证明在从二氧化碳制备具有工业价值的化学中间体(如甲酸盐和二乙基甲酰胺)方面具有活性。该配合物可溶于THF 而不溶于水,从而能够在催化后从THF/水溶剂体系的双相混合物中轻松回收催化剂。钳形配体为通过各种催化循环步骤的稳定活性中心提供了稳定的框架。钯(II)催化剂产生的甲酸盐的TONs高达1 881,而在24h后,基于Se^N^Se铂(II)的催化剂(C1、C2 和C3)催化CO2加氢生成甲酸盐的TONs分别为550、421和1 254。类似地,在C2存在下,使用CO2和H2对二乙胺进行N-甲酰化是有效的,产率高达71%。
Cao[21]等人开发了一种能在温和条件下促进N-甲酰化反应的高效催化剂,该催化剂活性高,可回收性好。单原子催化剂(SACs)具有极高的原子利用效率和出色的催化性能,因此,研究者基于简便的溶液法,在COF(TpPa-1)上合成锚定制备了Zn SACs(Zn-TpPa)。在 Zn-TpPa 的催化作用下,CO2和N-甲胺在温和的反应条件下,转化为N-甲基甲酰苯胺,TOF 为17 155h-1,是已报道的可回收Zn基催化剂中最高的。较高的反应性归因于,COF上分散良好的Zn活性位点以及由于COF的高表面积对CO2的有效吸附。研究者认为,此研究为构建SACs提供了一种简便的方法,也为CO2转化和环境保护提供了一条有效的途径。
2.5 制备其他化学品
早在20世纪80年代,美国、日本等国家已开展了采用二氧化碳和其他有机物单体制备可降解高分子材料的研究,该材料安全性好、生物兼容性好,可用于包装、医疗领域、农用薄膜等诸多领域,同时,该材料生物降解性好,有着广阔的利用空间。如CO2基聚碳酸酯及其共聚物具有优异的热性能,可用作泡沫塑料、粘合剂、工程塑料等。制约该技术大规模应用的关键在于其催化效率低、选择性差以及生产成本高等问题。海南师范大学的朱祺东[22]采用γ-氧化铝为助催化剂,制备了Zn-Fe(III)DMC 和 Zn-Co(III)DMC 催化剂用于二氧化碳、PO共聚反应。研究者发现,Zn-Fe(III)DMC催化剂的催化活性受助催化剂加入量的影响较大,助催化剂含量1%时催化活性较高,聚合产物的数均分子量可达8 873,分子量分布较窄,随着助催化剂的含量升高,活性降低;而对于Zn-Co(III)DMC催化剂,助催化剂的最佳添加量为3%。研究者认为,助催化剂的加入和制备方法的探索可大幅改善催化剂的活性。
蓝健文[23]等人通过溶剂热法成功合成了Ni-MOF 催化剂,用于合成碳酸丙烯酯。研究显示,催化剂中的金属Ni 原子和咪唑中部分未参与配位的-NH 官能团分别作为Lewis 酸碱,活化环氧化物和CO2,促进开环反应的高效进行。研究者系统研究了反应温度、反应时间、助催化剂种类及用量等因素对催化活性的影响,并优化了反应参数,在120℃、2MPa、6h 条件下,碳酸丙烯酯的收率为97%,选择性为99%,相同的条件下,对其他的环氧化物如环氧氯丙烷、环氧丁烷以及氧化苯乙烯也有较好的催化活性,相应产物的收率分别为95%、98%、88%,具有较好的普适性。此外,Ni-MOF 催化剂具有良好催化稳定性,三次循环后,结构没有明显变化。
近年来,许多研究结果提出,通过CO2经碳酸乙烯酯加氢制甲醇联产乙二醇,是CO2高效转化的重要生产工艺之一,这一结果备受学术界和工业界的关注。铜基催化剂表面具有高度稳定分散的Cu纳米颗粒、较强的传质和在低Cu 负载量下平衡的Cu0/Cu+比,非常适合作为碳酸乙烯酯选择性加氢制乙二醇和甲醇的催化剂。Yu[24]等人开发了分层核/壳结构的Silicalite-1@Cu 复合材料用于碳酸乙烯酯加氢反应。原位产生的介孔和强的Cu-硅酸盐相互作用,使得Cu NPs 均匀牢固地固定并高度分散在核心S-1晶体之外。S-1@Cu杂化物具有以合适比例共存的Cu0/Cu+活性物质,是一种高活性、选择性和稳健的碳酸乙烯酯加氢催化剂,可在350h内实现99%以上碳酸乙烯酯转化率和99%以上的乙二醇收率,更重要的是,在相对较低的Cu负载量下(21.4wt%),甲醇收率可达93%。
3 展望
降低二氧化碳大气浓度对世界能源和环境的可持续性发展是挑战,也是机遇。尽管有一些令人鼓舞的报道,但到目前为止,CO2合成高附加值化学品的工业应用很少。这是因为制备过程基本为耗能反应,且目前反应物的转化率、产物的选择性以及能量效率均未达到理想效果。为了确定这些化学品的潜力,有必要对二氧化碳的有效利用技术进行更多的研究,获得更多基本原理、技术和成本方面的细节,以便对这些化学品进行全面评估。
随着国内外学术界对CO2活化机理基础研究的深入,辅之以计算和试验相结合的研究方法,有助于催化剂设计,增加催化剂活性位点数量和催化活性,也有助于开发多种功能的新型催化剂,实现催化剂的高活性和选择性。此外,3E(能源、经济、环境)评估在不久的将来是必不可少的。考虑到化石燃料的短缺、负碳排放目标及碳排放交易政策的逐渐落实,以及先进技术的使用,利用二氧化碳生产能源产品具有巨大潜力,同时,在耗能方面,如采用可再生的风能、太阳能等作为CO2转化的能量来源,对CO2的大规模应用将会是一个重大利好。

