易栓症患者继发慢性缺血性结肠炎误诊为溃疡性结肠炎1例报道
邹诗诗,陈琰琰,徐国斌,黄梅芳,赵 秋,陈 敏,肖书渊
1.武汉大学中南医院消化内科,湖北 武汉 430071; 2.武汉大学病理中心; 3.武汉大学中南医院病理科; 4.武汉大学中南医院影像科; 5.美国芝加哥大学病理科
病例患者,男,34岁,因“间断腹痛腹泻半年余,加重伴便血2个月”于2020年12月入我院。患者于2020年6月无明显诱因出现下腹部阵发性绞痛,排便排气后可稍缓解,伴腹泻,黄色水样便,4~5次/d,无黏液及脓血。外院诊断为感染性肠炎,予抗生素治疗腹痛腹泻好转,停用抗生素后仍有间断腹痛及腹泻。2020年10月患者诉腹痛症状加重,腹泻次数增加,10次/d,伴血便,再次就诊于外院,完善结肠镜检查诊断为溃疡性结肠炎,予5-氨基水杨酸4 g/d口服及调节肠道菌群治疗后患者自觉症状无好转遂来我院复诊。既往肺栓塞及双下肢血管栓塞病史,否认特殊用药史,否认家族遗传病史。
入院体格检查:T 36.9 ℃,HR 93次/min,R 20次/min,BP 132/80 mmHg,全身浅表淋巴结未触及,腹软,下腹部轻压痛,无反跳痛,肝脾肋下未及,移动性浊音阴性,肠鸣音正常,双下肢可见大量斑片状色素沉着(见图1)。
实验室检查:血常规示白细胞13.96×109L-1,中性粒细胞比例87.6%,淋巴细胞比例6.0%,血红蛋白152 g/L,血小板135×109L-1;粪便常规示淡红色稀便,白细胞1~2/HP,红细胞+++,潜血+。红细胞沉降率12 mm/h,C-反应蛋白6.4 mg/L。EB病毒DNA阴性,巨细胞病毒DNA阴性。凝血像正常,D-二聚体3 588 ng/ml,抗心磷脂抗体阴性,抗凝血酶88%(正常范围内),蛋白C 107%(正常范围内)。

图1 患者双下肢可见大量斑片状色素沉着Fig 1 Patchy pigmentation in the lower limbs
CT全腹部血管成像(含平扫+腹腔干+门静脉+下腔静脉):左下腹降结肠及所及乙状结肠全程管壁明显增厚,呈分层状改变,肠周环绕明显水样密度絮状影,CTA示左下腹结肠周围可见多发小血管影伴行,腹腔干动脉未见明显异常(见图2);肝左内叶包膜下楔形弱强化区,动脉期可见其供应区局部分支小血管显示不清,灌注异常;CTV示门静脉多发分支迂曲血管,考虑门静脉海绵样变性表现(见图3)。
结肠镜检查:结肠距肛门35 cm至肛门黏膜弥漫性充血水肿,表面糜烂,覆脓性分泌物,血管网模糊,呈颗粒样增粗,发红黏膜间可见苍白区(见图4)。肠镜活检组织病理示表面上皮缺失,间质实变,隐窝萎缩,呈非特异性缺血改变,病理诊断炎症性肠病证据不足。
治疗:综合患者病史、症状、体征、实验室检查、CT、结肠镜及病理活检,诊断为易栓症继发的慢性缺血性结肠炎,给予低分子肝素及银杏叶片口服改善循环治疗1周,疗效欠佳,经多学科会诊后行手术治疗,手术病理大体见左半结肠黏膜弥漫鹅卵石样外观,部分肠壁增厚变硬,部分肠壁变薄,肠系膜大部呈暗红色伴梗死,肠周可见脂肪蔓生;镜下见结肠黏膜呈缺血性改变,部分隐窝凋零,局部溃疡并局灶上皮修复性改变(见图5A)。黏膜层淋巴浆细胞浸润不明显,黏膜固有层、黏膜下层及浆膜下层小血管增生及扩张、充血(见图5B),部分血管周围轻度纤维化。可见中等大小血管内血栓机化再通(见图5C)。术后予长期抗凝治疗,现患者一般情况良好,正在密切随访观察中。

注:A~B:轴位平扫图像,示降结肠、乙状结肠肠壁弥漫性增厚(白色箭头);C:冠状位平扫图像,示乙状结肠肠壁弥漫性增厚(白色箭头);D:冠状位动脉期图像,示左下腹结肠周围多发小血管影。
讨论缺血性结肠炎是结肠血流低灌注不足以维持细胞代谢和局部再灌注损伤所导致的结肠细胞酸中毒、功能失调直至死亡。2009年发表的大样本流行病学研究表明,缺血性结肠炎的发病率为16.3例/10万,2年和5年的累积复发率分别为3.3%和7.5%[1]。
缺血性结肠炎易发生于患有心血管疾病、肺部疾病、慢性肾脏疾病的老年患者。值得注意的是,易栓症与缺血性结肠炎的发生密切相关[2]。年轻患者出现缺血性结肠炎时,易栓症是必须评估的危险因素,遗传多态性在缺血性结肠炎的发病机制中起重要作用,蛋白C、蛋白S、抗凝血酶Ⅲ和因子Ⅴ Leiden突变据报道与易栓症高度相关[2-4]。我们报道的本例缺血性结肠炎患者为33岁的年轻男性,慢性复发性病程,综合既往肺栓塞及双下肢栓塞病史,体格检查见双下肢栓塞后导致的皮肤坏死,CT所见结肠周围多发迂曲小血管、肝左内叶包膜下楔形弱强化区及其供应区局部分支小血管灌注异常、门静脉海绵样变性,提示患者存在高血栓栓塞倾向即易栓症。

注:A:轴位图像,示肝左内叶包膜下楔形弱强化区;B:MIP图像,示肝内门静脉多发分支迂曲稍粗血管影,肝门部显著。
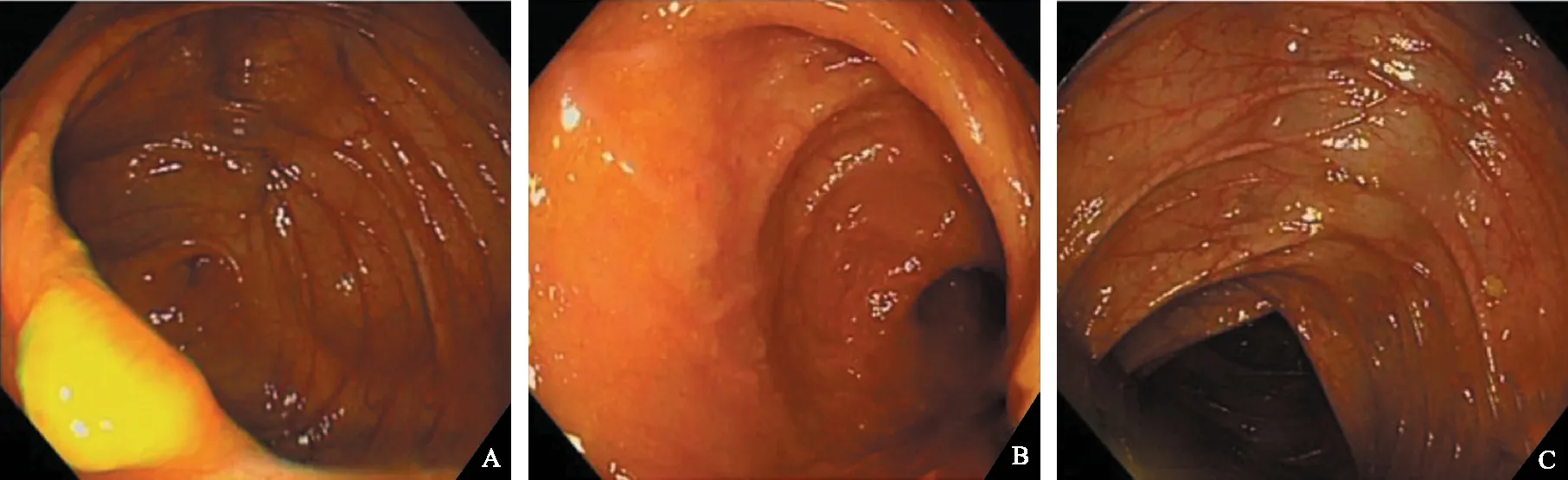
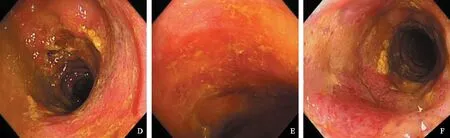
注:图A为回盲部,图B为升结肠,图C为横结肠,为正常肠黏膜;图D为降结肠,图E为乙状结肠,图F为直肠,示黏膜弥漫性充血水肿,表面糜烂,覆脓性分泌物,血管网模糊,呈颗粒样增粗,发红黏膜间可见苍白区。

注:A:手术病理:结肠陈旧性溃疡伴上皮修复性再生,邻近黏膜隐窝变小,固有层实变;B:黏膜坏死伴隐窝消失与炎性渗出,基底部残存少许隐窝,黏膜固有层内小血管玻璃样变伴透明血栓,黏膜下层小血管增生、扩张、充血,溃疡底部可见以淋巴细胞为主的少许炎症细胞浸润;C:血栓机化再通伴含铁血黄素沉着。
缺血性结肠炎由于其症状、影像学表现、结肠镜及活检缺乏特异性易被误诊为炎症性肠病,本例患者被误诊为溃疡性结肠炎有以下原因:(1)二者的临床症状相似,缺血性结肠炎最常见的症状为腹痛,其次为便血、腹泻及呕吐,溃疡性结肠炎同样表现为持续或反复发作的腹泻、黏液脓血便伴腹痛。(2)病程上炎症性肠病为慢性病程,缺血性结肠炎症状通常在2~3 d内消失,1~2周痊愈,但本患者因易栓症为不可逆的危险因素,结肠血流低灌注不可逆,故表现为慢性病程,慢性缺血性结肠炎的定义尚未统一,ACG指南建议将临床症状超过3个月并组织学证明的结肠缺血定义为慢性[5]。(3)发病部位上:结肠血流由三条血管供应:肠系膜上动脉、肠系膜下动脉和痔上动脉。由于结肠的解剖结构缺血易发生于结肠“分水岭”区,包括脾区及乙状结肠,直肠有相对丰富的内脏动脉和全身动脉系统的双重供血,较少出现缺血[6-8],但本患者的发病部位不典型,与溃疡性结肠炎相似,同样表现为从直肠开始的弥漫性、连续性病变。(4)溃疡性结肠炎活动期凝血纤溶亢进状态可继发于肠道炎症,与本例易栓症继发缺血性结肠炎查凝血功能均可表现为D-二聚体升高。(5)影像学上缺血性结肠炎典型征象为节段性肠壁增厚、拇指印、结肠周围脂肪滞留,无特异性,也可见于炎症性肠病患者,CTA可用于识别有无大血管闭塞但缺血性结肠炎通常为非闭塞性。(6)结肠镜下缺血性结肠炎的表现无特异性,也可模仿炎症性肠病,活检中黏膜结构改变易被缺乏经验的病理医师误诊为炎症性肠病。(7)病因学上,Wakefield和Sawyerr提出,多灶性胃肠道梗死和反复的血栓性肠系膜微血管闭塞在炎症性肠病的病因中起重要作用,易栓症患者的慢性缺血性结肠炎有相似的疾病发展过程[9-11],导致了两者难以鉴别。
但仔细分析,可以发现本病例与溃疡性结肠炎鉴别诊断的线索。(1)患者有除肠道外的多部位血管病变,溃疡性结肠炎可有肠外表现,但少见血管相关的异常。(2)结肠镜下我们发现患者病变结肠发红黏膜间可见苍白区,提示患者存在结肠缺血,有助于鉴别。(3)病理尤其是大标本切除病理检查是缺血性结肠炎与溃疡性结肠炎最重要的鉴别依据,大部分缺血性结肠炎患者病理表现不具特异性,部分患者仅见黏膜和黏膜下出血和水肿,毛细血管纤维蛋白血栓伴中性粒细胞浸润[12],而溃疡性结肠炎的病理表现具有特异性,活动期可见黏膜内弥漫性急性、慢性炎症细胞浸润,可见隐窝炎,乃至形成隐窝脓肿;隐窝结构改变,隐窝大小、形态不规则,分支、扭曲、排列紊乱等;黏膜表面糜烂、浅溃疡形成[13]。
目前报道的易栓症导致的慢性缺血性结肠炎病例中,病理一般只涉及活检,手术病理的相关报道少见,本文提供了手术病理证据,帮助临床医师更好地认识这一少见的疾病实体。
综上所述,我们报道了1例误诊为溃疡性结肠炎的易栓症继发的慢性缺血性结肠炎病例,通过本病例提醒临床医师慢性缺血的临床表现、内镜表现和影像学表现可能与急性缺血完全不同,可表现为酷似溃疡性结肠炎,需仔细鉴别,从细节中找差别;长期慢性缺血内科治疗疗效欠佳时可考虑手术治疗。

