鼠神经生长因子联合多奈哌齐对老年痴呆患者炎症因子和认知功能的影响*
刘长仁, 王乐, 王海兵, 田青
(中国人民解放军海军第九七一医院 保健三科, 山东 青岛 266071)
老年痴呆俗称阿尔兹海默病(alzheimer's disease,AD),是老年人群常见的神经系统疾病[1],以中枢神经系统退行病变导致的认知功能减退和记忆功能障碍为主要临床表现[2]。AD患者随着认知功能和记忆功能减退,会出现时间地点定向能力障碍,记忆能力严重损伤及自理能力丧失[3],患者生活不能自理,也给其照料者造成了较大的经济和心理负担[4]。AD的发生机制目前尚不明确,有研究认为小胶质细胞介导的炎症反应与AD的发生和发展有密切的关联,小胶质细胞能通过分泌白细胞介素-1β(interleukin-1β,IL-1β)、IL-6及肿瘤坏死因子-α(Tumor necrosis factor-α,TNF-α)等炎症因子,介导并增强神经细胞的炎症反应,从而加剧神经元的损伤[5]。多奈哌齐是治疗AD的常用药物,属于可逆性中枢乙酰胆碱酯酶(acetylcholine esterase,AChE)抑制剂,可通过提升中枢神经系统的乙酰胆碱的水平,调节胆碱能神经元从而改善认知功能;但是多奈哌齐对于神经炎症反应损伤并无明显的改善作用[6]。鼠神经生长因子(mouse nerve growth factor,mNGF)是一种新型的神经保护剂,能改善神经损伤、促进神经细胞再生,主要被用于外周神经损伤疾病的治疗[7]。目前关于mNGF对AD患者炎症因子和认知功能影响的相关研究比较少[8]。本次研究采用mNGF联合多奈哌齐对AD患者进行治疗,观察对AD患者炎症因子和认知功能的影响。报告如下。
1 资料与方法
1.1 一般资料
选择92例AD患者作为研究对象,其中男52例、女性40例,年龄65~83岁、平均(72.8±5.6)岁,病程0.8~7年、平均(3.1±1.5)年,受教育年限6~13年、平均(8.7±2.1)年,轻度痴呆39例、中度痴呆53例。纳入标准:(1)经相关影像学检查确诊符合《精神科疾病临床诊断与治疗方案》中AD的标准;(2)年龄65岁或以上;(3)家属知情并同意参与研究;(4)临床资料完整。排除标准:(1)血管性痴呆;(2)存在脑器质性疾病;(3)有脑外伤史;(4)合并癫痫等其他精神疾病造成的认知功能减退;(5)有药物成瘾史;(6)有听力或者交谈障碍;(7)中途退出本研究患者。采用随机数字表法将92例AD患者分为观察组和对照组,每组46例。
1.2 治疗方法
两组患者在入院后均予以控制血压、血糖、抗血小板治疗、补充维生素C、营养脑细胞等基础处理治疗,并进行认知、语言康复训练。对照组患者给予多奈哌齐(陕西方舟制药有限公司,H20030583,规格5 mg)5 mg/次,每日服药1次。观察组则选择mNGF[舒泰神(北京)药业有限公司,S20060023,规格30 μg]联合多奈哌齐治疗。多奈哌齐的用药剂量与对照组相同,mNGF 20 μg、采用2 mL生理盐水充分溶解后肌注,每日给药1次。2组患者均治疗8周。
1.3 观察指标
1.3.1血清IL-1β、IL-6及C反应蛋白(C reactive protein,CRP)水平测定 治疗前及治疗8周时,分别采集2组患者空腹静脉血2 mL,3 000 r/min离心10 min分离血清,采用酶联免疫吸附法检测血清IL-1β、IL-6及CRP水平,严格按试剂盒说明书进行相关操作。
1.3.2认知功能、痴呆程度评估 治疗前及治疗8周时,采用AD评定量表认知分量表(cognitive scale of AD rating scale,ADAS-cog)和临床痴呆评定量表(clinical dementia rating,CDR)进行评估2组患者的认知功能及痴呆程度。ADAS-cog量表共包括语言、结构、注意力、意向、定向力等12个条目,满分70分,分值越高,则认知障碍的程度越严重。CDR量表评估的内容主要包括记忆能力、空间定向能力、社会生活能力、个人生活自理能力等6个维度,分为0~3分共5个等级,等级越高则表示痴呆越严重。
1.3.3临床疗效和不良反应发生率 临床疗效根据AD病理行为量表(BEHAVE-AD)的减分率进行评估,减分率≥80%为基本痊愈、60%~<80%为显效、30%~<60%为好转、<30%为无效,总有效=基本痊愈+显效+好转。
1.4 统计学方法
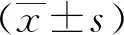
2 结果
2.1 一般资料
结果显示,2组AD患者的性别、年龄、病程、受教育时间、AD程度及合并症比较,差异无统计学意义(P>0.05)。见表1。
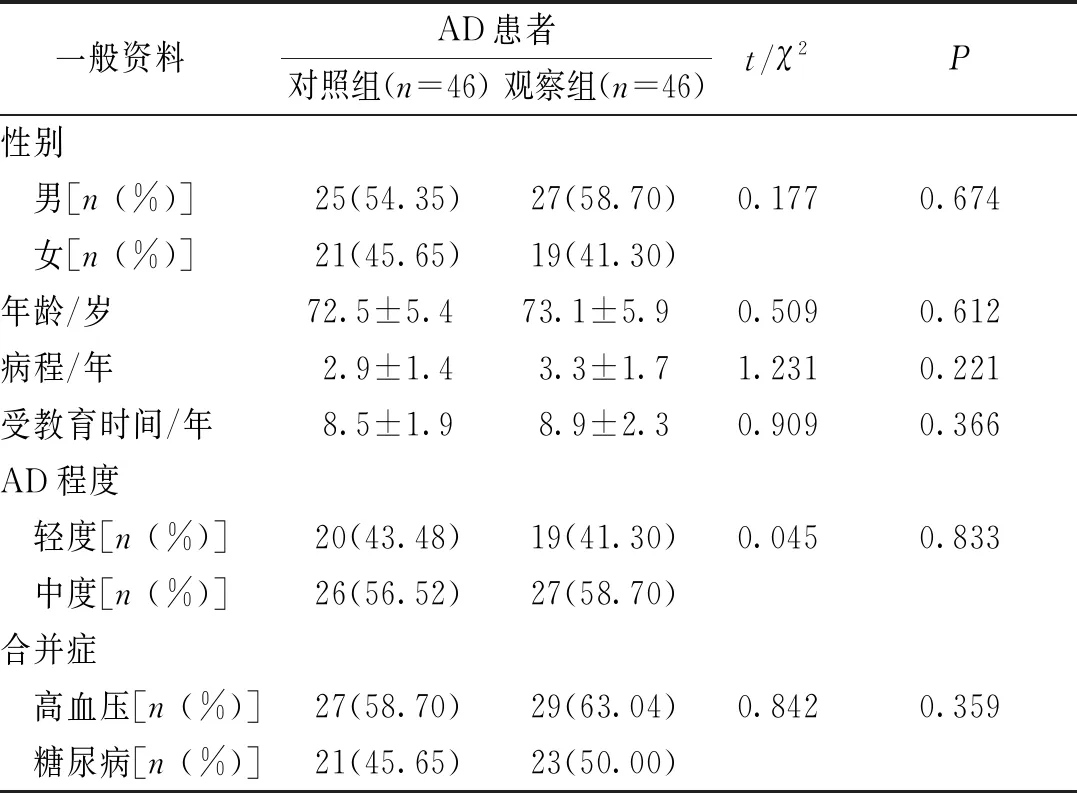
表1 两组AD患者一般资料比较
2.2 血清IL-1β、IL-6及CRP水平
结果显示,治疗前,2组AD患者血清IL-1β、IL-6及CRP水平比较,差异无统计学意义(P>0.05);治疗8周时,2组患者血清IL-1β、IL-6及CRP均低较治疗前降低,且观察组低于对照组,差异有统计学意义(P<0.05)。见表2。
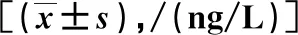
表2 治疗前后2组AD患者血清IL-1β、IL-6及CRP水平比较
2.3 ADAS-cog、CDR评分
结果显示,2组AD患者治疗前的 ADAS-cog、CDR评分比较,差异无统计学意义(P>0.05);治疗8周时,2组患者ADAS-cog、CDR评分均低较治疗前降低,且观察组低于对照组,差异有统计学意义(P<0.05)。见表3。 提示治疗后2组AD患者的认知功能均有改善,且观察组患者更明显。
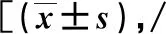
表3 治疗前后2组AD患者ADAS-cog、CDR评分比较分]
2.4 临床疗效
结果显示,观察组AD患者的治疗总有效率高于对照组,差异有统计学意义(χ2=4.420,P=0.036)。见表4。
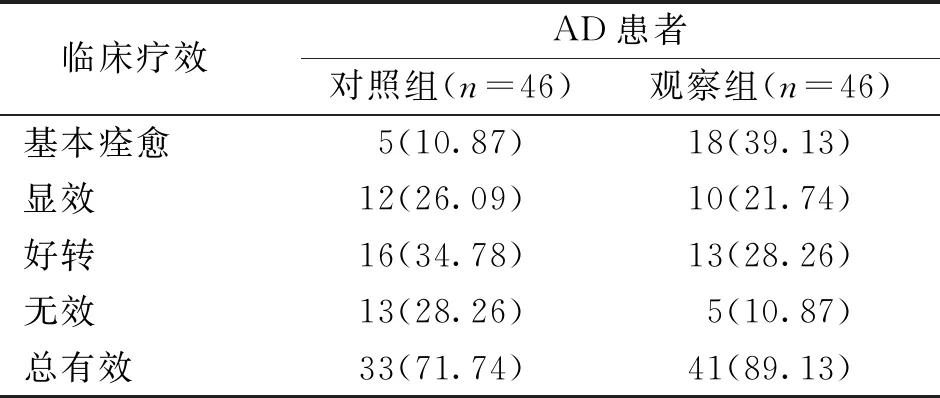
表4 两组AD患者的治疗有效率比较[n(%)]
2.5 不良反应发生率
2组患者的不良反应程度比较轻,未影响治疗,在停药后相关症状消失。2组患者的不良反应发生率差异无统计学意义(χ2=0.717,P=0.397)。见表5。

表5 两组AD患者的不良反应发生率比较[n(%)]
3 讨论
目前,AD缺乏有效的根治性治疗药物,主要以改善临床症状为主,其发病机制也尚不明确[9]。乙酰胆碱是参与认知功能和学习记忆的重要神经递质,有临床研究发现AD患者的乙酰胆碱合成分泌减少,造成摄取不足,活性下降[10]。多奈哌齐是AChE的抑制剂,是治疗AD的常见药物。主要通过选择性抑制中枢神经系统AChE的活性,控制乙酰胆碱的分解,提升它在突触间隙中的水平,从而增强胆碱能神经元的突触传递效能,改善认知功能减退[11]。它一定程度上还能拮抗β-淀粉样蛋白沉积造成的神经毒性作用,减少神经元的损伤。但是多奈哌齐单药应用对于AD患者的认知功能改善效果有限[12]。
脑部局灶性炎性反应是AD患者神经元损伤的重要影响因素。IL-1β、IL-6等促炎症因子,能促进炎症反应的发生和发展[13]。而CRP则是机体炎症反应的敏感指标。温国辉等[14]的研究显示,AD患者的认知功能障碍程度与其CRP、IL-6等促炎症因子水平之间呈正相关。因此改善脑部炎症反应,对于控制脑神经元损伤的进展有积极意义。本研究中,应用mNGF联合多奈哌齐治疗的观察组血清IL-1β、IL-6以及CRP均低于对照组,且观察组ADAS-cog、CDR评分均低于对照组,总有效率高于对照组(P<0.05)。提示在AD患者的治疗中,联用应用mNGF、多奈哌齐,能降低炎症细胞因子水平,改善炎症反应造成的神经损害,对于认知功能障碍和痴呆症状均有更好的改善作用,疗效更明显。mNGF是来源于小鼠的神经营养因子,具有较高的生物活性,能营养神经元,促进神经元的生长和分化,还能促进相关功能蛋白和结构蛋白的合成,有助于受损神经纤维的再生增殖,修复其损伤,从而改善相关的认知功能障碍。动物实验显示,肌注给药,对于大鼠周围神经损伤及交感神经末梢损伤的恢复均能起到较好的促进效果[15]。近年来,mNGF在颅脑损伤、癫痫、帕金森综合征等中枢神经损伤疾病的临床治疗中均有所应用,其神经损伤的修复作用已被临床所证实[16]。李晓飞等[17]研究也显示,mNGF能降低AD的IL-1β、IL-6等血清细胞因子。推测可能是由于mNGF还能增加血管内皮生长因子的分泌,能增加局部病灶的血氧供应,改善局部微循环,抑制活性氧自由基的过度产生,从而能一定程度上减轻局灶性的炎症反应,起到控制神经炎症反应损伤进展的功效。因此mNGF与多奈哌齐联用,能从修复神经元损伤、控制炎症反应以及增强乙酰胆碱能不同的作用机制进行改善认知功能,提升临床疗效[18-19]。本次研究对联用的不良反应进行分析了,结果显示,2组的不良反应发生率相比,差异无统计学意义(P>0.05)。提示mNGF不良反应主要为一过性的荨麻疹及局部疼痛,因此联用mNGF的安全性良好[20]。不过本次研究纳入的样本量有限,也没有进行远期疗效的随访,且mNGF具体的抗炎机制还未明确,因此后续还需扩大样本量进行进一步的深入研究。
综上,在AD患者的治疗中,联用应用mNGF、多奈哌齐,能改善炎症细胞因子水平,修复神经元损伤,从而有助于提升患者的认知功能,缓解其痴呆症状,疗效更明显,且不良反应较少。

