新型口服抗凝药物在遗传性易栓症中的应用
唐亮(Tang Liang),卢惠(Lu Hui),胡豫(Hu Yu)
(华中科技大学同济医学院附属协和医院血液病研究所,武汉 430022;
随着科学研究的不断发展,对于遗传性易栓症的了解也越来越深入[1-3]。遗传性易栓症的主要临床表现为静脉血栓栓塞症(venous thromboembolism,VTE),最多见于深静脉血栓形成(deep venous thrombosis,DVT)和肺栓塞(pulmonary embolism,PE)。因此,预防血栓形成是遗传性易栓症患者长期管理中的重要一环。传统的抗凝方式主要是通过口服维生素K 拮抗剂(vitamin K antagonists,VKAs)华法林或通过静脉或皮下注射肝素来治疗或预防VTE 的发生。但肝素类药物需注射使用,长期使用依从性难以保障;而华法林需定期监测国际标准化比值(international normalized ratio,INR),易受食物和众多药物间相互作用的影响[4]。目前已有新型口服抗凝药物(novel oral anticoagulants,NOACs)用于治疗遗传性易栓症的病例报道,也有关于NOACs治疗遗传性易栓症的更高质量的队列研究正在开展,希望能够为治疗遗传性易栓症提供更多和更优的方案。
1 NOACs 的概述
1.1 NOACs 的一般特性
不同于VKAs 作用于多种凝血因子,NOACs 通过抑制凝血级联反应中个别凝血因子的激活而发挥作用。NOACs 主要包括两类:一类是直接凝血酶抑制剂(direct thrombin inhibitor,DTI)——达比加群酯;另一类是FⅩa 抑制剂——国内主要有利伐沙班、阿哌沙班和艾多沙班。DTI 既能抑制游离的凝血酶也能抑制与血凝块结合的凝血酶;而FⅩa 抑制剂仅选择性的单独抑制FⅩa,从而影响凝血酶原复合物的生成,而不直接抑制凝血酶,且对血小板没有影响[5]。
达比加群酯于2013年在我国批准上市,药品经胃肠道吸收转化为达比加群后与凝血酶结合从而阻断纤维蛋白原转化为纤维蛋白以阻止血栓形成[6]。80%的达比加群在肾脏被代谢清除;利伐沙班是首个口服FⅩa 抑制剂,于2009年在我国上市销售。经口服吸收后,其生物利用度可达80%及以上。利伐沙班的半衰期约为5~9 h,35%由肾脏清除;阿哌沙班,同样也属于FⅩa 抑制剂,2013年CFDA 批准其在中国上市用于成人择期髋关节置换术患者VTE 的预防。其结构更优,具有良好的抗凝作用,被认为是一种安全、耐受性好、有效的口服抗凝剂。阿哌沙班的半衰期为12 h,25%由肾脏代谢清除;艾多沙班,是最新上市的FⅩa 抑制剂。2015年欧洲药品管理局(European Medicines Agency,EMA)批准其用于DVT 和PE 的预防和治疗。艾多沙班的半衰期为10~14 h,50%由肾脏代谢清除[7]。
抗凝药物使用过程中对于出血事件的预防管理不可或缺。使用传统抗凝药物VKAs 抗凝时,可使用VitK 作为解毒剂。使用NOACs 抗凝时,NOACs拮抗剂可用于紧急处理出血事件。达比加群与凝血酶的结合是可逆的,因而它也可从结合体上解离下来。此外,依达赛珠单抗(idarucizumab)是首个批准的NOACs 特异性拮抗剂,其与达比加群的亲和力是凝血酶的350 倍,可成功用于达比加群治疗后的大出血[8]。Andexanet alfa 作为FⅩa 抑制剂的拮抗剂,通过特异性结合FⅩa 抑制剂后,使得FⅩa 抑制剂血浆浓度迅速下降,进而恢复生理性FⅩa 的止血作用,已被FDA 批准用于逆转利伐沙班、阿哌沙班等使 用 后 的 大 出 血[9]。Ciraparantag (Aripazine/PER977)是一种广谱抗凝剂,通过氢键与凝血酶抑制剂及FⅩ抑制剂结合来逆转其抗凝作用[10-11]。
1.2 NOACs 的优势与缺点
与传统口服抗凝剂相比,NOACs 有其独特的优势:①安全性更优,NOACs 达峰时间短,起效快,代谢快,且使用NOACs 患者发生出血性事件(如颅内出血事件)的概率低[12];②与食物、药物之间的相互作用较传统抗凝药物少,因此无需常规监测凝血功能;③有效剂量变化范围小,固定剂量能适合大多数人,从而能提高患者的依从性。不可回避,NOACs也存在着一定缺点,如:①NOACs 半衰期短,若患者漏服,易引起严重的并发症;②NOACs 由肾脏及肝脏代谢排出体外,对于肝、肾功能不全的患者易造成进一步的负担;③对于服用NOACs 的患者还可能影响实验室检测,例如服用达比加群酯、利伐沙班及阿哌沙班可能影响对FVL 缺陷患者APCR 的监测,服用FⅩa 抑制剂可能影响抗凝血酶(AT)和PS 水平和活性的监测[13-14]。因此,对于服用NOACs 的患者,需注意可能造成的遗传性易栓症监测假阳性及假阴性风险的增加。
2 NOACs 在遗传性易栓症患者中的应用
对于遗传性易栓症患者给予NOACs 进行抗凝防治已在易栓症诊断与防治中国指南(2021年版)中得到推荐[15]。然而对于不同NOACs 治疗不同类型的易栓症患者的疗效及安全性的差异,目前仍无明确的答案。以下总结了部分关于NOACs 用于遗传性易栓症患者的病例报道(表1)及相关研究数据。
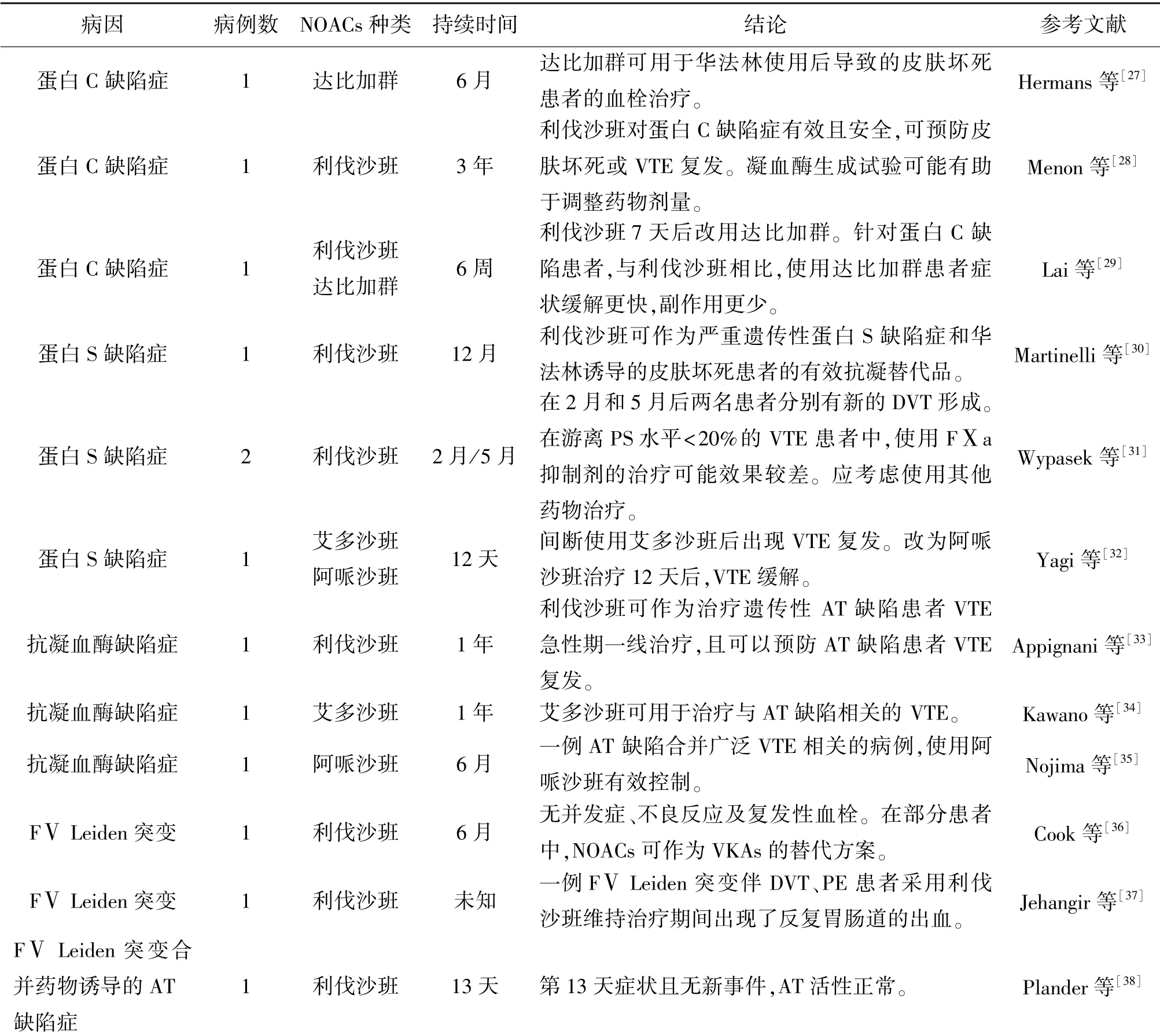
表1 NOACs 治疗遗传性易栓症的病例报道总结
McBride 等回顾性分析了13 名患有遗传性易栓症并诊断为VTE 的患者采用NOACs 进行抗凝治疗的情况。在经过2年的中位随访时间,1 例(8%)出现复发性VTE,2 例(15%)出现出血性事件。这表明NOACs 用于遗传性易栓症患者抗凝治疗及VTE 预防具有良好的疗效[16]。另一队列研究共纳入181 名遗传性/获得性易栓症患者,其中96 名(包括抗磷脂综合征患者10 名)接受NOACs 抗凝治疗,另外85 名(包括抗磷脂综合征患者12 名)接受VKAs 治疗,结果显示,NOACs 治疗组VTE 的有效性与VKAs 相似,并且导致的临床相关的出血事件显著减少[17]。Undas 团队于2017年报道33 名患有严重易栓症患者接受NOACs(包含阿哌沙班、达比加群和利伐沙班)治疗的疗效,其中3 名(9%)患者出现了复发性VTE[18]。随后该团队于2021年再次报道了一项包含56 名严重易栓症患者使用NOACs 治疗效果的队列研究,结果表明,全剂量的达比加群或阿哌沙班对严重遗传性易栓症患者有效且安全[19]。
除此之外,部分报道的NOACs 用于VTE 患者的随机临床试验中也涉及NOACs 在易栓症患者相关VTE 中应用的疗效数据。Gaddh 等荟萃了八项包含有易栓症患者应用NOACs 的2 至3 期随机对照试验,对其中比较NOACs 与肝素/VKAs 治疗易栓症患者相关VTE 疗效的数据进行提取分析,其中涉及遗传性易栓症研究的临床试验有三项(EINSTEIN-DVT,EINSTEIN-PE 和Hokusai-VTE),使用的NOACs 有利伐沙班和艾多沙班[20-22]。经荟萃分析后表明:NOACs 的疗效和安全性与VKAs相似,可用于治疗和预防各种易栓症患者的VTE[23]。在RE-MEDY 临床试验中,比较了在易栓症患者中使用达比加群(262 例)与华法林(263例)的疗效差异,结果显示两组患者的VTE 复发率及VTE 相关死亡率没有差异,即达比加群可作为易栓症患者传统抗凝药物的替代。然而,该人群中还包括获得性易栓症——抗磷脂综合征患者67例,且迄今为止没有报告任何亚组分析。因此仍无法确定具体某一类型的遗传性易栓症患者中NOACs 的疗效[24-26]。
2.1 抗凝血酶缺陷症和蛋白C/S 缺陷症
在我国及亚洲地区,遗传性易栓症以抗凝蛋白缺陷(抗凝血酶缺陷症、蛋白C 缺陷症和蛋白S 缺陷症)为主。对于AT 缺陷症并发血栓的患者,常用的治疗方法为肝素、华法林以及AT 替代疗法。几项病例报道分别发现利伐沙班、艾多沙班和阿哌沙班治疗AT 缺乏相关的VTE 效果显著,且可以预防VTE 复发[33-35]。此外,Plander 等的报道中还发现利伐沙班对于药物相关的获得性抗凝血酶缺陷症也有效,该患者同时合并FⅤLeiden 突变[38]。Fukuda等在动物实验中发现在血浆AT 抗原和活性低的小鼠中,FⅩa 抑制剂艾多沙班较肝素能展现出更好的抗血栓作用[39]。
PC 和PS 是肝脏合成的维生素K 依赖的糖蛋白。PS 可以作为蛋白C 的辅因子,协助灭活FⅤa和FⅧa;也可以作为组织因子途径抑制物辅因子,提高组织因子途径抑制物对FⅩa 的灭活能力;除此之外,还可以直接抑制FⅩ的激活。在口服华法林治疗蛋白C 或蛋白S 缺乏症时,由于华法林在抑制维生素K 依赖的凝血因子的同时也会抑制体内PC和PS 的合成。因此,口服华法林伴随机体PC、PS的缺乏会导致体内高凝状态从而形成微血栓造成皮肤坏死,引起华法林诱导的皮肤坏死(warfarininducedskin necrosis,WISN)。部分病例报道已展示利伐沙班、达比加群在治疗蛋白C 缺陷症患者中效果,且对于伴WISN 患者,使用NOACs 能使患者症状缓解更快,副作用更少[26-29]。然而对于NOACs在蛋白S 缺陷症患者中的应用,在不同的报道中却显示出相矛盾的结果。一名患者在使用利伐沙班治疗后展示出良好疗效,并且能使WISN 症状缓解[30]。然而另外两名患者分别使用利伐沙班治疗蛋白S 缺乏症2月和5月后均出现新的VTE[31]。这一矛盾的结果,可能是由于不同患者体内PS 的活性的差异导致的,还需要后续的大型研究来进一步说明。
2.2 FⅤLeiden 突变和凝血酶原基因G20210A 突变
在欧美人群中,遗传性易栓症主要以凝血功能增强的FⅤLeiden 突变和凝血酶原基因G20210A突变为主,该类突变我国人群中罕见。FⅤLeiden突变是发生在FⅤ基因10 号外显子第1691 位核苷酸的突变,该突变造成了活化蛋白C 抵抗(activated protein C resistance,APCR)现象,从而使得FⅤa 被APC 裂解速度减慢,凝血酶活性增强,血栓形成风险增加。FⅤLeiden 突变的患者初始治疗一般选用肝素,后续改为华法林。Cook 等曾报道一则使用利伐沙班成功治疗FⅤLeiden 突变患者相关VTE 的案例,患者无不良反应及复发性血栓形成[36]。而在另一报道中一例FⅤLeiden 突变伴DVT、PE 患者采用利伐沙班维持治疗期间出现了反复胃肠道的出血[37]。此外,达比加群也成功用于FⅤLeiden 突变的抗凝治疗[18]。这些病例报道提示我们NOACs可能可作为部分患者VKAs 的替代治疗。
凝血酶原基因G20210A 突变是较FⅤLeiden突变稍弱的VTE 危险因素。它发生在凝血酶原基因3’端非翻译区第20210 位G-A,可导致血浆凝血酶原水平升高,增加静脉血栓发生的风险。除了使用华法林进行抗凝治疗外,Undas 等报道了4 名凝血酶原基因G20210A 突变患者使用利伐沙班、达比加群抗凝治疗的情况。其中一名患者虽然在使用利伐沙班抗凝治疗12 个月后,出现了复发DVT,但随后的治疗采用达比加群后,在17 个月的随访期间,未观察到复发性VTE 或严重出血事件[18]。
3 展望
随着人们对遗传性易栓症的认识不断提高,越来越多的遗传性易栓症患者能找到确切病因。NOACs 由于其独有的优势,成为血栓性疾病治疗中的明星药物。NOACs 也可作为遗传性易栓症患者抗凝治疗的选择,现有的研究表明,其在安全性及有效性方面并不劣于传统抗凝药。根据既往病例报道及临床研究结果,除根据不同患者肝、肾功能等情况制定个体化的临床方案外,还得出以下提示:1.对于血浆AT 活性降低的AT 缺乏症患者,尤其是肝素结合区突变,因传统抗凝药物肝素的抗凝效果依赖于AT,可能导致肝素的抗凝效果不佳。因此,对于AT缺乏患者血栓急性期可以考虑使用NOACs 进行抗凝治疗,可能更具有理论上的优势[37-38];2.口服华法林治疗蛋白C 或蛋白S 缺乏症时,由于华法林在抑制维生素K 依赖的凝血因子的同时也会抑制体内PC 和PS 的合成,因此对于PC 或PS 缺乏的易栓症患者长期抗凝药物选择NOACs 亦具有可能的理论优势。此外,利伐沙班或达比加群可用于逆转华法林诱导的蛋白质C 缺乏症患者的WISN;3.对于FⅤLeiden 突变患者,使用NOACs 应注意可能会造成APCR 测定中的凝血时间的延长,造成检测结果的不准确。建议可以通过直接DNA 检测方法进行FVL 检 测 或在消除NOACs 干扰 后检 测[13,38]。当前,有关于NOACs 在遗传性易栓症中应用情况的大型临床研究还较少,且缺乏进一步的亚组分析以便指导不同病因的遗传性易栓症患者药物的选择。因此,今后还有待开展大型的随机对照临床研究来评估NOACs 抗凝治疗中VTE 复发率、出血事件发生率及致死致残率等指标,从而进一步指导临床上药物的选择以及治疗方案的制定。
作者贡献声明胡豫、唐亮、卢惠撰写该文章;胡豫负责整体的设计及修正
利益冲突所有作者均声明不存在利益冲突

