不同肾替代治疗下患者营养不良与生命质量的相关性研究
李家青,刘 青,周 竹,杨 晴,袁敦禄,李 青
(昆明医科大学第一附属医院 肾脏内科 云南省慢性肾病临床医学研究中心,云南 昆明 650031)
尿毒症是由各种原发性或继发性肾脏疾病引起的最严重的肾功能衰竭阶段,是一个全球性的公共卫生问题[1]。中国慢性肾脏疾病的患病率为10.8%,已有超过300万慢性肾脏病患者进展到尿毒症[2]。肾替代治疗(renal replacement therapy,RRT)是目前治疗尿毒症最有效的方法,常见的肾替代方式包括血液透析(hemodialysis,HD)、腹膜透析(peritoneal dialysis,PD)和肾移植(renal transplantation,RT)[3]。肾替代治疗可减轻尿毒症患者的症状,延长寿命。尽管在治疗尿毒症方面已经取得了进展,但患者的临床结局仍不理想[4]。患者常伴随营养不良,影响其生命质量、住院率和死亡率。因此,本研究通过修正的主观整体定量评估(modified quantitative subjective global assessment,MQSGA)评价3种肾替代治疗方式下的尿毒症患者的营养状况,探讨不同肾替代治疗方式下的营养状况与生命质量之间的相关性,从而为尿毒症患者的慢性疾病管理和治疗提供依据,现报告如下。
1 对象和方法
1.1 研究对象
选取2020年1-7月云南省昆明市、普洱市2家三甲医院中进行肾替代治疗的尿毒症患者,接受HD、PD和RT的患者基于年龄、并发症和治疗时间按1∶1∶1配对,共获取168个样本。纳入标准:(1)肾小球滤过率(GFR)<15 mL/min(1.73 m2);(2)RRT治疗3个月以上;(3)年龄≥18岁;(4)愿意接受问卷和体检评估。排除标准:神志不清、恶性肿瘤、近期大手术、不愿配合的患者。该研究经本院医学伦理会审批,所有参与者知情并签署知情同意书。HD、PD和RT 3种肾替代治疗的诊断依据ICD-10,治疗依据《中国肾脏病临床诊疗指南》。有部分病例采用HD+PD双重透析模式,为避免HD和PD的相互影响,我们排除了这些病例。
1.2 评估标准
1.2.1 MQSGA是一种广泛用于营养状况评估的无创评分量表
包括七个方面:在过去6个月内体重变化、饮食摄入量、胃肠症状、生理功能状态、透析并发症、皮下脂肪减少、肌肉消耗。每个方面的得分从1分(正常)到5分(严重),总分从7-35分,得分越低说明营养状况越好。
营养正常:总分不超过10分;轻中度营养不良:11~20分;严重营养不良:21~35分。
1.2.2 健康调查简表(the mddical outcomes study-short-from-36-item healthy survey,SF-36)
主要包括2个方面:心理健康总评(mental component summary,MCS)和躯体健康总评(physical health score,PHS)。从生理机能(physiological function,PF)、一般健康(general health,GH)、生理职能(role physical,RP)、身体疼痛(bodily pain,BP)、情绪状态(emotional state,ES)、情感职能(role emotional,RE)、社会功能(social function,Socf)和精力(Energy)8个方面评分[5]。根据SF-36量表的评分规则,将原始评分进行转换,然后计算各个领域的分支评分和最终评分。分数范围为0~100,得分越高,生命质量越好[6]。所有患者都被要求在研究人员的指导或协助下完成调查问卷。
1.3 统计分析
采用SPSS23.0软件进行分析,计数资料以百分比表示,不同组间比较采用卡方检验,方差分析比较生命质量等计量资料的组成部分,采用线性回归分析生命质量的影响因素。
2 结果
2.1 调查人群基本情况
入组样本共168例,其中男性102例,女性66例。MQSGA评分为7~27分,患者平均得分为11.6±3.6分,总的营养不良患病141例(83.9%),其中轻至中度营养不良120例(71.4%),重度营养不良21例(12.5%);HD、PD和RT患者营养不良的患病率分别为91.1%、94.6%和66.1%,RT组的受教育程度和收入最高(P<0.01),见表1。
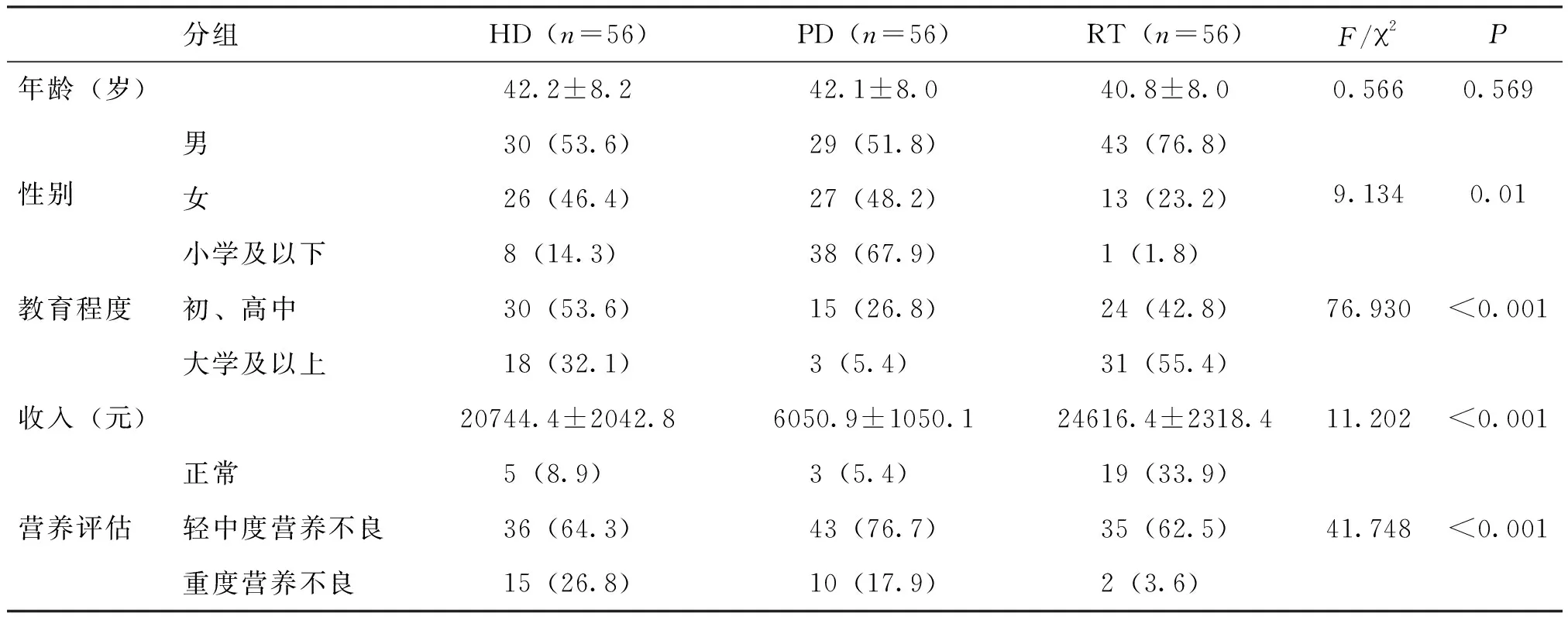
表1 研究人群的人口学特征 [n(%)]
2.2 不同营养状况下尿毒症患者生命质量比较
3组营养状态下在SF-36总分、MCS、PHS和各分支的组间比较,重度营养不良组得分均最低,轻中度营养不良组得分均低于营养正常组,存在显著统计学差异(P<0.001),见表2。
2.3 3种RRT患者的生命质量比较
比较HD、PD和RT 3组SF-36总评分、MCS总分、PHS总分和各分支得分,发现RT组在总评分和各分支得分均高于HD组和PD组,均存在显著性差异(P<0.001),见表3。
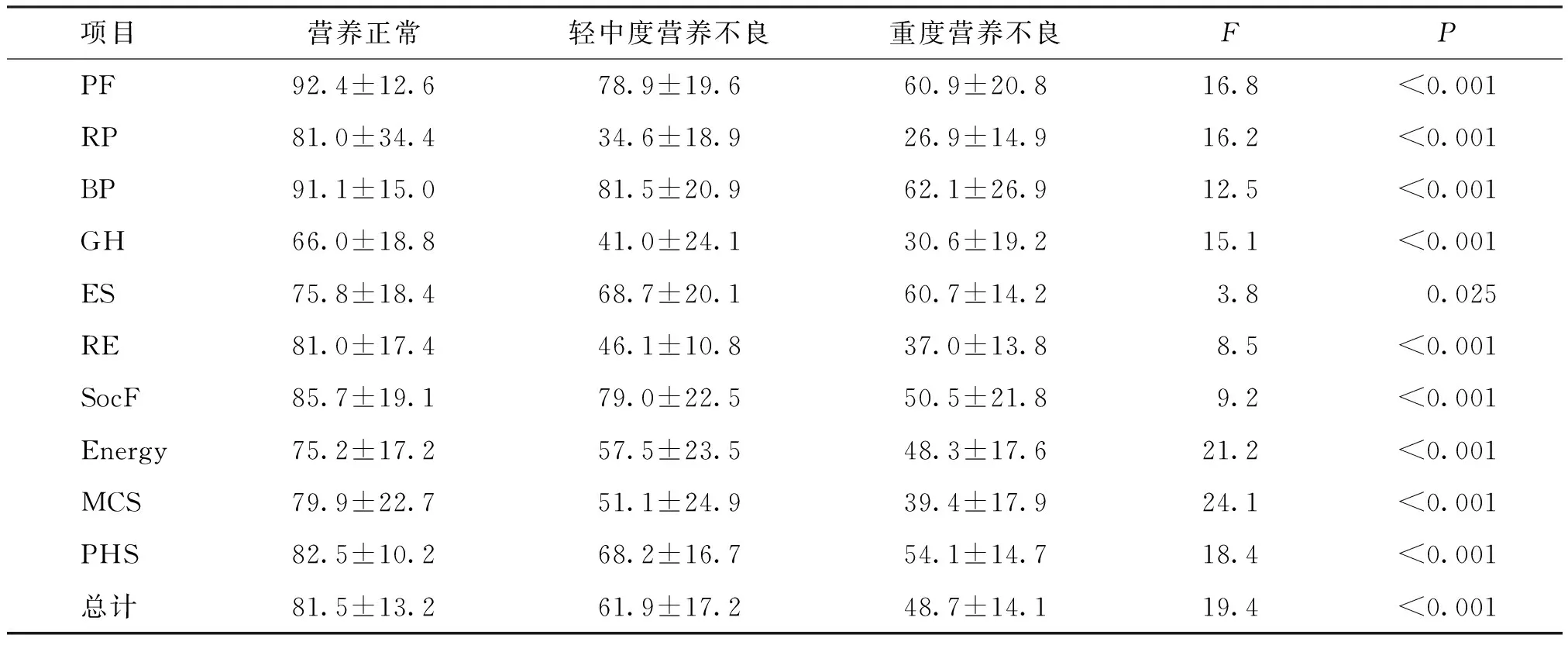
表2 不同营养状态下的生命质量评分比较
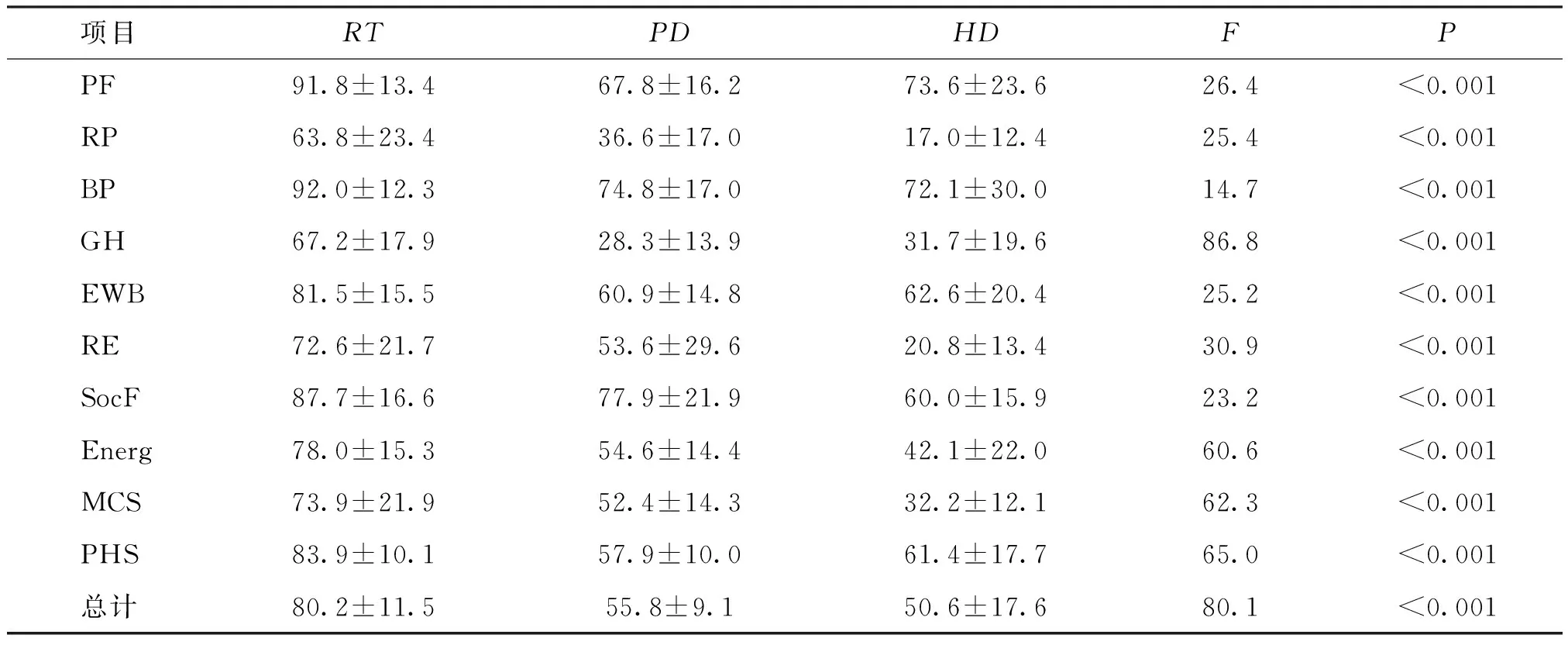
表3 3种肾替代治疗患者的生命质量评分比较
2.4 影响生命质量的因素
本研究分别以尿毒症患者的PHS和MCS作为应变量,以年龄、治疗时间(月)、有无并发症(0-无,1-有)、有无保险(0-无保险,1-有保险)、有无工作(0-无工作,1-有工作)、营养评估等级(0-重度营养不良,1-轻中度营养不良,2-营养正常)、是否肾移植(0-RT,1-HD/PD)作为自变量进行多元线性回归分析,见表4。
结果显示影响患者PHS评分的影响因素包括有并发症(B=-4.79,P=0.04),营养状况(B=5.74,P<0.01),年龄(B=-0.45,P<0.001),采用肾移植(B=19.67,P<0.001)。其中,PHS评分与年龄、并发症发生呈负相关,提示患者年龄越大、发生并发症,则其生理相关生命质量越差;PHS评分与营养评估等级、采用肾移植呈正相关,即营养状况越好,选择肾移植的治疗方式,则患者生理相关生命质量越好。同时,影响MCS评分的因素包括有无工作(B=10.7,P=0.024),营养状况(B=10.01,P<0.01),采用肾移植(B=28.47,P<0.001)。其中,MCS评分与有工作、营养状况、采取肾移植呈正相关,提示患者有工作、营养水平越好、采取肾移植的肾替代治疗方式,则其心理相关生命质量越好。
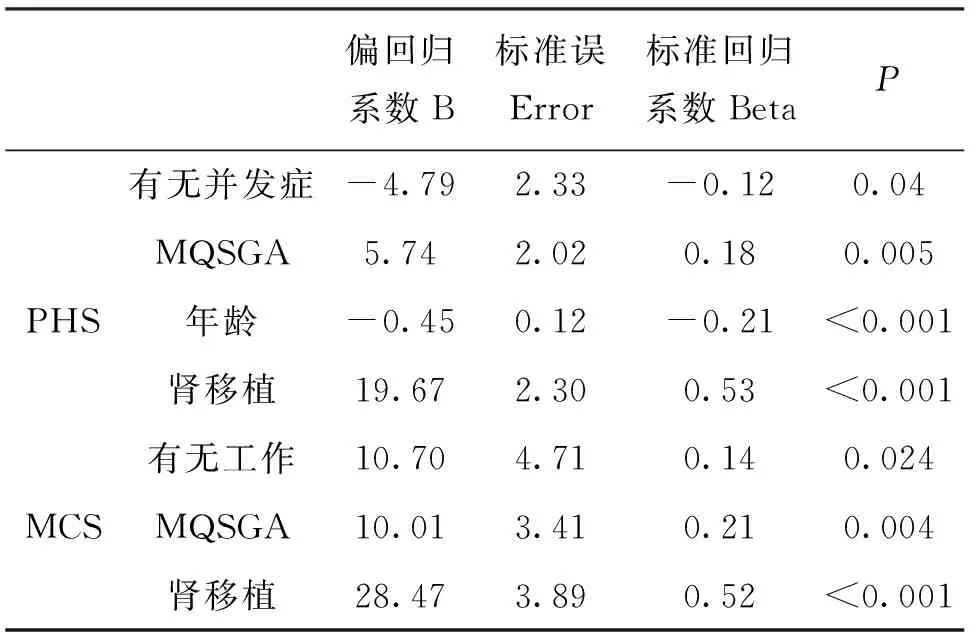
表4 尿毒症患者生命质量的相关影响因素
3 讨论
在本研究中,肾移植组在受教育程度、经济收入方面均为最高。肾移植不仅需要合适的供体肾脏,而且需要支付昂贵的手术及长期免疫抑制剂费用,因此社会经济状况是尿毒症患者治疗方式选择中一个重要的考虑因素[7]。
随着医学的进步,尿毒症患者肾替代治疗后生存期延长,但是营养不良的发生率偏高,蛋白质-能量消耗(protein energy wasting,PEW)指慢性病患者因为代谢紊乱,体内能量和蛋白质储存减少的状态,常见于尿毒症患者[8]。目前缺乏针对尿毒症患者专有的营养状态筛查工具[9]。MQSGA是一种简便、廉价、无创的营养水平评估工具[11]。本研究使用MQSGA评估尿毒症患者的营养状况,发现尿毒症患者营养不良率高达83.9%,其中肾移植组的营养不良率最低,腹透组最高。腹透患者大量蛋白质丢失、菌群失调等都可能加重营养不良[10],应定期监测患者的营养状况。
研究表明,营养不良是尿毒症常见并发症之一,与预后密切相关[12]。本研究发现,尿毒症合并营养不良组几乎在生命质量所有领域都低于营养正常组。因尿毒症患者常伴有恶心、呕吐等症状,影响营养摄入,同时慢性炎症、饮食磷限制、氨基酸丢失、酸中毒、矿物质和骨骼疾病等也会引起营养消耗[13]。肾移植患者的整体营养状况和生命质量均优于血透和腹透患者,与之前的研究一致[14]。本研究中多因素分析表明,尿毒症患者营养不良是PHS和MCS方面生命质量下降的独立因素,营养不良越严重,生命质量越差。应定期进行营养筛查,纠正营养不良可以有效改善生命质量。
4 结论
本研究结果表明,营养不良与尿毒症患者的生命质量密切相关,特别是血透或腹透的尿毒症患者,严重的营养不良会降低其生命质量,定期营养状况评估应是终末期肾病治疗方案的重要组成部分,需针对营养不良采取严格的预防和控制策略,从而改善尿毒症患者生命质量。

