辛酸甲酯与正丁醇在低速柴油机中的氮氧化物排放特性仿真分析
田策,姚丽
(上海海事大学 商船学院,上海 201306)
辛酸甲酯与生物柴油的主要特性指标相似,有学者探究了辛酸甲酯(MO,CHO)的化学反应机理,通过射流搅拌器(JSR)装置对辛酸甲酯与正丁醇混合燃料进行氧化动力学实验研究,提出其动力学反应机理,确定可以选辛酸甲酯作为生物柴油替代燃料进行燃烧模拟。
因为生物柴油的含氧特性,在燃烧过程中会促进NO的生成,从而导致NO排放增加。均质充量压燃(homogeneous charge compression ignition,HCCI)模型因NO排放低和燃烧效率高的特点备受关注。均匀的空气和燃料混合气引入气缸,然后活塞压缩混合气使之升温到一定程度自行燃烧,同时气缸内没有明显的火焰传播。这些特点导致较低的NO和颗粒物排放,同时保持高的热效率。
考虑将生物柴油替代燃料辛酸甲酯与不同比例正丁醇混合形成的混合燃料和船用低速柴油机相结合,采用HCCI燃烧提升发动机燃烧效率,以达到降低船用低速柴油机NO排放的目的。计算辛酸甲酯与正丁醇不同混合比例的情况下NO体积分数随曲柄转角的变化关系,并详细分析NO在反应器内的转化情况。同时计算不同工况下,1∶1混合比例的混合燃料HCCI燃烧的氮氧化物排放特性。
1 分析的思路及方法
1.1 发动机参数与反应机理
选取MAN B&W 6S35ME-B9型船用低速柴油机作为分析对象,通过CHEMKIN软件的HCCI反应器进行燃烧仿真。仿真计算的发动机参数均来源6S35ME-B9型发动机,其规格及主要参数见表1。
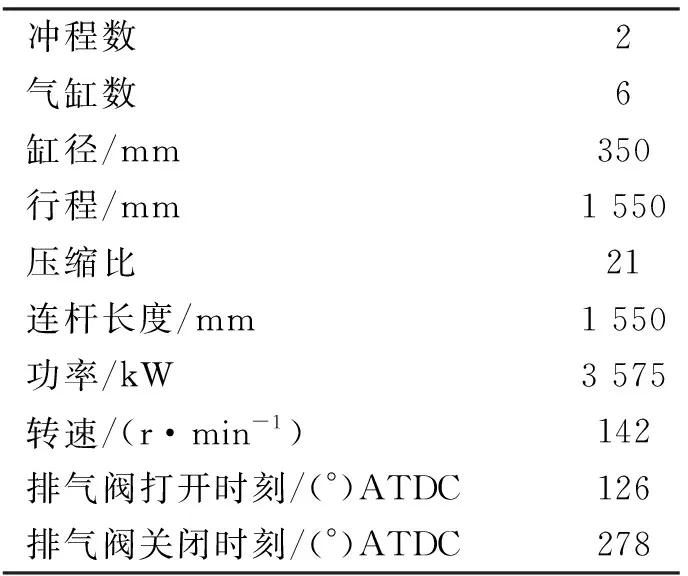
表1 6S35ME-B9型发动机规格及主要参数
仿真计算采用辛酸甲酯与正丁醇混合的反应机理来源于文献[1],加入NO的反应机理,用于计算和分析NO的反应与生成。辛酸甲酯(MO, CAS 111-11-5)和正丁醇(NBA,CAS 71-36-3)的主要性质见表2。
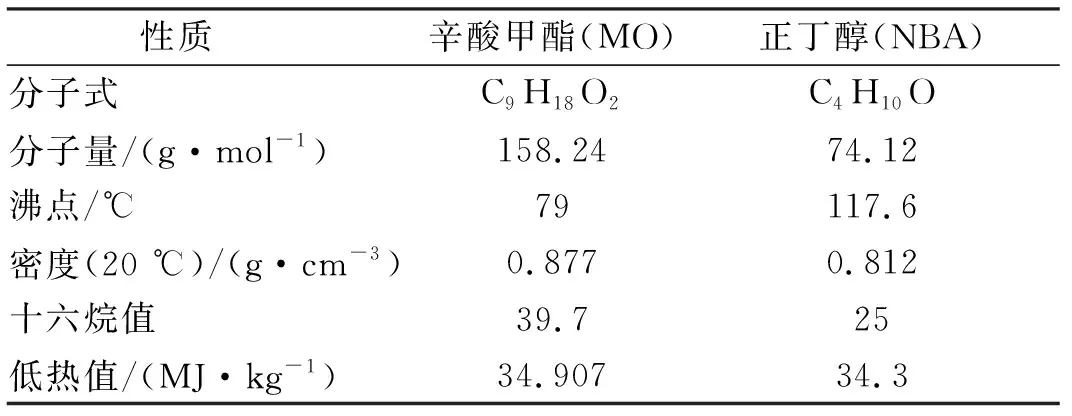
表2 辛酸甲酯和正丁醇的主要性质
1.2 模型计算参数
计算不同比例正丁醇混合条件下的氮氧化物排放特性时,考虑到船用低速柴油机实际航行时为了充分燃烧,通常空气过量系数定在2.0,因此计算将过量空气系数选为2.0。在CHEMKIN软件的闭式HCCI反应模块中进行辛酸甲酯和正丁醇的HCCI燃烧计算,设置初始温度460 K,固定在100%负荷,转速142 r/min,扫气压力为0.265 MPa,在混合物总摩尔分数不变的前提下,将辛酸甲酯和正丁醇按照0%、10%、20%和50%的比例混合。辛酸甲酯和正丁醇完全燃烧的化学反应方程式如下。
2CHO+25O→18CO+18HO
(1)
CHO+6O→4CO+5HO
(2)
计算过量空气系数在2.0时不同混合比例下辛酸甲酯和正丁醇完全燃烧时消耗的空气量,具体的混合成分见表3。
考虑到氩气(AR)是惰性气体,不参与反应,因此作为填充气维持混合物的总摩尔分数不变。十六烷值是影响燃料性能的最重要的因素之一,是着火延迟的主要原因。大型低速船用柴油机所用的柴油十六烷值一般在30~35之间。从表3可见,当正丁醇掺混比例为50%时最接近船用低速柴油机燃油的十六烷值。
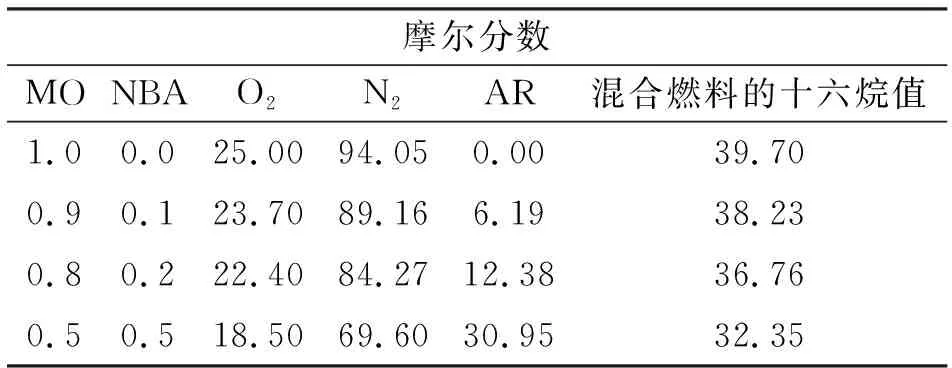
表3 混合燃料的摩尔分数和十六烷值
计算不同工况下混合燃料的氮氧化物排放特性时,选取辛酸甲酯与正丁醇混合比例1∶1,分析混合燃料在100%负荷,转速142 r/min、75%负荷,129 r/min和50%负荷,112.8 r/min种不同工况下的氮氧化物排放特性。
2 结果讨论
2.1 NOx排放特性以及NOx的生成与转化
总摩尔分数不变,发动机固定在142 r/min,辛酸甲酯与不同比例正丁醇混合时NO体积分数随曲柄转角的变化见图1。
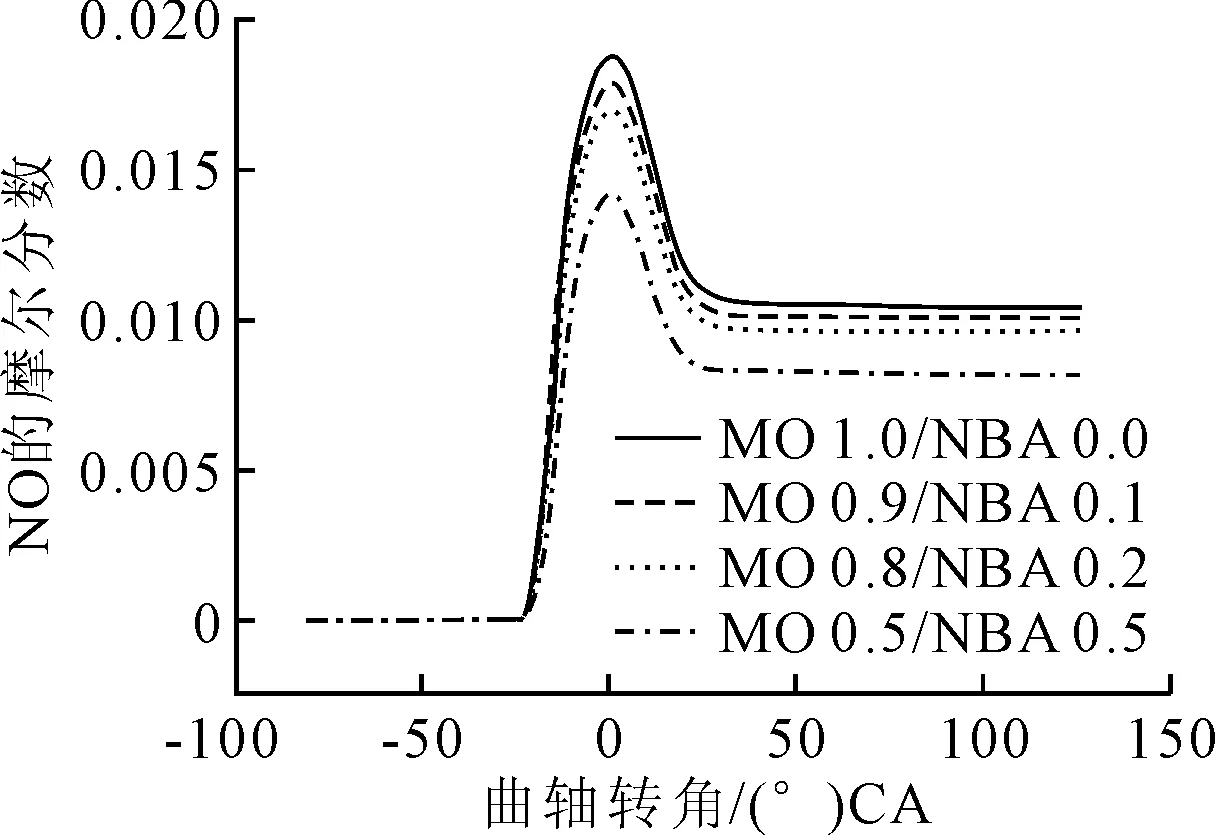
图1 不同混合比例下的NO体积分数与曲轴转角的变化
从图1可见,起初体积分数随曲柄转角增加没有明显变化,当到-23.6 (°)CA时,NO体积分数骤增,然后在1.2~26.1 (°)CA区间下降之后基本保持不变,直至排气口打开。同时,NO的体积分数随正丁醇混合比例的增加而下降。
分析1.2~26.1 (°)CA区间内NO所参与的反应。11.6 (°)CA,正丁醇掺混比例为0%,142 r/min的情况下NO参与的主要反应方程式及产率见图2。
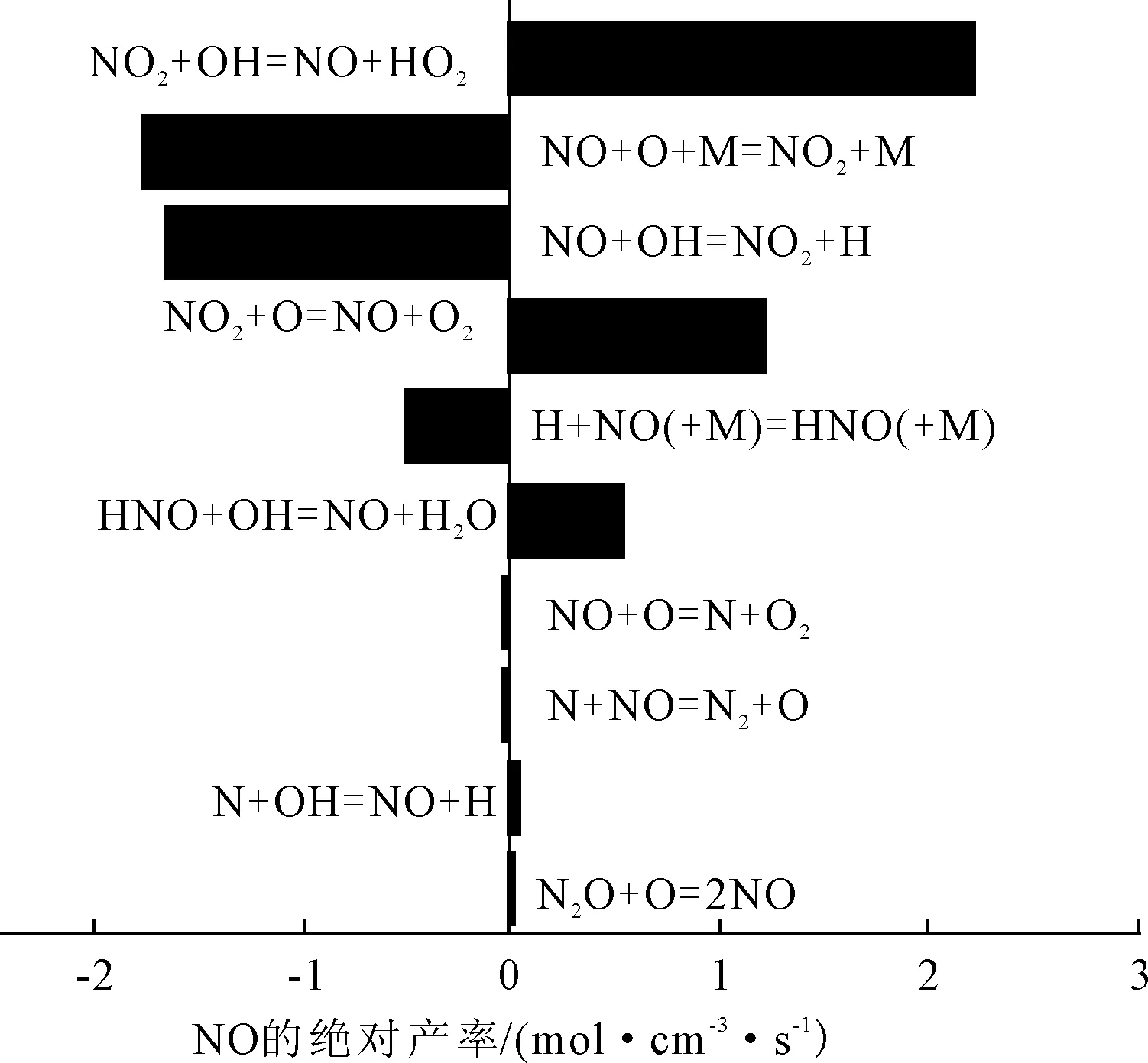
图2 NO参与的主要反应方程式及产率
由图2可见,NO在这些反应中既作反应物又作生成物,相互转化发生反应,由于参与反应众多,于是进一步分析同样情况下NO的反应路径,见图3。
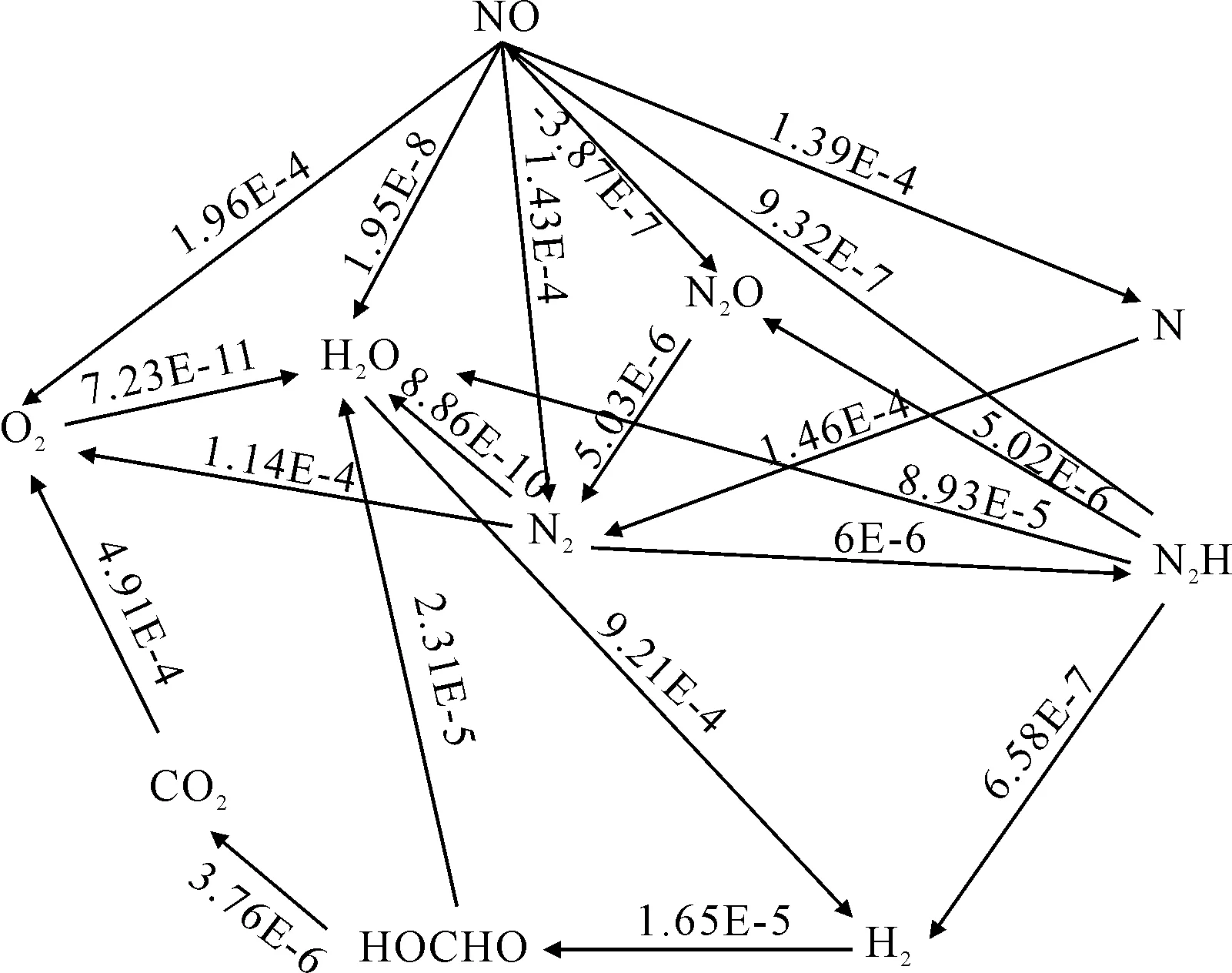
图3 NO的反应路径
由图3可见, NO的一级产物有O、HO、N、NO和N。然后一级产物继续发生反应生成其他物质,NO可以直接生成N,也可以通过生成NO和N再发生反应生成N。由此推论NO降低可能转化成了N,为了验证推论,计算N的体积分数变化情况。
转速为142 r/min,不同比例正丁醇混合,N的体积分数随曲柄转角的变化见图4。
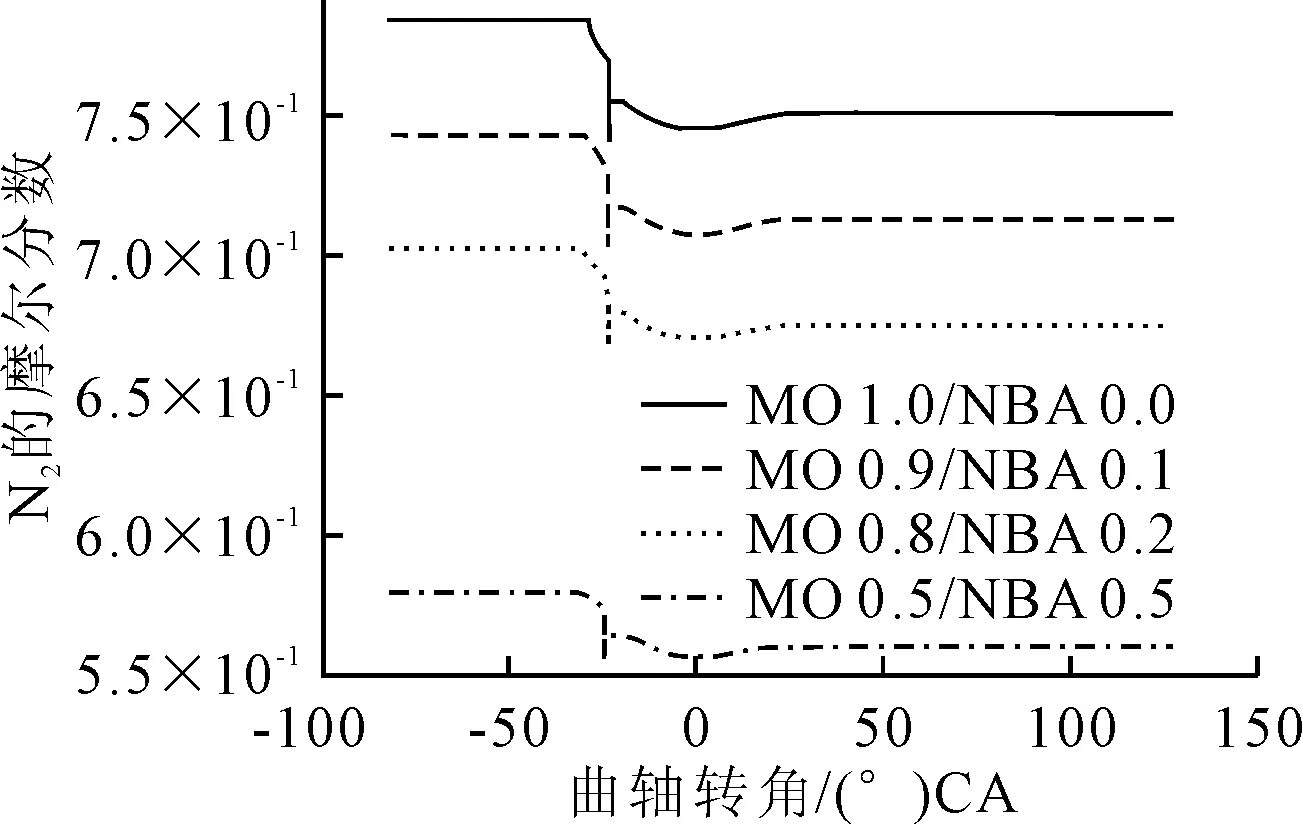
图4 不同混合比例下的N2体积分数与曲轴转角的变化
图4中1.2~26.1 (°)CA区间,N呈缓慢上升趋势,之后基本保持不变。N上升区间和NO的下降区间吻合。分析11.6 (°)CA,正丁醇混合比例为0%,142 r/min的情况下N参与的主要反应方程式及产率,见图5。
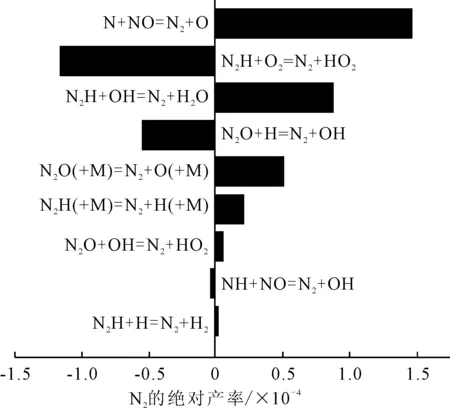
图5 N2参与的主要反应方程式及产率
重点分析N作为生成物参与的主要反应N+NO=N+O,反应中N作为生成物,NO作为反应物,由此验证了NO下降主要原因之一是转化成了N。
分析NO反应过程,在142 r/min的情况下,辛酸甲酯与不同比例正丁醇混合时NO体积分数随曲轴转角的变化见图6。
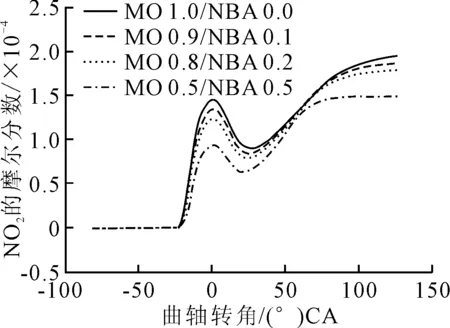
图6 不同混合比例下的NO2体积分数与曲轴转角的变化
NO体积分数在1.2~26.1 (°)CA区间下降,在26.1~126 (°)CA区间上升,还可以看出NO的体积分数随着正丁醇混合比例的增加而下降。选取11.6 (°)CA和61.52 (°)CA两处进行分析,见图7、图8。
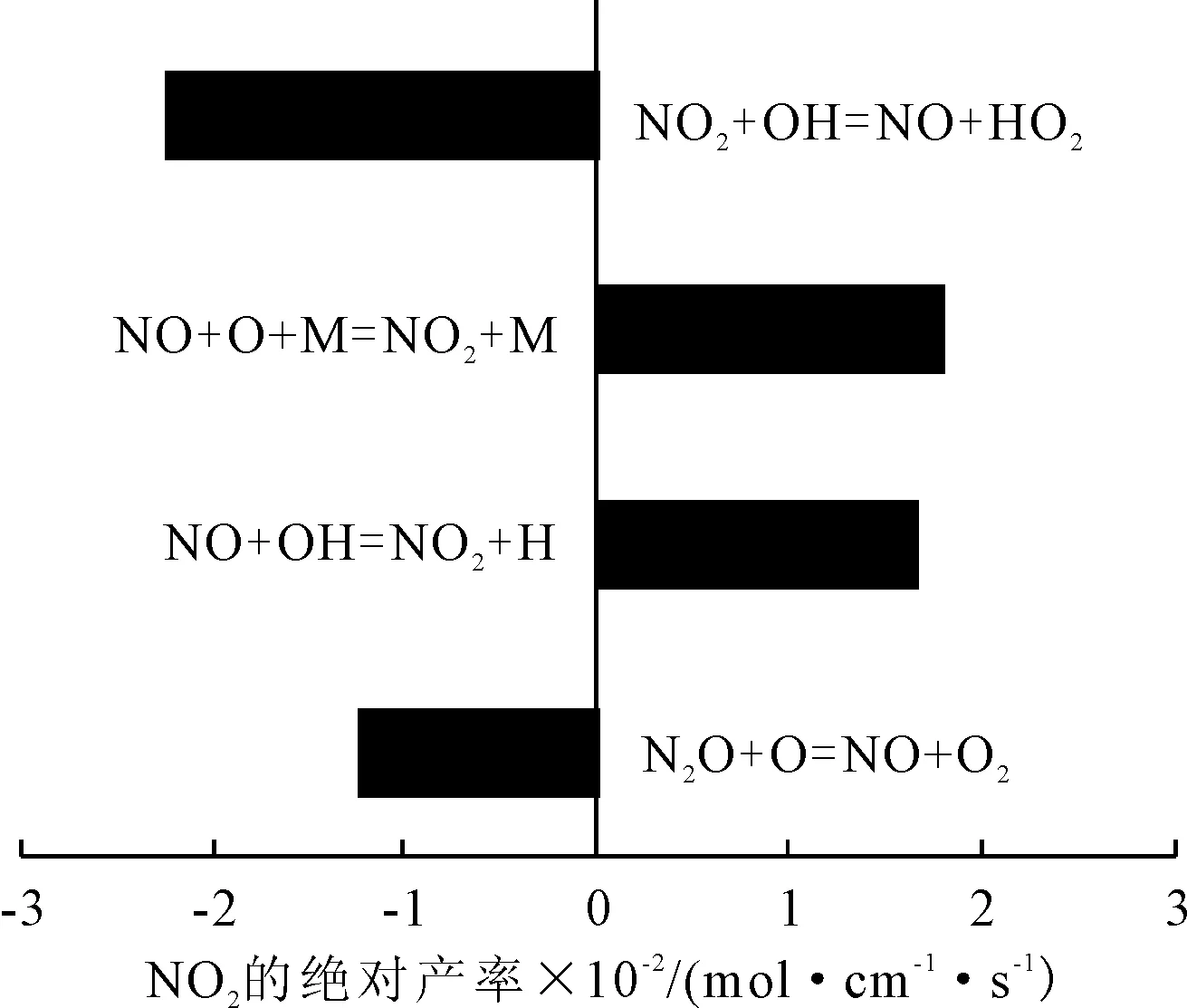
图7 NO2参与的主要反应方程式及产率(11.6 (°)CA时)

图8 NO2参与的主要反应方程式及产率(61.52 (°)CA时)
由图7可以看出,NO既作生成物又作反应物。经对比,NO作为生成物的产率低于其作为反应物的产率,所以在1.2~26.1 (°)CA区间内NO的体积分数呈下降趋势的原因是NO反应生成NO。
由图8可以看出,NO在NO+O+M=NO+M、NO+OH=NO+H和NO+HO=NO+OH这3个反应中作为生成物,在NO+O=NO+O中作为反应物。NO作为生成物的产率大于其作为反应物的产率。所以在26.1 (°)CA以后NO的体积分数呈上升趋势的原因是NO反应生成NO。
142 r/min情况下,辛酸甲酯与不同比例正丁醇混合时NO体积分数随曲柄转角的变化见图9。
由图9可见,NO的体积分数随着正丁醇混合比例的增加而下降,在1.2 (°)CA后呈下降趋势,选取11.6 (°)CA处进行分析。

图9 不同混合比例下N2O体积分数与曲轴转角的变化
11.6 (°)CA,正丁醇掺混比例为0%,142 r/min情况下NO参与的主要反应方程式及产率见图10。
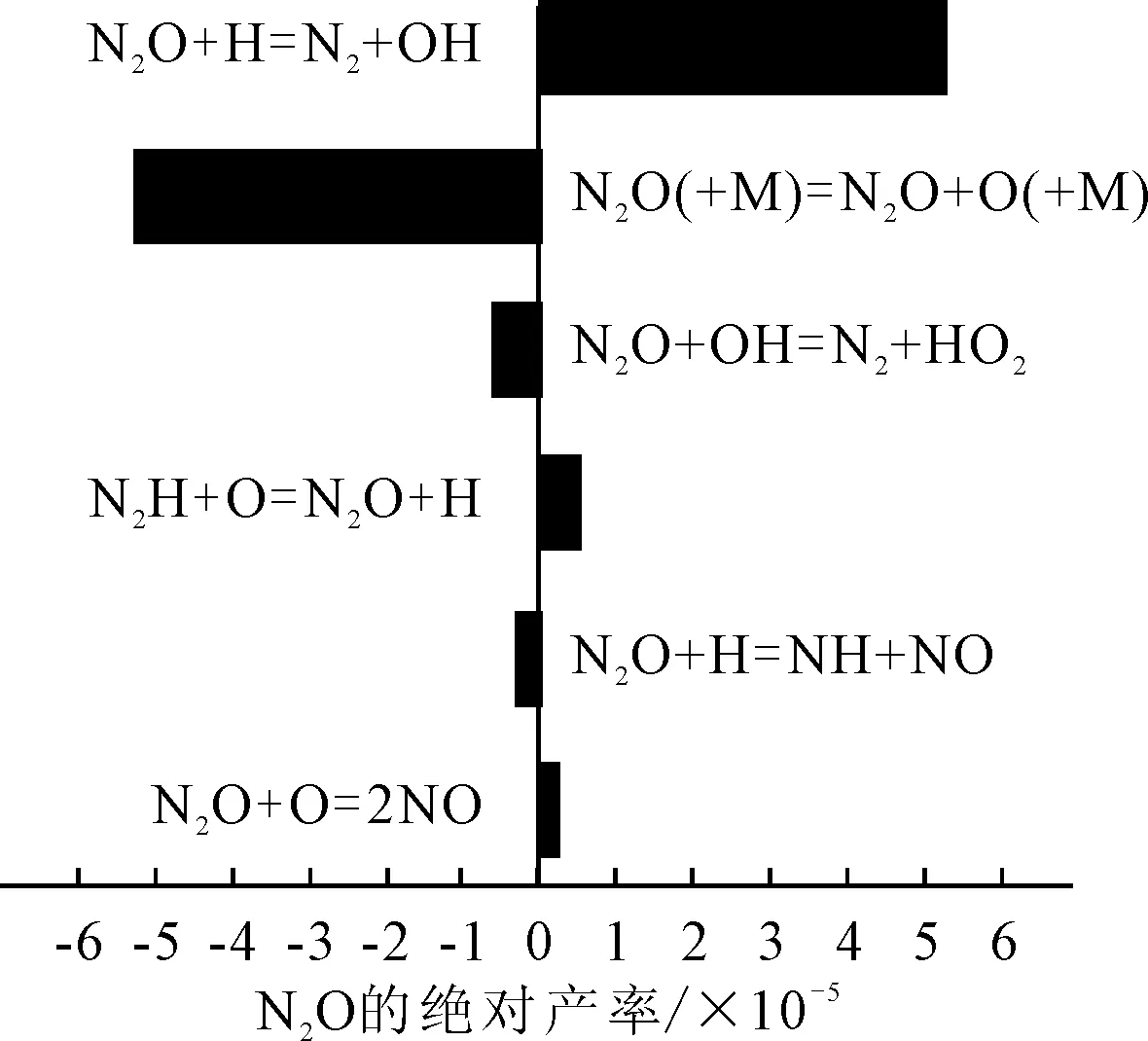
图10 N2O参与的主要反应方程式及产率
从图10可以看出,NO在NO+H=N+OH反应中作为生成物,在NO(+M)=N+O(+M)中作为反应物。数据对比表明,NO作为反应物的产率大于其作为生成物的产率,所以NO的体积分数在1.2 (°)CA后呈下降趋势的原因之一是NO转化成了N。
2.2 不同工况下NOx的排放特性
选择辛酸甲酯与正丁醇1∶1掺混,分析不同转速下混合燃料在HCCI燃烧中的NO排放特性,见图11、12和13。

图11 降低转速对NO的排放影响

图12 降低转速对NO2排放的影响

图13 降低转速对N2O排放的影响
从图11~13可见,NO的体积分数随着转速的降低而减少。由于过量空气系数设定为2.0,热力型NO成了NO排放的主要类型。热力型NO主要受温度、氧含量和反应时间等因素的影响。降低转速对缸内温度的影响见图14。

图14 降低转速对缸内温度的影响
由图14可见,气缸内峰值温度随转速降低而降低,因此NO的反应生成速率降低进而导致排放量降低;其次分析氧含量,由于过量空气恒定,燃料总量不变,所以氧含量不变;最后分析反应时间,发动机转速从142 r/min降到112.8 r/min,NO的反应分解时间变长,反应分解充分,因此NO的体积分数降低。综上,适当降低转速也可以降低NO排放。
3 结论
1)模拟生物柴油替代燃料辛酸甲酯与正丁醇混合燃料在船用柴油机中的燃烧情况,根据反应机理对NO的反应过程进行分析,可以准确地观察到NO、NO和NO的主要化学反应路径和化学反应速率。
2)辛酸甲酯与正丁醇的混合燃料在均质压燃反应器内,设定过量空气系数为2.0,转速为142 r/min时,燃料总摩尔分数不变,随着正丁醇混合比例的增加,NO的体积分数随之下降。因此在应用生物柴油时可以通过混合一定比例的正丁醇来减少NO的排放。
3)在辛酸甲酯与正丁醇1∶1混合比例的前提下,降低发动机转速,反应器内NO的体积分数也随之降低。因此,在燃用生物柴油和正丁醇混合燃料时,可以在适当范围内降低柴油机转速来减少NO的排放。

