用网络药理学和分子对接研究宣肺解热颗粒治疗COVID-19
张 雪,邹俊波,张小飞,彭 磊,陈志泽,郭东艳,梁玉洁,张恩户,史亚军
陕西中医药大学药学院,咸阳 712046
宣肺解热方是江夏方舱1号处方,是主要用于控制新型冠状病毒肺炎(COVID-19)早期发热症状的临床验方。本方以柴胡清透少阳半表之邪,桂枝散寒解肌、辟秽化浊、从外而解,共为君药;黄芩清泄少阳半里之热,芍药敛阴和营,百部有益肺止咳之功效,可助君药散邪,共为臣药;党参益气扶正,半夏降逆和中,共为佐药;生姜助柴胡祛邪、助半夏和胃、助桂枝解肌,大枣助参、草益气并助柴胡、白芍和里营,姜、枣合用,又可调和营卫,甘草益气和中,调和诸药为使。配合成方,共奏和解少阳、解肌退热、调和营卫之功。
1 方法
1.1 宣肺解热颗粒的药效成分及靶点信息库构建
由TCMSP数据库(http://tcmspw.com/tcmsp.php)和batman(http://bionet.ncpsb.org/batman-tcm/)得到宣肺解热颗粒中柴胡、黄芩、半夏、生姜、大枣、党参、炙甘草、桂枝、白芍与百部10味中药的性味归经。在TCMSP数据库(http://tcmspw.com/tcmsp.php)中以药物口服生物利用度(OB)≥30%、类药性(DL)≥0.18为筛选条件,在Batman数据库(http://bionet.ncpsb.org/batman-tcm/)中以分数大于20和P值0.05为筛选条件,得到宣肺解热颗粒中各个药材的潜在成分。
通过PubChem数据库(https://pubchem.ncbi.nlm.nih.gov/)查询其潜在成分的SMILES字符串,将其输入Swiss Target Prediction(http://www.swisstargetprediction.ch/)中预测靶点,从而得到宣肺解热颗粒潜在成分的相关靶点。用TCMSP数据库查询上述得到的潜在活性化合物对应的药物蛋白靶点,并用Uniprot在线数据库查询每个蛋白靶点对应的基因名,确定物种来源为“human”并建立数据集,用于后续分析。
1.2 冠状病毒相关靶点的检索
分别以“COVID-19”和“FEVER”为关键词输入GeneCards数据库(https://www.genecards.org/)和CTD数据库(https://ctdbase.org/),即得到COVID-19合并发热的靶点信息。
用在线工具Venny2.1(https://bioinfogp.cnb.csic.es/tools/venny/index.html)将冠状病毒靶点与发热靶点进行交集,得到二者的共有靶点(即冠状病毒-发热共同靶点)。
将宣肺解热颗粒潜在成分靶点与冠状病毒-发热共同靶点进行交集,得到二者的共有靶点(即药物-疾病共同靶点)。将筛选出的共同靶点在已经总结的各单味药材成分-靶点数据中查找到对应的化学成分及所属药材。
1.3 宣肺解热颗粒治疗COVID-19-FEVER关系网络
将宣肺解热颗粒的共同靶点及其对应成分一同导入Cytoscape 3.2.1中,利用其软件中Merge功能将筛选出的活性成分、潜在靶点及疾病靶点构建一个成分-靶点-疾病三元综合网络,用Cytoscape的插件Network Analyzer对网络特征进行进一步分析。
1.4 宣肺解热颗粒治疗COVID-19-FEVER潜在作用靶点的蛋白相互作用网络(PPI)
STRING蛋白相互作用在线分析数据库(Version 11.0)是整合已知和待预测的蛋白-蛋白相互作用的数据库,而且具备强大的可视化展示相互作用网络体系的功能。进入页面选择“multiple proteins”条目,将上一步得到的潜在靶点名称输入,并选择“Homo sapiens”进行下一步的检索,将蛋白-蛋白相互作用结果(.tsv格式文件)下载并保存。将文件中的node1、node2信息导入Cytoscape软件绘制蛋白相互作用(PPI)网络,并对其网络拓扑结构进行分析,以节点的Degree值反映其靶点大小,从而构建获得蛋白相互作用网络。
1.5 关键核心基因与基因组百科全书(KEGG)分析
用R语言对靶点蛋白进行生物功能及分子信号通路的富集分析,探究其靶点蛋白在生物过程(biological process,BP)、细胞组分(cellularcomponent,CC)以及分子功能(molecular function,MF)方面的作用机制。
1.6 分子对接
用Discovery Studio 4.0软件进行分子对接。在宣肺解热颗粒治疗新型冠状肺炎早期发热靶点中选取核心靶点,借助PDB数据库(https://www.rcsb.org/)找出靶点score值排序靠前的靶点蛋白结构,配体为该靶点所对应的化合物,用Drugbank在线平台找出核心靶点对应的阳性药物并在PubChem中下载阳性药物和所对应化合物的2D 结构。将整理好的靶点蛋白3D结构和对应化合物及阳性药物的2D结构导入Discovery Studio,用DOCK ligand(libDock)进行分子对接,得到核心靶点蛋白和对应化合物及阳性药物的相互作用关系图。
2 结果
2.1 宣肺解热方成分及靶点的筛选
通过借助中药系统药理学数据库与分析平台,总共筛选出化合物450个,其中柴胡中的化合物59个,黄芩中的化合物55个,半夏中的化合物37个,生姜中的化合物72个,大枣中的化合物50个,党参中的化合物71个,炙甘草中的化合物11个,桂枝中的化合物26个,白芍中的化合物28个,百部中的化合物41个。全面总结每种化合物对应的靶点。最终宣肺解热颗粒全方的候选靶基因共有1 947个。
2.2 冠状病毒合并发热相关靶点的检索
通过Genecards数据库搜集后,得到339个冠状病毒的相关靶点,CTD数据库搜集得到冠状病毒相关的靶点1 208个,将2个数据库找到的靶点合并,去除重复靶点,冠状病毒的相关靶点有1 519个。通过Genecards数据库搜集后,得到899个发热的相关靶点,CTD数据库搜集发热相关的靶点899个,将2个数据库找到的靶点合并去除重复靶点后发热的相关靶点有1 446个,将其与冠状病毒的1 519个靶点在Venny 2.1.0中映射筛选后,得出530个共同靶点。与宣肺解热颗粒1 947个候选靶基因在Venny 2.1.0中映射筛选出309个共同靶点。见图1。

图1 活性成分作用靶点与疾病靶点维恩图
2.3 宣肺解热颗粒治疗COVID-19-FEVER关系网络
将筛选出的共同靶点在已经总结的各单味药材成分-靶点-疾病数据中查找到对应的成分及所属药材,共378个成分。将宣肺解热颗粒的共同靶点及对应成分导入Cytoscape3.2.1中,构建网络关系图,导出其相关的拓扑数据度值,见图2。节点的平均度值为7.428,大于该平均度值的节点有167个,其中成分有84个,靶点有82个。
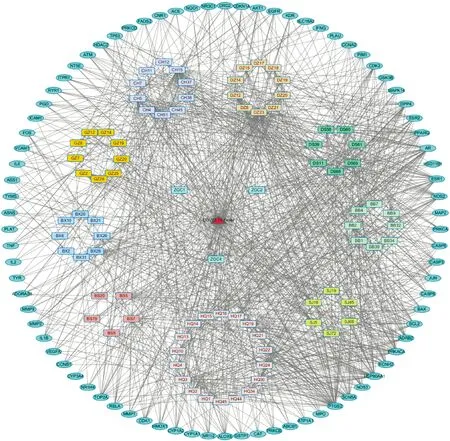
图2 成分-靶点-疾病网络
2.4 宣肺解热颗粒靶蛋白PPI网络
将宣肺解热颗粒82个冠状病毒合并发热的相关靶点蛋白输入至STRING数据库,构建靶蛋白PPI网络。将分析得到的蛋白相互作用关系数据结果(.tsv格式)导入到Cytoscape 3.2.1软件中,得到其可视化的蛋白质相互作用体系网络,见图3,该网络共有82个节点、976条相互作用关系,平均度值为23.805,各节点分别代表潜在作用靶点对应的蛋白,节点大小与颜色表示靶点蛋白的“Degree”值大小,节点越大、颜色越深,该靶点蛋白在网络体系中的度值越大;节点间连线表示靶点蛋白间存在潜在的相互作用关系。从图3可知,宣肺解热颗粒对治疗COVID-19合并发热的靶标中Degree值排名前20的靶标为蛋白激酶(AKT1)、肿瘤蛋白P53(TP53)、白细胞介素6(IL6)、血管内皮生长因子A(VEGFA)、半胱氨酸天冬氨酸蛋白酶3(CASP3)、转录因子AP-1(JUN)、肿瘤坏死因子(TNF)、表皮生长因子受体(EGFR)、前列腺素氧化环化酶2(PTGS2)、雌激素受体1(ESR1)、热休克蛋白HSP90-α(HSP90AA1)、原癌基因c-fos(FOS)、基质金属蛋白酶-9(MMP9)、过氧化氢酶(CAT)、一氧化氮合酶(NOS3)、基质金属蛋白酶2(MMP2)、丝裂原活化蛋白激酶1(MAPK1)、白细胞介素1β(IL1β)、转录因子p65(RELA)以及PPARG(过氧化物酶体增生激活受体γ),认为这些核心作用靶点在网络中起到关键作用,即为较重要的靶点。

图3 潜在作用靶点的蛋白相互作用网络示意图
2.5 宣肺解热颗粒治疗COVID-19-FEVER的潜在核心靶点基因富集分析
将上述得到的82个潜在核心靶点利用R语言的Cluster Profiler软件包分别进行GO与KEGG富集分析,目的是从整体角度出发,从而系统研究宣肺解热颗粒在对COVID-19-FEVER治疗方面可能影响的生物功能及相关分子机制。前10条路径见表1。由表1可知,可以看出治疗可能与影响流体剪切应力与动脉粥样硬化、人巨细胞病毒感染、糖尿病并发症中的AGE-RAGE信号通路及乙型肝炎等有关。这些路径上的靶点如HSP90AA1、TP53、AKT1、BCL2、MMP9、FOS、RELA、TNF、JUN、MAPK14、IL6、CASP3和IL1B是同时作用于许多不同的路径,见图4和表2。通过Cluster Profiler包重建了围棋交互网络,此网络反映这些围棋术语之间的内部关系,圆点颜色越红形状越大表示此路径与该病理发展越明显,见图5。

表1 Kegg通路富集前10条路径

表2 数字所表示的靶点

表2(续) 数字所表示的靶点
GO富集分析所得到的相关结果:(按照重要显著程度选取排名前10的结果)Biological Process(GO-BP)结果提示,宣肺解热颗粒治疗COVID-19-FEVER与活性氧代谢过程、对脂多糖的反应、对细菌源分子的反应和活性氧的反应等过程密切相关。Molecular Function(GO-MF)结果提示,治疗可能与泛素样蛋白连接酶结合、核受体活性、配体激活的转录因子活性和类固醇激素受体活性等功能密切相关。(GO-CC)结果提示,治疗可能与膜筏、膜微域、膜区和细胞周期素依赖性蛋白激酶全酶复合物等密切相关。结果见表3。

表3 GO富集分析BP、CC与MF前10条路径

表3(续) GO富集分析BP、CC与MF前10条路径
2.6 分子对接结果分析
为进一步说明靶点蛋白与对应化合物之间的结合活性,本研究选择宣肺解热方治疗COVID-19早期发热中度值较高的4个核心靶点AR、SCN5A、ESR1和HSP90AA1,与其对应的化合物进行分子对接,结合活性越高,得分越高,见表 4。其中β-谷甾醇与AR,β-谷甾醇与SCN5A,刺芒柄花素与ESR1,N-反式阿魏酰酪胺与HSP90AA1的结合活性最高。用Discovery Studio 4.0软件进行阳性药物验证实验和分子对接,并选择与表4中对接得分最高的化合物即核心成分进行比较,对比情况见表5。核心靶点与核心成分、阳性药物的对接结果见图6。结果表明,4个核心靶点与核心成分的对接得分均高于与阳性药物的对接得分。

图4 Kegg相互作用网络图

图5 核心靶点调控途径网络图

表4 核心靶点与对应化合物结合活性得分
3 讨论
随着COVID-19的全球流行和升级,中医药发挥了显著疗效,其对新型冠状病毒感染者在疾病的预防治疗、综合治疗和康复等取得了治疗优势[1]。中医理论认为COVID-19属于“邪”范畴,其病机特点为“湿、毒、瘀、闭”,自古以来在防治新发传染病方面都发挥着独特作用[2-4]。中药治疗病毒感染性疾病不仅以清除体内病原体为目的,而且能通过调动机体特异性和非特异性免疫功能增强抗病毒感染的能力[5]。而网络药理学能对“药物-靶点-疾病”之间的相互关系进行系统地研究,已成为研究中药作用机制的最有效的方法之一[6]。宣肺解热方作为江夏方舱用于控制COVID-19早期发热症状的临床验方,宣肺解热方为小柴胡汤与桂枝汤的化裁方,其主要功效是和解少阳、解肌退热、调和营卫,治伤寒少阳证。
本研究通过网络药理学借助多种生物信息学数据库及 Cytoscape软件等构建了宣肺解热方治疗COVID-19-FEVER的“成分-靶点”网络以及蛋白-蛋白相互作用,并对关键节点以及通路进行了分析。通过以上的研究与分析,发现宣肺解热方中中药的化学成分主要集中在流体剪切应力与动脉粥样硬化、人巨细胞病毒感染、糖尿病并发症中的AGE-RAGE信号通路、HSP90AA1、TP53、AKT1、BCL2、MMP9、FOS、RELA、TNF、JUN、MAPK14、IL6、CASP3、IL1B与PTGS2等通路或靶点。
TP53也称肿瘤抑制蛋白(P53),其体细胞突变体的异位表达诱导转录组变化,从而导致了炎症反应的异常激活[7]。HOLLA S等研究发现,肺泡Ⅱ型上皮细胞被BCG感染时,P53可通过抑制TNF-α介导细胞死亡[8]。王媛等研究发现,BCG感染A549细胞时, P53信号通路中的P53协同p300抑制NF-kB、TLR-4和TRAF6的活化及负调控TNF-α、IFN-γ、IL-6和IL-8的分泌,从而抵抗MTB的侵染[9]。AKT1是一种丝氨酸/苏氨酸蛋白激酶,参与包括代谢、增殖、细胞存活、生长等多种生物学过程[10]。IL6、IL1B属于炎症细胞因子,由巨噬细胞产生,参与免疫反应的细胞增殖、分化并提高其功能[11],其中《新型冠状病毒感染肺炎诊疗方案(试行第七版)》已将IL-6作为COVID-19病情恶化的临床警示指标[12],其编码的蛋白质被证明是一种内源性热原,能够在自身免疫性疾病或感染患者中引起发热[13]。肿瘤坏死因子(tumor necrosis factor,TNF)是可以损伤肿瘤细胞并使其坏死的物质,TNF-α是一种内源性致热源,可刺激下丘脑体温调节中枢及刺激巨噬细胞释放炎性介质,并且能进一步诱导IL-6等细胞因子的产生,这些促炎性细胞因子参与体内急性反应、发热反应,引起趋化因子的释放等,还可使内皮细胞活化而导致血管通透性增加[14]。MMP家族参与调节一些与炎症相关的分子,如生长因子、细胞因子和趋化因子,MMP9可以通过调节炎症反应和炎症细胞的分布介导炎症相关疾病的发展[15]。PTGS2负责

表5 核心靶点与核心成分、阳性药物的结合活性得分比较
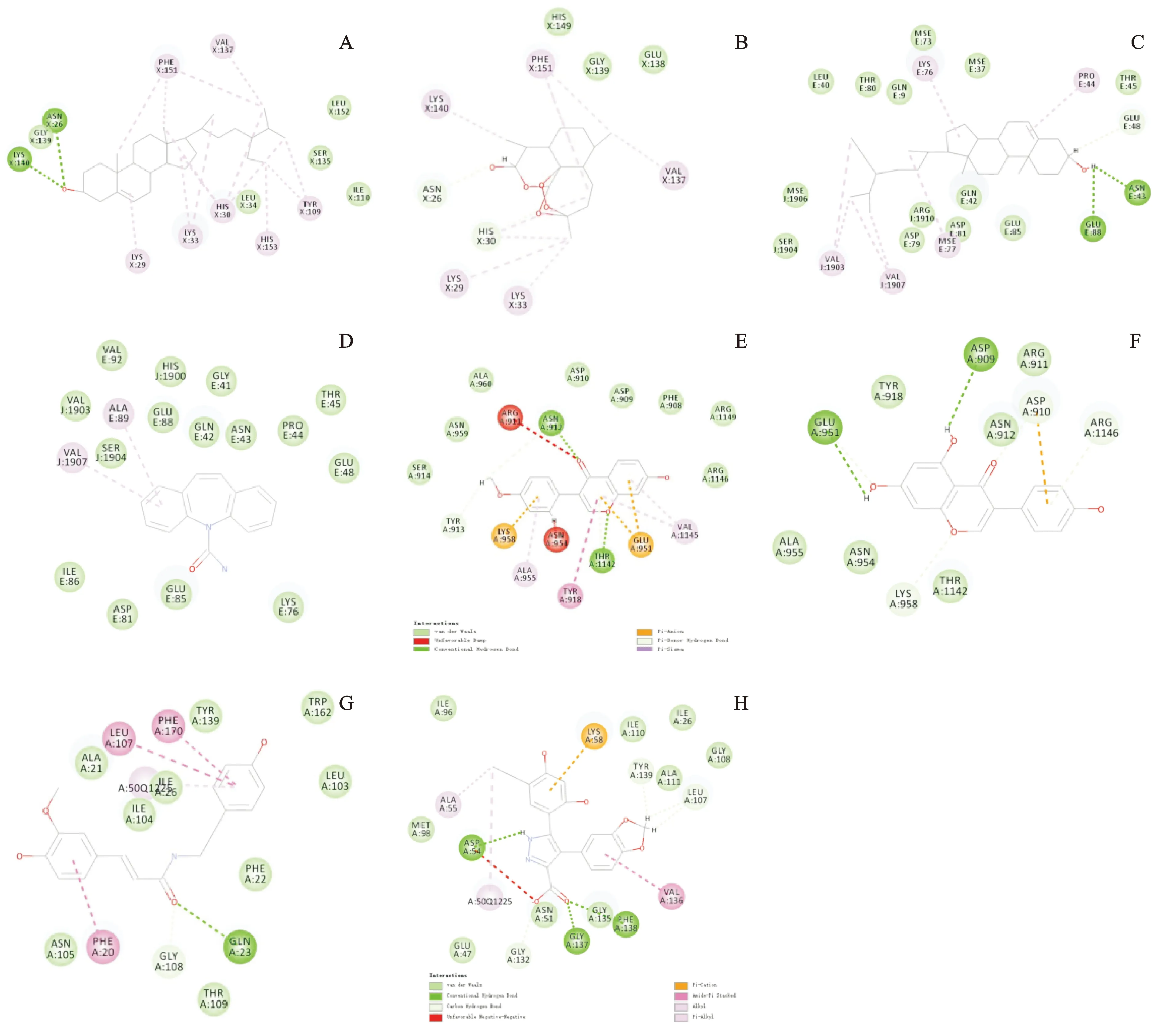
注:A.谷甾醇;B.双氢青蒿素;C.谷甾醇;D.卡马西平;E.刺芒柄花素;F.己烯雌酚;G.反式阿魏酰酪胺;H. 4-(1,3-苯并二氧代L-5-基)-5-(5-乙基-2,4-二羟基苯基)-1H-吡唑-3-羧酸。
前列腺素的产生,而前列腺素是导致发热的重要介质,因此这些化合物和靶点是宣肺解热方发挥解热作用的主要成分和靶点。
通过在TCMSP中的筛选发现,宣肺解热方中含有黄芩素、槲皮素、山柰酚、木犀草素、芍药苷等化学成分,其中槲皮素、山柰酚等成分已被证明可能是治疗COVID-19的关键性成分[16-18]。黄芩素是黄芩中含量最高的黄酮类,也是黄芩的主要活性成分。黄芩素对感染性疾病具有较好的防治作用,可发挥抗菌、抗病毒[19]、抗炎[20]、解热等药理活性。黄芩素可能是黄芩治疗COVID-19的主要活性成分。黄芩素可与SARS-CoV-2 3CL水解酶对接,且具有较强的结合性,意味着黄芩素可能在抑制病毒复制上发挥潜在的作用[21]。槲皮素分子式为C15H10O7,是一种广泛存在于自然界的植物次生代谢物,在体内和体外都具有抗氧化作用[22]、调节炎症[23]等作用。槲皮素也是一种植物源杀菌剂,具有较强的体内外抑菌作用与广谱抗菌性[24],能抑制感染细胞Casepase-3蛋白的高表达,拮抗病毒诱导的细胞凋亡,达到抗病毒作用[25]。芍药苷(peoniflorin)是一种水溶性单萜类糖苷,具有解痉镇痛、解热、抗炎、抗癌等药理作用[26]。芍药苷具有降低血清MDA含量,提高血清SOD、CAT、谷胱甘肽过氧化物酶(GSH-Px)水平,减少血清炎症因子水平,改善肺组织病理改变,对MRL/lpr狼疮小鼠肺损伤起到保护作用[27]。
GO和KEGG富集结果表明,宣肺解热颗粒通过多种生物学过程和多条信号通路参与COVID-19早期发热症状的治疗过程。从GO富集分析结果可得知,共同靶点主要涉及生物学过程有活性氧代谢过程、对脂多糖的反应、对细菌源分子的反应和活性氧的反应等。KEGG通路富集分析结果显示,宣肺解热颗粒作用于COVID-19早期发热症状的靶点主要涉及影响流体剪切应力与动脉粥样硬化、人巨细胞病毒感染、糖尿病并发症中的AGE-RAGE信号通路及多种疾病等多条通路。其中与糖尿病并发症相关的AGE-RAGE信号通路已被证实与COVID-19感染相关[28]。糖尿病并发症中的AGE-RAGE信号通路与血管损伤、炎症反应和动脉粥样硬化密切相关,通路激活可导致活性氧过量产生、NF-κB活化、黏附分子和细胞因子表达增加[29]。
为进一步说明蛋白与相应配体化合物的结合活性,结合文献报道,在宣肺解热方治疗COVID-19早期发热作用度值较大的靶点中选取4个核心靶点AR、SCN5A、ESR1和HSP90AA1,在Drugbank里找出与蛋白有关的4个阳性药双氢青蒿素、卡马西平、己烯雌酚与4-(1,3-苯并二氧代l-5-基)-5-(5-乙基-2,4-二羟基苯基)-1H-吡唑-3-羧酸,配体即为该蛋白所对应的成分。用Discovery Studio 4.0对该蛋白和配体及阳性药进行分子对接,结果表明,该蛋白与配体的结合活性分数高于与阳性药的结合活性分数,即蛋白与配体的结合活性较高。
综上所述,基于网络药理学分析得到的宣肺解热方中有效成分,明确具有抗菌、抗病毒、抗炎等作用,并且能够通过作用于相关的靶点对COVID-19早期发热引发的机体代谢异常、炎症反应发挥潜在的治疗作用,可为临床上COVID-19的治疗奠定一定的研究基础。

