4T1细胞成瘤的乳腺癌小鼠模型临床转化过程中的几个问题
刘梓昕牛东芹王 东
(江汉大学 医学院,武汉 430056)
世界卫生组织国际癌症研究机构在报告中指出,2020年乳腺癌成为全球发病率最高的癌症[1]。我国情况也不容乐观,2020年乳腺癌新发病例约42万,死亡约12万。在众多乳腺癌亚型中,三阴性乳腺癌(triple negative breast cancer, TNBC)的治疗最为困难[2-4],因其不表达或低表达人表皮生长因子受体2(human epidermal growth factor receptor-2, HER-2)、雌激素受体(estrogen receptor, ER)和孕激素受体(progesterone receptor, PR)而难以从分子靶向等现代疗法中受益[5-6],化疗成为当前较为有效的治疗方法[7]。蒽环类与铂类药物是治疗TNBC的主要选择,其中铂类药物在临床实践中被推选为治疗TNBC的优选方案[8-9]。但是这并非是最优方案,与其他亚型乳腺癌相比,其治疗手段有待拓展、疗效有待提高。
顺铂是铂类药物的典型代表,为第一个被FDA批准用于治疗恶性肿瘤的铂类药物[10],然而,耐药性和严重的毒副作用使顺铂的应用大打折扣[11-12]。近年来,通过结构修饰或者开发纳米药物[13]等方法来克服铂类药物的不足成为临床前研究的热点。但无论使用哪种方法都要经过动物模型的验证,因此,正确选取动物模型和准确造模是药物获得临床应用的关键[14-17]。但是,在具体实践中即使对于同一种动物模型,不同课题组的造模手段也会存在较大差异,这为客观评价实验效果带来诸多偏差。为了推进动物模型选择和构建的同质化,本文仅以顺铂参与的使用4T1细胞株构建的TNBC异体移植瘤模型为例,论述与分析实验研究中存在的问题并提出解决方案。
1 4T1细胞株的应用中存在的问题及讨论
4T1细胞株是由Fred Miller等学者分离得到的可移植型乳腺癌细胞[18],因其恶性程度高易成瘤,自发向肺、肝、脑等部位转移成为广泛使用的移植瘤细胞。此外,4T1细胞移植瘤模型的生长状态及转移部位非常类似于人类晚期乳腺癌,成为评估晚期乳腺癌药物的良好模型。笔者统计了近年来4T1细胞在有顺铂参与的药效实验中的使用情况(表1),并从细胞的种类、使用浓度、分散介质等方面进行总结。
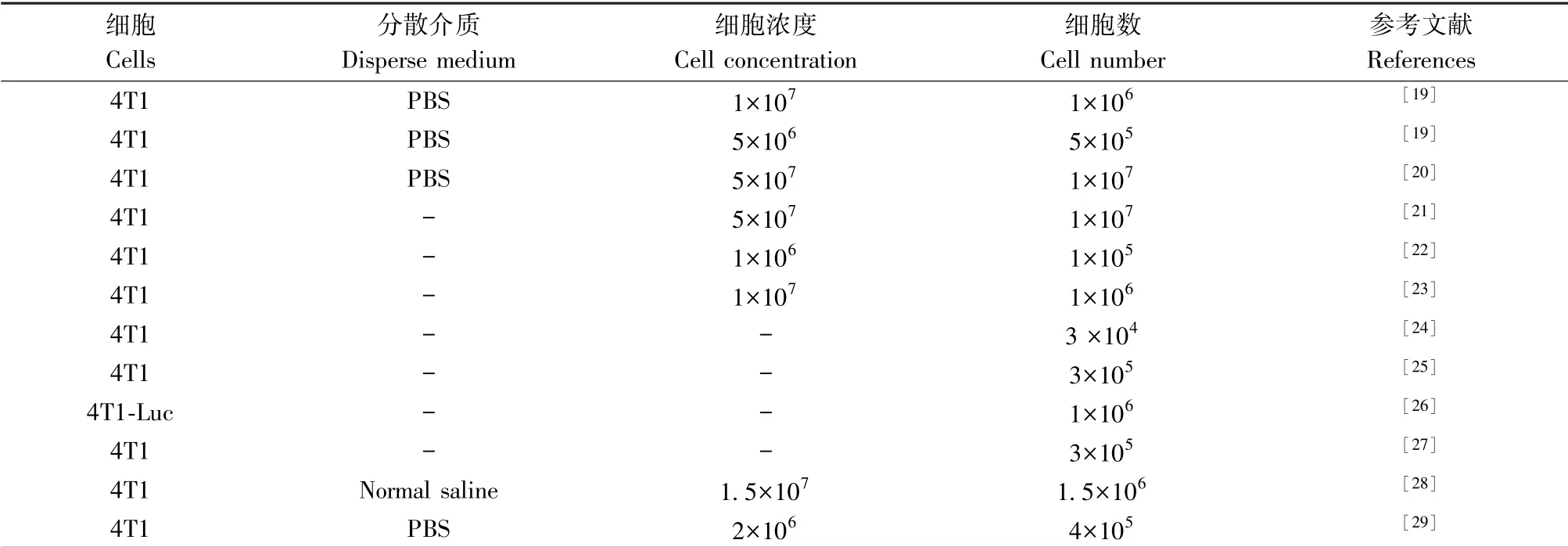
表1 4T1细胞在异体移植瘤模型中的应用统计Table 1 Application statistics of 4T1 cells in xenograft tumor model
由表可见,研究者在细胞的选用方面非常统一,绝大多数采用未经荧光素酶转染的细胞系进行相关研究,植瘤前细胞分散介质的选择上也比较一致,然而细胞数目与注射浓度在各研究中呈多样化。首先,在细胞类型选择方面两个亚类的4T1细胞被使用。就传统的4T1细胞而言,移植瘤的大小通过测量肿瘤的长径和短径尺寸计算而来,不同实验者对同一肿瘤的测量结果无法从客观上统一。而荧光素酶转染的细胞从一定程度上克服了上述缺点,可实现荧光定量测定,结果直观明了,具备更强的说服力,但其过渡依赖于贵重仪器,加之细胞构建方面费用较高未被广泛采用。笔者认为在采取适当措施的情况下,比如始终由同一测量者进行实验,传统4T1细胞即可满足实验精度要求。
其次,在细胞数目方面尚未有统一标准。从统计结果来看,细胞数目的使用范围在3×104~1×107个/只小鼠之间,跨度可达300倍以上,这必然会影响药效评价,不利于临床转化。因此,确立相对统一的细胞使用数目十分必要与急迫。但这并不是容易解决的事情,细胞数目的选择还涉及到移植瘤的类型(原位或皮下)、植瘤方式(直接注射或者手术植入)、实验目的(抑制转移或者抑制原发灶)等多方面的问题。作为一个折中方案,(0.3~1.0)×106个/只小鼠的细胞数目值得考虑。
第三,在确认细胞数目的前提下,细胞浓度对植瘤效果也有显著影响。其影响往往是隐性的,比如细胞被悬浮在分散介质中有自发聚集沉淀的倾向,细胞浓度越大沉淀可能越快;细胞过密也会影响自身活性,最终导致移植瘤不均一。细胞浓度由细胞使用数目与注射体积确定,在一般的移植瘤模型中注射体积多为100 μL,因此细胞浓度在107级别及以下较为合理。为了保证模型均匀、药效评价客观,在实验过程中仍需注意某些问题:(1)最好将细胞按每只小鼠的注射量单独分装;(2)临注射前轻柔吹打使细胞充分分散;(3)在尽量短的时间内用完细胞,防止活性降低影响成瘤。
最后,细胞分散介质对成瘤有一定影响但不如其他因素重要,研究中使用PBS者较多,无血清的培养基与生理盐水[28]也能满足植瘤需要。鉴于多篇参考文献没有明确给出所用介质,笔者不能做更详细的评价。
笔者课题组曾以1×105个/只小鼠的4T1细胞进行脂肪垫原位植瘤研究某种铜(Ⅱ)配合物的药效学实验,实验共使用30只BALB/c小鼠,通过手术切开小鼠第4、5对乳头附近的皮肤暴露脂肪垫注射100 μL 4T1细胞。在注射后的第2天观察并测量肿瘤体积,30只小鼠均成功植入肿瘤,平均体积为(90±9)mm3,第4天观察平均体积为(260±71)mm3,在第16天处死小鼠后检测肺转移结节,发现所有小鼠都有明显肺转移,说明植瘤成功且成功率100%。在另外的实验中,笔者以尾静脉注射观察肺转移,在4T1细胞低至3×104个/只小鼠的数量时也能很好的发生肺转移,且成功率也为100%。4T1细胞易成瘤的特性为乳腺癌的药效学评价提供了极大的方便,然而,作为科研人员即使在使用4T1这种容易造模的细胞时也应该仔细选择成瘤的最佳条件以,从而避免实验偏差或资源浪费。
2 4T1异体移植瘤模型中实验动物操作的问题及讨论
在乳腺癌异体移植瘤模型中,BALB/c小鼠为近交系品种,具备遗传背景一致,对4T1细胞没有免疫排异,植瘤成功率高的特点[30-31],成为使用最为普遍实验动物[32-33]。笔者对表1所列文献的小鼠使用情况进行总结(表2)。
由表可知,除Zhou等[26]使用BALB/c裸鼠外,其余研究均使用BALB/c小鼠建立移植瘤模型,这是由所使用的细胞株决定的。Zhou等[26]使用荧光素酶转染的4T1细胞,裸鼠方便成像观测。也有研究者将4T1细胞植入BALB/c裸鼠以对比普通BALB/c小鼠的成瘤状况,为合理选择实验动物提供理论依据[34]。至于小鼠的年龄与体重则由植瘤方式和位置决定,多数研究采用4~6周龄、体重18~22 g的小鼠,然而这并非最佳选择。如果构建皮下瘤模型,4~6周龄的小鼠足以满足要求;若是制作原位瘤采取脂肪垫注射的方法,此时小鼠的乳腺发育不够充分,接种时容易漏掉细胞。显然,7~8周龄的小鼠更适合原位脂肪垫注射。鉴于4T1细胞为乳腺癌细胞系,脂肪垫注射比皮下植瘤在模拟病 理 状 态 上更加合理,由此而得出的药效学评价才能更客观和科学[15]。即使在这样的前提下,笔者发现在造模过程中仍然存在较为严重的偏差,比如表2中多数研究者通过直接注射的方法造模。然而,这种方法不能准确的将细胞植入脂肪垫内,笔者曾以台盼蓝对小鼠直接脂肪垫注射然后剖开检测注射效果,结果表明部分台盼蓝泄漏至皮下组织。因此,笔者建议采取手术暴露脂肪垫的方式植瘤,这样可以保证均一和精确的模型构造。在减少小鼠创伤保证植瘤有效的前提下,Tavera-Mendoza等[35]提出了一种微创手术乳腺原位植瘤的方法,图1列出了操作流程。在注射体积的问题上,等于或少于100 μL的注射量是正确的选择,否则将面临细胞泄漏的难题。
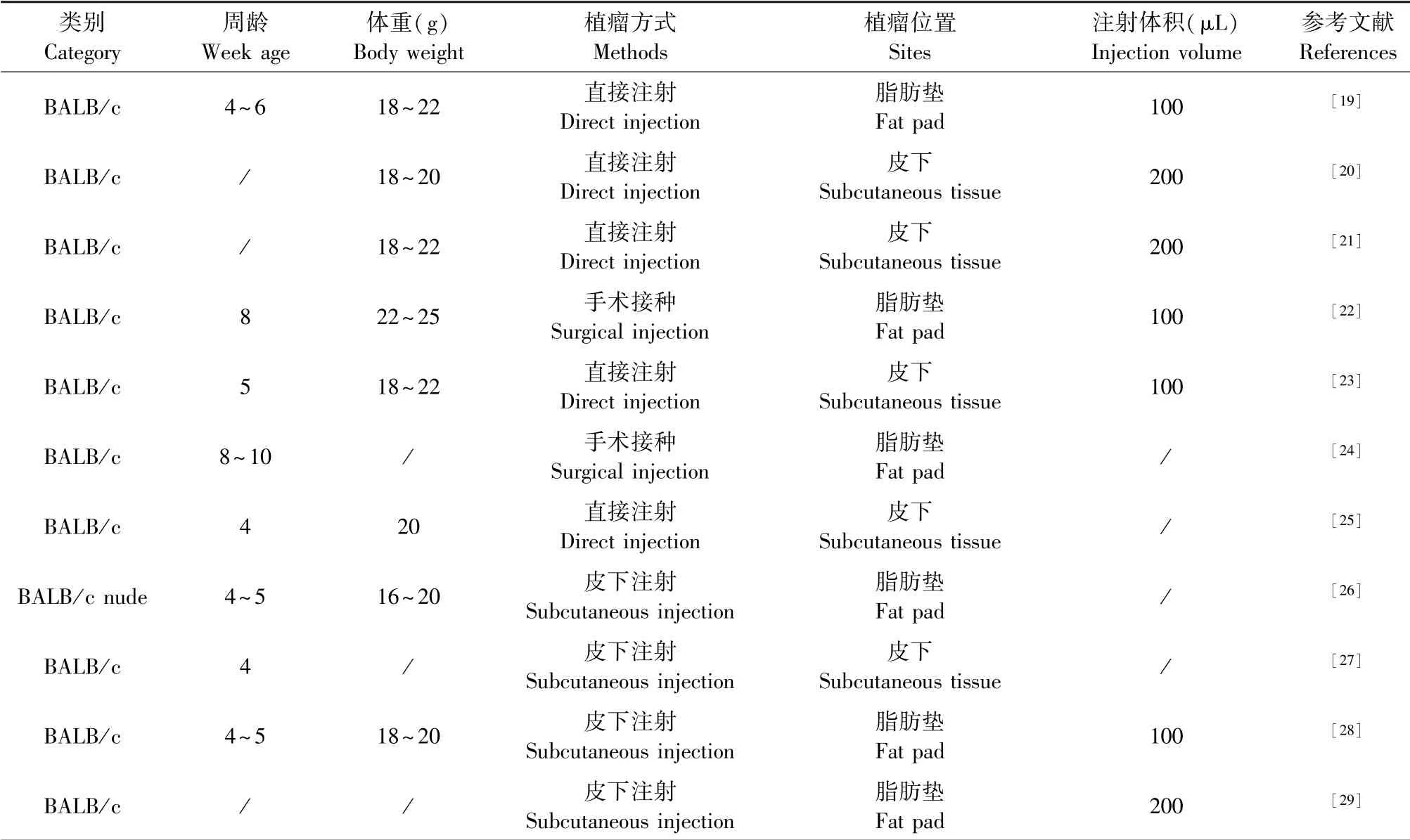
表2 4T1异体移植瘤模型中实验动物操作状况Table 2 Operation status of experimental animals in 4T1 xenograft tumor model
3 在4T1异体移植瘤中顺铂的使用问题及讨论
铂类药物以形成DNA-铂交联物干扰DNA复制而抑制肿瘤增殖[8],因其对携带乳腺癌易感基因1/2(Breast Cancer gene 1/2, BRCA 1/2)突变的细胞敏感[36],被推荐为晚期TNBC患者的救治药物,这些患者约75%携带BRCA 1/2突变。顺铂是最早开发的铂类药物,但其副作用大,应用受限,所以多种结构优化的铂类药物如卡铂[37]、奥沙利铂[38]等先后应用于临床。目前,仍有较多铂类化合物正处于临床前研究阶段[10],如Cheng等[39]报道了反式铂与DNA的作用,Muhammad等[40]研究了含有生物素的Pt(Ⅳ)配合物对乳腺癌细胞的抑制作用。纳米化的铂类药物也处于不断被开发的过程并取得突出进展,曾沛玉等[41]制备了一种含顺铂前药的介孔硅纳米粒,任玉双等[42]进行了顺铂前药接枝修饰硫代DNA及其自组装靶向纳米药物研究。顺铂在这些研究中通常当做阳性对照来使用,规范的给药方式及剂量是衡量新药药效的基础,然而在实践中存在较多问题,笔者对顺铂在4T1细胞移植瘤中的应用现状进行总结,表3展示了研究中存在的某些问题。
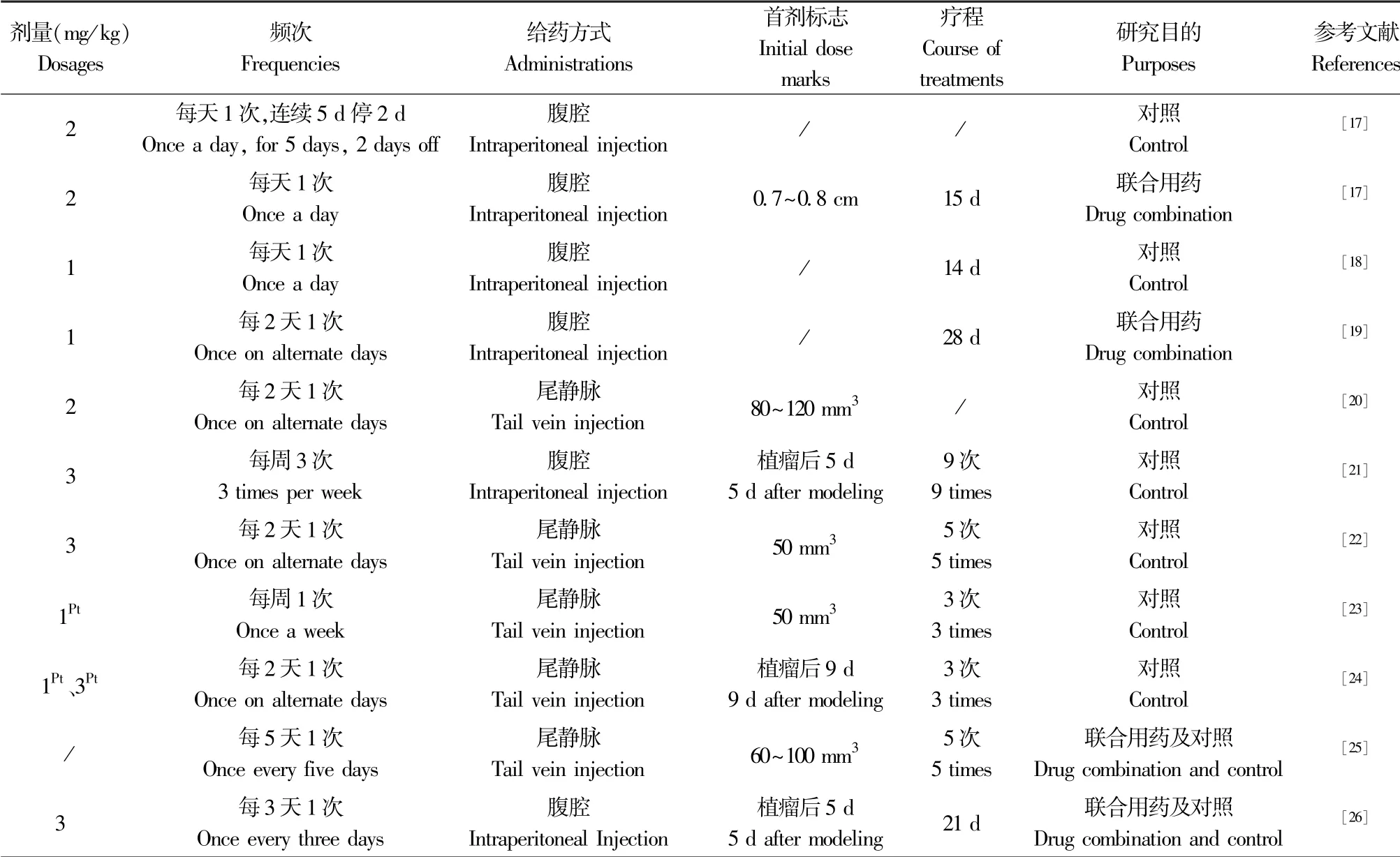
表3 顺铂在4T1异体移植瘤中的应用现状Table 3 Application status of cisplatin in 4T1 xenograft tumor
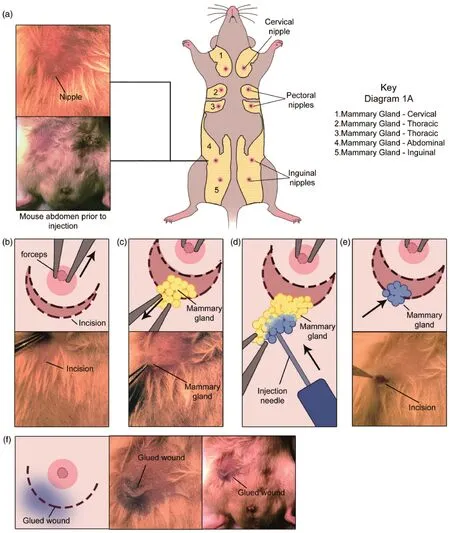
注:a:腹部乳腺和乳头;b:在第四个乳头下方作小于3 mm(外部和尾部)的切口;c:暴露脂肪垫;d:细胞注射体积小于120 μL;e:脂肪垫复位;f:用组织粘合剂密封切口。图片来自于参考文献[35]。图1 小鼠乳腺原位注射乳腺癌细胞的微创手术Note.a, Abdominal mammary gland and nipple.B, Small incision 3 mm (external and caudal) below the fourth nipple.c, Exposed fat pad.d, Exposed fat pad can be injected with a volume 120 μL.e, Fat pad is allowed to go back to its position.f, Incision is sealed using tissue adhesive.The pictures are from reference[35].Figure 1 Less invasive procedure for orthotopic injection of breast cancer cells into the mouse mammary gland
顺铂是当前临床使用的抗肿瘤药物,在乳腺癌治疗中常规剂量为75 mg/m2[43],在联合治疗中的用量常为25 mg/m2[44],另有文献报道大剂量顺铂疗法,其用量为150 mg/m2[45]。按照等效剂量换算[46],小鼠对应的等效剂量分别为25、8.3、50 mg/kg。然而,在实际动物实验中小鼠的使用剂量通常为1、2、3 mg/kg,这可能是由小鼠对顺铂的耐受剂量决定的。所以,在选择剂量的同时有必要评价药物对实验动物的毒副作用,在相对安全的剂量下从事药效学研究。在药物剂量表达方式上也存在影响药效评估的问题,大多数研究以化合物本身为度量标准,个别文献则以铂元素的质量为度量标准,Zhou等[26]和Sengupta等[27]以1或3 mg /kg铂元素的剂量给药,忽略了配体对药物活性的影响,显然不符合临床用药标准,但是从实验目的上来看这又是合理的,因为二者均采用纳米药物提高顺铂的活性,顺铂被偶联在高分子聚合物上。在动物实验中另外一项不规范在于给药频次,从表3的数据可知,即使相同的给药剂量,不同研究者的给药频次相差较大,这些偏差都应该以符合临床用药的标准予以校正。第三,各研究者在初次给药标志与疗程的问题上也远没有达到统一,笔者认为初次给药时间设定在移植瘤模型造模成功之后较为合理,即肿瘤大小在50~100 mm3之间即可实施给药,总给药时间则由药物长期毒性实验确定。在给药方式上,多数研究者使用腹腔注射,少数报道采用尾静脉注射,这是实验目的决定的,例如纳米药物需尾静脉注射,作为对照的顺铂也应采取尾静脉注射的方式,在这一点上研究者们意见一致。在4T1细胞移植瘤药效学研究的实验中,顺铂的使用存在诸如剂量、频次、初次给药时间与疗程不统一的问题,作为研究者应充分考虑动物实验与临床应用有效转化的问题。
4 结语
常见的乳腺癌荷瘤小鼠模型包括皮下瘤、原位瘤和肺转移等模型。由于模型的多样性和实验目的的不同,所以在构建的模型方面并没有一个统一的参数,笔者仅就文献报道和个人经验做一个大体的总结,以供读者探讨。在构建皮下瘤模型中,(3~5)×105细胞/小鼠较为合理,植瘤5~9 d可达到给药标准,且早期不会出现肿瘤迅速生长的现象,便于延长治疗周期及提高疗效;原位瘤则无需注射过多细胞,以(0.5~1)×105细胞/小鼠较好;尾静脉注射肺转移模型注射细胞相对较多,以(0.5~1)×106细胞/小鼠较为理想,若细胞注射过多则会导致肺组织损伤严重,小鼠过早死亡。就注射体积而言,应特别注意将脂肪垫造模的注射体积控制在100 μL以内,以防止泄露;其他的植瘤方式可将体积控制在200 μL以下。细胞浓度则由细胞数目与注射体积决定。在分散介质的选择上相对宽松,3种造模方式均可选择PBS和无血清培养基,但是在注射肿瘤细胞时要注意不能一次在注射器中吸取过多细胞,可保持在5只注射量以下,并及时更换注射器,防止注射期间细胞聚沉吸附到注射器壁上,从而避免植瘤不均一。在小鼠选择上,以4~6周龄的小鼠居多,但脂肪垫注射最好选择7~8周龄的小鼠,此时小鼠性成熟脂肪垫发育完善方便注射。如何选择实验条件最终由实验目的确定,考察物质的肿瘤抑制作用可选用皮下或脂肪垫植瘤,而肺转移则可以选用尾静脉造模。
临床前药物评价是衔接临床应用与基础研究的桥梁[47],而动物实验扮演着不可或缺的角色,准确而客观的动物实验包括细胞选择、动物选择、造模与给药观测等多个流程,每一步都可能对药效学研究产生重大影响。笔者以顺铂参与的使用4T1细胞株构建的TNBC异体移植瘤模型为例总结了研究中存在的问题,这些问题涉及到实验的每一个流程,从而使得动物实验中取得良好抗肿瘤效果的化合物在临床试验中屡屡失效,由此可见一斑。截至2020年7月,小鼠肿瘤生物学数据库显示至少有19242篇研究论文与小鼠肿瘤模型有关,仅由美国国立卫生研究院资助的正在进行的人源性异种移植瘤相关研究的总预算达到1.16亿美元之多。临床试验的失败沉重打击了药物开发的积极性,Yuan等[48]针对肿瘤模型探讨了临床试验失败的原因,在184个人源性异种移植瘤模型中有170个感染了小鼠病毒,这很可能导致该模型的评价药效的可靠性。除了实验过程存在偏差外,有些文献报道缺失相关信息,甚至是细胞数目、给药剂量、初次给药标志以及疗程等重要信息,这给不同研究者的交流带来很多不确定性,进而影响实验评价的客观性。全世界每年开展大量癌症移植瘤模型相关动物实验,错误设定实验条件将浪费大量人力、财力,而且给临床转化制造不可估量的困难,这就要求科研工作者慎重选择动物模型,以权威的参考文献为指导,严格执行实验流程,客观评价实验结果。新化合物进入临床研究的前提是动物实验,而动物实验的关键则在于统一而准确的操作规范,只有纠正实验偏差动物实验的数据才能更好的为临床转化服务。

