亚硫酸钠分银的试验研究
文 婷 梁柱俊 李文凯
(江西铜业集团公司贵溪冶炼厂,江西 贵溪 335424)
0 引言
铜电解精炼过程中产生的阳极泥一般含有金、银、铂以及钯等贵重金属,是提取贵金属的重要原料,铜阳极泥处理一般采用“预处理除杂—硫酸化焙烧—低酸分铜—氯化分金—亚硫酸钠分银—银还原”工艺。亚硫酸钠分银是以铜阳极泥中间物料分金渣为原料,加入亚硫酸钠溶液,使分金渣中的银浸出到液相中,达到分离提纯银的目的,银的浸出率是亚硫酸钠分银工艺的重要控制指标,直接影响铜阳极泥处理工艺过程银的收率。影响亚硫酸钠分银效果的关键因素是亚硫酸钠浓度、反应温度、反应pH值、反应液固比和反应时间,如何控制好以上关键因素需要进行深入研究。同时,亚硫酸钠属于强碱弱酸盐,容易水解,在生产实践中检测亚硫酸钠浓度的准确性关系到亚硫酸钠分银指标,采用碘量法滴定亚硫酸钠浓度,定容过程需要加入甘油和乙酸锌作为添加剂,以保证结果的准确性。因此,探究甘油和乙酸锌对碘量法测亚硫酸钠浓度的影响,对提高亚硫酸钠浓度的准确性,提升生产实践过程中亚硫酸钠分银效果有重要意义。
1 试验部分
1.1 试验原料
亚硫酸钠分银试验原料采用铜阳极泥中间物料分金渣,其典型化学成分见表1。
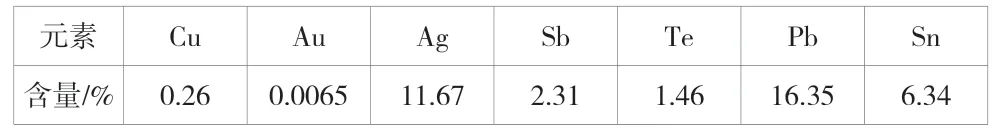
表1 分金渣典型化学成分
碘量法测亚硫酸钠浓度试验原料采用亚硫酸钠分银上清液,亚硫酸钠浓度为240g/L左右,pH值为7~9,温度为室温。
1.2 试验原理
在一定的亚硫酸钠浓度下,分金渣中的AgCl与溶液中NaSO反应生成亚硫酸钠银络合离子,继而进入溶液,实现与其他杂质分离的目的,主要化学方程式见式(1)。
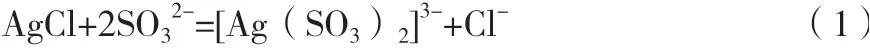
碘量法测亚硫酸钠浓度原理是在弱酸性环境下,以淀粉溶液作指示剂,用碘标液滴定,碘会将溶液中的亚硫酸盐氧化成硫酸盐,即碘与溶液中的亚硫酸根离子反应生成碘离子和硫酸根离子。当亚硫酸根离子消耗完以后,过量的碘与淀粉结合显蓝色,即显示滴定终点,将消耗的碘液换算后即可得到溶液中的亚钠浓度,主要化学方程式见式(2)。
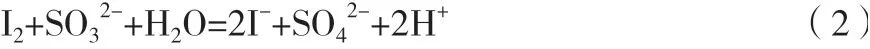
亚硫酸钠化学式为NaSO,亚硫酸钠水溶液在50℃以下易结晶沉淀;甘油又叫丙三醇,化学式为CH8O,可增加溶液的黏度;乙酸锌化学式Zn(CHCOO),弱酸性溶液。
1.3 试验方法
取分金渣,按照一定的固液比加入亚硫酸钠溶液,利用液碱或硫酸调节反应pH值,在恒温水浴锅内进行加热,同时进行搅拌反应。反应结果后进行固液分离,取分银渣烘干后检测主要化学元素成分。
取亚硫酸钠待测液10mL于250mL容量瓶内,加入一定的蒸馏水,再加入甘油和乙酸锌添加剂,最后加入蒸馏水定容。摇匀后用5mL移液管取液5mL于锥形瓶,加入少许淀粉溶液作为指示剂,再用碘标液进行滴定。
1.4 试验试剂及设备
试剂:亚硫酸钠溶液、31%液碱、98%硫酸。
设备:烧杯、电子秤、量筒、恒温水浴锅、搅拌装置、pH计、过滤装置、烘干箱。
试剂:甘油(CHO,分析纯)、乙酸锌(Zn(CHCOO),10%浓度)、碘标液(I,0.105mol/L)、淀粉溶液。
设备:250mL容量瓶、250mL锥形瓶、10mL移液管、5mL移液管、酸式滴定管、量筒。
2 结果与讨论
2.1 亚硫酸钠分银结果与讨论
在亚硫酸钠分银过程中,利用亚硫酸钠根(SO
)与分金渣中的AgCl作用生成可溶于水的银络合离子,进而把银从固态化合物浸出到液相中,达到分离提纯的目的,亚硫酸钠浓度直接影响到银的浸出率。试验在恒定温度35℃条件下,液固比为7,起始pH值为7条件下,控制不同浓度的亚硫酸钠浓度,搅拌反应40min进行试验,亚硫酸钠浓度对银浸出率的影响结果如图1所示。
根据图1可知,银的浸出率随着亚硫酸钠浓度的提高而上升,当亚硫酸钠浓度提高到240g/L~270g/L时,再提高亚硫酸钠浓度对浸出率影响不明显,但亚硫酸钠浓度过高会造成溶液黏性大,容易结晶,影响沉降效果,固液分离难度加大等问题。所以,为了达到较高的银浸出率,亚硫酸钠浓度控制在240g/L~270g/L为宜。
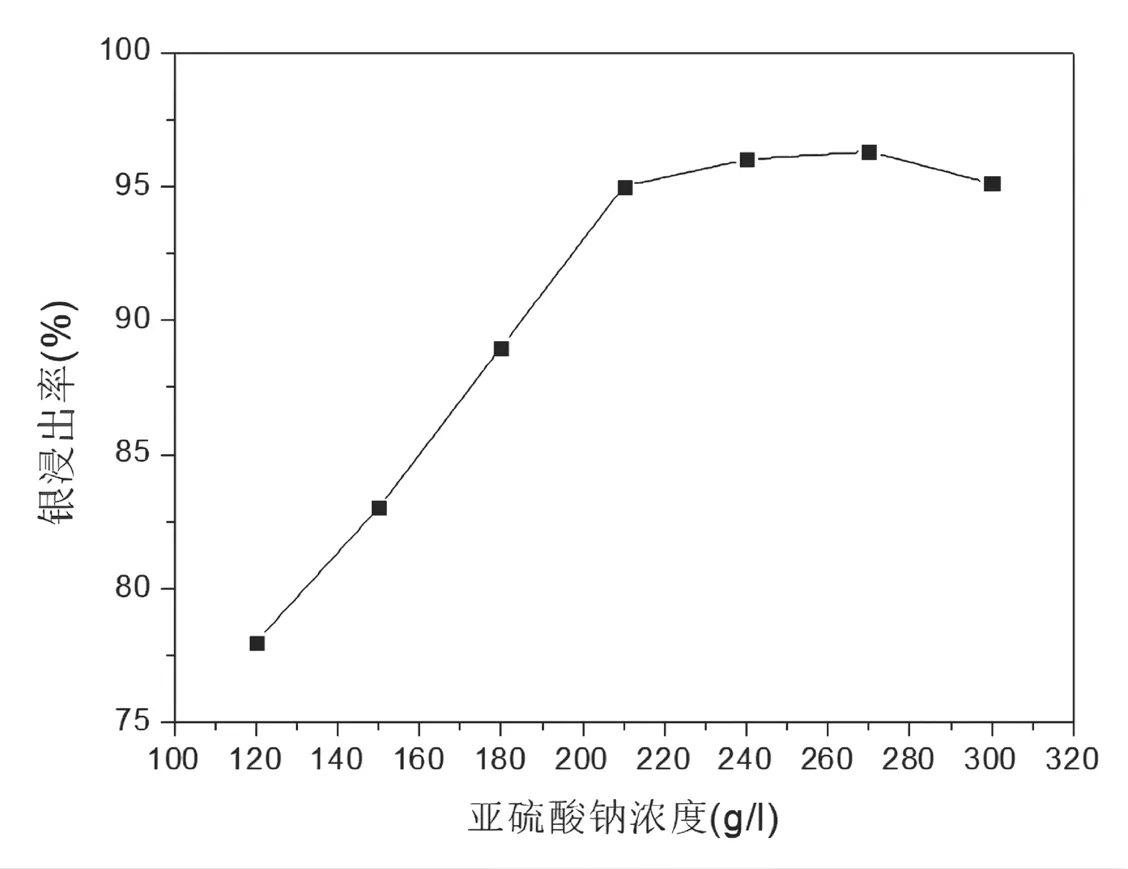
图1 亚硫酸钠浓度对银浸出率的影响
亚硫酸根与氯化银生成的银络合离子极其不稳定,受温度影响较大,温度过高时,银络合离子容易被分解,而银则以金属形态沉于渣中,影响银的浸出率,主要化学反应方程式见式(3)。试验在液固比为7,起始pH值为7,亚硫酸钠浓度为240g/L,控制不同的反应温度,搅拌反应40min进行试验,反应温度对银浸出率的影响结果如图2所示。

根据图2可知,银的浸出率随着反应温度的升高而上升,当温度达到32℃~38℃时,再提高反应温度,银的浸出率反而下降。主要原因是银络合离子([Ag(SO)])在高温下不稳定,容易分解生成单质银,降低分银效果。所以,为了尽可能提高银的浸出率,反应温度控制在32℃~38℃为宜。
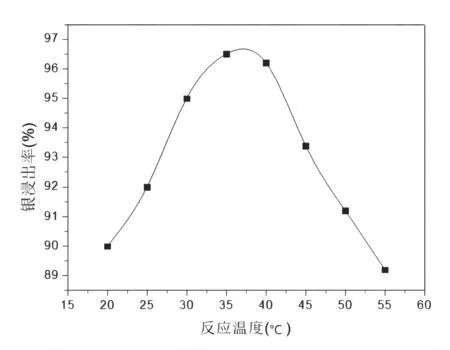
图2 反应温度对银浸出率的影响
亚硫酸根与氯化银生成的银络合离子除了受温度影响外,同时也受反应pH值的影响,pH值过低时,银络合离子容易分解,影响银的浸出率;pH值过高时,分金渣中的氯化银容易生成氧化银,不易与亚硫酸根形成银络合离子,主要反应方程式如式(4)~式(7)所示。试验在液固比为7,恒定温度35℃条件下,亚硫酸钠浓度为240g/L,控制不同的反应pH值,搅拌反应40min进行试验,反应pH值对银浸出率的影响结果如图3所示。

根据图3可知,银的浸出率随着反应PH值的升高而上升,当pH达到7~9时,再提高反应pH值,银的浸出率反而下降。主要原因是在酸性条件下银络合离子不稳定,而在碱性条件下氯化银容易生成氧化银,影响银络合离子反应,降低银的浸出率。所以,反应过程中控制pH值尤为关键,为了尽可能提高银的浸出率,反应pH值控制在7~9为宜。
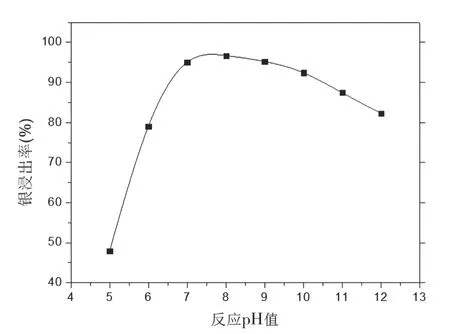
图3 反应pH值对银浸出率的影响
亚硫酸根与氯化银生成的银络合离子在溶液中的溶解度并不高,溶液中的银含量一般最高为18g/L~22g/L,而分金渣中银含量高达11.67%。因此,亚硫酸钠分银过程中液固比在很大程度上制约着银的浸出。试验在恒定温度35℃条件,反应pH值为7,亚硫酸钠浓度为240g/L,控制不同的反应液固比,搅拌反应40min进行试验,液固比对银浸出率的影响结果如图4所示。
根据图4可知,银的浸出率随着反应液固比的增大而上升,当液固达到7~9时,再扩大反应液固比值,对银的浸出率影响不明显,但会降低分金渣处理效率,增加废水处理量,增加生产成本。所以,要达到较高的银浸出率,同时减少废水处理量,反应液固比控制在7~9为宜。
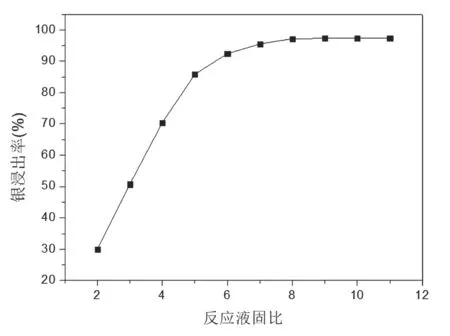
图4 反应液固比对银浸出率的影响
亚硫酸钠分银反应时间主要体现在反应速度的快慢,而反应速度由反应物中活化分子和活化能的影响。试验在恒定温度35℃条件,反应液固比为7,反应pH值为7,亚硫酸钠浓度为240g/L,对不同时间搅拌反应进行试验,反应时间对银浸出率的影响结果如图5所示。
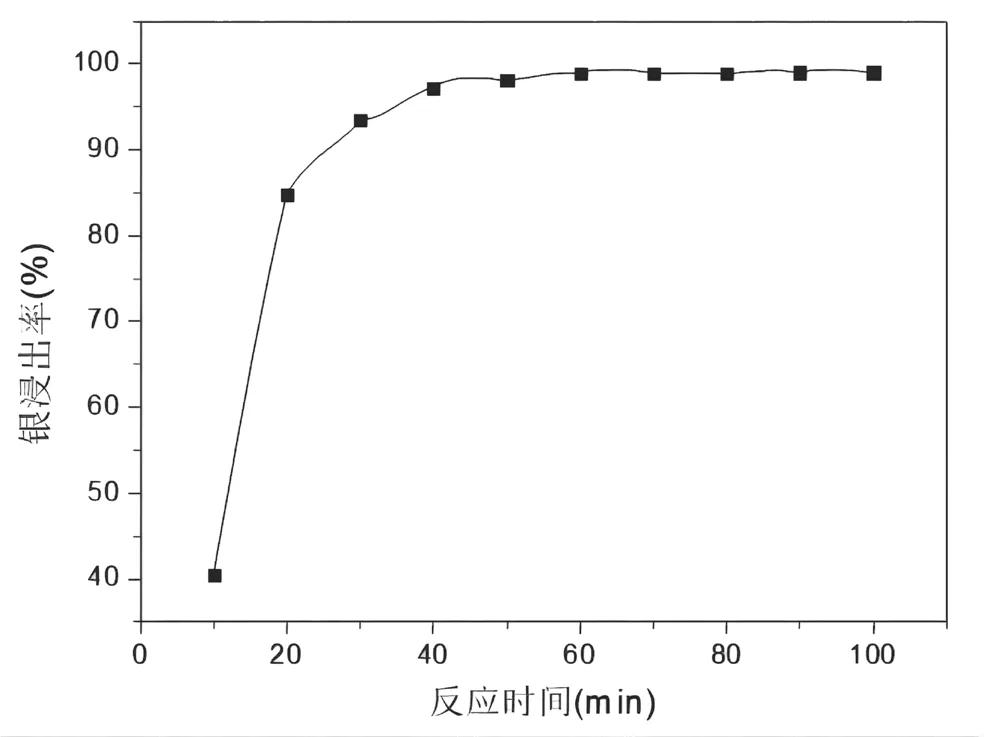
图5 反应时间对银浸出率的影响
图5显示,银的浸出率随着反应时间的延长而上升,当时间达到40min~60min,再继续进行反应,对银的浸出率影响不明显,但会增加搅拌电机电能的消耗。所以,要尽可能提高银的浸出率,节约电能,反应时间控制在40min~60min为宜。
2.2 碘量法测亚硫酸钠浓度结果与讨论
亚硫酸钠属于强碱弱酸盐,容易水解,直接测量亚硫酸钠浓度误差较大。乙酸锌加入亚硫酸钠溶液后可形成白色沉淀吸附亚硫酸钠,有抑制亚硫酸钠分解的作用,可以提高碘量法测亚硫酸钠浓度的准确性。试验取亚硫酸钠待测液10mL于250mL容量瓶内,加入一定的蒸馏水,加入4mL甘油,控制不同的乙酸锌溶液添加量,最后加入蒸馏水定容。摇匀后用5mL移液管取液5mL于锥形瓶,加入少许淀粉溶液作为指示剂,再用碘标液进行滴定,测量结果如图6所示。
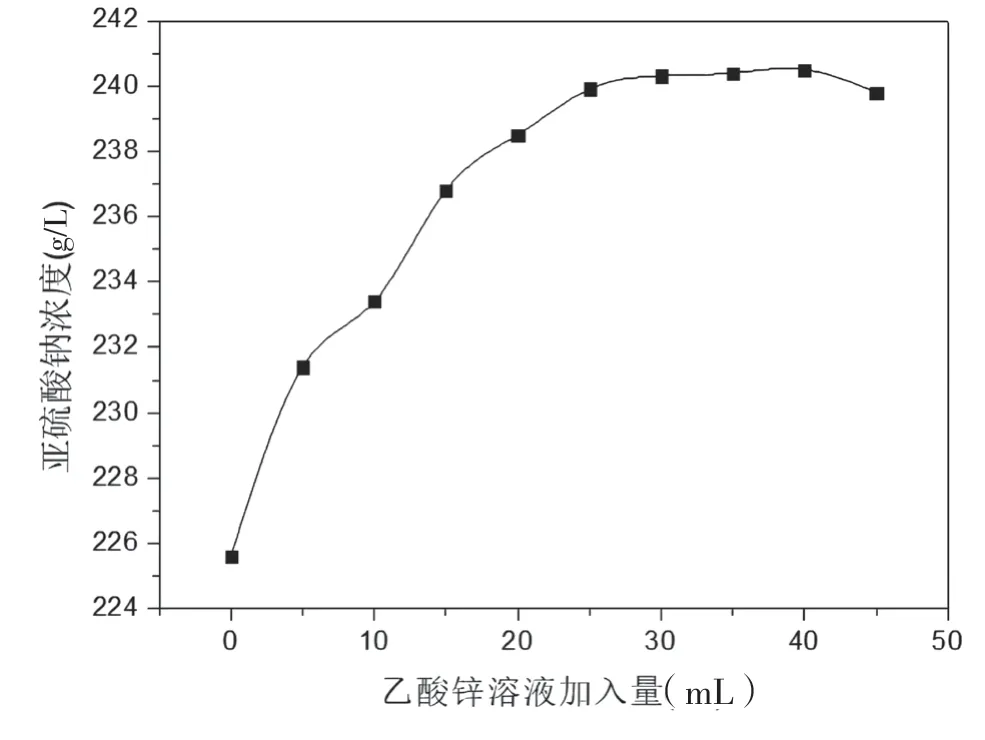
图6 乙酸锌溶液对碘量法测亚硫酸钠浓度的影响
根据图6可知,亚硫酸钠浓度测量结果随乙酸锌溶液加入量增大而上升,当乙酸锌溶液加入量达到25mL~35mL时,再加大乙酸锌溶液的加入量,亚硫酸钠浓度测量结果变化不明显,但会加大试剂的用量。所以,为使碘量法测亚硫酸钠浓度结果误差尽可能减小,测量过程中加入乙酸锌溶液量应控制在25mL~35mL为宜。
碘量法测亚硫酸钠浓度时加入乙酸锌后会产生白色沉淀,且其沉降速度很快,溶液中的亚硫酸钠会向白色沉淀中富集,加入甘油可以有效延缓白色沉淀的沉降速度,提高亚硫酸钠浓度测量结果的准确性。试验取亚硫酸钠待测液10mL于250mL容量瓶内,加入一定的蒸馏水,加入25mL乙酸锌溶液,控制不同的甘油添加剂,最后加入蒸馏水定容。摇匀后用5mL移液管取液5mL于锥形瓶,加入少许淀粉溶液作为指示剂,再用碘标液进行滴定。之后,静置5min,取容量瓶上中下不同部位亚硫酸钠溶液测量,结果见表2。
根据表2可知,加入甘油和乙酸锌溶液摇匀后,立刻进行碘量法测量时,只需要加入4mL~8mL甘油就可以大幅度降低测量误差,再增加甘油量,对测量结果影响不明显。静置5min后,没有加入甘油的试验样产生的亚硫酸钠浓度分层最明显,加入甘油量越多,亚硫酸钠浓度分层效果越不明显。因此,碘量法测量亚硫酸浓度在摇匀后,不宜放置时间过长,应该立即进行取样测量。为了节约试剂用量,同时提高测量的准确性,碘量法测量亚硫酸钠浓度时甘油的加油量为4mL~8mL为宜。
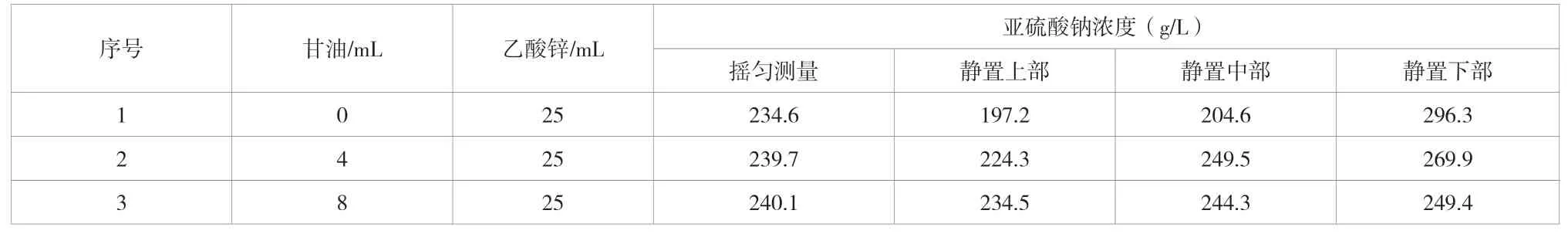
表2 甘油对碘量法测亚硫酸钠浓度结果的影响
3 结论
该文根据亚硫酸钠分银试验研究,确定了最佳控制条件:亚硫酸钠溶液浓度240g/L~270g/L,反应温度32℃~38℃,反应pH值为7~9,反应液固比为7~9,反应时间40min~60min。碘量法测量亚硫酸钠浓度的误差可以降低到小于1%,确保了分银过程亚硫酸钠浓度控制得当,进而提高了银的浸出率。该文经过3个月的试验验证,确定了分银最佳控制条件后,银的浸出率由95.6%提高到98.9%。

