RI与大隐静脉曲张合并股腘深静脉反流患者VCSS评分的相关性分析
杜建青, 汪 立, 吴忠隐, 李荣华, 张 弘
承德医学院附属医院血管外科, 河北 承德 067000
下肢浅静脉曲张是血管外科常见疾病,以小腿浅静脉曲张最多见,好发于大隐静脉,由多种不同疾病引起,多表现为下肢浅静脉扩张、迂曲[1]。对原发性下肢浅静脉曲张的规范评估和治疗有利于中断病程,改善患者预后[2]。临床实践中,大隐静脉曲张患者多合并股腘深静脉反流,准确评估下肢深静脉瓣的功能对临床医师合理准确地选择治疗方法具有重要指导价值。彩色多普勒超声是临床诊断下肢浅静脉曲张的常用方法,可获得可靠诊断结果[3]。但彩色多普勒超声在大隐静脉曲张合并股腘深静脉反流中的应用研究较少。静脉临床严重程度评分(VCSS)是评估下肢浅静脉曲张病情程度的常用工具[4],本研究重点探讨基于彩色多普勒超声检查的深静脉反流指数(RI)与大隐静脉曲张合并股腘深静脉反流患者VCSS评分的关联性,旨在为临床治疗本病提供参考依据。
1 资料与方法
1.1 一般资料
选取2018年1月至2022年1月我院150例大隐静脉曲张合并股腘深静脉反流患者作为研究组,其中男83例、女67例;年龄38~76岁,平均年龄(51.24±6.61)岁;平均病程(12.19±3.87)年;平均体质量指数(22.86±0.51)kg/m2;患侧:左下肢71例、右下肢79例;下肢静脉曲张临床-病因-解剖-病理生理(CEAP)分级[5]:C2级75例,C3级62例,C4级13例。选取60例同期未合并股腘深静脉反流的大隐静脉曲张患者作为对照组,其中男37例、女23例;年龄35~75岁,平均年龄(49.51±7.25)岁;平均病程(11.46±3.59)年;平均体质量指数(22.79±0.50)kg/m2;患侧:左下肢33例、右下肢27例;下肢静脉曲张CEAP分级:C2级37例,C3级21例,C4级2例。两组患者基线资料比较,差异无统计学意义(P>0.05)。本研究经我院伦理委员会审批通过。纳入标准:经下肢静脉造影证实为大隐静脉曲张,对照组未合并股腘深静脉反流,研究组合并股腘深静脉反流;病程≥3年;下肢静脉曲张CEAP分级C2~C4级;无神经系统疾病及沟通交流障碍;近1年CEAP分级无加重;患者知晓本研究,已签署同意书。排除标准:深静脉血栓形成患者;下腔静脉或髂静脉有狭窄或梗阻者;先天性下肢血管畸形者;手术后复发者;有严重心肺肾功能不全者;下肢深静脉血栓后遗症及髂静脉受压综合征患者。
1.2 方法
所有患者均于入院当天行下肢彩色多普勒超声检查,仪器为美国GE Logiq 9型彩色多普勒超声诊断仪,探头频率7.5~12.0 MHz,检查时患者仰卧,逐一检查下肢静脉,自大腿根部偏内侧开始自下而上,依次检查股总静脉至浅静脉及交通支的分布、走行,最终以腘横纹为中心测定腘静脉反流速度、反流时间,计算RI,RI=反流时间×静脉反流平均速度/正常回流平均速度。
判定静脉反流程度:无反流:反流速度<10 mm/s,持续时间<0.6 s;轻度反流:反流速度10~<20 mm/s,持续时间0.6~<1.0 s;中度反流:反流速度20~40 mm/s,持续时间1.0~3.0 s;重度反流:反流速度>40 mm/s,持续时间>3 s[6]。
评估VCSS评分:VCSS包括静脉曲张、疼痛、静脉水肿等共10个项目,每项0~3分,分别对应无反流、轻度反流、中度反流、重度反流,总分0~30分,分值越高,下肢静脉症状越严重[7]。
1.3 统计学方法
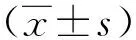
2 结果
2.1 两组反流时间、反流速度及RI比较
研究组反流时间、反流速度及RI均较对照组高,差异有统计学意义(P<0.05)。见表1。

表1 两组反流时间、反流速度及RI比较
2.2 反流时间、反流速度及RI对大隐静脉曲张合并股腘深静脉反流的诊断价值
以研究组作为阳性样本,对照组作为阴性样本,绘制ROC曲线,结果显示,反流时间、反流速度及RI诊断大隐静脉曲张患者股腘深静脉反流的曲线下面积(AUC)分别为0.820、0.749、0.832。将反流时间、反流速度及RI经Logistic回归模型拟合生成联合预测因子,列出联合预测因子取不同值时对应的敏感度、特异度和预测准确率,取约登指数为最大值时联合预测因子所对应的数值作为最佳临界值,AUC为0.875。见表2。

表2 反流时间、反流速度及RI对大隐静脉曲张合并股腘深静脉反流的诊断价值
2.3 反流时间、反流速度及RI与大隐静脉曲张合并股腘深静脉反流风险的关系
以大隐静脉曲张合并股腘深静脉反流与否为因变量(否=0,是=1),反流时间、反流速度及RI作为自变量(以ROC曲线截断值为界:≤截断值=1,>截断值=2),Logistic回归分析,调整其他混杂因素后,反流时间、反流速度及RI仍与大隐静脉曲张合并股腘深静脉反流独立相关,反流时间、反流速度及RI越高,大隐静脉曲张患者合并股腘深静脉反流风险越大(P<0.05)。见表3。

表3 反流时间、反流速度及RI与大隐静脉曲张合并股腘深静脉反流风险的关系
2.4 研究组不同静脉反流程度患者RI、VCSS评分比较
由表4可知,大隐静脉曲张合并股腘深静脉反流的不同静脉反流程度患者RI、VCSS评分比较,差异有统计学意义(P<0.05)。经Spearman相关性模型分析可知,大隐静脉曲张合并股腘深静脉反流患者RI、VCSS评分与静脉反流程度呈正相关关系(r=0.912、0.806,P<0.05)。

表4 不同静脉反流程度患者RI、VCSS评分比较
2.5 大隐静脉曲张合并股腘深静脉反流患者RI与VCSS评分的相关性分析
大隐静脉曲张合并股腘深静脉反流患者RI与VCSS评分呈正相关关系(r=0.738,P<0.05)。见图1。

图1 大隐静脉曲张合并股腘深静脉反流患者RI与VCSS评分的相关性
3 讨论
按血流动力学变化,可将下肢静脉曲张分为血液倒流性和回流障碍性两大类,前者主要由静脉瓣膜关闭不全引起,后者则为静脉回流受阻所致[8]。大隐静脉曲张合并股腘深静脉反流属于血液倒流,临床诊断以下肢静脉造影技术为“金标准”。但下肢静脉造影属于有创操作,操作复杂且价格昂贵,临床应用存在一定局限性[9,10]。
彩色多普勒超声具有无创、操作简便、准确度高、可重复性强等优势,在下肢静脉曲张诊断方面具有较强优势。陈竹等[11]研究结果显示,与常规的诊断方式比较,采用彩色多普勒超声诊断下肢静脉曲张合并血栓性浅静脉炎能清晰观察患者实际静脉内径情况,可明显提高诊断效果。且有报道显示彩色多普勒超声可准确评估大隐静脉曲张患者分支静脉与隐静脉连接的局部解剖关系,有助于指导临床评估患者病情[12]。由于下肢浅静脉与深静脉关系密切,深静脉病变可直接引起血液倒流,增高静脉压,促进静脉曲张进展,了解深静脉血流畅通度及静脉瓣功能情况,对临床选择适宜的手术方式至关重要[13]。国外有报道指出,彩色多普勒超声可准确检出大隐静脉和小隐静脉反流情况[14]。大隐静脉曲张合并股腘深静脉反流患者存在深静脉瓣功能障碍,但国内关于彩色多普勒超声诊断大隐静脉曲张合并股腘深静脉反流的报道较少,为弥补国内此方面研究的不足,本研究以大隐静脉曲张患者是否合并股腘深静脉反流为切入点,通过对比分析发现,合并股腘深静脉反流的大隐静脉曲张反流时间、反流速度及RI均明显高于未合并股腘深静脉反流患者,分析其原因可能在于,大隐静脉曲张合并股腘深静脉反流患者长期存在深静脉瓣功能障碍,深静脉回流长期处于超负荷状态,导致静脉壁变薄、静脉腔扩张[15,16],从而增大反流时间、反流速度及RI,加重患者病情。本研究进一步通过多因素分析发现,反流时间、反流速度及RI越高,大隐静脉曲张患者合并股腘深静脉反流风险越大,进一步说明基于彩色多普勒超声检测的反流时间、反流速度及RI与大隐静脉曲张患者合并股腘深静脉反流显著相关。基于上述研究结果,笔者推测反流时间、反流速度、RI或许能应用于大隐静脉曲张患者合并股腘深静脉反流的诊断,而本研究ROC曲线分析结果显示,反流时间、反流速度、RI诊断大隐静脉曲张患者股腘深静脉反流的AUC均在0.7以上,具有良好诊断效能,验证了上述推测的正确性,且各指标联合诊断的AUC为0.875,高于单独诊断,说明各指标联合有助于提高诊断效能,可为临床判断大隐静脉曲张患者合并股腘深静脉反流提供更准确参考依据。
此外,VCSS是目前评估下肢浅静脉曲张患者病情、疗效及预后最常用的评分系统,其评价内容涉及10个方面,涵盖疼痛、水肿、炎症反应程度等方面,能较为客观、全面反映慢性静脉疾病严重程度[17,18]。本研究结果显示,大隐静脉曲张合并股腘深静脉反流患者RI与VCSS评分存在较强相关性,且RI、VCSS评分与静脉反流程度呈正相关,说明RI也可作为反映大隐静脉曲张合并股腘深静脉反流患者疾病严重程度的参考指标,且能评估静脉反流程度,且彩色多普勒超声检测RI的可行性及可重复性高,具有较高临床应用价值。
综上可知,通过彩色多普勒超声检测深静脉RI与大隐静脉曲张合并股腘深静脉反流患者VCSS评分存在较强相关性,可辅助临床评估疾病严重程度及静脉反流程度,且反流时间、反流速度及RI联合诊断大隐静脉曲张合并股腘深静脉反流的效能较高,值得推广应用。但本研究仍存在一定不足,如未明确RI评估患者疾病严重程度及静脉反流程度的具体价值,未来工作中仍需深入探讨。

