超声心动图参数联合系统性炎症反应指数对急性心力衰竭患者短期预后的预测价值
尹玉莲, 戴朝晖, 李利, 金静
急性心力衰竭(acute heart failure,AHF)是一种危及患者生命的临床综合征,是指突发性心力衰竭或原有心力衰竭的体征加重[1]。AHF患者临床表现为心肌收缩力明显下降,心力衰竭明显增加。心负荷、心输出量突然下降,肺循环压力急剧上升,从而引发肺充血、肺水肿和心源性休克等症状[2]。AHF起病急,疾病进展迅速,严重危害患者的生命健康和生活质量[3]。随着全球老龄化的发展,AHF的发病率及由其导致的死亡也逐年上升[4]。因此,尽早准确判断患者病情和评估预后对治疗方式的选择至关重要。近年来,随着影像学技术的发展,超声心动图成为了AHF诊断及评估预后的重要方式[5]。然而,最近的研究显示,仅利用超声心动图预测患者预后的效能较为一般[6]。目前,已有多种分子标志物被报道在AHF患者预后的预测中具有一定价值,如成纤维细胞生长因子21[7]、神经调节蛋白1[8]等。然而,这些分子标志物并非AHF患者的常规检测指标,且检测结果出来得较晚。若能从常规检查的血常规等简便、快速、廉价的检测指标入手,寻找可用于预测AHF患者预后的指标,则更能被患者接受。综合中性粒细胞、单核细胞和淋巴细胞绝对值的系统性炎症反应指数(systemic inflammatory response index,SIRI)作为一种新的炎症性指标,近年来在疾病诊断和预后评估等方面广受关注[9-11]。因此,本研究旨在探讨超声心动图参数联合SIRI对AHF患者短期预后的预测价值,以期为临床应用提供参考依据。
材料与方法
1.病例资料
搜集2020年12月至2022年4月于长沙市第四医院就诊的AHF患者作为研究对象。病例纳入标准:①依据《中国心力衰竭诊断和治疗指南2018》中的诊断标准;②年龄≥18周岁;③在我院接受规范改善心力衰竭的治疗;④影像学及临床资料完整。病例排除标准:①合并严重肝、肾功能不全;②合并恶性肿瘤、自身免疫性疾病或神经系统疾病;③合并肺源性心脏病、肺动脉高压、急性脑血管病、感染性休克等;④随访期间失访。经纳入标准及排除标准筛选后,共纳入120例患者,其中男75例,女45例,平均年龄(66.45±5.28)岁,平均体质量指数(body mass index,BMI)为(24.32±3.18) kg/m2。本研究得到了医院伦理委员会的批准(编号:CCCDSYY-LLSC-KYXM-2020-01),所有患者均自愿参与研究,并签署了知情同意书。
2.研究方法
超声心动图检测:采用飞利浦IU Elite型超声心动仪及S5-1单晶体探头,频率2.0~4.0 MHz,配备PW-TDI技术。就诊后24 h内,由2位超声科副主任及以上职称医师对所有研究对象进行超声心动图检查,患者取左侧卧位及仰卧位,平静呼吸,于胸骨旁左室长轴、心尖二腔及心尖四腔切面测量左心室收缩期末容积(left ventricular end-systolic volume,LVESV)、左心室舒张期末容积(left ventricular end-diastolic volume,LVEDV)、左心室射血分数(left ventricular ejection fraction,LVEF)、二尖瓣舒张早期血流峰值速度与二尖瓣环舒张早期运动峰值速度比值(E/E')和左心室整体纵向应变(global longitudinal strain,GLS),所有参数均取3个心动周期测值的平均值。
临床指标和系统性炎症反应指数的搜集:记录所有研究对象的性别、年龄、BMI、高血压及糖尿病史。查阅病历和化验单,记录入院后首次检测的中性粒细胞(neutrophils,N)、单核细胞(monocytes,M)、淋巴细胞(lymphocyte,L)数值、B型钠尿肽前体(B-type natriuretic peptide precursor,NT-proBNP)及高敏C反应蛋白(high sensitivity C-reactive protein,hs-CRP)水平,计算SIRI,SIRI=N×M/L。根据美国纽约心脏病协会(New York Heart Association,NYHA)心功能分级对所有研究对象的心功能水平进行分级并记录。
随访:所有患者接受规范化治疗,出院后随访6个月,每周通过门诊、电话或微信等方式随访,随访终点为患者因心衰再入院或全因死亡,根据患者预后将所有患者分为终点事件组和无终点事件组。
3.统计学分析
采用SPSS 22.0软件进行统计学分析。符合正态分布的定量数据以均值±标准差表示,组间比较采用t检验。定性资料以频数和百分比表示,组间比较采用χ2检验。应用二元Logistic回归分析多个因素对患者预后的影响,应用受试者工作特征(receiver operating characteristic,ROC)曲线评估超声心动图参数和SIRI预测AHF患者预后的效能。以P<0.05为差异有统计学意义。
结 果
1.两组患者基本资料比较
随访6个月后,52例(43.33%)患者发生了终点事件,68例(56.67%)患者未发生终点事件。终点事件组与无终点事件组患者的性别、BMI、高血压史、糖尿病史、AHF病因、NT-proBNP及hs-CRP比较差异均无统计学意义(P>0.05),而年龄、NYHA分级在两组间差异有统计学意义(P<0.05,表1)。
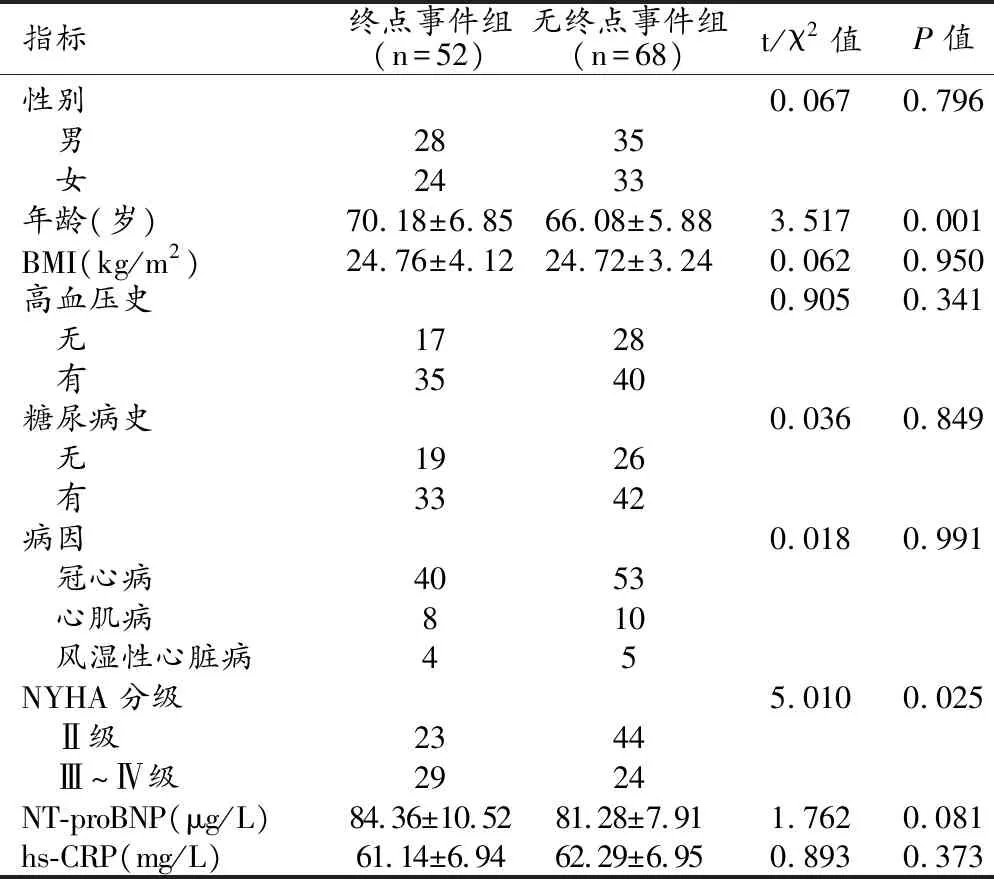
表1 两组患者基本资料的比较 (例)
2.两组超声心动图参数及SIRI的比较
终点事件组患者的LVEF显著低于无终点事件组,GLS绝对值显著低于无终点事件组,SIRI显著高于无终点事件组,差异有统计学意义(P<0.05),而LVESV、LVEDV和E/E'在两组间差异无统计学意义(P>0.05,表2,图1~2)。
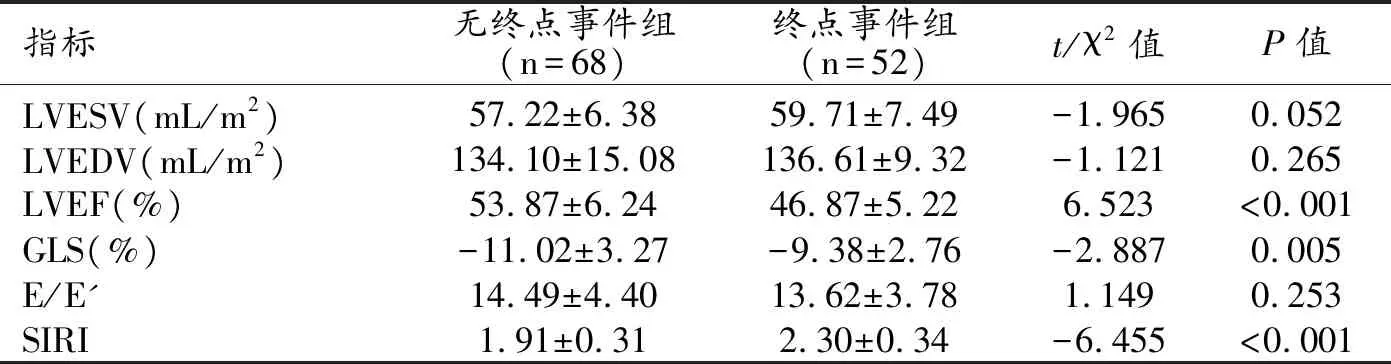
表2 两组超声心动图参数及SIRI的比较
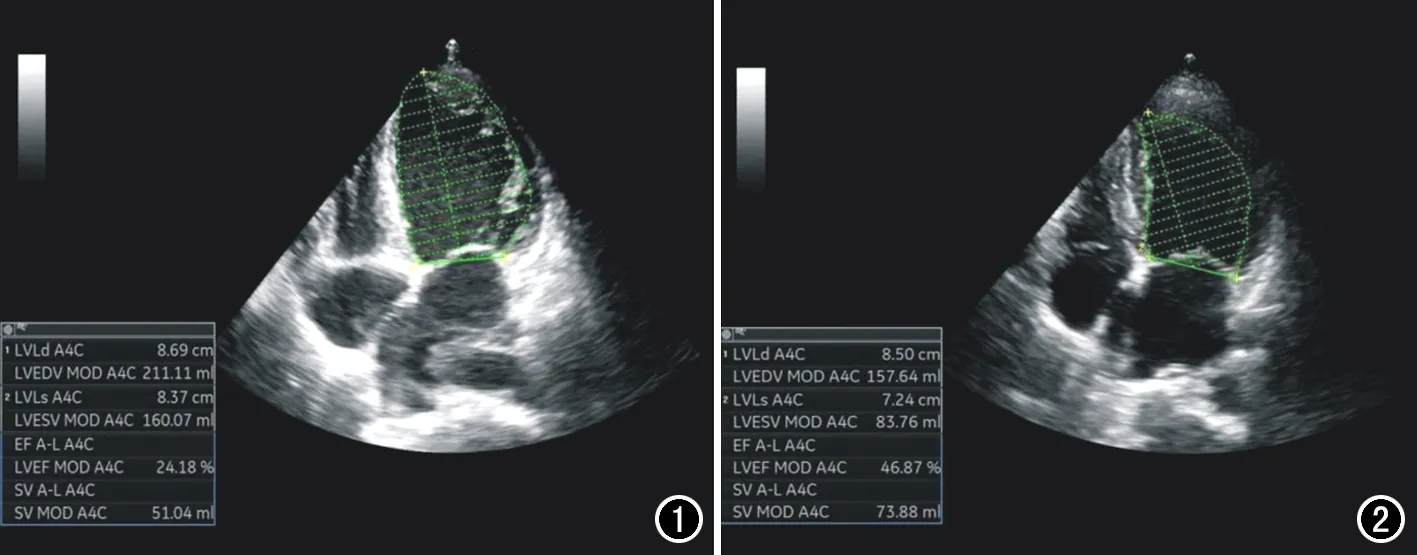
图1 AFH患者,男,年龄68岁,随访期间因心衰再次入院。图2 AHF患者,男,年龄65岁,随访期间未发生终点事件。
3.不同心功能分级患者超声心动图参数及SIRI的比较
NYHA分级ⅡI级患者的LVEF显著高于Ⅲ~Ⅳ级患者,GLS绝对值显著低于Ⅲ~Ⅳ级患者,SIRI显著低于Ⅲ~Ⅳ级患者,差异有统计学意义(P<0.05),而LVESV、LVEDV和E/E'在两组间的差异无统计学意义(P>0.05,表3)。
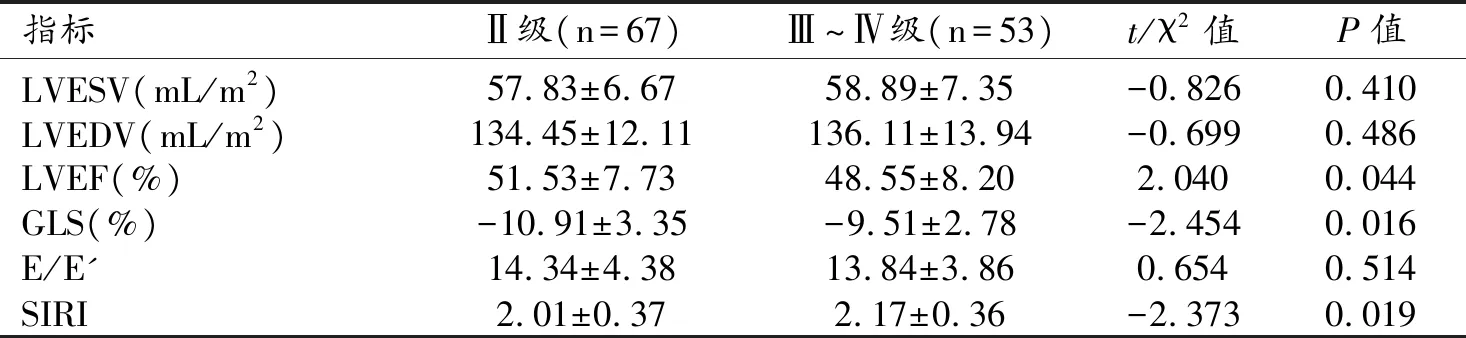
表3 不同心功能分级患者超声心动图参数及SIRI的比较
4.影响AHF患者预后的多因素Logistic回归分析
以AHF患者是否发生终点事件为因变量(未发生=0,发生=1),将单因素分析中有统计学意义的变量纳为自变量,进行多因素Logistic回归分析,结果显示,LVEF、GLS和SIRI是AHF患者短期预后不良的独立危险因素(P<0.05,表4)。

表4 影响AHF患者预后的多因素Logistic回归分析
5.超声心动图参数及SIRI对患者预后的预测效能
以AHF患者是否发生终点事件作为状态变量(未发生=0,发生=1),将LVEF、GLS、SIRI及三者联合分别作为检验变量,进行ROC曲线分析。ROC曲线分析结果显示,LVEF预测AHF患者短期预后不良的曲线下面积(area under the curve,AUC)为0.804,95% CI为0.727~0.881(P<0.001),敏感度和特异度分别为65.4%和82.4%;GLS预测AHF患者短期预后不良的AUC为0.843,95% CI为0.772~0.914(P<0.001),敏感度和特异度分别为78.8%和77.9%;SIRI预测AHF患者短期预后不良的AUC为0.793,95%CI为0.714~0.873(P<0.001),敏感度和特异度分别为71.2%和73.5%;三者联合(LVEF+GLS+SIRI)预测AHF患者短期预后不良的AUC为0.950,95%CI为0.915~0.986 (P<0.001),敏感度和特异度分别为88.5%和92.6%。三者联合预测AHF患者短期预后不良的效能显著优于单独使用LVEF、GLS或SIRI(图3)。
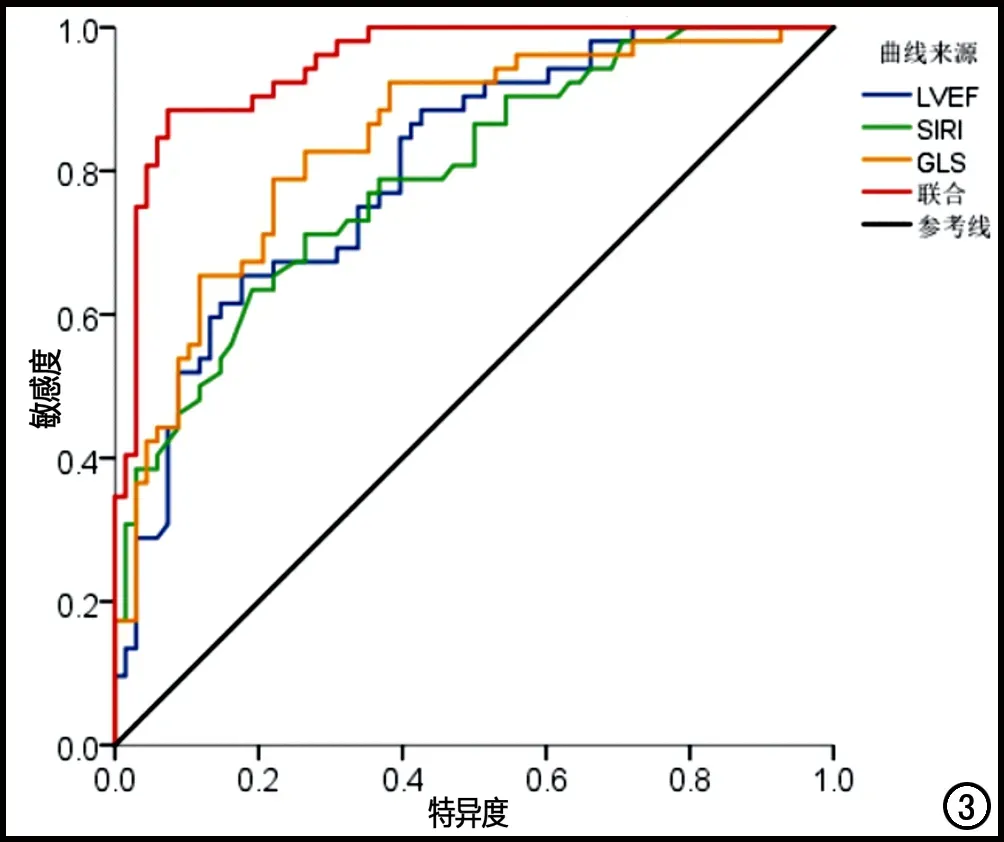
图3 LVEF、GLS、SIRI及三者联合预测患者预后的ROC曲线。
讨 论
尽管近几十年来心力衰竭的诊断和治疗策略有了显著改进,但该病仍然是导致全球人群死亡的重要心血管疾病。AHF是指心功能失代偿状态,以容量超负荷和肺水肿症状为主要表现。从病理上看,AHF可由急性心脏事件如心肌梗死引起,也可由感染、心律失常或心肌缺血等危险因素诱发慢性心力衰竭患者心功能恶化引起。尽管在住院期间进行了强化治疗,但AHF患者的预后非常差,Rigopoulos等的研究报道AHF患者出院后3个月内死亡或再住院的比例高达50%。国内的一项研究发现,在北京14家医院前瞻性登记的3335例AHF患者中,15%的患者在30天内死亡,32.3%的患者在1年内死亡,患者死亡或再入院率高达60.0%[12]。因此,在临床实践中,早期识别有较高不良临床结局风险的AHF患者具有重要意义。超声检查方便、快捷、费用相对低廉且无辐射[13],目前超声心动图被广泛应用于AHF患者的诊断和预后评估中,然而预测效能不尽如人意。SIRI是一种新型复合性炎症指标,近年来被广泛报道与多种疾病的预后有关。Wang等[10]的研究显示,SIRI可作为急性缺血性脑卒中患者早期神经系统恶化的预测指标。Lv等[14]的研究表明,术前SIRI水平升高可提示肾细胞癌合并下腔静脉肿瘤血栓切除术患者的预后不良。
本研究结果显示,在随访6个月时间内,43.33%的患者死亡或因心衰再入院,这与之前研究报道的结果类似[15]。不同预后患者的年龄、NYHA分级差异有统计学差异。多项研究显示年龄是AHF患者短期预后的影响因素,随着年龄的增加,AHF患者短期预后不良的风险增大[8,15]。NYHA分级是按诱发心力衰竭症状的活动程度将心功能的受损状况分为四级,在一定程度上反映了AHF患者的病情严重程度,包艳春等[8]的研究显示NYHA分级与AHF患者短期预后不良显著相关。本研究结果显示,发生终点事件患者的LVEF显著低于未发生终点事件的患者,且NYHA分级Ⅲ~Ⅳ级患者的LVEF显著低于II级患者,这与之前研究报道的结果一致[6]。发生终点事件患者的SIRI显著高于未发生终点事件的患者,且NYHA分级Ⅲ~Ⅳ级患者的SIRI显著高于Ⅱ级患者。因此,笔者推测超声心动图参数、SIRI与AHF患者的预后有关,于是进一步应用多因素Logistic回归分析了影响AHF患者预后的危险因素;结果显示,LVEF、GLS和SIRI是AHF患者短期预后不良的独立危险因素。LVEF是指左心室每一次收缩泵到主动脉的血液占左心室内血液的百分比,LVEF减低意味着心脏每次搏动射出的动脉血减少,外周器官也容易出现缺血缺氧改变。GLS是研究较多并广为接受的评价左心室整体收缩功能的应变指标,可反映早期收缩功能障碍,对检测心脏亚临床受累较敏感。心衰导致患者的心脏射血功能下降,左心室射血功能下降将严重影响预后。Palazzuoli等[16]的研究结果表明伴随LVEF降低的心衰患者预后更差,再次入院率也更高。Sengelov等[17]的研究显示GLS与心衰患者发生全因死亡或心衰再住院独立相关。SIRI作为一种炎性复合指标,一定程度上反映患者的炎症水平。炎症细胞因子在心力衰竭患者体内过度表达,可通过影响心肌收缩力,引起心肌肥大,诱导心肌纤维化和凋亡,促进心脏重构等作用促进心力衰竭的发生发展,而且炎症因子预示着心血管不良事件的发生,抗炎治疗在AHF的治疗中至关重要。相关研究表明,AHF患者的血清炎症因子水平显著升高,降低炎症因子水平可改善患者左心室重构及患者预后[18]。本研究进一步的ROC曲线分析结果显示,LVEF、GLS、SIRI预测AHF患者短期预后不良的敏感度和特异度分别为65.4%和82.4%、78.8%和77.9%、71.2%和73.5%,效能均较为一般。应用LVEF、GLS联合SIRI预测AHF患者短期预后不良的敏感度和特异度分别为88.5%和92.6%,敏感度和特异度均较好。
综上所述,LEVF、GLS、SIRI与AHF患者的短期预后有关,具有一定临床应用价值。

