Na+掺杂V2O5电极材料的制备及其储锌性能
陈文昊 武目选 颉雨佳 朱裔荣
湖南工业大学材料与先进制造学院 湖南 株洲 412007
1 研究背景
为解决过度使用化石燃料造成的环境问题和能源危机,人们开始使用可再生能源,如太阳能、风能等[1-3]。然而, 太阳能和风能受气候、纬度位置、地形等自然条件的限制,不是定期可靠和恒定的。为了有效地利用可再生能源,开发具有高比能、大功率密度和良好的循环稳定性等特点的大规模电能存储系统迫在眉睫[4-5]。
锂离子电池作为传统储能装置具有高比能的优势,但面临安全性低、锂储量低、成本高等问题[6-9]。在寻找新的储能装置过程中,与Li电化学性质相近的Al、Mg、Zn进入了人们视野[10-12]。Zn元素在地球储量丰富,可用于水系电解液二次电池。以Zn为负极的锌离子电池的理论比容量高达820 mA·h/g。其具有以下优势:1)相对标准氢电极,Zn的氧化还原电位较低(-0.76 V),有利于提高工作电压窗口范围和能量密度;2)Zn的析氢过电位较高,因而Zn在水溶液中的电化学性质稳定;3)Zn在氧化还原反应过程中能转移2个电子,相比锂离子电池、钠离子电池具有更高的能量密度[13-14]。尽管如此,锌离子电池的进一步发展仍受制于锌离子电池正极有限的比容量和较差的倍率性能[13,15]。
钒在地壳中储量丰富,具有成本低、多种氧化价态以及安全性高等特点,因而钒基化合物成为了锌离子电池正极材料的研究热点[16-19]。五氧化二钒(V2O5)具有层状结构,适合锌离子的嵌入和脱嵌,但V2O5的电化学活性位点有限以及电导率较低,导致其能量密度较低和倍率性能较差。目前,已有大量的研究工作着眼于提高V2O5正极材料的电导特性,如制备碳基复合钒氧化物、阳离子掺杂等。V2O5具有开放的骨架结构,通过阳离子掺杂可有效改变V2O5晶体几何结构,如改变层间距或离子重排,进而改善V2O5晶体中电子传导和离子扩散,提高电化学性能[21-22]。因此,选择合适的掺杂离子和便捷的合成方法对于研发高性能V2O5锌离子电池正极材料具有重要意义。
Na+离子具有合适的离子半径,可将层状结构转为隧道结构,且该结构更稳定。故本文拟以Na+作为掺杂阳离子,采用一步水热法制备Na0.4V2O5纳米粉体,并用于锌离子电池正极材料,进行循环伏安(CV)测试、交流阻抗(EIS)测试,以期为锌离子电池正极材料改性提供新思路。
2 实验
2.1 试剂与材料
所有试剂均为分析纯。五氧化二钒,上海阿拉丁化学有限公司;草酸钠,广州化学试剂厂;三氟甲烷磺酸锌(Zn(CF3SO3)2),上海毕得医药科技有限公司;过氧化氢(质量分数30%)、无水乙醇,天津市天力化学试剂有限公司。去离子水为实验室自制。纽扣电池壳,武汉格瑞斯新能源有限公司;泡沫镍,苏州钻五电子科技有限公司;乙炔黑,河北墨钰化工有限公司;不锈钢箔,东莞市天申金属材料有限公司;锌片,深圳市阿满达五金钢材有限公司;玻璃纸,济南贝亚特化工科技有限公司。
2.2 仪器与设备
电子天平,FA1204型,常州科源电子仪器有限公司;磁力搅拌器,C-MAG MS 7S25型,艾卡(广州)仪器设备有限公司;分析天平,H0503型,河北德科机械科技有限公司;超声波清洗机,XTF-1030型,广东顺德先泰超声工程设备有限公司;鼓风干燥箱(HG-9035A型)、真空干燥箱(DZF-6730A型),上海精宏实验设备有限公司;纽扣电池压片机(MSK-T-07型)、涂片机(AFA-I型)、切片机(MSK-T10型)、封装机(MSK-110D型),深圳科晶智达科技有限公司;X射线衍射仪,Ultima IV型,日本理学株式会社;电化学工作站,CHI-660F型,上海辰华仪器有限公司;充放电测试仪,BTS-5 V/10 mA,深圳新威尔电子有限公司。
2.3 实验步骤
1)Na0.4V2O5纳米棒的制备
采用简单的一步水热合成法制备Na0.4V2O5。将1 g V2O5加入到50 mL去离子水中,并加入10 mL H2O2,磁力搅拌30 min,然后加入0.0737 g Na2C2O4继续搅拌30 min,将得到的悬浮液转移至聚四氟乙烯不锈钢反应釜中,并置入电热鼓风干燥箱中200 ℃恒温24 h,待反应釜自然冷却至室温,将反应所得的沉淀物真空抽滤并采用去离子水和无水乙醇分别洗涤3次,最后在真空干燥箱70 ℃干燥12 h。
2)V2O5纳米棒的制备
V2O5纳米棒也采用一步水热合成法制备。首先将1 g V2O5加入到50 mL去离子水,再加入10 mL H2O2并磁力搅拌30 min,将所得溶液转移至聚四氟乙烯不锈钢反应釜中,并置入电热鼓风干燥箱中200℃恒温反应24 h,待反应釜自然冷却至室温,将反应所得的沉淀物真空抽滤并用去离子水和无水乙醇分别洗3次,最后放置于真空干燥箱70 ℃干燥12 h。
3)电极片的制备
按m(活性物质)∶m(导电剂)∶m(黏 结剂)=6∶3∶1制备电极片。将活性物质(Na0.4V2O5或V2O5)和导电剂(乙炔黑)置于玛瑙研钵中研磨,再加入黏结剂聚偏二氟乙烯(polyvinylidene difluoride,PVDF)和N-甲基吡咯烷酮研磨成黑色膏状物质。将研磨后得到的电极材料放在对辊机上,压制成有一定厚度的电极片,并将电极片置于80 ℃真空干燥12 h,然后冲成直径10 mm的小圆片待用。
2.4 材料表征和电化学测试
采用X射线衍射仪表征Na0.4V2O5的物相结构。将制备的电极片作为正极,金属锌作为负极,电解液为3 mol/L的Zn(CF3SO3)2,隔膜为玻璃纤维,集流体为不锈钢箔,组装成CR2016型纽扣电池,使用电池性能测试仪进行恒电流充放电性能测试。使用电化学工作站进行循环伏安测试和交流阻抗测试,频率为(0.1~105)Hz。
3 结果与分析
3.1 Na0.4V2O5的物相表征
图1 是Na0.4V2O5的X射线衍射(XRD)图谱。由图1可知,Na0.4V2O5大部分的衍射峰与V2O5的标准卡片PDF 52-0794一致。其中,8°处的衍射峰较为尖锐,属于V2O5的(001)晶面衍射峰,证明用一步水热法制备的Na0.4V2O5结晶度较高。Na0.4V2O5的(001)晶面的衍射角度略低于V2O5标准卡片,证明随着Na离子掺杂,Na0.4V2O5的(001)晶面间距增大,更有利于Zn2+离子的嵌入和脱嵌[20,22]。另外,47.13°, 50.43°处衍射峰分别与Na0.33V2O5(PDF 48-0382)的(40-7)和(31-7)对应,说明Na离子除了掺杂进入V2O5晶格外还形成了少量其它钒基氧化物相。

图1 Na0.4V2O5的XRD图谱Fig. 1 XRD pattern of Na0.4V2O5
3.2 Na0.4V2O5和V2O5的电化学性能
图2为扫描速率为0.1 mV·s-1,电压测试范围为0.2~2.0 V,Na0.4V2O5和V2O5电极的循环伏安曲线。
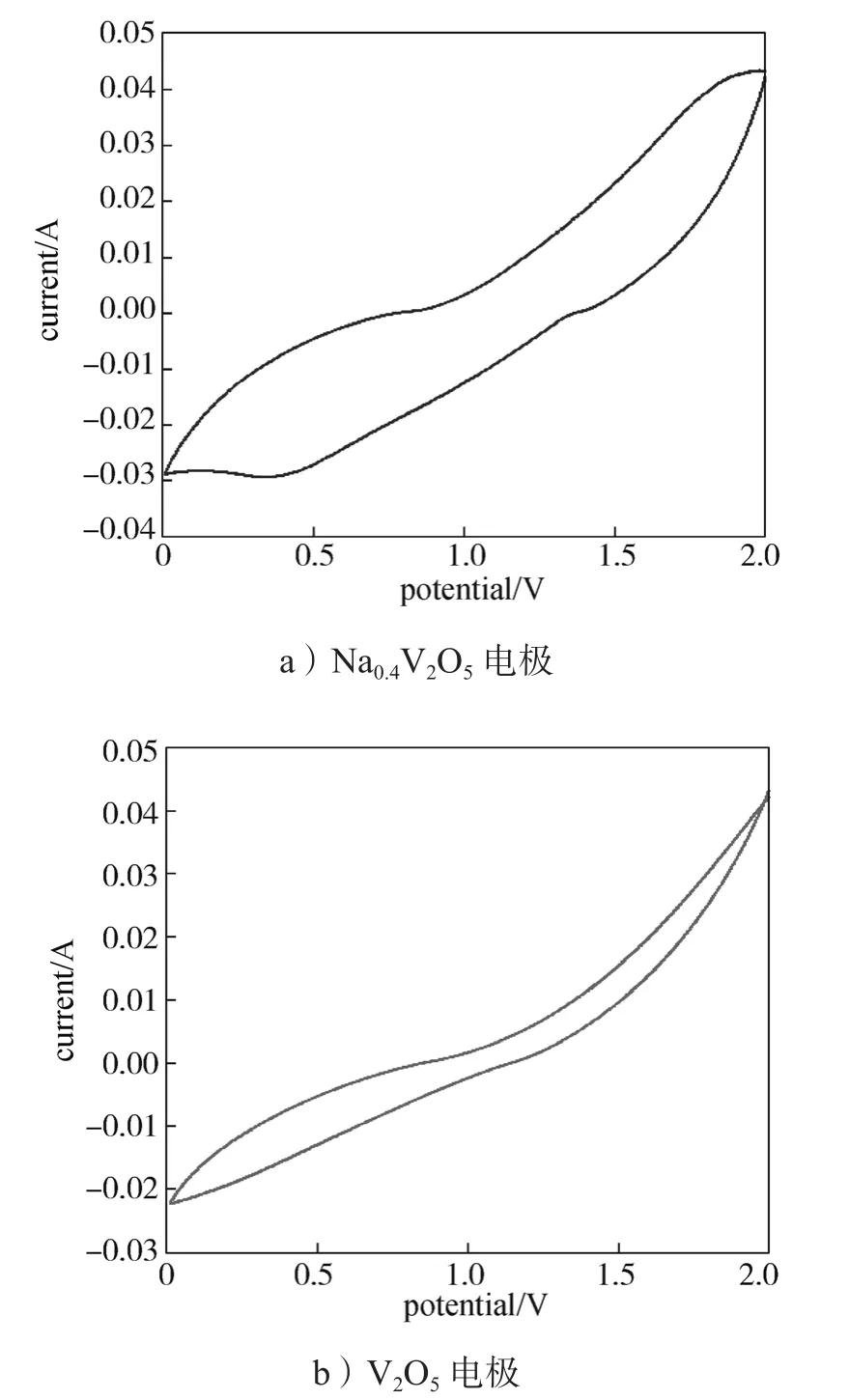
图2 Na0.4V2O5和V2O5电极的循环伏安曲线Fig. 2 CV curves of Na0.4V2O5 and V2O5 electrodes
由图2可知:1)Na0.4V2O5的还原峰在1.7 V处,对应Zn2+嵌入钒基氧化物的隧道结构;在氧化扫描过程中,氧化峰位于0.6 V处,对应Zn2+的脱嵌[23]。2)V2O5的氧化还原峰强度较弱。在同样的扫描速率下,Na0.4V2O5的CV曲线的积分面积明显大于V2O5电极的,说明Na0.4V2O5电极相比V2O5电极能存储更多的锌离子,比电容更高。
图3为Na0.4V2O5和V2O5电极在电流密度为100 mA/g下的首次充放电曲线。
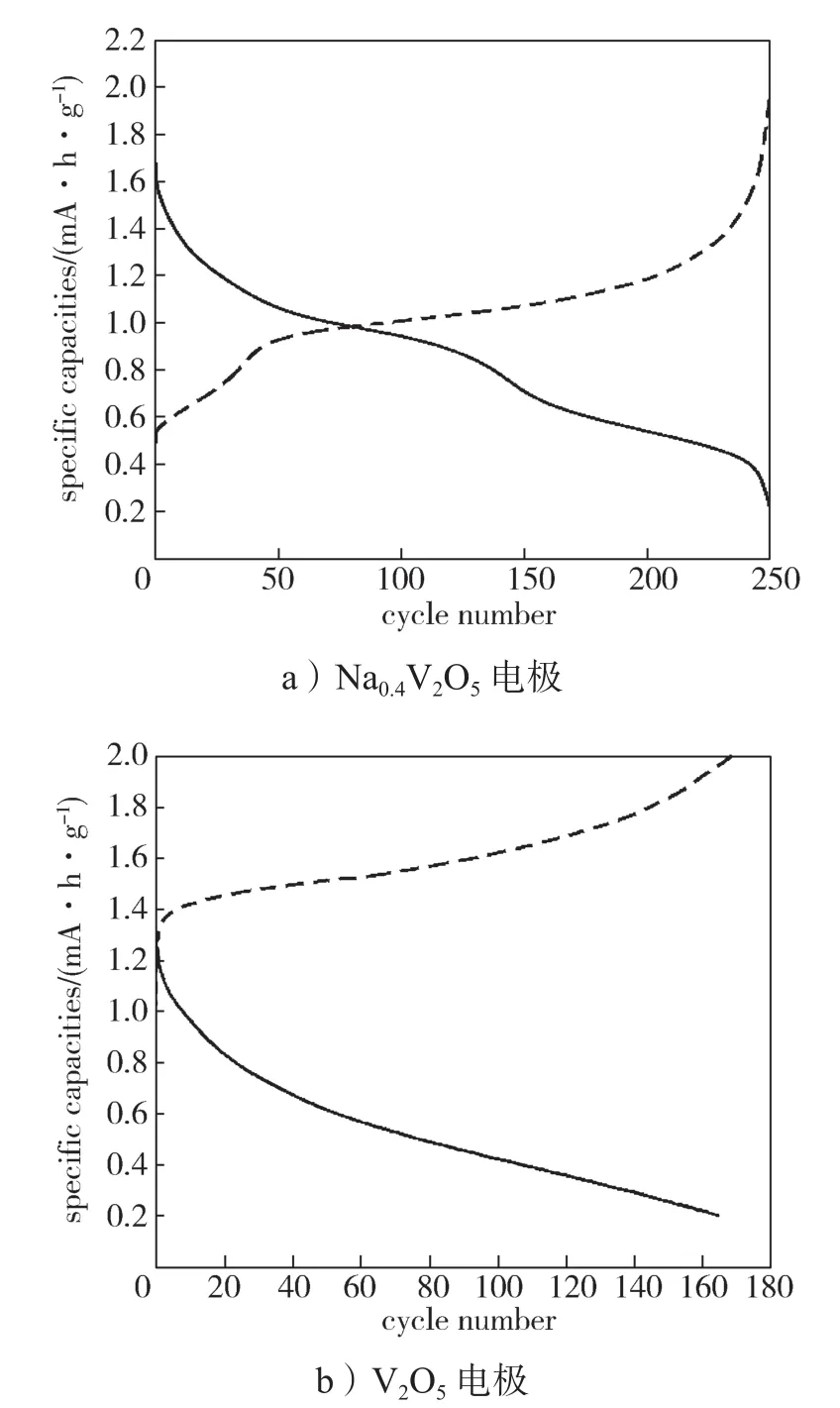
图3 Na0.4V2O5电极和V2O5电极首次充放电曲线Fig. 3 First charge-discharge curves of Na0.4V2O5 and V2O5 electrodes
由图3可知,在首次放电曲线中,Na0.4V2O5电极在1.5~0.8 V处出现斜长放电平台,对应Zn2+嵌入Na0.4V2O5正极材料;在首次充电曲线中,Na0.4V2O5电极的充电平台在0.9~1.4 V处,对应Zn2+脱嵌。充放电曲线中充放电平台电位与CV曲线中氧化还原峰电位的差异是由电极在不同电化学反应条件下极化程度不同引起。V2O5电极的首次充放电容量为168 mA·h/g,Na0.4V2O5电极的首次充放电容量为251 mA·h/g。可见,Na0.4V2O5电极的首次充放电容量更大,且充放电平台间的电压差更小,说明Na+掺杂能有效改善V2O5的晶体结构和储锌能力。
图4为Na0.4V2O5和V2O5电极的倍率性能测试结果。由图4可知,在50, 100, 200, 100, 50 mA/g的电流密度下,V2O5电极的平均放电比容量分别约为124, 81, 30, 15, 43 mA·h/g,Na0.4V2O5电极的平均放电比容量分别为209, 158, 126, 156, 169 mA·h/g。对比可知,Na0.4V2O5电极在各电流密度下的放电比容量均高于V2O5电极,且在大电流密度时依然能保持较高的放电比容量,说明Na+掺杂对V2O5的储锌倍率性能有所改善。Na+掺杂可使V2O5由层状结构转变为隧道结构,有利于提高其结构稳定性;另外,基于阳离子跃迁等机制,Na+掺杂可提高V2O5的电导特性,加快电极材料中的电子转移和离子扩散,有利于提高Na0.4V2O5电极的倍率性能[22-23]。

图4 Na0.4V2O5和V2O5电极的倍率性能Fig. 4 The rate performance of Na0.4V2O5 and V2O5 electrodes
图5为恒流充放电电流密度为100 mA/g,Na0.4V2O5和V2O5电极的循环稳定性测试结果。由图5可知:V2O5电极的首次放电比容量约为280 mA·h/g,由于激活效应,第二、第三次循环可逆容量略微升高。经20个循环后V2O5的可逆放电比容量趋于稳定,经100次循环后的放电比容量为80 mA·h/g,容量保持率为28. 57%。Na0.4V2O5电极的的首次放电比容量约为260 mA·h/g。经100次循环后,Na0.4V2O5电极的放电比容量为125 mA·h/g,容量保持率为48.08%。经对比可知,Na0.4V2O5作为二次锌离子电池正极的循环稳定性更好,这与Na+掺杂提高V2O5结构稳定性有关。

图5 V2O5和Na0.4V2O5电极在电流密度100 mA/g下的循环性能Fig. 5 The cyclic performance of V2O5 and Na0.4V2O5 electrodes at current density of 100 mA/g
图6为Na0.4V2O5正极材料循环前后的EIS分析结果。
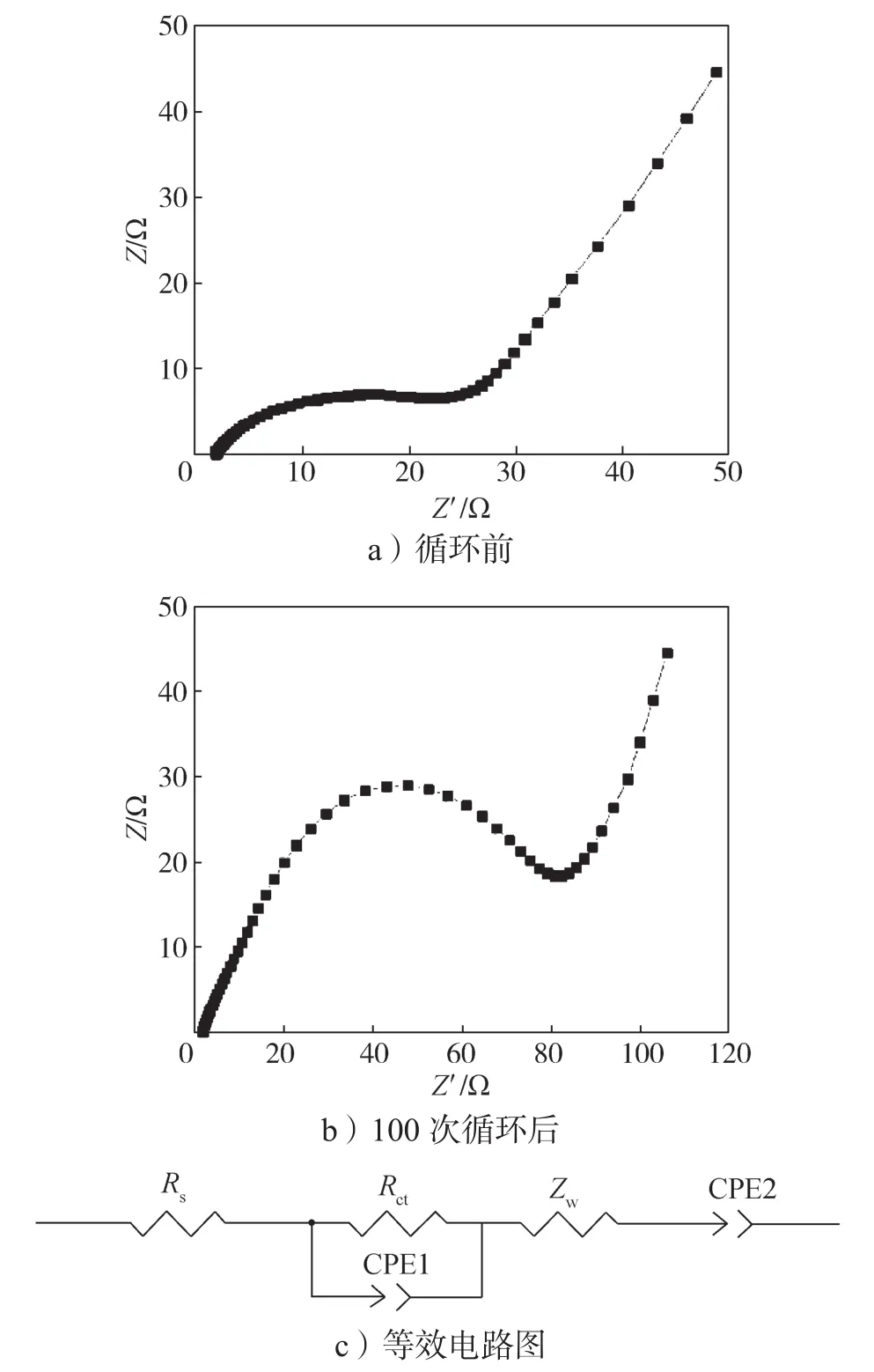
图6 Na0.4V2O5电极循环前后EIS分析Fig. 6 EIS analysis of Na0.4V2O5 electrode before and after cycling
由图6可知,Na0.4V2O5电极循环前后的Nyquist曲线均由一段高频区圆弧和一段低频区斜线构成,高频区圆弧部分与电荷在电极与电解液界面转移有关,低频区斜线与Zn2+在电极内部扩散有关[24]。通过对比高频区可以看出,Na0.4V2O5循环前后电极的电阻变化较小,说明Na0.4V2O5电极在循环过程中能较好地保持结构的稳定性,有助于锌离子快速扩散,因而具有比V2O5电极更好的循环稳定性。在低频区100次循环后的Na0.4V2O5电极与没有经过循环的Na0.4V2O5电极相比,斜率更大,说明经过多次循环,电极活化,离子扩散速率提高。
4 结语
钒基氧化物是最具前景的水系锌离子电池正极材料之一。针对其电子传输慢、离子扩散受阻以及循环性能不够稳定等问题,本文通过一步水热法制备了Na0.4V2O5纳米粉体材料。利用XRD对所制备的粉体材料进行了物相表征,并进行循环伏安、恒流充放电等电化学性能测试。测试结果表明,Na0.4V2O5电极的首次充放电容量为251 mA·h/g,比V2O5电极高,且其电极充放电平台间的电压差更小;不同电流密度下,Na0.4V2O5电极的放电比容量均高于V2O5电极,且在大电流密度时仍能保持较高的放电比容量;经100次循环后,Na0.4V2O5电极的放电比容量为125 mA·h/g,容量保持率为48.08%,其作为二次锌离子电池正极的循环稳定性更好。可见,Na+掺杂能改变V2O5的层状结构,有效改善V2O5的电子传输和离子扩散,从而提高电极电导特性和结构稳定性。

