增氧微咸水灌溉对土壤氮素转化的影响
辛 亮 王文章 范锐锋
(陕西博润检测服务有限公司,陕西 西安 710199)
0 引言
我国拥有丰富的地下微咸水资源,科学合理开发利用地下微咸水资源,对于缓解淡水资源短缺、丰富农业水源、实现作物抗旱增产有着极其重要的作用。但是,直接使用微咸水进行灌溉会造成土壤盐碱 化,使土壤质量恶化,降低作物产量与品质。因此,调控灌溉水质量,提高灌溉水生产效率,更加安全高效地利用微咸水进行灌溉是农业可持续发展的必然要求。将微咸水利用与微纳米增氧技术相结合,可发展安全高效的微咸水灌溉技术,有利于缓解淡水资源紧缺,实现农业节约用水。
氮是植物和微生物生长发育的限制元素。土壤中各形态氮素含量的高低及其变化,不仅深刻影响着作物的产量和品质,更对全球气候环境产生重大影响。因此,开展增氧微咸水灌溉条件下土壤氮素转化的研究十分必要,可以补充利用增氧微咸水灌溉技术提升作物养分利用率的依据。
1 材料与方法
1.1 供试土壤
供试土壤采自陕西省杨凌农业高新技术产业示范区的农田。杨凌处于渭河三级阶地,海拔525 m,多年平均温度为12.9 ℃,年均降水量为550~600 mm。试验土壤属褐土的塿土亚类,土壤质地为粉沙黏壤土,通透性好。采集5~20 cm耕层深度土样,剔除砂砾和植物残根等杂物后充分混合,风干,过孔径 2 mm筛,备用。
1.2 试验设计
1.2.1 试验用水制备。试验处理用水类型包括常规增氧淡水(F)和增氧微咸水(B),其中增氧浓度设置3个梯度(8、15、20 mg/L),矿化度设置2个水平(0、3 g/L),每组3个重复,共计18组试验,具体试验处理见表1。此次试验采用微纳米气泡快速发生装置对水进行增氧处理,增氧过程中利用HQ40型便携式溶氧仪监测水体溶解氧浓度变化。试验前对自来水进行增氧处理,使其溶解氧浓度达到并稳定在 15、20 mg/L,装入容器中密封备用。

表1 试验处理组合
1.2.2 土壤样品培养与采集。试验按照10 g/kg的比例向土壤中加入过孔径0.25 mm筛的玉米芯粉,并加水至土壤含水率为25%,后置于20℃恒温培养箱中,避光培养2周,以提高土壤微生物活性。
试验前向培养好的土壤均匀喷洒硫酸铵溶液,使土壤中氮含量为0.1 mg/kg。试验时将预处理土壤按34 g/瓶装入50 mL蓝盖瓶中,并加入6.4 mL提前制备好的微纳米增氧水,使土壤含水率达到25%,记录加水时间,置于20 ℃恒温培养箱中避光培养。培养过程中于第0、1、2、3、4、6、8、10天进行破坏性取样,取样完成后立即将样品放入液氮中速冻,随后放入-80 ℃冰箱中保存,待全部样品取完后统一进行无机氮测定。另外,采用烘干法记录各时段土壤的水分变化情况。此次试验利用AA3型连续流动分析仪测定各土壤样品的无机氮含量。
1.3 数据处理与分析
此次试验利用Excel 2016、Origin 2021软件进行数据处理及绘图。
2 结果与分析
2.1 增氧微咸水添加对土壤无机氮浓度的影响
由图1(a)可知,土壤中铵态氮浓度从第0天到第6天由60~70 mg/kg逐渐降低至8~10 mg/kg;第6天直到试验结束,土壤中铵态氮浓度一直处于8~10 mg/kg的稳定水平。整体上来看,不同处理的土壤铵态氮含量均呈现先下降后稳定的趋势,这是由于硝化作用使得土壤中的铵态氮持续被消耗。另外,不同处理对铵态氮消耗的影响无显著差异。
由图1(b)可知,各处理土壤中亚硝态氮浓度在第0天至第3天无显著差异,第4天开始出现显著差异且均在第4天达到最大亚硝态氮浓度,其中F、F、F、B、B、B分别为2.94、3.99、3.85、4.12、4.75、 4.67 mg/kg,呈现出B≈B>B≈F≈F≈F的规律;F、B在第6天率先降至极低值,其他处理均在第8天降至极低值。
由图1(c)可知,各处理土壤中硝态氮浓度均呈现先升后降趋势;各处理间硝态氮含量在第4天开始出现显著差异。F、F、B、B均在第4天达到最大硝态氮浓度,分别为5.84、5.96、4.71、5.20 mg/kg,呈现F≈F>B>B的规律;F、B于第6天达到最大硝态氮浓度,分别为5.89、5.81 mg/kg;第8天F、F的硝态氮浓度率先降至最低值,而其他处理在第10天降至此水平。

图1 土壤各形态无机氮素含量变化
2.2 增氧微咸水添加对土壤氮素转化速率的影响
图2为土壤中各形态无机氮素平均转化速率随时间的变化情况。由图2(a)可知,各处理土壤中铵态氮消耗速率呈先增后减趋势,且均在第3天左右达到最大消耗速率,F、F、F、B、B、B的最大平均消耗速率分别为0.70、0.71、0.79、0.66、0.80、 0.68 mg/(kg·h),呈 现 出F≈B>F>F≈ B>B的规律。图2(b)、(c)为硝态氮和亚硝态氮生成速率的变化情况,二者的变化规律较为一致,呈现出生成速率存在正负2个峰的“反S”型曲线。第0天至第5天,即生成速率为正的时期,被称为生成阶段;第5天至第10天其速率为负数,被称为消耗阶段。由图2(b)可知,就未增氧的处理F、B而言,二者的趋势较为平缓,其中B亚硝态氮的生成速率峰值高于F;其他处理的峰值均高于F、B。需要注意的是,在消耗阶段,F、F亚硝态氮的生成速率较其他处理提前2 d升至0。由图2(c)可知,在生成阶段,F、B、B、B在第3天硝态氮生成速率达到最大,分别为0.055、0.046、0.054、0.057 mg/(kg·h),表现为F≈B≈B>B;F、F在第4天硝态氮生成速率达到最大,分别为0.068、0.072 mg/(kg·h)。
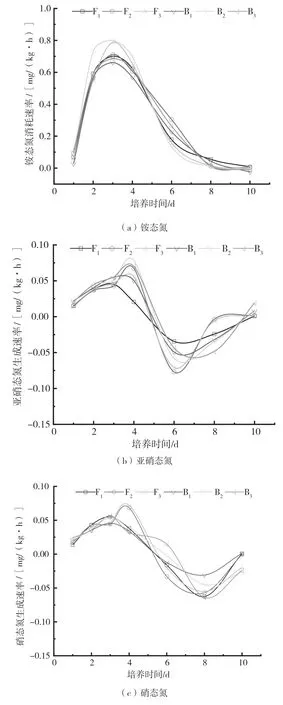
图2 土壤中各形态无机氮素转化速率变化
3 结论
①增氧淡水和增氧微咸水添加对土壤中铵态氮的转化过程无显著影响,对土壤中亚硝态氮和硝态氮的累积有一定的促进作用;②从无机氮转化速率来看,对淡水和微咸水进行增氧处理都能提高土壤中无机氮的转化速率。
4 讨论
该试验中土壤铵态氮最大消耗速率呈现出F≈B>F>F≈B>B的规律,说明不论是微咸水还是淡水,增氧处理都能显著提高土壤中铵态氮的转化速率,且在淡水中表现为增氧浓度越大,效果越明显。增氧微咸水和增氧淡水均能促进土壤亚硝态氮和硝态氮转化,这种促进效果与水中较高的氧气浓度有直接关系。较高的氧气浓度为好氧微生物提供了适宜的环境,影响了微生物的生理活性,从而促进了土壤中无机氮的转化。
虽然在该研究中增氧处理均产生了显著影响,但是试验中设计的氧气梯度和矿化梯度未能在土壤铵态氮消耗上表现出较好的规律,其原因可能有以下两方面:①增氧水添加到土壤中后,水中的溶解氧会发生逸散,而且可能氧气浓度越高,逸散现象越明显; ②矿化度梯度设置太少,3 g/L的矿化度可能仍然在微生物的耐受范围内。

