Bi2O3/Bi2S3二元异质结光催化剂的合成与制备
马 玲
(齐齐哈尔大学 化学与化学工程学院,黑龙江 齐齐哈尔 161006)
能源短缺和环境污染是当今人们所关心的两个问题。半导体光催化是一种理想的“绿色”技术[1],有望解决这两个问题。多年来,研究人员一直在寻找高效的光催化剂。目前已经发现了许多光催化剂,如TiO2[2,3]、CeO2[4,5]、BiOX(X=Br,Cl,I)[6,7]、BiPO4[8,9]和ZnO[10,11]。这些光催化剂具有效率高、危害低[12]、价格低等优点,在光催化领域应用广泛。
硫化铋是一种环境友好并且不会产生严重污染物的材料,在制备其他铋合物、易切削钢添加剂、 微电子工业[13]等领域都有应用,并且硫化铋具有毒性小、价格便宜、稳定性比好等特点,引起研究者的广泛关注。但是,由于硫化铋半导体在可见光的作用下有严重的光致腐蚀,并且电荷复合率较高,使其在光催化降解污染物方面有着较弱的性能。因此,寻找更加先进有效的方法对其进行修饰改性,以提高催化剂对复杂有机污染物的可见光催化降解效果就显得尤为迫切。
氧化铋作为一种金属半导体催化剂,其带隙为2.8eV,具有很多优异的特性,如具有良好的可见光响应能力,对环境也非常友好。因此,氧化铋是非常具有前景的可见光催化降解有机污染物的催化材料。然而纯氧化铋光量子效率比较低,电子-空穴对复合率比较快,载流子寿命短,因此它在光催化领域的应用具有一定的局限性。这些年来研究者们做了大量的努力去提高纯氧化铋的光催化活性。Dai[14]等人将碳元素引入到氧化铋的晶格中,经过碳的掺杂,氧化铋在可见光区域的光吸收范围有了明显的拓宽,增强了氧化铋对污染物的降解能力。Liu[15]等人报道了采用Er3+掺杂的具有选择性暴露活性晶面的β-Bi2O3单晶纳米片,该多孔的β-Bi2O3表现出增强的光活性。这是因为当掺杂适量的Er3+时,材料可以将长波光有效地转化为短波光,或者可以通过捕获低能光子产生具有更高能量的激发电子,从而增强光催化活性。然而,目前关于Bi2O3和Bi2S3复合催化剂的研究鲜见报道,所以利用Bi2O3和Bi2S3的特殊性能构建复合光催化剂仍然是个艰巨的任务。
1 实验部分
1.1 仪器与试剂
Spectrum One B傅里叶变换红外光谱仪(美国PE公司);D8 FOCUS X-射线衍射仪(德国布鲁克AXS公司);ESCALAB 250Xi X-射线光电子能谱仪(美国Thermo公司);S-4300扫描电子显微镜(日本日立公司);H-7650透射电子显微镜(日本日立公司);Navo Win2全自动气体吸附分析仪(美国康塔仪器公司);KQ-B玻璃仪器气流烘干器(巩义市予华仪器有限责任公司);80-1离心沉淀机(巩义市予华仪器有限责任公司);BL-GHX-V光化学反应仪(上海比朗仪器公司);FA1604电子分析天平(上海天平仪器厂);TU-1900双光束紫外可见分光光度计(北京普析通用仪器有限责任公司);KQ-700B超声波清洗器(昆山市超声仪器有限公司);SX2-8-10箱式电阻炉(天津市泰斯特仪器有限公司);电热恒温鼓风干燥箱(天津市泰斯特仪器有限公司)。
硝酸铋(天津凯通化学试剂有限公司);无水乙醇(天津福晨化学试剂厂);硫脲(天津凯通化学试剂有限公司);盐酸(天津凯通化学试剂有限公司);氢氧化钠(天津凯通化学试剂有限公司);聚乙二醇(天津凯通化学试剂有限公司);左氧氟沙星(天津凯通化学试剂有限公司);尿素(天津凯通化学试剂有限公司);亚甲基蓝(沈阳化工厂);罗丹明B(天津凯通化学试剂有限公司)。
1.2 纳米Bi2O3的制备
将0.428 0 g硝酸铋和0.184 4 g尿素装入烧杯中,加入32 mL聚乙二醇,在磁力搅拌器上搅拌20 min,将溶液转入不锈钢型聚四氟乙烯反应釜中,在160 ℃的烘箱中保存12 h。得到的产物进行离心,分离出固体,并用去离子水和乙醇洗涤固体三次。然后,在80 ℃烘箱中干燥4 h,得到Bi2O3。
1.3 纳米Bi2S3的制备
称量1.704 g硝酸铋、3.050 g硫脲和32 mL去离子水倒入烧杯中,搅拌15 min,将白色溶液转入不锈钢型聚四氟乙烯反应釜中,在160 ℃的烘箱中保存12 h,反应结束后冷却至室温。得到的产物进行离心,分离出固体,并用去离子水和乙醇洗涤固体三次。在80 ℃烘箱中干燥4 h,得到Bi2S3。
1.4 复合物 Bi2O3/Bi2S3的制备
将0.400 6 g氧化铋和0.106 5 g硫脲装入烧杯中,加入32 mL聚乙二醇,在磁力搅拌器上搅拌10 min,将溶液转入不锈钢型聚四氟乙烯反应釜中,在160 ℃的烘箱中保存6 h,反应结束后放置室温冷却,得到的产物离心分离得固体,并用去离子水和乙醇洗涤三次。然后,在80 ℃烘箱中干燥4 h,记为复合物 Bi2O3/Bi2S34∶1。用同样的方法制备不同比例的复合物,分别记为Bi2O3/Bi2S33∶1;Bi2O3/Bi2S31∶1。
1.5 光催化活性评价
用染料模拟废水,来检测催化剂的催化活性。选用500 W紫外灯作为模拟可见光源,光谱发射范围在10~380 nm。在光催化反应之前,通过改变不同的实验变量,检测光催化剂的活性,即染料的降解残留率(C/C0),残留率越高则说明催化剂的光催化活性越低。当实验变量为催化剂的用量时,依次量取10 mg、20 mg、30 mg、40 mg、50 mg的光催化剂分别放入五个装有50 mL最佳降解浓度的染料溶液中进行试验;当实验变量是染料溶液的pH值时,在五个光催化管中分别称量出最佳降解浓度的50 mL 染料溶液,调节pH值分别为3、5、7、9、11,并称量最佳用量的催化剂放入光催化管中进行试验。
2 结果与讨论
2.1 表征
2.1.1 XRD分析
图1中,2θ为26.7°、27.8°、29.3°和33.4°出现的衍射峰分别对应Bi2S3(148)、(151)、(137)、(149)晶面。在复合物的X射线衍射图中可以观察到存在Bi2S3特征峰,表明该复合物成功复合。但相比于单体Bi2S3来说,复合物特征峰有拓宽现象,可能是由于洗涤过程没有洗干净造成的。
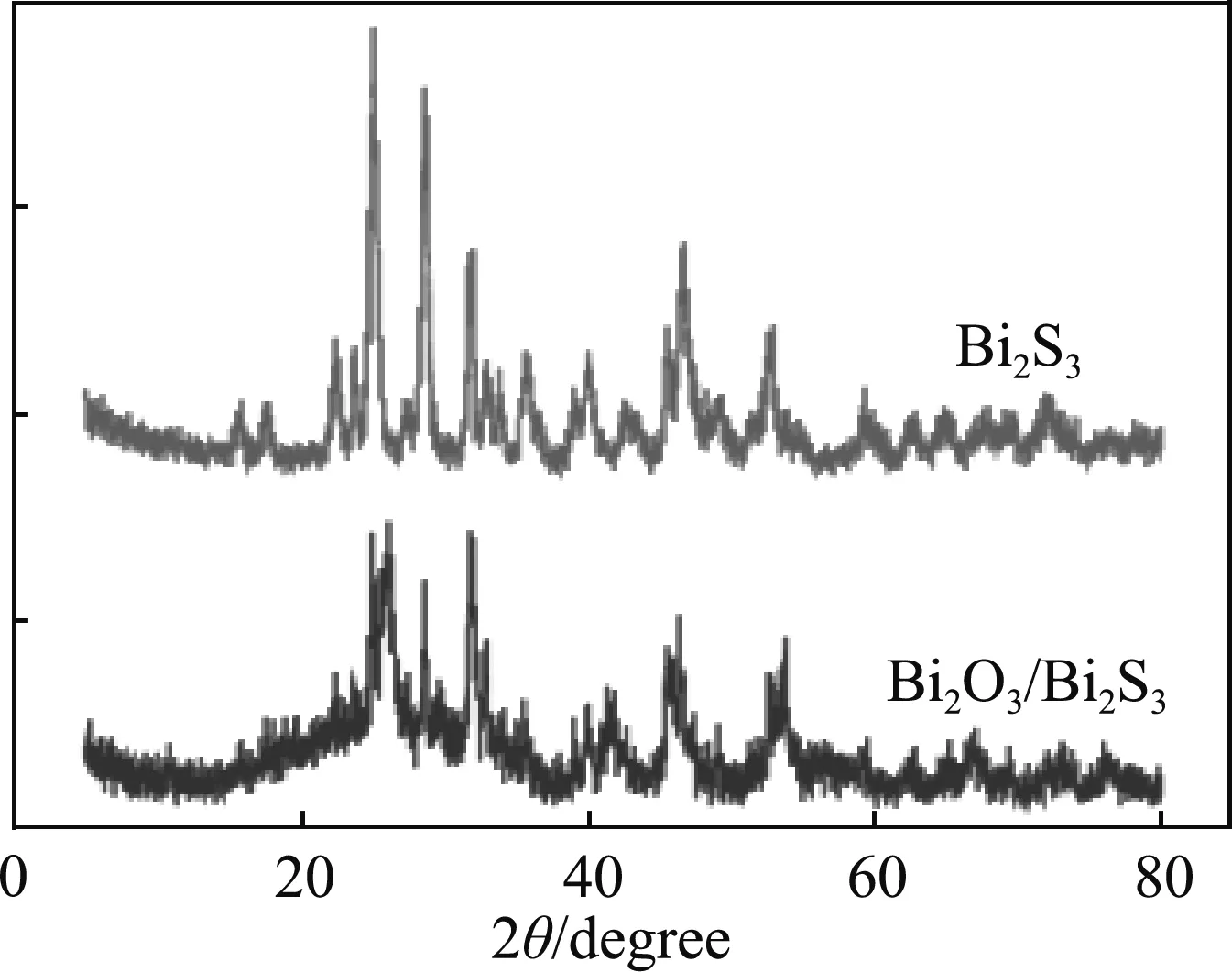
图1 Bi2O3/Bi2S3、Bi2S3X射线衍射分析
2.1.2 红外光谱分析
图2为Bi2O3/Bi2S3复合物与Bi2O3的红外光谱图。在图中Bi2O3在3 433.53 cm-1处有明显的宽峰,在1 606.74 cm-1有较明显的吸收峰,这两处峰是Bi2O3产生的-OH伸缩振动和弯曲振动。1 390.79 cm-1处为Bi2O3的特征吸收峰,该峰足以证明此物质是Bi2O3。Bi2O3/Bi2S3在3 430.44 cm-1处有较强的吸收峰,是-OH 伸缩振动产生的吸收峰。在2 915.83 cm-1处有较强的吸收峰,由于在半导体复合时有部分有机成分的残留,推测此峰可能是C-H 的伸缩振动产生的,1 627.70 cm-1处的吸收峰是-OH弯曲振动产生的。在1 107.75 cm-1处是硫的特征峰,所以我们可以认为此复合物是Bi2O3/Bi2S3复合物。
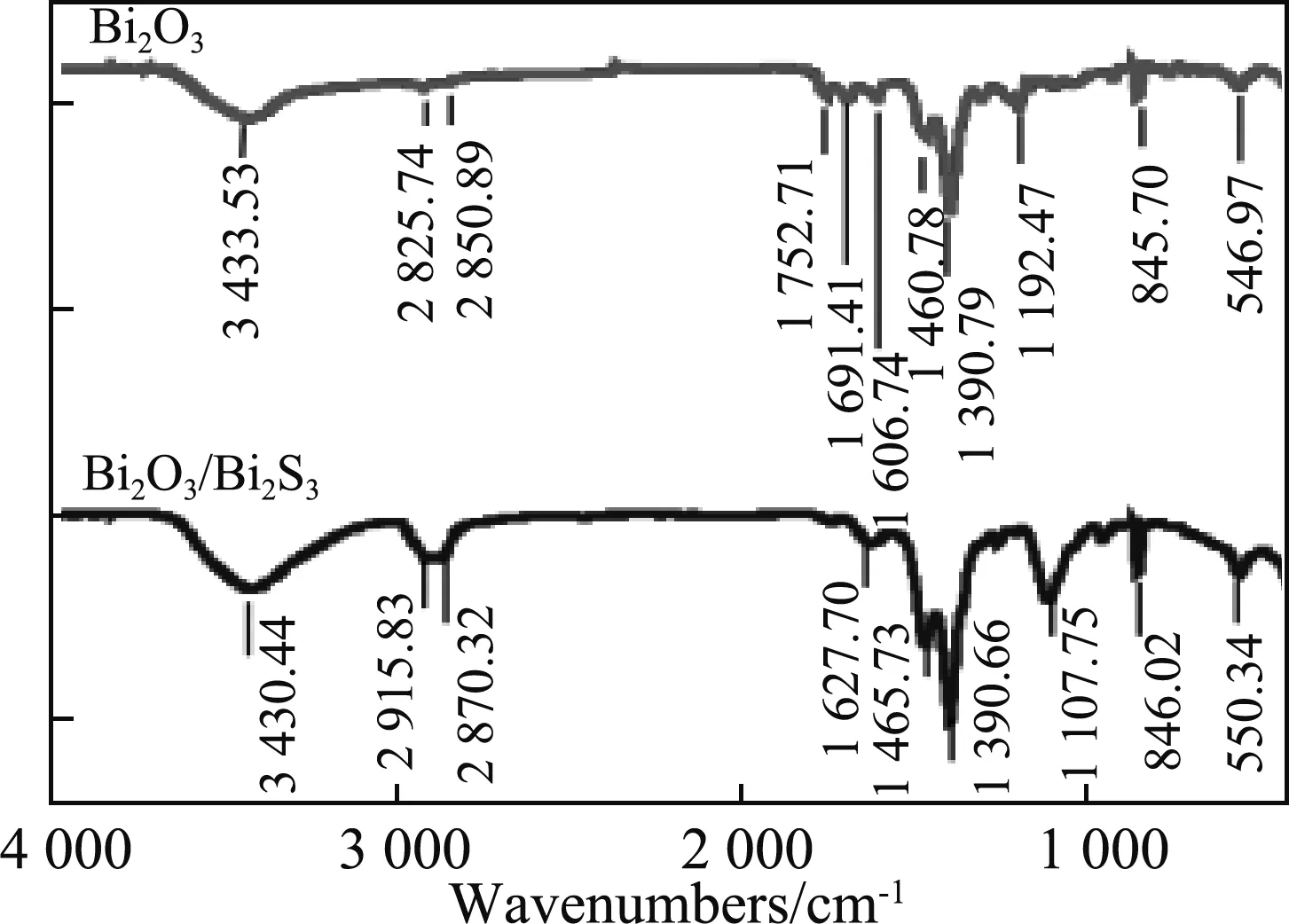
图2 Bi2O3/Bi2S3及Bi2O3红外光谱图
2.1.3 SEM分析
对复合光催化剂进行了扫描电镜分析(图3)。在图3中可以观察到复合物是一种片状晶体结构。不同于单体存在时的密集聚集状态,复合物成均匀分散状态。这种结构可以增强复合催化剂的光捕获能力,增大比表面积,从而增强催化剂的光催化能力以及对染料的降解效率。

图3 Bi2O3/Bi2S3复合物扫描电镜图
2.2 Bi2O3/Bi2S3对染料催化降解研究
2.2.1 Bi2O3/Bi2S3复合物配比的影响
为了找到实验所需的复合物的最佳比例,本实验对氧化铋与硫脲的不同配比进行了研究。为了精确检测复合物配比对光催化活性影响的实验研究结果,将催化剂的用量、染料浓度以及染料溶液的pH值统一控制,光催化降解染料实验结果如图4所示。从图4中可以观察到复合物Bi2O3/Bi2S34∶1的催化效果最好,其相对于单体的催化效果有明显的提高。
2.2.2 Bi2O3/Bi2S3复合物用量的影响
为了能够有效地测量降解效果与单一变量的关系,在开始实验前控制染料溶液的浓度及pH值,分别用10 mg、20 mg、30 mg、40 mg、50 mg的催化剂进行光催化实验,结果如图5所示。
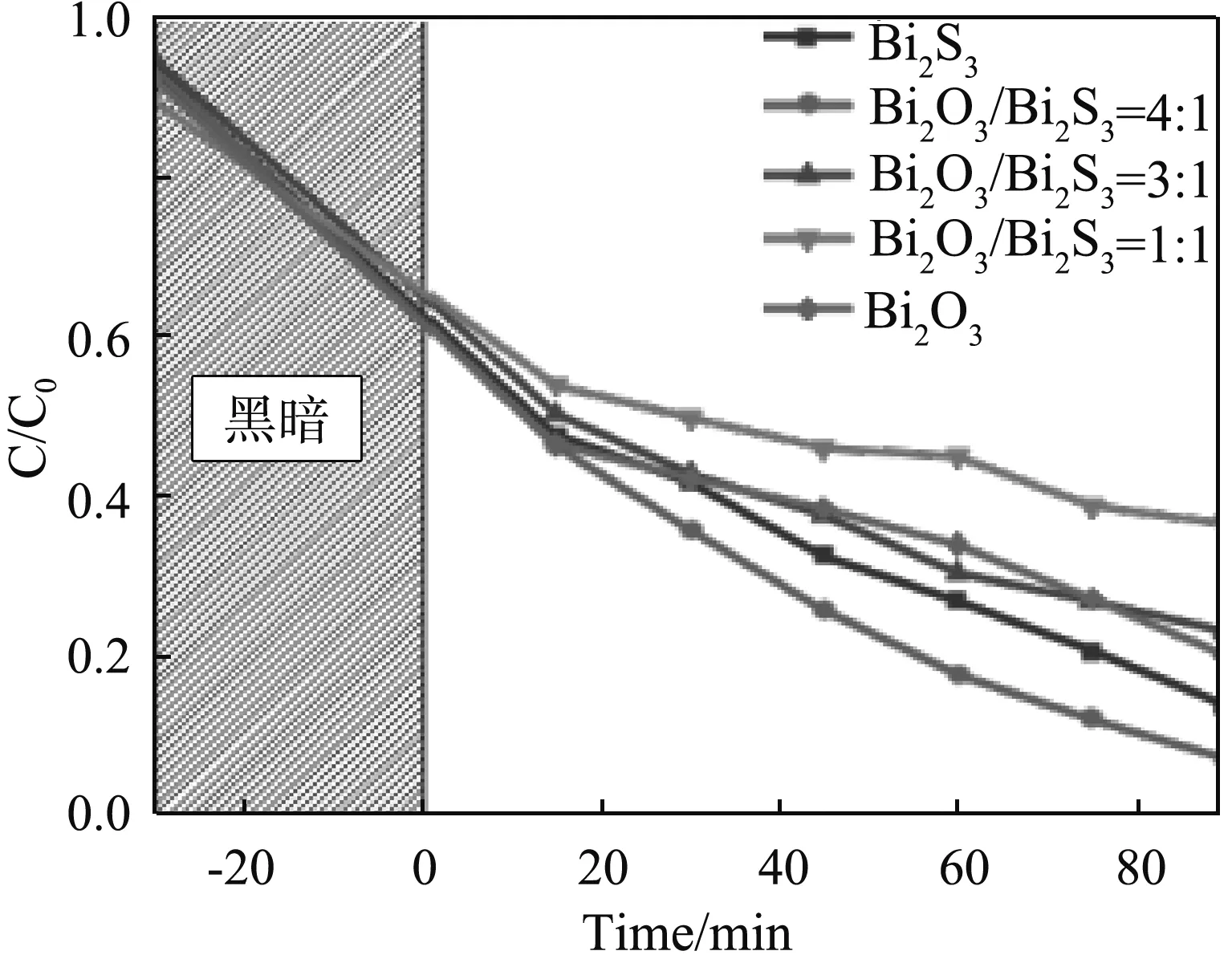
图4 不同配比 Bi2O3/Bi2S3的选择
在图5中可以观察到,当催化剂的用量为10 mg时,染料在90 min内降解率高达96%,而随着催化剂用量的不断增加,对染料的降解能力逐渐降低,可能是因为过量的催化剂不能够很好地利用光源发出的光,阻碍了对光的吸收,从而导致光催化活性的降低。
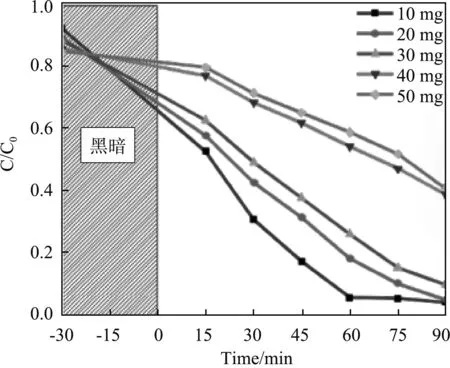
图5 Bi2O3/Bi2S3的用量对染料的影响
2.2.3 染料的pH值的影响
控制染料浓度为100 mg/L,催化剂用量为10 mg,将染料溶液的pH值调整为3、5、7、9、11进行实验,结果如图6。
由图6可以看出当染料溶液pH=3时,在 90 min内,染料的降解率高达95%,并且随着pH值的增加,降解率逐渐降低,主要是因为高pH值抑制了氧生成羟基自由基的副反应,抑制了染料的降解。
通过以上实验可以得出,当催化剂的用量为10 mg、染料的浓度为100 mg/L,pH值为3时,催化剂的光催化活性最好。在图7中观察到随着降解时间的增加,对应的染料降解率逐渐增大,75 min以后降解完全。
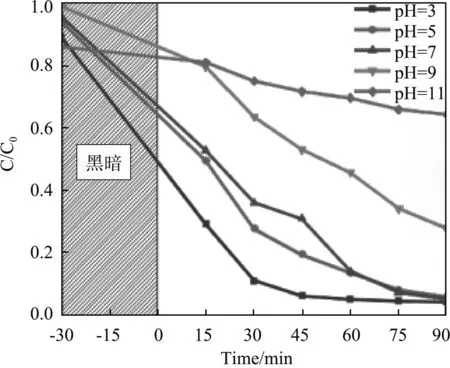
图6 染料pH值对光催化活性的影响
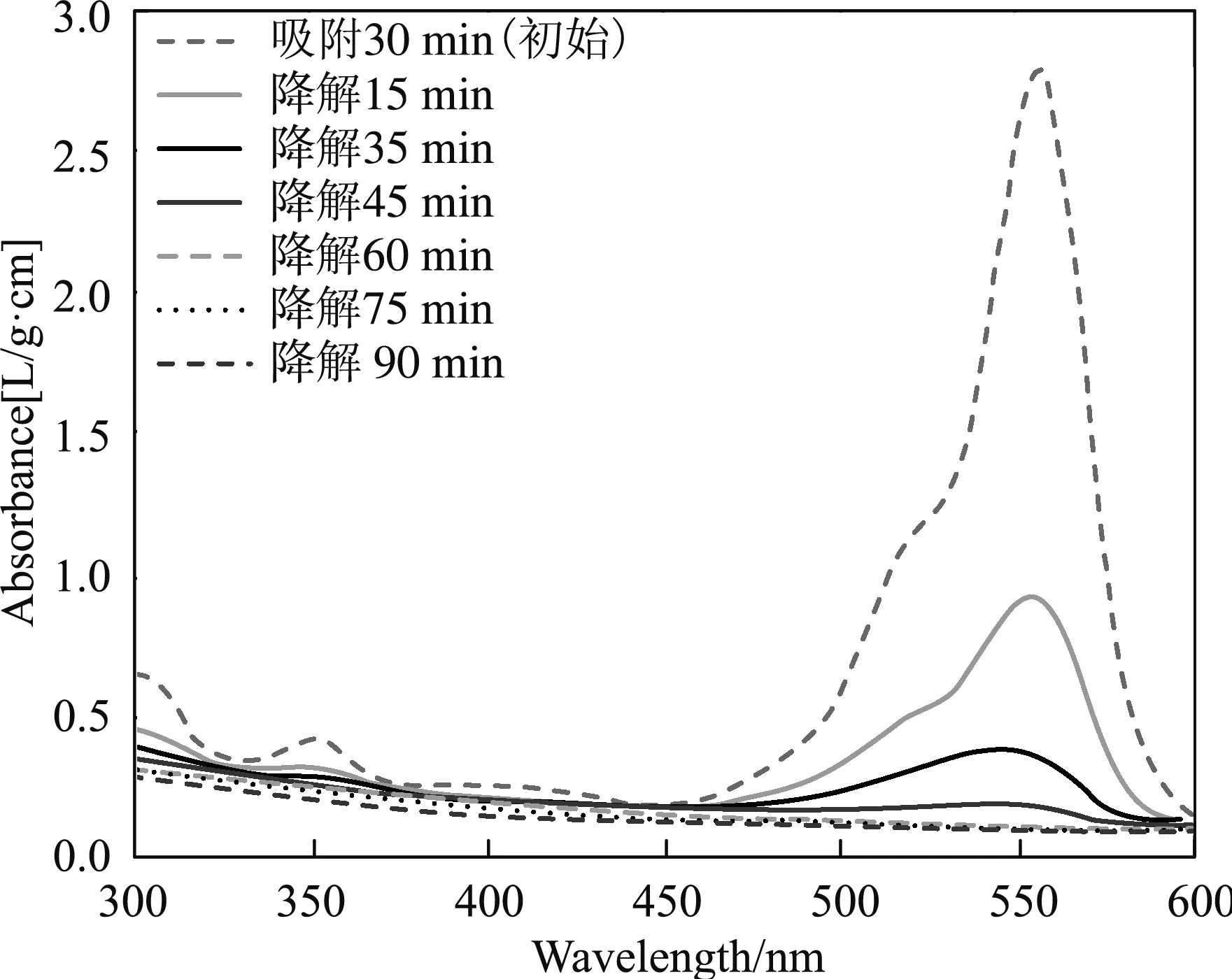
图7 催化剂降解染料最佳条件
3 结论
本实验通过水热法制备Bi2O3、Bi3S3及Bi2O3/Bi3S3复合物,并且对Bi2O3、Bi3S3不同配比的复合物光催化染料降解的活性进行对比,择优进行下一步的光催化降解实验。
采用X射线衍射(XRD)、红外光谱图(IR)以及扫描电镜图(SEM)对制备出的单体及复合物进行了表征。针对染料溶液的pH值以及催化剂的用量、配比三个因素进行光催化降解实验。在催化剂对染料进行降解,当染料溶液pH值为3、催化剂用量为10 mg、Bi2O3/Bi3S3配比为4∶1时,降解效果最好,最大降解率可达96%,表明在解决实际废水处理问题时,此催化剂具有一定的应用价值。

