熟地黄配方颗粒和标准汤剂中地黄苷D的含量测定
★ 徐雄飞 王海燕 何清(江西百神药业股份有限公司 江西 宜春 336000)
地黄来源于玄参科植物地黄Rehmannm glutinosaLibosch.的块根,生地黄具有清热凉血、养阴生津的功效,熟地黄则具有够滋阴补血、益精填髓功效。熟地黄配方颗粒由地黄经蒸制、干燥、水煎煮、浓缩干燥、制粒等过程制备而成,而其有效成分之一毛蕊花糖苷经炮制、煎煮易损失,不能很好的体现熟地黄配方颗粒的质量。药理学试验表明地黄苷D具有滋阴、补血及降血糖活性,其药效作用与中医临床传统用药相符合。根据2020版药典熟地黄饮片选择地黄苷D作为熟地黄配方颗粒的含量测定指标,体现中医临床功效和中药传统炮制特色,更好的控制熟地黄配方颗粒的质量。本实验通过对熟地黄标准汤剂和配方颗粒的地黄苷D的含量进行研究,经方法学考察和样品的测定,表明方法可靠,可以用于熟地黄配方颗粒的质量控制。
1 仪器与试药
1.1 仪器
H-Class超高效液相色谱仪(美国Waters公司);XSE205Du电子分析天平(梅特勒托利多公司);KQ400DE数控超声波清洗器(昆山市超声仪器有限公司);LGJ-10型真空冷冻干燥机(北京松源华兴科技发展有限公司);ZLG-10型喷雾干燥机(常州一步干燥设备有限公司)。
1.2 试药
地黄苷D对照品(批号7433,纯度100%,上海诗丹德);地黄配方颗粒(批号20190701,江西百神药业股份有限公司);甲醇(色谱纯,美国天地有限公司);磷酸(分析纯,西陇科学股份有限公司);水为超纯水。
2 实验方法与结果
2.1 色谱条件
色 谱 柱:ACQUITY UPLC BEH C18(2.1 mm×100 mm,1.7 μm);流动相:甲醇-0.1%磷酸溶液(5∶95);流速:0.2 mL/min;柱温:20 ℃;检测波长:203 nm。理论板数按地黄苷D峰计算应不低于5 000。
2.2 溶液的制备
对照品溶液的制备:取地黄苷D对照品适量,精密称定,加流动相制成每1 mL含70 μg的溶液,即得。
供试品溶液的制备:取装量差异项下的本品,混匀,取适量,研细,取约1 g,精密称定,置具塞锥形瓶中,精密加流动相25 mL,称定重量,超声处理(功率250 W,频率40 kHz)30 min,放冷,再称定重量,用流动相补足减失的重量,摇匀,滤过,即得。
2.3 标准汤剂制备
称取熟地黄150 g,煎煮2次,第1次加水9倍量,浸泡30 min,煎煮60 min,滤过,滤液备用;第2次加水7倍量,煎煮40 min,滤过,合并两次滤液,混匀;减压浓缩至饮片投料量:浓缩液体积约为1∶2(g∶mL)的浸膏,冷冻干燥,即得。
2.4 方法学考察
2.4.1 系统适用性与专属性试验分别精密吸取对照品溶液、供试品溶液、阴性样品溶液各2 μL,注入超高效液相色谱仪,按“2.1”项下色谱条件进样测定,如图1。结果显示,供试品溶液中地黄苷D和相邻色谱峰分离度为1.94;且阴性样品在与对照品溶液色谱峰相应的保留时间无色谱峰,不受辅料、溶剂等因素的干扰,表明该方法专属性良好。

图1 熟地黄配方颗粒含量专属性试验
2.4.2 线性关系考察取地黄苷D对照品适量,精密称定,加25%甲醇制成每l mL含350 μg的溶液,摇匀。分别精密量取1.0,2.0,4.0,6.0,10,30 mL置于50 mL棕色瓶中,用流动相稀释至刻度,摇匀,制成浓度分别7.0,14.0,28.0,42.0,70.0,210 μg/mL的标准溶液,分别精密量取上述溶液2 μL注入液相色谱仪;以其峰面积为纵坐标(Y),进样量为横坐标(X),得线性回归方程Y=477 220X-1 350.2(r=0.999 9),结果表明地黄苷D在0.014 3~0.717 μg范围内线性关系良好。
2.4.3 精密度试验取本品(批号20190701)约1 g,精密称定,按“2.2”项制备供试品溶液,精密吸取2 μL,按2.2项下色谱条件测定峰面积,连续进样6次,结果地黄苷D峰面积的RSD为0.96%,表明本方法精密度良好。
2.4.4 稳定性试验取本品(批号20190701),研细,取约1 g,精密称定,按“2.2”项制备供试品溶液,分别在制备后放置0,2,4,8,12,24 h进样测定,结果地黄苷D峰面积的RSD为1.30%(n=6),供试品溶液在24 h内稳定性良好。
2.4.5 重现性试验取本品(批号20190701),研细,取约1 g(共6份),精密称定,按“2.2”项制备供试品溶液,精密吸取2 μL,按“2.1项色谱条件测定峰面积,平均含量为1.18 mg/g,RSD=0.98%,表明本法重现性良好。
2.4.6 准确度试验精密称取地黄苷D(批号7433,纯度100%)11.66 mg,置20 mL量瓶中,加适量25%甲醇超声处理使溶解,取出,放冷,加25%甲醇稀释至刻度,摇匀,得浓度为0.583 mg/mL地黄苷D对照品贮备溶液。分别精密量取1 mL(共6份),置锥形瓶中,蒸干。取本品(批号20190701),研细,取约0.5 g(共6份),精密称定,分置上述具塞锥形瓶中,分别精密加流动相25 mL,称定重量,超声处理(功率250 W,频率40 kHz)30 min,放冷,再称定重量,用地黄苷D补足减失的重量,摇匀,滤过,精密吸取续滤液2 μL,注入液相色谱仪,测定,即得。结果见表1,地黄配方颗粒(批号20190701)中地黄苷D的含量为1.176 mg/g。结果,地黄苷D平均回收率为98.70%,RSD为1.65%,表明本方法准确度较好。
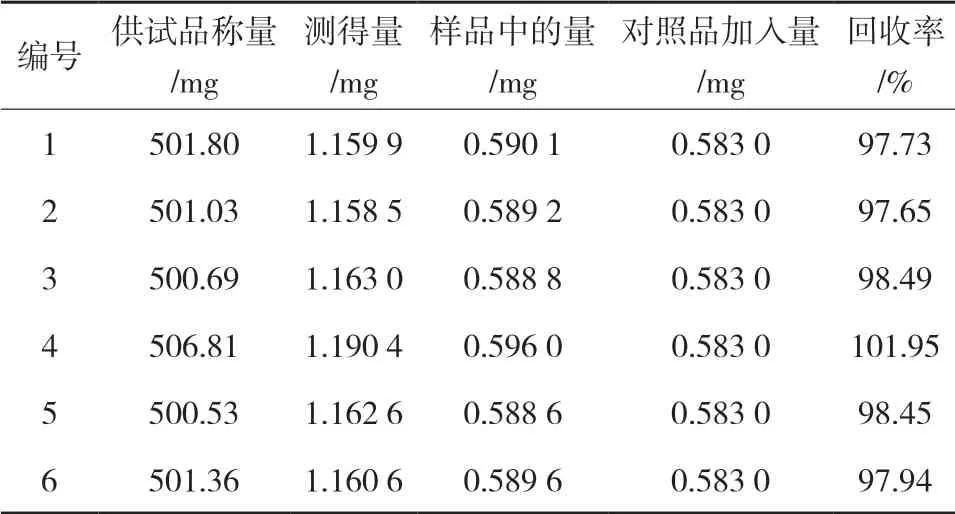
表1 地黄苷D准确度试验结果(n=6)
2.5 样品含量测定
取3批不同批号的样品适量,研细,取约1 g,精密称定,按“2.2”项制备供试品溶液,精密吸取2 μL,按“2.1”项色谱条件测定3批熟地黄配方颗粒样品中地黄苷D的含量,结果见表2。

表2 3批熟地黄配方颗粒中地黄苷D含量测定结果 mg/g
2.6 标准汤剂含量及转移率
取3批不同的熟地黄饮片(批号20190601P、20191201P、20200101P)按照2020版《中国药典》一部熟地黄饮片含量测定项下方法分别测定地黄苷D含量。取以上3批饮片按“2.3”项下方法制备标准汤剂样品,分别得到干膏粉99.24,98.60,107.26 g。取上述标准汤剂干膏粉约1g,精密称定,按“2.2”项制备供试品溶液,精密吸取2 μL,按“2.1”项色谱条件测定3批标准汤剂中地黄苷D的含量并计算转移率,结果见表3。通过3批标准汤剂含量转移实验,表明地黄苷D经煎煮可从饮片转移到配方颗粒中,且转移率达到80%,表明饮片和配方颗粒的地黄苷D的含量可以保持质量一致性。

表3 3批熟地黄饮片和标准汤剂地黄苷D含量及物质转移测定结果
2.7 喷雾干燥对含量及转移率的影响
取3批不同的熟地黄饮片(批号20190601P、20191201P、20200101P)各15 kg,按“2.3”项方法制备浓缩液至相对密度1.08~1.10(60℃)的浸膏,采用喷雾干燥进行干燥。喷雾干燥参数为:进风温度165~170 ℃,雾化器转速100 Hz;进液物料温度:70~75 ℃;进液速度:30 r/min;出风温度:70~75 ℃。分别得到干膏粉10.29,10.53,10.83 kg,取上述干膏粉约1 g,精密称定,按“2.2”项制备供试品溶液,精密吸取2 μL,按“2.1”项下色谱条件测定峰面积,测定3批标准汤剂中地黄苷的含量转移数据,结果见表4。通过3批喷雾干燥含量转移实验,表明喷雾干燥对地黄苷D含量基本无影响,表明采用喷雾干燥和标准汤剂的地黄苷D的含量可以保持质量一致性。

表4 3批喷雾干燥熟地黄干膏粉地黄苷D含量及物质转移测定结果
3 讨论
在样品提取条件的筛选试验中,分别采用本方法流动相、20%甲醇、50%甲醇、纯甲醇超声提取,结果表明采用本实验流动相的结果最高,20%甲醇、50%甲醇的结果稍低,并且用流动相做溶剂可避免效应,故采用流动相制备供试品溶液。同时还考察了加热回流提取和超声提取2种方法的效果,结果显示,2种提取方法含量结果相近,超声提取更简便,故最终选择超声提取。以甲醇-0.1%磷酸溶液(5∶95)作为提取溶剂时,考察了超声提取15,30,45 min对提取率的影响,结果超声提取30 min时,地黄苷D基本提取完全,故选择超声提取30 min处理供试品。
因喷雾干燥具有干燥速度快、物料受热时间短、生产工序简单、操作简便、可控性好、产品质地均匀、溶解性好等特点。因此按标准汤剂的加水量、煎煮时间、煎煮次数进行提取浓缩,浸膏干燥由冷冻干燥改为喷雾干燥进行试验比较,考察喷雾干燥工艺对地黄苷D的影响。结果喷雾干燥的平均出膏率为70.1%,与平均含量转移率89.7%基本一致,表明地黄苷D对热比较稳定,喷雾干燥的过程对地黄苷D含量基本无影响,熟地黄配方颗粒与标准汤剂具有一致性且质量稳定可控。放大生产后含量转移率和出膏率有所提高,主要是一煎的出膏率和含量有所提高,因为批量加大投料后煮沸所需时间增加了约15 min。按照每1 g配方颗粒相当于饮片1.3 g,结合标准汤剂中平均含量转移率与平均出膏率计算,暂定本品按每1 g含地黄苷D(C27H42O20)应为不低于0.55 mg。

