基于羧甲基壳聚糖-氧化透明质酸自组装行为构建的pH响应型纳米乳水凝胶给药系统
汤小涵,王 哲,闫 巧,秦祉剑,袁海龙*
基于羧甲基壳聚糖-氧化透明质酸自组装行为构建的pH响应型纳米乳水凝胶给药系统
汤小涵1, 2,王 哲2,闫 巧2,秦祉剑1,袁海龙1, 2*
1. 安徽医科大学药学院,安徽 合肥 230032 2. 空军特色医学中心 药学部,北京 100142
基于羧甲基壳聚糖(carboxymethyl chitosan,CMC)-氧化透明质酸(oxidized hyaluronic acid,OHA)的自组装行为,构建一种用于局部递送难溶性药物的pH响应型纳米乳水凝胶给药系统。采用自乳化法制备丹参酮IIA(tanshinone ⅡA,Tan IIA)纳米乳,通过平衡溶解度的考察和伪三元相图的绘制优化纳米乳处方,对纳米乳进行理化性质考察。高碘酸钠氧化法制备OHA,以成胶时间为指标优选CMC和OHA的浓度。将OHA溶解于纳米乳中与CMC溶液自组装形成Tan IIA纳米乳水凝胶(CMC-OHA/Tan IIA-NBHs)。对得到的CMC-OHA/Tan IIA-NBHs进行理化性质和体外抑菌活性评价。优化处方可制备得到O/W型Tan IIA纳米乳,粒径为(52.18±0.15)nm,PDI为0.165±0.012。自组装得到的CMC-OHA/Tan IIA-NBHs具有良好的稳定性、酸响应性和药物缓释性能。抑菌圈实验表明CMC-OHA/Tan IIA-NBHs体外可显著抑制痤疮丙酸杆菌和金黄色葡萄球菌的生长。CMC-OHA/Tan IIA-NBHs制备方法简便、稳定性好,可以有效改善难溶性药物的体外溶出行为,为纳米乳局部递送难溶性药物提供了新的思路和方法。
自组装;水凝胶;药物递送;pH响应性;缓释;丹参酮IIA
丹参酮IIA(tanshinone IIA,TanIIA)作为中药丹参中的主要活性成分,对痤疮丙酸杆菌和金黄色葡萄球菌有较好的抑制作用,但由于Tan IIA属于BCS II类药物,水溶性极差(2 μg/mL),严重影响了其在临床上的使用效果[8]。因此本研究以Tan IIA为模型药物,制备了粒径小、分散均匀的Tan IIA纳米乳,然后将OHA溶于Tan IIA纳米乳形成药物前体溶液,与CMC溶液自组装形成Tan IIA纳米乳水凝胶给药系统(CMC-OHA Tan IIAnanoemulsion- based hydrogels,CMC-OHA/Tan IIA-NBHs),并对其稳定性、pH响应性和体外抑菌活性进行评价,为功能型水凝胶递送难溶性药物的研究提供新思路。
1 仪器与材料
1.1 仪器
DF101S型集热式恒温加热磁力搅拌器,北京恒丰长伟科技有限公司;Winner802型纳米激光粒度仪,济南微纳颗粒仪器股份有限公司;Tecnai G2 F30型场发射透射电子显微镜(TEM),美国FEI公司;KQ-100E型超声波清洗器,昆山市超声仪器有限公司;BT125D型电子天平,赛多利斯科学仪器有限公司;TGL-16G型台式离心机,上海安亭科学仪器厂;LC-20A型高效液相色谱系统,日本岛津公司;Nicolet-5799型傅里叶红外光谱仪,美国热力公司;ZRS-8G型智能溶出试验仪,天津市天大天发科技有限公司。
1.2 材料
Tan IIA原料药,质量分数95%,西安鸿生生物技术有限公司,批号150301;Tan IIA对照品,质量分数98%,中国食品药品检定研究院,批号110766- 201520;蓖麻油,湖南尔康制药股份有限公司;油酸乙酯,国药集团化学试剂有限公司;肉豆蔻酸异丙酯(isopropyl myristate)、聚氧乙烯蓖麻油(cremophor EL,CEL)购自长沙研邦化工科技有限公司;聚氧乙烯氢化蓖麻油(cremopher RH 40,CRH),北京凤礼精求商贸有限责任公司;乙醇、聚山梨酯80、聚乙二醇(PEG)400购自天津市光复精细化工研究所;甘油、1,2-丙二醇购自北京化工厂;辛癸酸甘油酯,Sigma生物科技有限公司;磷酸,天津福晨试剂厂;色谱甲醇,Fisher Chemical公司;蒸馏水由实验室超纯水机生产;痤疮丙酸杆菌、金黄色葡萄球菌标准株及培养基购自西安国联质量检测技术股份有限公司。
2 方法
2.1 TanIIAHPLC分析方法的建立
2.1.1 色谱条件 色谱柱为Inerteil ODS-3柱(250 mm×4.6 mm,5 μm);流动相为甲醇-0.1%磷酸水溶液(85∶15);柱温30 ℃;体积流量1 mL/min;检测波长270 nm;进样量20 μL[9]。
2.1.2 溶液的配制
现阶段,经济环境发生了比较显著的变化,工资水平也越来越高,交个税的群体也越来越多,不过由于物价水平的持续提升,抛除通货膨胀的影响,整体的购买能力还是比较低,不过还是需要缴纳个人所得税,个人税收负担会增加,随着二胎政策的推广,一些家庭的生活压力越来越大,要想显示出税收的公平性,就需要进行个人所得税扣除项目改革。
(1)对照品溶液的制备:精密称定5.00 mg对照品Tan IIA置于10 mL量瓶中,加适当甲醇溶解后,甲醇定容至刻度得质量浓度为500 μg/mL的对照品储备液。精密吸取对照品储备液适量,用甲醇按不同比例稀释,得质量浓度为1.00、2.00、4.00、8.00、10.00、20.00、40.00 μg/mL系列对照品溶液。
(2)供试品溶液的配制:精密称取Tan IIA纳米乳1.0 g于50 mL量瓶中,加甲醇超声破乳,定容得母液;再精密量取0.5 mL母液于10 mL量瓶中甲醇定容,摇匀得Tan IIA纳米乳供试品溶液。
(3)阴性对照溶液的配制:精密称取空白纳米乳1.0 g于25 mL量瓶中,甲醇超声破乳,定容得母液;精密量取0.5 mL母液至10 mL量瓶中加甲醇定容,摇匀得阴性对照溶液。
2.1.3 专属性考察 分别取对照品溶液、供试品溶液和阴性对照溶液,0.22 μm微孔滤膜滤过后,按“2.1.1”项下条件测定。图1显示,Tan IIA峰形对称且达到基线分离,供试品与对照品溶液中Tan IIA保留时间基本一致,纳米乳辅料和水凝胶基质对测定无干扰。

图1 CMC-OHA/Tan IIA-NBHs (A)、Tan IIA对照品(B)和空白纳米乳水凝胶(C) 的HPLC图
2.1.4 线性关系考察 以Tan IIA质量浓度为横坐标()、峰面积为纵坐标()进行线性回归,得回归方程为=127 733+28 346,=0.999 6,表明Tan IIA在质量浓度为1.00~40.00 μg/mL线性关系良好。
2.1.5 精密度试验 取“2.1.2”项下质量浓度为8.00 μg/mL的Tan IIA对照品溶液,按“2.1.1”项下的色谱条件进样分析,计算精密度。结果显示Tan IIA峰面积RSD为1.35%,表明仪器精密度良好。
2.1.6 稳定性试验 吸取“2.1.2”项下的供试品溶液适量,分别于0、2、4、6、8、16、24 h按“2.1.1”项下的色谱条件进样分析。结果显示Tan IIA峰面积RSD为0.83%,表明供试品溶液在24 h内稳定。
2.1.7 重复性试验 取同一批的Tan IIA纳米乳3份,每个样品按“2.1.2”项下供试品的制备方法平行配制6个样品,共制备18个样品,按“2.1.1”项下的色谱条件进样分析,记录峰面积。结果RSD为1.38%,表明此方法重复性良好。
2.1.8 加样回收率试验 按“2.1.2”项下供试品的制备方法制备供试品溶液9份,分别加入对照品储备液适量,配制成质量浓度为12.85、14.35、15.75 μg/mL的样品溶液。按“2.1.1”项下色谱条件进样测定,记录峰面积,计算加样回收率。结果低、中、高不同质量浓度的平均回收率分别为99.53%、100.07%、99.03%,RSD值均小于1.5%。表明回收率符合要求。
2.2 TanIIA在纳米乳成分中的溶解度测定
取各辅料1.00 g于2 mL离心管中,分别加入过量Tan IIA,涡旋混匀5 min后超声4 h助溶,静置过夜后,5000 r/min离心10 min,取上清液用甲醇稀释至适当质量浓度,过0.22 μm微孔滤膜后,使用HPLC法测定Tan IIA在各辅料中的平衡溶解度[10]。平衡溶解度测定结果如图2所示,结合辅料的性质,初步选择对Tan IIA溶解度大的聚山梨酯80和PEG 400作为纳米乳的乳化剂和助乳化剂,辛癸酸甘油酯为油相。

图2 Tan IIA在不同辅料中的溶解度
2.3 伪三元相图的绘制及Km值的确定
将确定的乳化剂(聚山梨酯80)和助乳化剂(PEG 400)分别按质量比(m)为3∶1、2∶1、1∶1、1∶2的比例混合,然后将油相和混合乳化剂按1∶9、2∶8、3∶7、4∶6、5∶5、6∶4、7∶3、8∶2、9∶1的比例加入西林瓶中,于37 ℃水浴下搅拌15 min混匀,缓慢滴加蒸馏水继续搅拌直至形成澄清透明的纳米乳,记录体系从黏稠变为流动性良好时的临界点用水量,以该点为相图中可形成纳米乳的边界点。用Origin 7.5软件绘制伪三元相图,比较不同比例油相、乳化剂、助乳化剂所形成纳米乳区域的大小。结果如图3所示,m值(聚山梨酯80和PEG 400的质量比)为2∶1时,该体系形成的纳米乳区面积最大。根据伪三元相图确定聚山梨酯80和PEG 400比例为2∶1。
2.4 Tan IIA纳米乳的制备
按处方量加入乳化剂、助乳化剂、油相和Tan IIA原料药粉末,37 ℃水浴下600 r/min搅拌15 min混匀,缓慢滴加1 mL蒸馏水,即得Tan IIA纳米乳。取同法制备的空白纳米乳于西林瓶中,不同比例油相形成的纳米乳放置7 d后观察乳液形态,结果显示辛癸酸甘油酯与混合乳化剂的比例为1∶9时形成的乳液更加稳定,没有出现分层,絮凝或粒径增大的情况。最终确定Tan IIA纳米乳的最佳处方为聚山梨酯80-PEG 400-辛癸酸甘油酯(6∶3∶1)。

图3 不同Km值的伪三元相图
2.5 Tan IIA纳米乳的表征
为鉴定纳米乳的类别分别加入适量苏丹红和亚甲蓝染料,静置3 min后观察2种染料的扩散速度。如图4-A所示,最优处方制备的Tan IIA纳米乳为澄清透明的橙红色液体,没有沉淀或絮凝。如图4-B和4-C所示,亚甲蓝的扩散速度快于苏丹红,表明所制备的Tan IIA纳米乳为水包油型。
取Tan IIA纳米乳稀释20倍后用激光粒度分析仪测定其平均粒径。粒径测定结果(图5)表明,Tan IIA纳米乳粒径为(52.18±0.21)nm,多分散系数为0.165±0.012,说明该处方制备的纳米乳粒径小,分布范围窄,是均一稳定的分散体系。

图4 Tan IIA纳米乳的外观(A) 及鉴定研究示意图(B, C)

图5 Tan IIA纳米乳的粒径分布
将Tan IIA纳米乳稀释5倍和20倍后滴于覆有支持膜的铜网上,滤纸吸去多余液体后,静置10 min自然晾干,再滴加入质量浓度为10 mg/mL的磷钨酸溶液于铜网上负染10 min,自然挥干,TEM观察纳米乳外观。Tan IIA纳米乳的形态可见图6-a、b所示,稀释倍数为5倍时Tan IIA纳米乳的乳滴大多团聚在一起,粒径大小均在1 μm内,稀释倍数为20倍时Tan IIA纳米乳的乳滴被均匀分散,呈类圆形,粒子间无黏连。

a-5倍稀释 b-20倍稀释
2.6 氧化透明质酸的制备和表征
采用高碘酸钠氧化法制备OHA[11],将2.00 g透明质酸溶于50 mL蒸馏水中,37 ℃水浴以600 r/min的速度搅拌直至完全溶解,室温冷却后加入1.30 g高碘酸钠,在25 ℃水浴条件下持续搅拌12 h后,加入1 mL乙二醇淬灭未反应的高碘酸钠,继续搅拌1 h,随后将产物装入透析袋(截留相对分子质量3500),以蒸馏水透析48 h,然后冷冻干燥得到OHA。
取少许新鲜制备的OHA于研钵中,加入100倍左右的溴化钾粉末,研磨后压片利用红外吸收光谱对合成产物进行表征。结果如图7所示,与HA的红外光谱图对比,1726 cm−1处醛基的特征吸收峰表明使用该方法成功制备OHA。
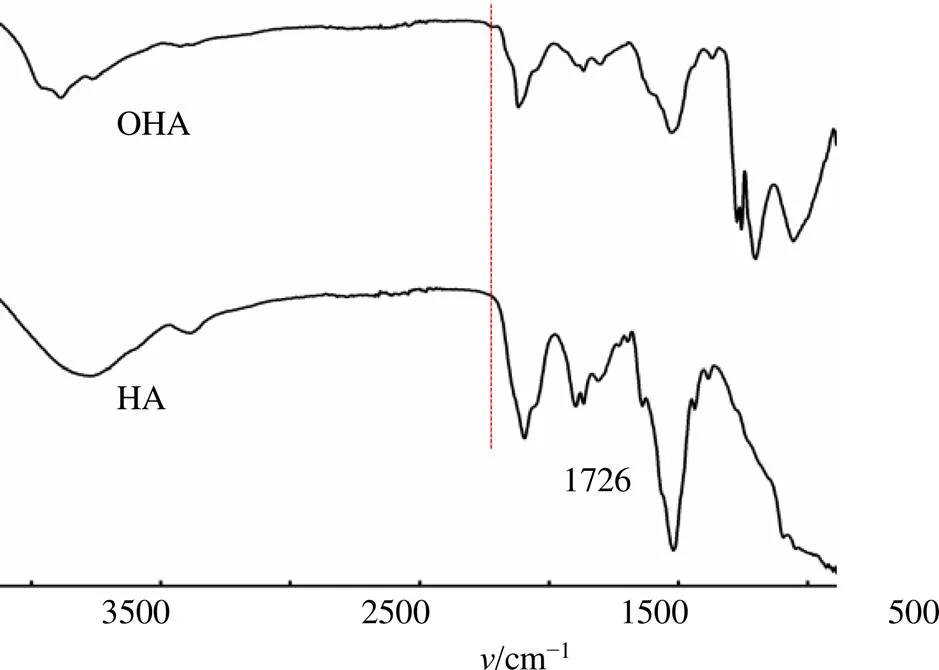
图7 HA和OHA的FT-IR图
2.7 CMC-OHA/Tan IIA-NBHs的制备
2.7.1 成胶时间的测定和空白水凝胶基质的选择 采用倾斜法测定成胶时间,OHA和CMC溶液接触后开始计时,然后倾斜西林瓶,观察溶液的流动情况,待倾斜西林瓶时体系不再流动则停止计时,该时间即为成胶时间。以成胶时间为评价指标,优化凝胶的处方比例。取制备好的OHA粉末溶解在蒸馏水中,形成质量浓度为10、20、30 mg/mL的均匀溶液;CMC溶解在蒸馏水中,形成质量浓度为10、20、30、40 mg/mL的均匀溶液。将等体积的OHA和CMC溶液在37 ℃水浴下混合均匀,并保持在37 ℃直至成胶。形成的空白基质根据组成基质的初溶液质量浓度进行命名,例如20 mg/mL的OHA溶液和30 mg/mL的CMC溶液形成的空白基质命名为O2C3。各组水凝胶的成胶时间和混合1 min时的成胶状态见图8、9。可以发现OHA和CMC的质量浓度均对凝胶的成胶时间有显著影响,随着二者质量浓度的增大凝胶时间逐渐缩短。当OHA质量浓度和CMC质量浓度均为10 mg/mL时,无法形成稳定的水凝胶。当OHA质量浓度为10 mg/mL,随着CMC的质量浓度由20 mg/mL增大到40 mg/mL,成胶时间由261.67 s缩短至176.33 s。当OHA质量浓度为30 mg/mL时,随着CMC的质量浓度由10 mg/mL增大到40 mg/mL,成胶时间进一步由152.00 s缩短至24.00 s。进一步提高质量浓度会延长前体溶液的制备时间,导致总体制备时间增大,因此,最终优选O3C4进行后续研究。

图8 不同质量分数CMC和OHA形成水凝胶的成胶时间

图9 1 min时各组水凝胶的状态
2.7.2 载药水凝胶的制备和载药量的测定 取制备好的OHA粉末用Tan IIA纳米乳溶解,随后与等体积的CMC溶液在37 ℃水浴下混合均匀直至成胶,即得CMC-OHA/Tan IIA-NBHs。最佳处方制备得到的CMC-OHA/Tan IIA-NBHs可见图10,其外观均匀且成胶性能良好。经测定,CMC-OHA/Tan IIA-NBHs的成胶时间为(24.32±0.03)s,与O3C4空白水凝胶基质的成胶时间没有显著性差异。取1.00 g CMC-OHA/Tan IIA-NBHs置于10 mL量瓶中,加入适量甲醇超声15 min后用甲醇定容至刻度,过0.22 μm滤膜后用HPLC法测得CMC-OHA/Tan IIA- NBHs中Tan IIA的质量分数为1.0 mg/g。

图10 CMC-OHA/Tan IIA-NBHs的外观
2.8 CMC-OHA/Tan IIA-NBHs的稳定性考察
2.8.1 离心稳定性 将Tan IIA和CMC-OHA/Tan IIA-NBHs以8000 r/min的速度离心20 min,观察离心后其外观是否有变化[12]。离心稳定性结果如图11所示,8000 r/min离心20 min后Tan IIA纳米乳(b)仍澄清透明,未产生分层破乳现象,但有少量药物析出沉积在底部,而CMC-OHA/Tan IIA-NBHs(a)经过离心处理没有药物析出,表明CMC-OHA/Tan IIA-NBHs离心稳定性良好。
2.8.2 光稳定性 Tan IIA作为一种具有醌式结构的化合物,易被氧化,并有研究显示其光稳定性较差,因此对CMC-OHA/Tan IIA-NBHs(a)的光稳定性进行了考察,与Tan IIA纳米乳(b)和Tan IIA乙醇溶液(c)进行对比。将Tan IIA乙醇溶液、Tan IIA纳米乳和CMC-OHA/Tan IIA-NBHs置于透明西林瓶中,于25 ℃、日光灯下(4500 lx)保存。分别于0、1、2、4、8、12、24、36、48、72 h取样0.50 g,用甲醇稀释并超声后定容至刻度,过0.22 μm滤膜后用HPLC法测定Tan IIA含量。如图12所示,在25 ℃、日光灯下(4500 lx)保存3 d后,Tan IIA乙醇溶液中Tan IIA的含量下降了44.66%,Tan IIA纳米乳含量下降了30.92%,而CMC-OHA/Tan IIA-NBHs中Tan IIA含量变化最小,仅下降了6.92%。说明将Tan IIA制备成纳米乳水凝胶能显著提升其光稳定性。

a-CMC-OHA/Tan IIA-NBHs b-Tan IIA纳米乳

a-CMC-OHA/Tan IIA-NBHs b-Tan IIA纳米乳 c-Tan IIA乙醇溶液
2.8.3 长期稳定性 将CMC-OHA/Tan IIA-NBHs置于密闭器皿中,于4、25、40 ℃不同温度条件下避光放置,在0、3、7、14、21、30 d取样,HPLC法测定Tan IIA的含量。如图13所示,于4 ℃和25 ℃条件下储存的CMC-OHA/Tan IIA-NBHs在30 d内Tan IIA质量分数分别下降2.82%和2.99%,在40 ℃条件下储存的CMC-OHA/Tan IIA-NBHs在30 d内Tan IIA含量下降8.48%。因而CMC-OHA/Tan IIA-NBHs在室温或冷藏的避光储存条件下具备较好的药物稳定性,但热稳定性较差。

图13 CMC-OHA/Tan IIA-NBHs的长期稳定性(, n = 3)
2.9 CMC-OHA/Tan IIA-NBHs的体外响应性释放
采用透析袋法考察CMC-OHA/Tan IIA-NBHs在pH为5.0、5.5、7.4的PBS缓冲溶液中的释放。取10.00 g CMC-OHA/Tan IIA-NBHs于活化好的透析袋(截留相对分子质量14 000)中,两端夹紧,置于盛有200 mL PBS的溶出杯中,温度为37 ℃,转速为100 r/min,分别于0.5、1、2、4、6、8、10、12、24、32、48、54、72 h取样0.5 mL,同时补加同温同体积的溶出介质,样品用0.22 μm的微孔滤膜滤过,HPLC法测定Tan IIA含量,并计算Tan IIA累积释放量。CMC-OHA/Tan IIA-NBHs的体外响应性释放结果如图14所示,在pH 5.0、5.5的PBS缓冲液中,72 h内Tan IIA的释放度分别为73.74%和67.56%,而在pH为7.4的缓冲溶液中,72 h内Tan IIA的释放度仅为37.11%。此外,在酸性缓冲溶液中,CMC- OHA/Tan IIA-NBHs在24 h内释放率超过40%,而在中性缓冲溶液中的释放度不足30%。结果表明CMC-OHA/Tan IIA-NBHs具有明显的酸响应性,并有良好的缓释作用,可以在接触微酸性皮肤时缓慢释放药物。

图14 CMC-OHA/Tan IIA-NBHs在PBS缓冲液中释放曲线(, n = 3)
2.10 抑菌效果评价
为了考察CMC-OHA/Tan IIA-NBHs的抑菌活性,分别考察了CMC-OHA/Tan IIA-NBHs对痤疮丙酸杆菌和金黄色葡萄球菌的抑菌能力。痤疮丙酸杆菌和金黄色葡萄球菌于培养平板上活化,将2种菌转移至硫乙醇酸盐培养基中,分别于37 ℃培养箱进行无氧和有氧培养,然后使用无菌水将二者稀释至活菌量在1×105~1×106cfu/mL,作为供试菌液备用。精密量取2种供试菌液各150 μL,分别均匀涂抹于培养基,并平行制备3份。使用直径为0.5 cm的圆形模圈在含菌培养基表面分别涂抹等质量0.20 g的CMC-OHA/Tan IIA-NBHs、阳性药红霉素、O3C4空白凝胶和卡波姆空白凝胶后痤疮丙酸杆菌于37 ℃培养箱内进行无氧培养,金黄色葡萄球菌于37 ℃培养箱内进行有氧培养。48 h后观察测量各给药部位的抑菌圈直径,并按表1评判标准进行评判[13]。
表1 抑菌圈评分
Table 1 Scoring table of bacteriostatic ring
抑菌圈直径敏感度评分 直径>20 mm极度敏感4 20 mm>直径≥15 mm高度敏感3 15 mm>直径≥10 mm中度敏感2 10 mm>直径≥7 mm低度敏感1 直径<7 mm不敏感0
CMC-OHA/Tan IIA-NBHs的体外抑菌活性评估结果如表2所示。对于痤疮丙酸杆菌,阳性药红霉素抑菌圈大小为(27.30±1.27)mm,敏感程度评分4级,CMC-OHA/Tan IIA-NBHs的抑菌圈大小为(23.70±0.71)mm,敏感程度评分4级,O3C4空白凝胶的抑菌圈大小为(15.60±1.12)mm,敏感程度评分3级。对于金黄色葡萄球菌,阳性药红霉素抑菌圈大小为(29.10±1.00)mm,敏感程度评分4级,CMC-OHA/Tan IIA-NBHs的抑菌圈大小为(33.10±1.40)mm,敏感程度评分4级,O3C4空白凝胶的抑菌圈大小为(17.60±1.33)mm,敏感程度评分3级,卡波姆空白凝胶对痤疮丙酸杆菌和金黄色葡萄球菌没有抑菌能力。结果证明CMC- OHA/Tan IIA-NBHs具有良好的抑菌活性,体外能抑制痤疮丙酸杆菌和金黄色葡萄球菌的生长。
表2 CMC-OHA/Tan IIA-NBHs的体外抑菌活性
Table 2 Antibacterial activity of CMC-OHA/Tan IIA-NBHs in vitro
药物痤疮丙酸杆菌金黄色葡萄球菌 抑菌圈直径评分抑菌圈直径评分 红霉素27.30±1.27429.1±1.004 CMC-OHA/Tan IIA-23.70±0.71433.1±1.404 NBHs O3C415.60±1.12317.6±1.333 卡波姆凝胶1.40±0.9702.9±0.750
3 讨论
制备简单、工艺成熟的纳米乳液近年来在食品和药品领域引起了广泛关注,制备纳米乳的辅料具有生物相容性好毒性低的特点,因此,纳米乳很适合封装和递送亲脂性活性成分。然而由于其低黏度性和不稳定性,纳米乳不适合局部给药,为了解决这些问题,将纳米乳和凝胶剂结合是一个很有效的解决方案[14-15]。在成胶时间的测定中发现,随着OHA和CMC质量浓度的升高,凝胶的成胶时间会显著缩短。这是因为OHA-CMC水凝胶是通过席夫碱反应形成,OHA的氨基和CMC的醛基生成具有pH响应性的亚胺键,因此水凝胶的成胶时间主要和溶液中的活性氨基和醛基数有关,随着OHA和CMC质量浓度的升高,溶液中发生交联的活性基团密度会增加,凝胶的成胶时间会显著缩短[16]。
皮肤面部的pH与多种因素有关,有研究显示在多种皮肤屏障受损的疾病中,均观察到了不同程度的皮肤表面pH的升高[17-18]。因此本研究选择考察CMC-OHA/Tan IIA-NBHs中Tan IIA在pH为5.0、5.5的缓冲溶液中的释放,同时以pH为7.4的缓冲溶液组作为对照。体外释放实验结果表明,CMC-OHA/Tan IIA-NBHs在pH为5.0的PBS缓冲液中,Tan IIA72 h的累积释放度可达到70%以上,而在pH 7.4时仅仅不到30%,表明具有较好的酸响应性。根据Chen等[19]实验结果发现,席夫碱结构在弱酸性环境下降解缓慢,完全降解需要10 d左右,因此CMC-OHA/Tan IIA-NBHs在72 h内难以释放完全。而在pH7.4的缓冲液中,席夫碱键较为稳定,CMC和OHA水凝胶网络结构降解程度较低,不利于药物释放。因此这种pH响应型的药物载体在药物递送领域有着巨大的应用潜力。
体外抑菌活性实验表明,CMC-OHA/Tan IIA- NBHs在体外能够有效抑制痤疮丙酸杆菌和金黄色葡萄球菌的生长。此外O3C4水凝胶基质也有一定的抑菌活性,这是因为壳聚糖的高电荷多阳离子结构与带负电的细菌磷脂膜成分会产生强烈的静电相互作用,通过膜损伤和随后的内容物泄漏导致细菌死亡,因此适当提高壳聚糖的浓度有利于提高凝胶的抗菌性能[20-21]。
本研究利用CMC和OHA的自组装行为,在温和的反应条件下,一步制备完成了纳米乳和水凝胶的结合,得到的CMC-OHA/Tan IIA-NBHs具有良好的稳定性、pH响应性和缓释能力,可在体外显著抑制痤疮丙酸杆菌和金黄色葡萄球菌的生长。为纳米乳和难溶性药物的外用产品开发与临床应用提供理论依据和实验基础。
利益冲突 所有作者均声明不存在利益冲突
[1] Yan S Q, Zhang Q, Wang J N,. Silk fibroin/ chondroitin sulfate/hyaluronic acid ternary scaffolds for dermal tissue reconstruction [J]., 2013, 9(6): 6771-6782.
[2] Su H Y, Zhang W, Wu Y Y,. Schiff base-containing dextran nanogel as pH-sensitive drug delivery system of doxorubicin: Synthesis and characterization [J]., 2018, 33(2): 170-181.
[3] Hu M, Yang J L, Xu J H. Structural and biological investigation of chitosan/hyaluronic acid with silanized- hydroxypropyl methylcellulose as an injectable reinforced interpenetrating network hydrogel for cartilage tissue engineering [J]., 2021, 28(1): 607-619.
[4] Moradi S, Barati A, Salehi E,. Preparation and characterization of chitosan based hydrogels containing cyclodextrin inclusion compounds or nanoemulsions of thyme oil [J]., 2019, 68(11): 1891-1902.
[5] Liang Y P, Zhao X, Hu T L,. Adhesive hemostatic conducting injectable composite hydrogels with sustained drug release and photothermal antibacterial activity to promote full-thickness skin regeneration during wound healing [J]., 2019, 15(12): e1900046.
[6] Ma X Z, Xiang S Y, Xie H J,. Fabrication of pH- sensitive tetramycin releasing gel and its antibacterial bioactivity against[J]., 2019, 24(19): 3606.
[7] Omidi S, Pirhayati M, Kakanejadifard A. Co-delivery of doxorubicin and curcumin by a pH-sensitive, injectable, andhydrogel composed of chitosan, graphene, and cellulose nanowhisker [J]., 2020, 231: 115745.
[8] 王秀环, 孙伟卫, 季新燕, 等. 丹参酮IIA微乳及微乳凝胶的抑菌效果及痤疮临床疗效的初步研究 [J]. 山西中医学院学报, 2015, 16(6): 36-38.
[9] 郑娟, 沈成英, 庞建云,等. 丹参酮IIA纳米结构脂质载体的体外评价及其对HaCaT细胞增殖的影响 [J]. 中草药, 2016, 47(24): 4340-4344.
[10] 钟钰, 胡鹏翼, 郑琴, 等. 紫苏精油纳米乳的处方工艺研究与初步质量评价 [J]. 中草药, 2020, 51(22): 5714-5722.
[11] Zhang R Y, Li X, He K W,. Preparation and properties of redox responsive modified hyaluronic acid hydrogels for drug release [J]., 2017, 28(12): 1759-1763.
[12] 邓茂, 李小芳, 陈慧娟, 等. 以茶皂素为天然乳化剂制备水飞蓟素纳米乳及其理化性质考察 [J]. 中草药, 2021, 52(21): 6528-6536.
[13] 吕好新, 赵玲丽, 霍珊珊, 等. 肉桂-山苍子复合植物精油对发霉花生黑曲霉BQM菌的抑菌效果 [J]. 中国食品学报, 2021, 21(12): 222-229.
[14] Komaiko J, McClements D J. Food-grade nanoemulsion filled hydrogels formed by spontaneous emulsification and gelation: Optical properties, rheology, and stability [J]., 2015, 46: 67-75.
[15] Hu Q, Lin H, Wang Y F,. Design, optimization and evaluation of a microemulsion-based hydrogel with high malleability for enhanced transdermal delivery of levamisole [J]., 2021, 605: 120829.
[16] Hu B, Gao M Z, Boakye-Yiadom K O,. An intrinsically bioactive hydrogel with on-demand drug release behaviors for diabetic wound healing [J]., 2021, 6(12): 4592-4606.
[17] 陈思璇, 李泓莹, 杨洋, 等. 点阵激光用于痤疮患者的临床治疗对疗效、皮损改善、经表皮失水量、皮肤表面pH值、血红素含量的影响观察 [J]. 中国中西医结合皮肤性病学杂志, 2021, 20(1): 60-62.
[18] Schürer N. pH and acne [J]., 2018, 54: 115-122.
[19] Chen T Y, Wen T K, Dai N T,. Cryogel/hydrogel biomaterials and acupuncture combined to promote diabetic skin wound healing through immunomodulation [J]., 2021, 269: 120608.
[20] Moeini A, Pedram P, Makvandi P,. Wound healing and antimicrobial effect of active secondary metabolites in chitosan-based wound dressings: A review [J]., 2020, 233: 115839.
[21] Qu J, Zhao X, Liang YAntibacterial adhesive injectable hydrogels with rapid self-healing, extensibility and compressibility as wound dressing for joints skin wound healing [J]., 2018, 183(11): 185-199.
pH-responsive nanoemulsion hydrogel drug delivery system based on self- assembly behavior of carboxymethyl chitosan-oxidized hyaluronic acid
TANG Xiao-han1, 2, WANG Zhe2, YAN Qiao2, QIN Zhi-jian1, YUAN Hai-long1, 2
1. School of Pharmacy, Anhui Medical University, Hefei 230032, China 2. Department of Pharmacy, Air Force Medical Center, PLA, Beijing 100142, China
To construct a pH-responsive nanoemulsion hydrogel drug delivery system based on the self-assembly behavior of carboxymethyl chitosan (CMC)-oxidized hyaluronic acid (OHA) for the topical delivery of in poor solubility drugs.The optimum prescription of nanoemulsion was determined according to the amount of tanshinone ⅡA(Tan IIA) dissolved in various excipients and the pseudo-ternary phase diagram and the physicochemical properties of the nanoemulsion were investigated. Furthermore, OHA was prepared by sodium periodate oxidation and the concentration of CMC and OHA is optimized by using the gel formation time as an indicator. CMC-OHA Tan IIAnanoemulsion-based hydrogels (CMC-OHA/ Tan IIA-MBHs) were prepared by dissolving OHA in nanoemulsion and self-assembling the mixture with CMC solution. Physicochemical properties andantibacterial activity of CMC-OHA/Tan IIA-MBHs were observed and detected.The mean particle size of the prepared Tan IIAnanoemulsion was (52.18 ± 0.21) nm and PDI was 0.165 ± 0.012. Theevaluation results showed CMC-OHA/Tan IIA-NBHs had good centrifugal stability, light stability, pH responsiveness, and sustained-release properties. The bacterial inhibition ring test showed that CMC-OHA/TanIIA-NBHs could significantly inhibit the growth of Propionibacterium acnes and Staphylococcus aureus.With the advantages of simple preparation and good stability, CMC-OHA/Tan ⅡA-MBHs could effectively improve thedissolution behavior of insoluble drugs, providing a new idea and method for topical delivery of poorly soluble drugs by nanoemulsion.
self-assembly; hydrogel; drug delivery; pH-sensitive; sustained-released; tanshinone IIA
R283.6
A
0253 - 2670(2022)16 - 4992 - 09
10.7501/j.issn.0253-2670.2022.16.008
2022-02-21
国家自然科学基金面上项目(81873092)
汤小涵,硕士研究生,研究方向为中药新型给药系统研究。E-mail: 3206820156@qq.com
袁海龙,研究员,博士生导师,研究方向为中药新型给药系统研究。Tel: (010)66928505 E-mail: yhlpharm@126.com
[责任编辑 郑礼胜]

