腹腔镜保脾脾门淋巴结清扫在进展期近端胃癌根治术中的应用
沈 阳,程元光,何 磊
(安徽医科大学第三附属医院胃肠外科,安徽 合肥,230061)
近端胃癌的发病率在世界范围内呈逐渐上升趋势,针对近端胃癌的规范化治疗应受到足够重视[1-3]。全胃切除+D2根治性淋巴结清扫术是治疗进展期近端胃癌的标准术式。但目前文献报道的No.10淋巴结转移率存在较大差异,脾门淋巴结清扫的临床适应证仍不明确。第5版日本《胃癌治疗指南》建议,仅对侵犯大弯侧的进展期近端胃癌患者施行脾门淋巴结清扫术[4]。既往开腹手术中,需将脾脏、胰尾充分游离并拖出体外进行彻底的No.10淋巴结清扫,手术难度较大,且术后并发症较多。随着腹腔镜技术的迅速发展,结合“黄氏三步法”程序化的术式,使保脾脾门淋巴结清扫术操作相对简单[5]。本文回顾分析2018年10月至2021年10月安徽医科大学第三附属医院为25例进展期近端胃癌患者行腹腔镜保脾脾门淋巴结清扫术的临床资料,并与同期行开腹保脾脾门淋巴结清扫的30例患者进行对比分析,以探讨腹腔镜保脾脾门淋巴结清扫术的可行性及安全性。
1 资料与方法
1.1 临床资料 收集2018年10月至2021年10月安徽医科大学第三附属医院收治的55例进展期近端胃癌患者的临床资料,均行根治性全胃切除术+D2淋巴结清扫术。按术式分为腹腔镜组与开腹组,两组患者临床资料差异均无统计学意义,具有可比性。见表1。
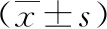
表1 两组患者临床资料的比较
1.2 纳入与排除标准 纳入标准:(1)胃镜及影像学检查明确诊断进展期胃癌;(2)病灶位于胃中上部且侵犯大弯侧;(3)临床及病理资料完整;(4)患者及其家属知情同意。排除标准:(1)周围脏器侵犯或远处转移;(2)合并其他脏器恶性肿瘤;(3)全身情况较差不能耐受手术。
1.3 手术方法 腹腔镜保脾脾门淋巴结清扫术:第一步,胰尾处显露脾下叶血管,于根部离断胃网膜左动静脉,继续离断1~2支胃短血管,见图1、图2;第二步,沿脾动脉中部向脾门方向清扫,裸化脾中叶血管,离断胃后血管及2~3支胃短血管,见图3、图4;第三步,于脾上极附近裸化脾上叶血管,离断最后一支胃短血管,No.10淋巴结清扫结束,见图5、图6。开腹保脾脾门淋巴结清扫:离断脾膈韧带、脾结肠韧带及脾肾韧带后,充分游离脾脏、胰体尾,并将其托出体外,见图7;先由右向左骨骼化清扫脾动静脉及脾门各血管分支,再清扫脾门腹面及背面的淋巴结,见图8。
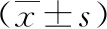

图1 胰尾处显露脾下叶血管,于根部离断胃网膜左动静脉 图2 离断脾下极1~2支胃短血管
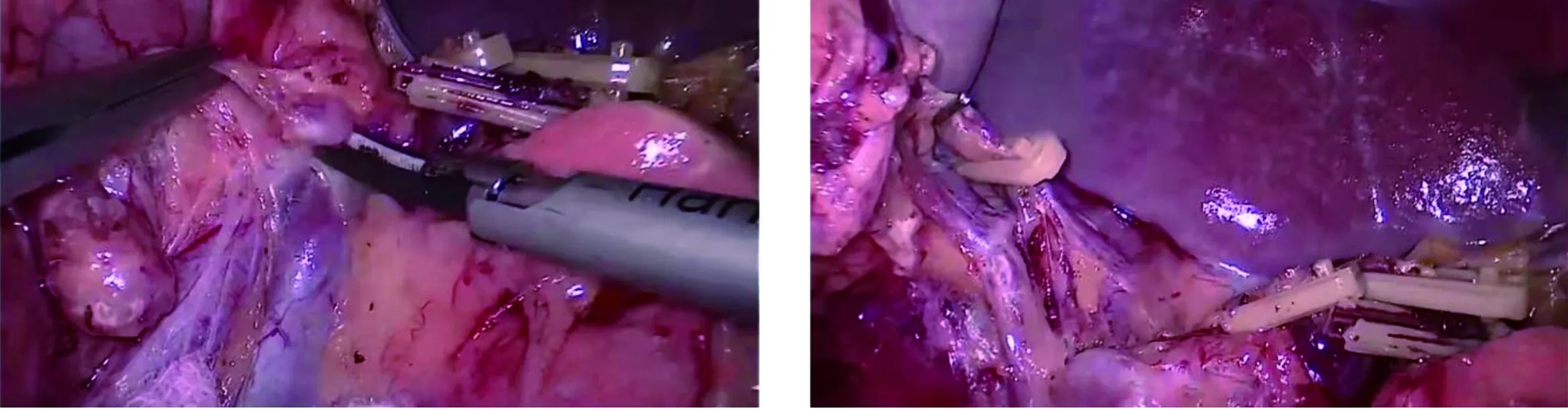
图3 沿脾动脉中部向脾门方向清扫,裸化脾中叶血管 图4 离断2~3支胃短血管
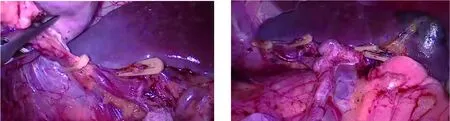
图5 在脾上极附近裸化脾上叶血管,离断最后一支胃短血管 图6 腹腔镜保脾脾门淋巴结清扫效果

图7 充分游离脾脏、胰体尾并将其托出体外 图8 开腹保脾脾门淋巴结清扫效果
2 结 果
两组手术均顺利完成,腹腔镜组无一例中转开腹。两组术后排气时间、术后住院时间及术后并发症发生率差异有统计学意义(P<0.05);两组其他手术相关指标(No.10淋巴结清扫时间、No.10淋巴结清扫出血量、No.10淋巴结清扫数量、No.10淋巴结阳性率)差异无统计学意义(P>0.05),见表2。腹腔镜组术后发生炎性肠梗阻1例,经禁食、抗炎、石蜡油润肠通便等保守治疗后治愈;开腹组术后发生切口感染1例、淋巴瘘2例、腹腔感染1例,均经保守治疗后治愈。

表2 两组患者手术相关指标的比较
3 讨 论
3.1 脾门淋巴结清扫的临床意义及适应证 No.10淋巴结转移是影响近端胃癌患者预后的独立危险因素[6]。既往研究显示,近端胃癌No.10淋巴结转移率为7.3%~18.3%,5年生存率仅为11.0%~22.2%[7-9]。因此,较早版本的日本《胃癌治疗指南》规定,近端胃癌D2淋巴结清扫术必须包括No.10淋巴结[10-11]。关于脾门淋巴结清扫的适应证选择仍存在争议。日本的一项前瞻性随机对照研究(JCOG 0110)显示,在不侵犯大弯侧的近端胃癌患者中,保脾组与脾切除组No.10淋巴结转移率分别为3.5%与2.7%[12]。Maezawa等[13]回顾分析85例侵犯大弯侧的近端胃癌患者,No.10淋巴结转移率为13%。Aoyagi等[14]的研究也发现,侵犯大弯侧的近端胃癌患者中No.10淋巴结转移率高达19.8%。最新版日本《胃癌治疗指南》建议,仅对侵犯大弯侧的近端胃癌患者施行脾门淋巴结清扫术[4]。本研究中选择的病例均为侵犯大弯侧的进展期近端胃癌。近期国内学者对既往的四项前瞻性随机对照试验(CLASS-04、FUGES-001、FUGES-002、FUGES-012)进行汇总分析,结果发现,在未侵犯大弯侧的患者中,肿瘤直径>5 cm且术前胃周淋巴结阳性的患者No.10淋巴结转移率高达19.2%,因此建议此类患者也应施行脾门淋巴结清扫术[15]。
3.2 腹腔镜下保脾脾门淋巴结清扫的优势及安全性 既往很长一段时间预防性脾切除术被作为No.10淋巴结清扫的标准术式,但有研究显示,脾切除相对保脾脾门淋巴结清扫并未带来远期生存优势,反而存在较高的术后并发症发生率[12,16-17]。笔者的前期研究也显示,脾脏拖出式脾门淋巴结清扫相对脾切除术具有并发症少、住院时间短的优势,而清扫效果相当[18]。但开腹保脾脾门淋巴结清扫需将脾脏、胰体尾充分游离并拖出体外,操作上具有相当大的挑战性,且术后可能出现脾扭转、脾梗死等严重并发症。随着微创与功能保护理念的发展,腹腔镜技术逐渐被应用于保脾脾门淋巴结清扫中。由于腹腔镜的放大效应、相对充分的操作空间及超声刀良好的止血效果,使腹腔镜下脾门淋巴结清扫在操作上相对容易。我国学者的一项单中心随机对照研究中,将222例进展期近端胃癌患者分为腹腔镜组与开腹组,结果显示,腹腔镜组术中清扫No.10淋巴结时间、出血量明显少于开腹组;两组No.10淋巴结清扫数量差异无统计学意义,同时腹腔镜组亦显示出微创手术进食早、康复快、住院时间短的优势[19]。本研究中,腹腔镜组较开腹组排气时间短、住院时间短、术后并发症少,充分显示了腹腔镜技术的微创优势,但No.10淋巴结清扫时间、出血量两组差异无统计学意义,可能与笔者开展病例数较少、团队配合尚不熟练等因素有关。
脾脏质脆、位置深在,脾门血管解剖变异复杂,无论开腹抑或腹腔镜辅助下清扫难度都很大。福建协和医院的研究发现,在腹腔镜胃癌手术操作熟练的基础上,经历约40例腹腔镜保脾脾门淋巴结清扫术,术者才可完成学习曲线、技术达到稳定成熟[20]。因此外科医师应进行规范化培训,并选择年轻、体型较瘦、术前合并症少、肿瘤分期较早的患者开展此类手术。
总之,笔者认为腹腔镜保脾脾门淋巴结清扫术相对开腹手术创伤小、康复快、术后并发症少,而肿瘤学治疗效果相当,可使患者获益,手术方式合理,值得推广应用。

