Calypso系统在肝脏立体定向放疗中的临床作用观察
詹梦娜, 魏晓为, 何侠, 尹丽, 冯勇
体部立体定向放射治疗(stereotactic body radiotherapy,SBRT)在肝恶性肿瘤局部治疗中占据重要地位,但治疗过程中的准确性会受到呼吸运动、脏器蠕动等生理和物理因素的影响,肝脏肿瘤运动幅度可能超过2 cm[1]。比较理想的方法是通过肿瘤实时追踪放疗来降低治疗分次内肿瘤运动对治疗效果的负面影响[2]。
Calypso系统(瓦里安医疗系统有限责任公司,美国)是一种实时目标定位和运动管理的解决方案。使用可植入的3枚不同频率的电磁转发器将实时位置信息传输到追踪站。治疗时患者可以自由呼吸,在超出阈值范围时直线加速器自动停止出束,且当肿瘤位置还原后恢复出束。该系统于2014年获得欧洲统一认证及美国食品和药物管理局的许可,用于肿瘤放射治疗图像引导[3],并在前列腺癌放疗中报告了可靠的临床经验[4]。2015年3月路易维尔大学第一次在肝脏肿瘤中使用Calypso系统[5],研究表明Calypso引导的肿瘤追踪剂量学准确性很高[6]。江苏省肿瘤医院是中国第一个使用该系统辅助肝脏精准放疗的机构,本文从临床角度介绍和探讨电磁导航门控肝脏立体定向放射治疗的初步经验和价值。
1 材料与方法
1.1 一般资料 2019年4月至2020年7月,江苏省肿瘤医院4例肝脏恶性肿瘤患者签署知情同意书后,在Calypso引导下行肝脏SBRT治疗,本研究经医院伦理委员会审核通过。因高龄、肺功能不佳等原因无法耐受呼吸门控者,按Calypso系统设计初衷在治疗时允许患者自由呼吸。
1.2 治疗计划及过程 根据Calypso电磁转发器植入要求,转发器距患者前部皮肤19 cm以内(仰卧为治疗位置),所以需对所有患者体内肿瘤的深度进行评估。然后医生在CT引导下经皮穿刺植入3枚电磁转发器至患者肝脏肿瘤周围。转发器是一个长度为8.7 mm、直径为1.3 mm的圆柱体(Calypso软组织电磁转发器、瓦里安医疗系统、美国)。根据说明书,在植入后第5天,即转发器位置稳定后,获得呼气末屏气扫描和自由呼吸扫描CT图像,厚度应在1.0~1.5 mm。所有患者使用负压真空垫固定,未使用腹部加压。
计划靶区(planning target volume,PTV)是通过在左右、前后和颅尾方向将临床靶区(clinical target volume,CTV)扩大5 mm边缘而形成的。4例患者的放疗计划分别是48Gy/12f、50Gy/10f、30Gy/6f和40Gy/5f的调强放疗,平均剂量为100%的处方剂量覆盖95%的PTV。除了通常为肝SBRT患者勾画的结构外,物理师设计计划时还需标明3个电磁转发器的中心,外照射放疗计划系统可自动得到电磁转发器相对于等中心的坐标,然后这些坐标被Calypso系统控制计算机在治疗期间使用。
运动监测处理是在呼气末端屏气模式与光子直线加速器跟踪系统相配合。能量在无均整器(flattening filter free,FFF)治疗模式下为6MV,剂量率为每分钟1 200个监测单元(MU)。在每次治疗之前,进行质量保证(quality assurance,QA)测试,以保持追踪系统等分中心的准确性。关键点包括测试坐标系、延迟或异常条件下的射束和剂量测定测试。门控窗位大小在3个方向上均为5 mm。在治疗期间如果肝脏肿瘤移动>5 mm,照射束将由Calypso系统进行门控,直到肿瘤移回位置。
本中心开发了一种用于跟踪视频信号的同步设备,将内部电磁运动、光学表面监测系统和实时位置管理的视频信号通过三路开关从控制室传输到治疗室。患者可以通过连接到视频图形阵列(video graphics array,VGA)信号电缆的显示屏观察到与控制室显示屏完全相同的肿瘤目标运动曲线,从而接受辅助呼吸指令,找到最佳屏气区间(图1)。
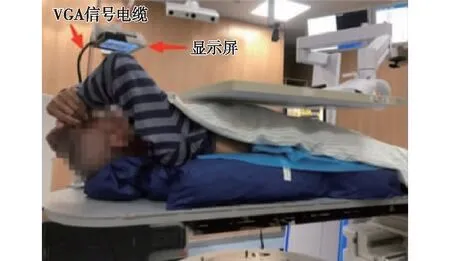
注:患者治疗床末端安装有一个跟踪视频信号的同步装置,患者的头部上方设置了一个迷你显示屏供患者接受辅助呼吸指令图1 治疗室中患者放疗时情形图
1.3 观察指标 收集所有患者的临床特征,包括性别、年龄、体力状况美国东部肿瘤协作组(eastern cooperative oncology group,ECOG)评分、肝功能CHILD PUGH评分等。为了解是否出现放射性肝损伤(radiation-induced liver damage,RILD),监测治疗前1周、治疗结束时、治疗结束后1个月及3个月的肝功能、血甲胎蛋白(AFP)、凝血情况及CHILD PUGH评分;并在治疗结束时,对所有患者进行有关急性反应及不良反应的临床评估,在SBRT结束后1~2个月进行临床评估和影像学检查。然后每2~3个月进行一次随访,评估急性(3个月内)和慢性(3个月以上)不良反应。根据RECIST标准,疗效评估定义为完全缓解(complete response,CR)、部分缓解(partial response,PR)、无反应或疾病稳定(stable disease,SD)和疾病进展(progressive disease,PD)4种[4]。
1.4 问卷设计 为了更好地评估患者的主观接受程度以及为后续患者的治疗进行优化,我们设计了患者问卷(表1),使用五点量表对项目进行评分。

表1 患者主观结果调查问卷
2 结果
2.1 患者特点 自2019年4月至2020年7月共4例患者使用了电磁转发器辅助肝脏恶性肿瘤SBRT。患者临床特点见表2。
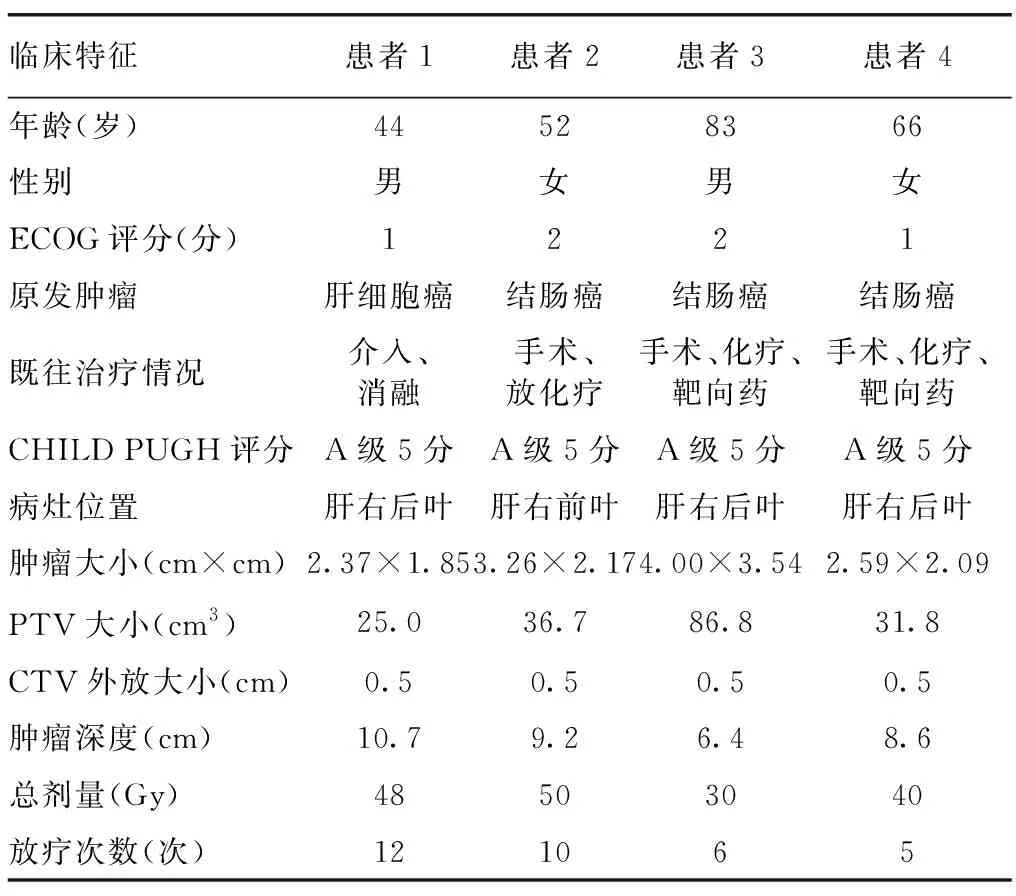
表2 4例患者临床特点
2.2 治疗情况 所有患者在肝脏病灶旁分别植入3枚Calypso电磁转发器,呈三角形分布。操作过程顺利,复扫CT确认转发器位置准确。4例患者在植入过程中耐受性良好,术后即刻CT扫描均无出血、气胸等并发症发生。植入后第5天行定位CT检查,4例患者肝内转发器均无明显移位。
每两个转发器距离的中位标准差为0.082 cm,最大值不超过0.200 cm,保证了目标准确的追踪。Calypso系统每天通过3个电磁转发器的空间位置,进一步进行几何残差、俯仰、滚动和偏航角的测量,以确保目标位置未发生偏移。结果显示所有患者的所有分次治疗监测到的最大测量值分别为0.08 cm(阈值0.20 cm)、5°(阈值10°)、5°(阈值10°)和8°(阈值10°),保证放疗准确性。
每日跟踪的报告示例如图2所示,目标运动沿横向、纵向和垂直轴(从上到下)显示。y轴显示以cm为单位的偏移;x轴显示以s为单位的时间,在追踪过程中,光束被传送时,跟踪显示为灰色,可见实际的剂量传递时间非常短。在所有三个方向门控窗位大小均为5 mm。

2A:患者1示例报告跟踪显示灰色部分较均匀,表示该患者配合指令屏气依从性较好, Calypso系统联合呼吸门控配合度较高;2B:患者4示例报告跟踪显示灰色部分较杂乱,表示该患者配合指令屏气依从性较差, Calypso系统联合呼吸门控配合度较低图2 放射治疗跟踪报告图
4例患者治疗时间(6.37~41.37)min,患者1和患者2的Calypso系统联合呼吸门控配合度较好,患者3和患者4配合度较差,部分治疗场次允许其自由呼吸。4例患者中位治疗时间分别为9.78 min、11.60 min、27.14 min和18.48 min。每位患者从追踪开始到结束每次治疗持续时间详见表3,每次治疗每个照射野时间4例患者平均为12.25 s(10.32~14.74 s)。
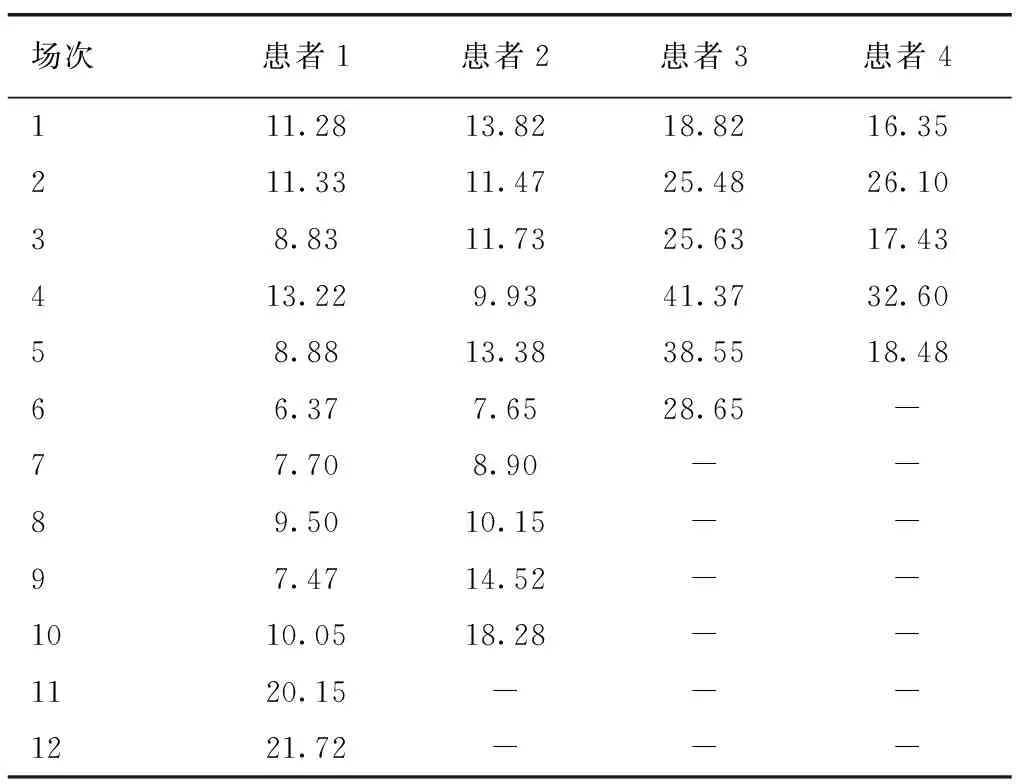
表3 4例患者治疗时间(min)
2.3 疗效评价 在放疗结束后1个月及3个月对所有患者进行临床评估和影像学检查,4例患者疗效评价均为SD,未出现局部进展。
2.4 肝功能指标变化 4例患者血液碱性磷酸酶、AFP和凝血常规治疗前后均正常。患者1治疗前总胆红素和天门冬氨酸氨基转移酶偏高,治疗结束后降至正常范围。患者2在治疗结束时观察到短暂性肝功能不全,最高为总胆红素25.0 μmol/L,丙氨酸氨基转移酶157 U/L,放疗结束与短暂性肝功能异常之间的持续时间约为1.5个月。患者3在治疗结束后1个月观察到总胆红素的升高,但因为该患者后续接受了化疗和靶向药治疗,因此无法评估与SBRT的可靠因果关系。患者4在随访期内肝功能均无异常。所有患者治疗前后的CHILD PUGH评分均为A级5分。
2.5 其他不良反应 所有患者进行了放疗急性反应及远期不良反应的临床评估,总体耐受性良好,均顺利完成放疗。3例患者在治疗中观察到Ⅰ度骨髓抑制,予对症治疗后恢复,未出现与治疗相关的严重不良反应。在随访期内,未出现治疗相关严重(≥3级)晚期并发症。
2.6 调查问卷结果 4例患者均完成了治疗相关主观感受调查问卷,在治疗过程中均非常积极,没有明显焦虑问题。问卷显示年龄较大患者较易产生焦虑,且难以配合指令,或许与理解能力或肺功能较差相关。患者3和患者4治疗期间调整呼吸方式为自由呼吸后,患者反应的舒适度更好。问卷评分情况见表4。

表4 患者主观感受调查问卷结果
3 讨论
立体定向放射治疗在无法切除的肝脏恶性肿瘤患者的局部治疗中临床效果显著[7-10],但肝脏SBRT在治疗时应用传统的图像引导方式很难将肿瘤从正常肝脏组织中分辨出来,而且肝脏SBRT会受靶区运动的干扰。目前认为最佳方法是对肿瘤进行内部实时追踪[11]。Calypso系统是实现实时追踪肿瘤的方法之一,其需在放疗前将3枚电磁转发器永久性植入肿瘤附近。Mueller等[12]报道经皮肝穿刺出血发生率为 1.2%,在本研究中通过17G引导针植入Calypso电磁转发器至肝内肿瘤旁,术中、术后均无明显出血等并发症发生。
目前肝恶性肿瘤CTV靶区勾画各放疗中心标准不一,一般为大体肿瘤靶区(gross target volume,GTV)外加0~5 mm形成[13-15],PTV的外扩范围根据所采用的技术以及所在放疗中心的实际情况确定,可以为CTV(或GTV)外扩5~20 mm[16]。但由于SBRT的分次剂量较高,GTV外的梯度剂量已经能够满足CTV的剂量覆盖,所以也可以不单独定义CTV。Rusthoven等[17]根据照射技术不同,将PTV定义为GTV横向外扩5~7 mm,纵向外扩10~15 mm,包括呼吸运动引起的内靶区和摆位引起的误差。一般而言,SBRT治疗若使用主动呼吸控制技术进行干预,所需的PTV外放边界是可以进一步缩小的。在Lu等[18]研究中,所有肝癌SBRT患者均使用主动呼吸控制技术进行CT扫描,配准融合形成内靶区,PTV为内靶区均匀扩展5 mm形成,结果显示上下方向11%的患者偏移超过5 mm,14%的患者在任何方向上运动偏移>5 mm。而且依靠主动呼吸控制技术的门控治疗并不适合心肺功能差的患者,且要在治疗前对患者进行呼吸训练[19]。在本研究中因为有Calypso系统实时跟踪定位肿瘤,PTV是通过在左右、前后和颅尾方向将CTV扩大5 mm边缘而形成的,使靶区更加精确。
从调查追踪系统对治疗时间的影响来看,患者1和患者2采用Calypso系统联合呼吸门控,其中位治疗时间短于患者3和患者4。所有患者系统记录的治疗时间存在个别明显延长现象,这是由于锥形束CT(Cone-beam CT,CBCT)扫描、图像配准或治疗床移位等原因导致,因此研究分析中采用中位时间而不是平均时间,以尽量减少这种偏差对结果分析的影响。每分次每个治疗野的治疗时间为十几秒左右,身体素质较好的年轻患者基本可以适应,但对老年患者屏气仍是挑战,因此对于肺功能差或训练依从性差的患者,在Calypso系统下自由呼吸也是可以的,舒适度和准确度可以同时得到兼顾。
研究表明,RILD与肝功能、Child-Pugh分级、肝脏受照体积密切相关[20-22]。因此对于RILD的预防, 很大程度上依赖于肿瘤靶区照射的准确性。本研究中,患者2在治疗结束时出现了短暂性的肝功能不全,但没有达到RILD的诊断标准。患者3在治疗结束后1个月观察到轻度总胆红素的升高,但因为该患者接受了其它系统治疗,因此无法确定是否由前期放疗导致。后续临床评估所有患者无远期RILD出现,且肝脏肿瘤大小稳定,虽然在最后1次随访中患者2出现了腹腔淋巴结转移和肺转移病灶增大,但是肝脏病灶依然稳定。
本中心总结了4例初治患者的经验,对Calypso系统辅助肝脏恶性肿瘤SBRT制定了如下流程(图3)。
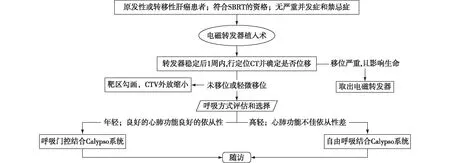
图3 Calypso系统辅助肝脏SBRT治疗流程
基于Calypso电磁追踪系统的肝脏SBRT可以使肿瘤靶区勾画范围更加精确,且为实时追踪肿瘤空间位置提供了一种直接有效的方法,值得推广。后续需要开展多中心研究增加样本量,进一步实践与探索Calypso系统在门控肝脏SBRT中的价值和意义。

