黄精冻干片质量标准的建立及其提取物薯蓣皂苷元抗肿瘤活性研究
徐雨生,高明菊,赵宁东,黄再强,田迎秋,胡展育,余正勇
(1.湖南农业大学农学院,长沙 410128;2.湖南杂交水稻研究中心杂交水稻国家重点实验室,长沙 410125;3.文山学院三七医药学院,云南 文山 663000)
黄精(Polygonatum sibiricumDelar. ex Redoute)为百合科黄精属多年生的草本植物,其根茎是药用成分最多的部位,主要分布在中国南部热带以外的地方[1]。黄精的药用历史已有2 000 多年,是目前中国常用的中药材之一。研究表明,黄精中含有很多对人体有利的成分,如薯蓣皂苷元、黄精多糖、强心苷、生物碱、氨基酸等[2,3],薯蓣皂苷元有抗炎和抗病毒的药理作用,黄精多糖有降血脂和血糖、抗动脉粥样硬化的药理作用,还有抗衰老、调节免疫等药理作用[4-6]。
目前黄精的开发利用现状存在诸多问题[7]:野生资源枯竭并且质量不稳定;人工栽培历史悠久但技术落后;对黄精的采收和加工等缺少科学依据。化学成分研究进展较明显,但是药效物质基础不明确;药品与保健品开发较少;行业规模与药材价格走势不明朗等问题[8]。薯蓣皂苷元和黄精多糖可能是黄精的质量标志性成分[9],但这些成分的有效性还需要进一步探究。
中国历代中医药典籍都有关于黄精及其炮制方法的记载,随着现代技术的发展,许多优良的炮制加工方法相继产生,如压力蒸气消毒干燥法、微波干燥法、综合评分干燥法等[10,11]。不同区域的黄精炮制加工各有其特点,在继承黄精传统加工工艺的同时,更需要不断创新和研究,为推行黄精饮片“安全、稳定、有效、可控”的质量生产管理规范化奠定基础。随着世界经济水平及人们生活水平的提高,消费者对冷冻干燥物资的需求量增大。近年来,电子计算机和传感测量技术使冷冻干燥技术的发展进入新时期,冷冻干燥中药饮片具有明显的市场优势[12]。
目前,建立中药材质量标准的方法主要有两种:采用分析仪器建立质量标准,能够相对较少地受个人主观因素的干扰;传统的人工经验判别法的优点是能够比较全面地反映与药物疗效相关中药材的质量,缺点是易受个人主观因素的干扰。中国虽然已经在中药质量控制和中药质量评价等方面取得较大的进步,定量控制药材的水平也在不断提高[13],但是总体水平还相对较低,与现代化还存在较大距离,需要进一步深入探究。
1 材料与方法
1.1 试验材料
所有样品均为黄精冻干片的粉末,分别来自云南省文山壮族苗族自治州文山市(简称云南文山)、云南省丽江市(简称云南丽江)、安徽省六安市(简称安徽六安)、广西省百色市(简称广西百色);氢氧化钠、丙三醇(天津市风船化学试剂科技有限公司);碘(成都市科隆化学品有限公司);碘化钾(上海市四赫维化工有限公司);酚酞(上海市四赫维化工有限公司);无水葡萄糖(北京世纪奥科生物技术有限公司);蒽酮(上海申博化工有限公司);浓硫酸(上海展云化工有限公司);3,5 二硝基水杨酸(成都市科隆化学品有限公司);甲醇、乙腈(均为色谱纯,天津市大茂化学试剂厂)。
1.2 性状鉴别
本试验参照《中华人民共和国药典》(2020 年版)(下文简称《中国药典》),根据3 批样品的形态、色泽、气、味、质地考察。
1.3 薄层色谱鉴别
称取黄精冻干片粉末1.0 g,放入锥形瓶内,加入20 mL 70%的甲醇溶液,再加热回流1 h,将处理好的样品抽滤,滤液需蒸干;待完全蒸干后再用去离子水10 mL 冲洗剩余的残渣,使残渣完全溶解,在锥形瓶内加入20 mL 正丁醇溶液,振荡3 min,重复提取1 次,合并正丁醇液,蒸干后剩余的残渣中加入1 mL 的甲醇溶液,使其溶解,待测。另外取冻干后的黄精对照药材1.0 g,同法制成对照品溶液。再用薄层色谱法进行试验,取供试品液和对照品液各10 μL,将其分别点在同一硅胶G 薄层板上,以石油醚(60~90 ℃)-乙酸乙酯-甲酸(5.0∶2.0∶0.1)作为展开剂,放入展开缸中展开,取出后晾干,用5%香草醛硫酸溶液喷在薄层板上,把薄层板放在烘箱中,温度调到105 ℃,待薄层板有清晰的斑点显示后,对其进行视检即可。
1.4 显微鉴别法
通过显微镜(尼康E400 型)对样品进行照片采集。
1.5 水分检测
将样品盘放入水分测定仪内,置零,在样品盘中放入冻干后的黄精粉末5 g,记录数据。计算出供试品的含水量(%)。
1.6 总灰分测定
按照《中国药典》中有关总灰分的测定方法,取粉碎至细的黄精冻干片粉末2.0 g,放在灼烧到恒定重量的坩埚内,称量其重(要求准确至0.01 g),慢慢炽灼,随时观察。灼烧至完全炭化后,慢慢升高温度到600 ℃左右,使灼烧后的黄精冻干粉末完全灰化到恒定的重量。最后根据残渣重量,计算出供试品内总灰分的含量。
1.7 醇溶性浸出物测定
按照《中国药典》(通则2201 热浸法)浸出物测定法进行测定。称取黄精冻干片粉末2 g,置250 mL的锥形瓶中,加50%乙醇50 mL,密塞,称重后静置1 h,连接回流冷凝管微沸1 h,放冷取下锥形管,称重后密塞,50%乙醇补足减重,摇匀,过滤,量取滤液25 mL 置已干燥至恒重的蒸发皿中,105 ℃下干燥3 h 后,干燥器中冷却30 min,精密称重后计算即可。
1.8 总多糖含量的测定
1.8.1 对照品溶液的制备 105 ℃下干燥至恒重的无水葡萄糖对照品33 mg,置100 mL 容量瓶中,加水溶解并定容至刻度线,摇匀,即得。
1.8.2 标准曲线的绘制 量取葡萄糖标准品配制的溶液(0、0.2、0.4、0.6、0.8、1.0 mL)至10 mL 具塞刻度试管,加去离子水至2.0 mL,摇匀,加0.2%蒽酮-硫酸溶液至刻度线并混匀,冰水浴至冷,取出即可。按照紫外-可见分光光度法(通则0401),计算绘制标准曲线。
1.8.3 供试品溶液的制备 称取4 个不同产地黄精冻干片粉末0.25 g,至圆底烧瓶中(60 ℃干燥至恒重),加80%乙醇150 mL 后加热回流1 h(水浴),趁热过滤,残渣用80%热乙醇洗涤3 次(每次10 mL),合并滤液,放冷后转移至250 mL,加水至刻度线摇匀。精确量取上述混合溶液1 mL,置10 mL 具塞干燥试管,加去离子水至2.0 mL 后,再加0.2%蒽酮-硫酸溶液至刻度线并混匀(以去离子水代替供试品为空白),于582 nm 波长下测定吸光度,计算黄精冻干片的总多糖。
1.9 薯蓣皂苷元含量的测定
1.9.1 波长的选择 色谱柱:Hypersil ODSC-18 色谱柱(4.6 mm×250 mm,5 μm);流动相:乙腈-超纯水(75∶25,V/V)进行梯度洗脱,柱温为30 ℃,流速为1 mL/min,进样量为10 μL,检测波长是190~440 nm;检测波长的选择:将各对照品溶液进行高效液相扫描,测出对照品溶液的最大吸收值。
1.9.2 对照品溶液制备 称取薯蓣皂苷元(批号为JS90124)1.08 mg,用50%乙醇溶液溶解、超声处理至溶解,然后定容到2 mL,作为对照品,最后用0.45 μm 微孔滤膜过滤后备用,待HPLC 测定。
1.9.3 供试品溶液制备 称取云南文山黄精冻干粉末1.000 g 于150 mL 具塞锥形瓶中,加50%乙醇溶液50 mL,密封,50 Hz 超声仪中超声处理30 min 后取出,放冷,用50%乙醇补足失重,振摇后过滤,滤液保留,通过0.45 μm 微孔滤膜即得供试品溶液。
1.9.4 样品含量测定 称取4 个不同产地的冻干黄精饮片粉末2 g,按照“1.9.3”的制备方法进行制备,依据上文所述的色谱条件进样测定并计算薯蓣皂苷元的含量。
1.10 薯蓣皂苷元对3 种癌细胞的影响
以阿霉素为对照品,采用噻唑蓝(MTT)法考察了黄精薯蓣皂苷元对A431(人表皮癌细胞)、H1975(人肺腺癌细胞)和Ramos(人B 淋巴细胞瘤细胞)的抗肿瘤活性。3 种细胞培养成熟后用酶联检测仪测定各孔吸光度,选择570 nm 波长,以RPMI-1640 培养液做空白对照,测各孔的吸光度。细胞生长抑制率=(对照组吸光度-试验组吸光度)/对照组吸光度×100%。
2 结果与分析
2.1 性状鉴别
由于4 个样品中有2 个样品来自同一省份,故选择3 个来自不同省份的样品。黄精冻干片性状鉴别结果(图1)显示,本品的性状为淡黄色至黄色的中空泡沫状薄片,切片后切面为角质样,有很多淡黄色的筋脉小点;气微,味苦但是略回甜,嚼之具有黏性;质脆,易折断。

图1 3 批样品的切片
2.2 薄层色谱鉴别
薄层色谱鉴别结果(图2)显示,在与黄精对照药材色谱图相对应的位置上,4 个产地的黄精冻干片均能显示出相同颜色的斑点,重现性良好。

图2 黄精冻干片薄层色谱图
2.3 显微鉴别
本品粉末为淡黄色至黄色。显微鉴别结果(图3)显示,表皮细胞的外壁较厚,薄壁组织散有大量的黏液细胞,内含的草酸钙针晶束散在,针晶长18~88 μm。有很多的维管束散列,大多数为周木型。

图3 黄精冻干粉末
2.4 含水量的测定
测定了4 个不同产地的黄精冻干片含水量(表1),其含水量均值为2.8%~4.7%,均没有超过5.0%。根据试验结果,可将本品含水量限度定为不得超过5.0%纳入标准。
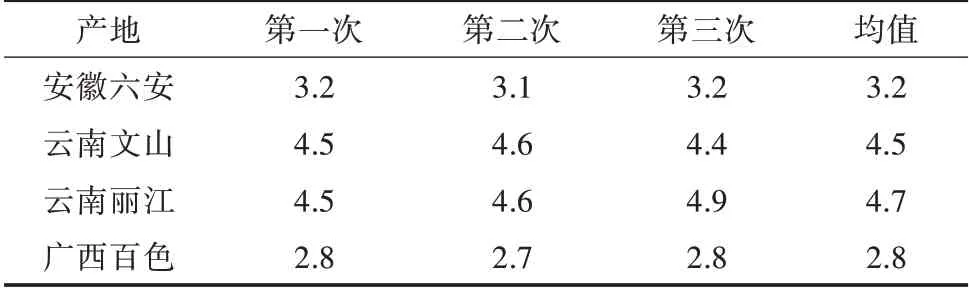
表1 不同产地黄精冻干片含水量 (单位:%)
2.5 总灰分含量的测定
根据测定所得残渣重量,计算出本试验中4 个不同产地的黄精冻干片的总灰分。结果(表2)显示,4 个不同产地的黄精冻干片总灰分范围为1.9%~3.4%(均没有超过4.0%)。根据测定结果,可将本品总灰分限度不得超过4.0%纳入标准。
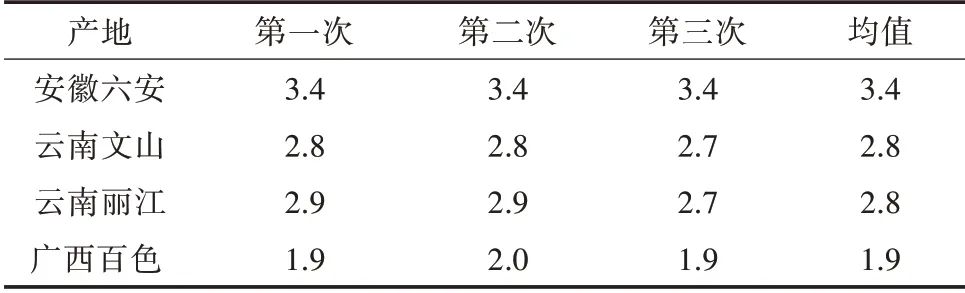
表2 不同产地黄精冻干片总灰分含量 (单位:%)
2.6 醇溶性浸出物的测定
根据相关数据计算乙醇浸出物含量,结果(表3)显示,4 个不同产地的黄精冻干片的醇溶性浸出物在72.19%~78.99%(均未低于70.0%)。根据测定结果,可将乙醇浸出物限度定为不低于70.0%纳入标准。

表3 不同产地黄精冻干片乙醇浸出物含量(单位:%)
2.7 总多糖含量的测定
2.7.1 标准储备液标准曲线的绘制 结果(图4)显示,线性方程为y=5.732 3x-0.033 3,r=0.998,结果表明无水葡萄糖在0.033~0.198 mg 范围内,线性关系良好。

图4 标准储备液的标准曲线
2.7.2 样品含量的测定 测定了4 个不同产地的黄精冻干片中总糖的含量,结果(表4)显示,其总糖都不低于7.0%。根据测定结果,可将本品总糖的限度定为不得少于7.0%纳入标准。
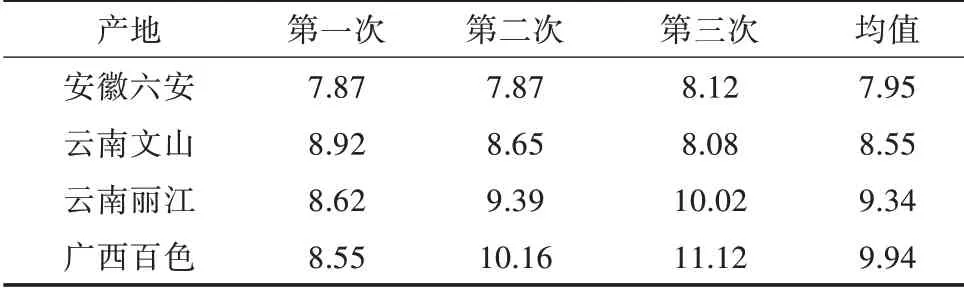
表4 不同产地的黄精冻干片总多糖含量(单位:%)
2.8 薯蓣皂苷元含量的测定
2.8.1 波长的选择 在最大吸收波长440 nm 处响应值较强,因此选择测定波长为440 nm。
2.8.2 黄精薯蓣皂苷元对照品HPLC 色谱图 用HPLC 检测已制备好的对照品溶液,得到含有明显薯蓣皂苷元主峰的色谱图(图5),图5 中的峰1 为薯蓣皂苷元色谱。

图5 黄精薯蓣皂苷元对照品HPLC 色谱图
2.8.3 黄精薯蓣皂苷元供试品HPLC 色谱图 用HPLC 检测已制备供试品溶液,得到含有多条明显锋的高效液相色谱图(图6),其中含有对应对照品溶液的明显薯蓣皂苷元峰,峰1 为薯蓣皂苷元。
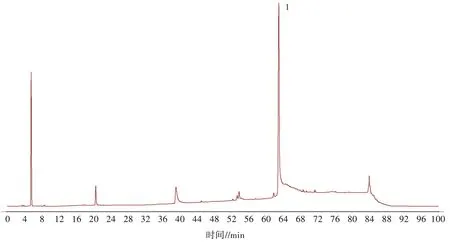
图6 黄精薯蓣皂苷元供试品HPLC 色谱图
2.8.4 样品含量测定 测定了4 个不同产地的黄精冻干片中薯蓣皂苷元的含量,结果(表5、表6)显示,r=0.999 2,线性范围为1.08~10.80 mg/mL,4 个不同产地的黄精经该法冻干后薯蓣皂苷元都不低于0.18%。根据测定结果,可将本品薯蓣皂苷元的限度定为不得少于0.18%纳入标准。

表5 不同产地黄精薯蓣皂苷元方程及其范围

表6 不同产地黄精的薯蓣皂苷元含量
2.9 黄精提取物薯蓣皂苷元对3 种癌细胞的影响
试验结果(表7)显示,薯蓣皂苷元对A431(人表皮癌细胞)细胞抑制活性与阿霉素相当,即抗A431肿瘤活性较佳,但是对H1975(人肺腺癌细胞)、Ra⁃mos(人B 淋巴细胞瘤细胞)均无抗肿瘤活性,为后期开发纯天然抗人表皮癌细胞新药提供一定的试验数据。

表7 薯蓣皂苷元的抗肿瘤活性(单位:L/(mol·cm))
3 讨论
本试验结果中4 个不同产地的黄精冻干片各种化学成分数值均在《中国药典》规定范围内,说明此项研究可为后续研究冻干黄精的药理活性、临床应用优势等提供理论依据,同时也可为后续普通炮制黄精提供借鉴。
试验发现不同产地黄精冻干片的水分、总灰分、醇溶性浸出物、总糖、薯蓣皂苷元含量存在一定差异,但测定结果在《中国药典》规定范围内。4 个产地的冻干黄精的含水量平均值为3.80%,总灰分平均值为2.70%,醇溶性浸出物平均值为75.78%,总糖平均值为8.95%,薯蓣皂苷元含量不低于0.18%。与《中国药典》要求相比,水分测定值虽然偏低,但在要求范围内,说明冻干后的黄精有一般冻干产品延长保存时间的优点。前期较少文献报道黄精冻干饮片的质量标准草案,因此,在撰写黄精冻干片的质量标准草案中,建议黄精冻干片含水量不超过5.0%,总灰分不超过4.0%,醇溶性浸出物含量不少于70.0%,总糖不少于7.0%,薯蓣皂苷元含量不低于0.18%。黄精冻干饮片中薯蓣皂苷元含量差异不大,但是相较其他炮制方法,冻干黄精饮片粉末的薯蓣皂苷元含量较高,且薯蓣皂苷元抗A431 肿瘤活性较佳,为后期冻干黄精质量标准的研究及补充提供了一定的试验依据。

