常压下玉米秸秆液化工艺的优化及其生物油分析
张 妍, 王慧乐, 赵会芳, 李 静, 童 欣, 刘 忠
1. 浙江科技学院浙江省废弃生物质循环利用与生态处理技术重点实验室, 浙江 杭州 310023
2. 天津科技大学天津市制浆造纸重点实验室, 天津 300457
引 言
常压催化液化技术是木质生物质资源综合利用的有效途径[1], 是在常压环境下, 通过催化剂、 液化剂作用, 使生物质转化成具有广泛分子量分布的液体混合物的热化学反应[2]。 此技术具有很多优势, 如产物可代替部分传统石化化学品、 液化过程中的设备要求较简单、 条件相对温和等。 所得液化产物具有高活泼性, 能够制备多种产品应用于多个领域, 因此科研工作者对生物质液化过程中使用的催化剂、 液化剂以及如何增加液化效率做了深入探究。
李学琴等研究了在最佳工艺条件为液化剂乙二醇(EG)、 聚乙二醇、 丙三醇的体积为1∶1.5∶1.5, 催化剂固体酸量为12 g, 液化温度为135 ℃, 反应时间为70 min时, 玉米秸秆最大液化得率为72.3%[3]。 Sabzoi等探索了以乙醇为溶剂将玉米秸秆转化为生物油的过程, 研究表明生物油得率随温度升高和时间的延长而增加, 直至达到特定水平, 然后开始下降[5]。 Zhang等探究了四种多元醇液化剂1,4-丁二醇及EG分别液化玉米秸秆, 结果表明, 在PG存在下, 秸秆在最适温度180 ℃下的得率达到99.18%, 高于其他的三种液化剂[5]。
常压液化技术目的是将木质生物质最大程度地转化为有机物质(液态), 然后加以利用。 故而改变液化过程的条件, 以便获取不同功能的液化产品, 了解液化所得生成物的分子结构和分布非常关键。 本实验利用单因素法, 针对玉米秸秆常压催化液化工艺进行优化, 并对此优化条件下所得生物油通过TGA、 GC-MS和NMR等分析手段对其热解特性和主要组成成分进行了探索, 为后续改善油品质量、 提高非木材生物质高效转化利用以及探索多元醇液化机理打下夯实的基础。
1 实验部分
1.1 材料
原料: 玉米秸秆(天津市郊区某农田), 粉碎后过筛, 留20~80目的部分。
主要试剂: 1,4-二氧六环、 PG、 DEG、 浓磷酸、 吡啶, 分析纯(国药集团化工有限公司); 氘代丙酮(美国Cambridge Isotope Laboratories Inc.)、 硅烷化试剂(TMCS 10%+BSTFA 90%)(东京化成工业株式会社), 色谱纯。
主要仪器: PARR-4848型高压反应釜(PARR, 美国); TGA-Q50型热重分析仪(Shimadzu, 日本); 7890A型气相色谱仪-5975C型质谱仪(Agilent, 美国); AV III 400M型核磁共振波谱仪(Bruker, 德国)。
1.2 方法
1.2.1 玉米秸秆的液化
取玉米秸秆粉、 催化剂和液化剂依次加入到高压反应釜内, 混合均匀, 开始液化实验。 转速设成338 r·min-1, 达到预设反应时间后, 反应完成, 冷却。
1.2.2 液化得率的计算[6]
使用80% 1,4-二氧六环溶液将冷却后液化产物转移, 搅拌、 离心、 旋蒸后获得生物油。 采用旋蒸回收的1,4-二氧六环溶液多次洗涤离心后的固体, 直到滤液无色, 恒重, 称量, 最后计算其液化得率, 如式(1)所示。
(1)
式(1)中:Y为液化得率, %;m1为液化残渣质量, g;m0为玉米秸秆绝干质量, g。
1.2.3 液化条件的优化
利用单因素法, 液化温度140~190 ℃(升温间隔10 ℃), DEG与PG混合比例15∶1, 9∶1, 6∶1, 4∶1, 2∶1, 1∶1, 1∶2, 1∶4和1∶6, 液固比1∶1, 3∶1, 5∶1, 7∶1和9∶1, H3PO4用量2%~16%(间隔2%), 反应时间15~90 min(间隔15 min)。
1.2.4 生物油的检测分析
1.2.4.1 TGA分析[7]
利用热重分析仪检测生物油挥发降解特性, 以10 ℃·min-1从30 ℃加至600 ℃。
1.2.4.2 GC-MS分析[6]
硅烷化方法: 称生物油20 mg, 溶剂用N2吹干, 40 ℃干燥30 min后, 注入80 μL吡啶、 150 μL硅烷化试剂, 进行硅烷化处理(70 ℃, 45 min)后, 过滤。
GC设定: 气流量、 分流比、 进样口温度、 进样量、 溶剂延迟依次设置1.00 mL·min-1、 10∶1、 300 ℃、 0.2 μL、 3 min。 以5 ℃·min-1从80.0 ℃初始温度(停滞3 min)升到150 ℃, 以10 ℃·min-1升至300 ℃(停滞5 min), 运行时间共37 min。
MS设定: 四级杆和离子源温度依次是150和230 ℃。
1.2.4.31H-NMR分析
约10 mg生物油, 溶解于氘代丙酮0.5 mL中, 扫描8次。
1.2.4.413C-NMR表征
约100 mg生物油, 溶解于氘代丙酮0.5 mL中, 扫描约20 000次。
2 结果与讨论
2.1 玉米秸秆液化影响因素的分析
2.1.1 温度对液化得率的影响
表1为液化温度对玉米秸秆液化得率的影响, 从140 ℃升至170 ℃, 液化得率明显提高, 从75.65%增加到98.57%。 提高液化温度, 促进了催化剂H3PO4的酸性基团迅速渗透到纤维组织中, 破坏了分子链及纤维素的晶体结构, 提高体系中液化速率。 当高于170 ℃时, 液化得率呈减小的趋势, 即190 ℃时, 液化得率减小到92.72%, 因为高温下促使液化产物间发生聚合、 炭化及粘壁现象。

表1 液化温度对液化得率的影响
2.1.2 DEG和PG混合比例对液化得率的影响
表2为液化剂DEG和PG混合比例对液化得率的影响, DEG∶PG从15∶1到1∶2, 随着复配液化剂中PG所占比例增大, 液化得率也随之增加; 当复配比例为1∶2时, 得率最高为99.40%。 这是由于相同质量PG所含的羟基要高于DEG, 使反应发生地更剧烈[8]。 当持续增加PG用量时, 得率呈减小的趋势; 当两者比例为1∶6时, 得率为98.52%。 此时反应已达到饱和, 某些物质可能会发生聚合产生残渣。

表2 复配比例对液化得率的影响
2.1.3 液固比对液化得率的影响
表3为液固比对液化得率的影响, 当液固比1∶1时, 液化得率较小, 为43.92%, 不利于秸秆的液化; 直至液固比增加至5∶1时, 液化得率最大, 为99.37%; 原因是液固比越大, 体系中液化剂的加入量越高, 大量多元醇可使秸秆浸润地更彻底, 促进液化剂向其内部纤维结构中渗透, 加快反应的进行。 但当液固比继续升高时, 得率却有所下降, 这可能是因为过多的液化剂和秸秆降解的小分子间发生聚合生成了不可溶的残渣[10], 另外, 液固比上升也会增加液化时的成本。
2.1.4 H3PO4用量对液化得率的影响
表4为催化剂加入量对液化得率的影响, 当H3PO4加入量较少时, 液化速率较慢, 得率也很低。 随着H3PO4用量加大, 得率先增大后缓慢减小, 在10%时出现拐点, 得率最高为99.38%; 继续加大其用量, 得率稍稍减小, 原因是过多的催化剂会造成某些较复杂的副反应发生, 如木素降解生成许多不稳定的中间产物, 这些产物在液化后期聚合产生残渣, 系统中酸浓度越高, 聚合作用就越突出。 故体系中, H3PO4不仅促进秸秆的降解, 也促进降解产物间的聚合作用。 另外, 过多的酸会加剧生物油的酸性、 成本的提高和化学品的浪费。
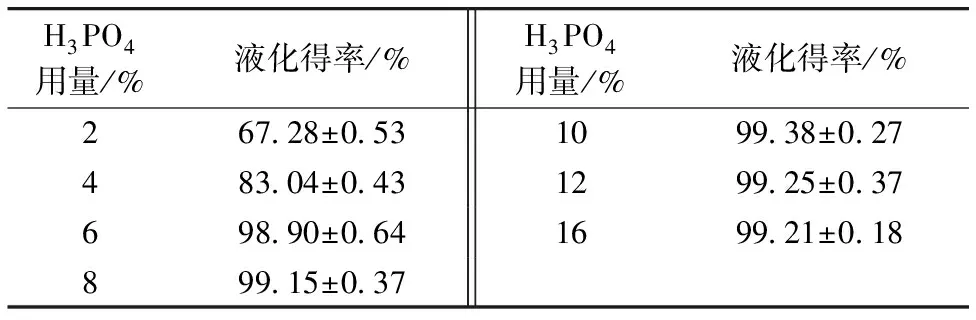
表4 催化剂用量对液化得率的影响
2.1.5 反应时间对液化得率的影响
表5为反应时间对液化得率的影响, 反应时间从15 min延长到45 min, 液化得率从97.75%增至99.50%, 当反应时间延长, 促使秸秆、 H3PO4和多元醇接触更充分, 进一步加快秸秆反应进程。 反应时间持续延长, 液化速率变慢, 得率也随之减小, 延长反应时间导致产物间产生聚合增大残渣率。
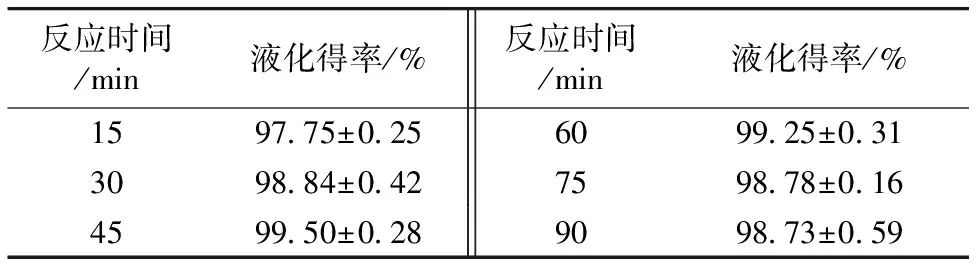
表5 反应时间对液化得率的影响
本实验玉米秸秆液化时优化的工艺参数: 液化温度为170 ℃, 液化剂DEG∶PG=1∶2, 液固比为5∶1, 催化剂用量为10%, 反应时间为45 min; 此时液化得率高达99.50%。
2.2 生物油的TGA分析
图1为生物油TG-DTG曲线图, 生物油中各组分碳数不同则沸点不同, 对应不同的信号峰[10]。 30~150 ℃间DTG上存在两个不同强度波谷, 生物油失重率约40%, 这是水分或轻石脑油及炼油气等碳数低于10的轻质油挥发造成的。 150~350 ℃间DTG上存在多个不同强度波谷, 失重率约40%, 说明生物油中含有部分碳数在10~25间的化合物(如柴油、 煤油、 重质油)[11]。 350~450 ℃间DTG上未发现明显波谷, 失重率约2%, 说明其含有较少润滑油或重燃料油等碳数在25~35间的物质。 450~600 ℃间DTG上存在一个弱波谷, 失重率约3%, 主要是碳数大于35的沥青、 胶质及蜡等化合物的热解。 生物油最终残炭量约为15%。

图1 生物油热失重的TG-DTG曲线
2.3 生物油的GC-MS分析
生物油总离子流图(见图2)中每个吸收峰对应的质谱图通过分析, 判别出生物油所含的主要成分及通过面积归一化方法算出其相对含量见表6。 某些色谱峰的峰面积较小或匹配度较差, 使得这些化合物不能辨别识出, 本实验辨别出的有机物是39种, 几乎都含有元素O, 即生物油中含氧量高, 其稳定性差[12]。 表6中, 生物油中醇类所占比例最大, 为70.70%; 其中含有10.64% PG和30.61% DEG, 部分是在液化中秸秆降解生成的, 还有部分可能是未参与反应的液化剂。 生物油含有25.63%的酚类物质; 在多元醇作用下, 使木素中部分醚键发生断裂, 特别是β-O-4键, 使其断裂降解为酚类物质, 即这些物质主要源于组成木素基本结构苯丙烷的裂解[13]。 生物油中还包含有机酸(2.80%)和醚类(0.64%), 这些酸和醚源于碳水化合物的降解; 这些酸也造成生物油呈酸性和腐蚀性。 此外, 生物油中还含有少量的酯类(0.10%)和酮类(0.13%)。

图2 生物油的GC-MS总离子流图

表6 生物油的主要化学族类含量分布
2.4 生物油的1H-NMR分析


图3 生物油的1H-NMR图
2.5 生物油的13C-NMR分析
图4表示生物油的碳谱图。 在δ为29.28和206.59 ppm附近的信号主要是溶剂氘代丙酮的体现[14]。δ=180~160 ppm主要是酰基与羧基的信号[16],δ=160~120 ppm主要为芳香C的信号,δ=110~60 ppm分布碳水化合物和糖类C的信号,δ=40~10 ppm分布烷烃C的信号。 但在56.3 ppm附近无信号, 说明甲氧基在液化体系中去掉, 经酸催化多元醇液化后, 玉米秸秆发生剧烈的降解生成了低分子物质。

图4 生物油的13C-NMR图
3 结 论
玉米秸秆液化时优化条件: 液化温度170 ℃, DEG∶PG=1∶2, 液固比5∶1, H3PO4用量10%, 反应时间45 min, 液化得率达99.50%。 此时液化所得生物油含80%以上碳数小于25的化合物; 组分复杂, 含70%以上醇类、 25%以上酚类及少量的有机酸、 醚类、 酯类和酮类物质, 含氧量高, 稳定性差。 另外, 明确了构成生物油的各种质子和碳原子的分布, 有利于对其分子结构进行深入研究。

