钇90 微球选择性内放射治疗在欧洲9 个国家的报销政策研究
——一项基于DRGs 的分析
王春露,于保荣
1 SynergusRWEAB,Stockholm 11331,Sweden;2 对外经济贸易大学保险学院,北京 100029
1 研究背景
肝脏恶性肿瘤包括原发性肝癌[如肝细胞癌(hepatocellular carcinoma,HCC)]和转移性肝癌[如转移性结直肠癌(metastatic colorectal cancer,mCRC)等][1]。以原发性肝癌为例,据GLOBOCAN 全球癌症统计数据,其在2020 年全球范围内是第6 大常见癌症和第3 位癌症死亡原因,其中新发病例905 677 例,新增死亡病例830 180例[2]。在我国,原发性肝癌是第5 大常见癌症和第2 位癌症死亡原因,2020 年新发病例410 038 例,新增死亡病例391 152 例[3]。
80%以上肝癌患者确诊时已处于中晚期,已错失手术切除或肝移植机会,需以非手术方式或通过局部疗法进行转化治疗,以重新获得手术机会[4]。居高不下的发病率和有限的治疗手段的背后,是患者及其家属沉重的经济负担,且随病情进展逐年快速增长。据国家肿瘤中心统计[5],肝癌患者医疗支出由2002 年的人均21 950 元增长至2011 年的40 386 元,并且在2014 年跃升至53 220 元。另据童叶青等[6]研究统计,2017 年湖北省肝癌患者的年人均医疗支出为92 015 元,是其家庭年可支配收入的2.17 倍,高于肺癌等其他重大疾病。
钇90 微球(yttrium 90 microspheres)选择性内放射治疗(selective internal radio therapy,SIRT)属于肝肿瘤局部治疗,与经导管动脉化疗栓塞(transcatheter arterial chemoembolization,TACE)方法类似。在欧洲,放射性微球最早于2002 年10 月获得CE 认证,用于治疗不可手术的晚期肝癌患者。放射性微球被众多国家和地区的卫生技术评估(health technology assessment,HTA)机构推荐用于临床使用,且其可获得医保部门的报销已有20 年的历史[7-10]。2021 年该医疗技术在中国完成首例特许准入[11]。
按疾病诊断相关分组(diagnosis-related groups,DRGs)支付方式是国际上重要的支付方式和医疗管理工具[12-13]。《国家医疗保障局关于印发DRG/DIP 支付方式改革三年行动计划的通知》[14]中提到:“到2025 年底,DRG/DIP 支付方式覆盖所有符合条件的开展住院服务的医疗机构,基本实现病种、医保基金全覆盖。”通过研究和探讨欧洲9个国家利用DRGs 支付方式对于SIRT 和相关产品的报销经验,分析其对医疗行为和产出的影响,及对医院管理和医保基金管理的影响,为不同参与方(如医生、医疗机构、医保支付方、药品监管方)以及相关企业的决策提供借鉴。
本研究选取9 个欧洲国家,包括德国、英国、法国、意大利、西班牙、瑞典、丹麦、芬兰、挪威。前5 个国家为欧洲人口数量多、经济体量大的5 个国家;后4 个国家均为北欧国家,其地理位置、人口数量、医疗水平、社会发展水平等方面高度相似。SIRT 在临床应用中涉及诸多流程,包括多学科会诊、预评估(肝肾功能、影像学评估、锝-99m-聚合白蛋白肺灌注显像模拟)、确定注射剂量、通过介入手术注入放射性微球、术后验证等。本研究中仅包括通过介入手术注入放射性微球步骤[7,13]。
2 研究方法
本研究采用DRGs 的分析方法(见图1)[15],确定钇90 微球SIRT 相关信息:①疾病诊断分类及代码[16]。②操作编码。③患者基本信息(性别、年龄、手术类型、住院天数等)。
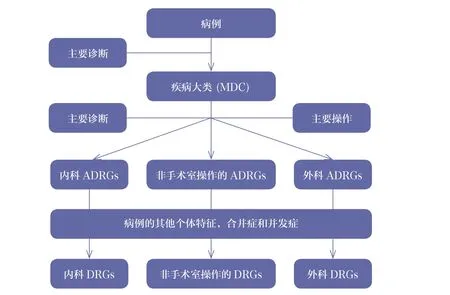
图1 DRGs 分组原理
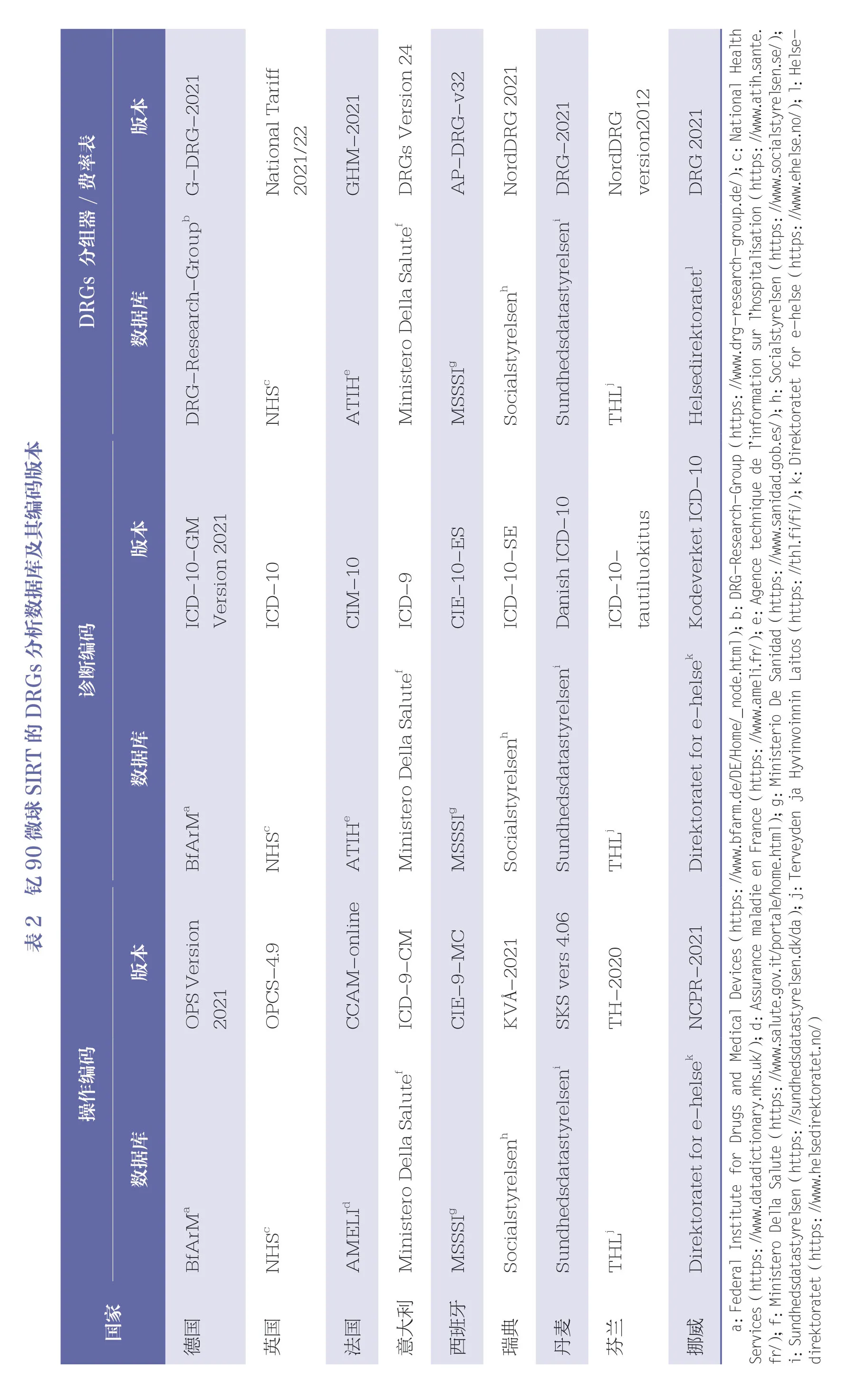
疾病诊断分类及代码来自于文献报道[7,17],代码根据各国的官方诊断代码库进行修订;操作编码检索自各国官方编码库;患者基本信息来自于文献报道[7]、专家共识[1](见表1)。在上述信息基础上,应用分组器进行DRGs 归类,并在各个国家的官方数据库和医院数据库查询以确定DRGs 编码、名称、权重值、费率,以及其他追加报销(addon reimbursement)方式。本研究中所选择的各种编码库、代码库和DRG 分组器见表2。对于德国、英国和法国,以操作编码进行相关操作的用量分析(volume analysis);对于德国和法国,对相关DRGs 进行成本矩阵分析(cost-matrix analysis)。
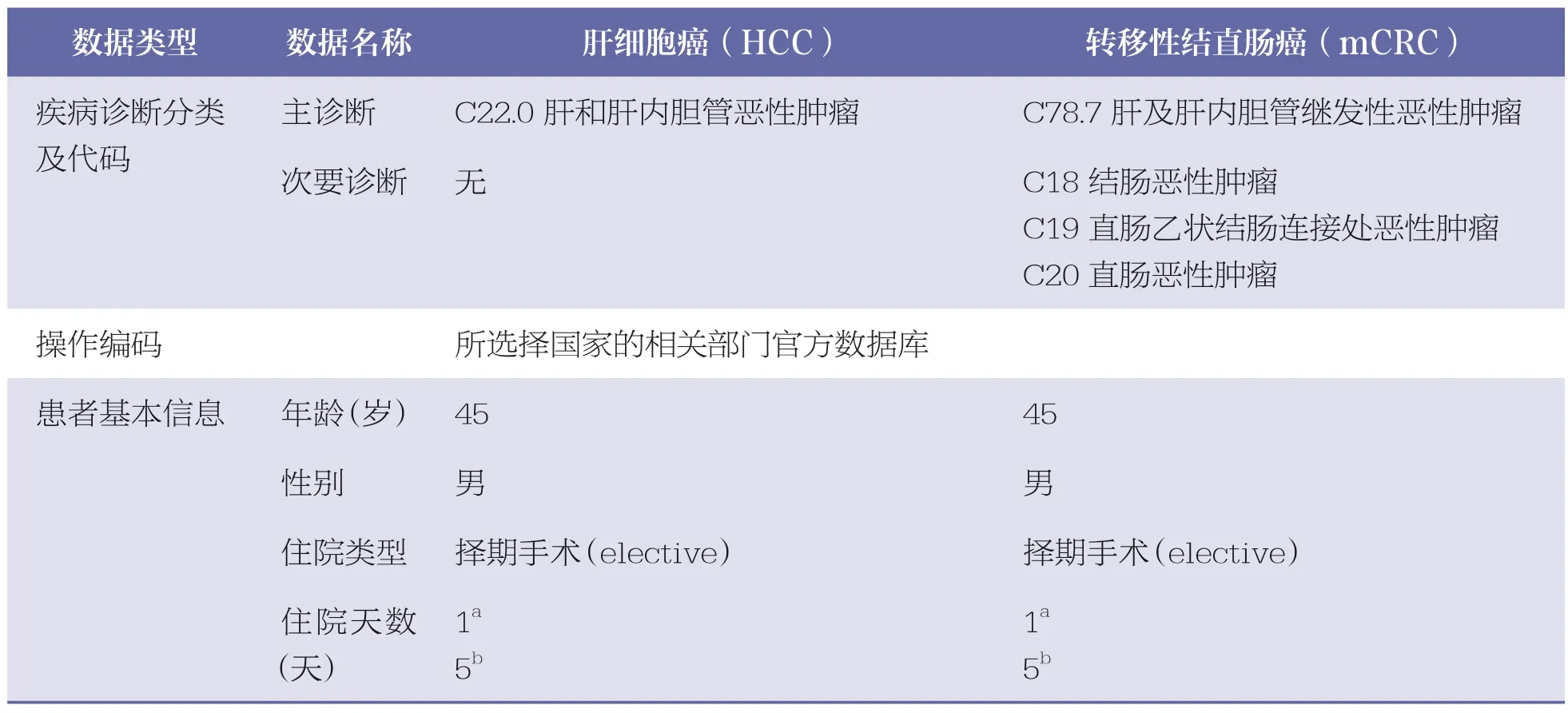
表1 钇90 微球SIRT 的DRGs 分析参数选择
3 结果
3.1 研究国家的基本信息
表3 对比了本研究所选择的欧洲9 个国家和我国在2020 年的基本情况与原发性肝肿瘤情况。从人口总量来看,德国、英国、法国、意大利、西班牙5 国约在4600 万~8300 万人之间,瑞典、丹麦、芬兰、挪威4 国约在550 万~1000 万人之间,均少于我国,但人均国内生产总值(GDP)高于我国。从疾病谱来看,原发性肝癌在欧洲9 个国家的肿瘤新发病例排名11~18 位,死亡病例排名5~9 位,与我国的排名情况有很大差异。10 个国家原发性肝癌患者死亡病例总量在癌症总死亡病例中的占比均高于新发病例占比。
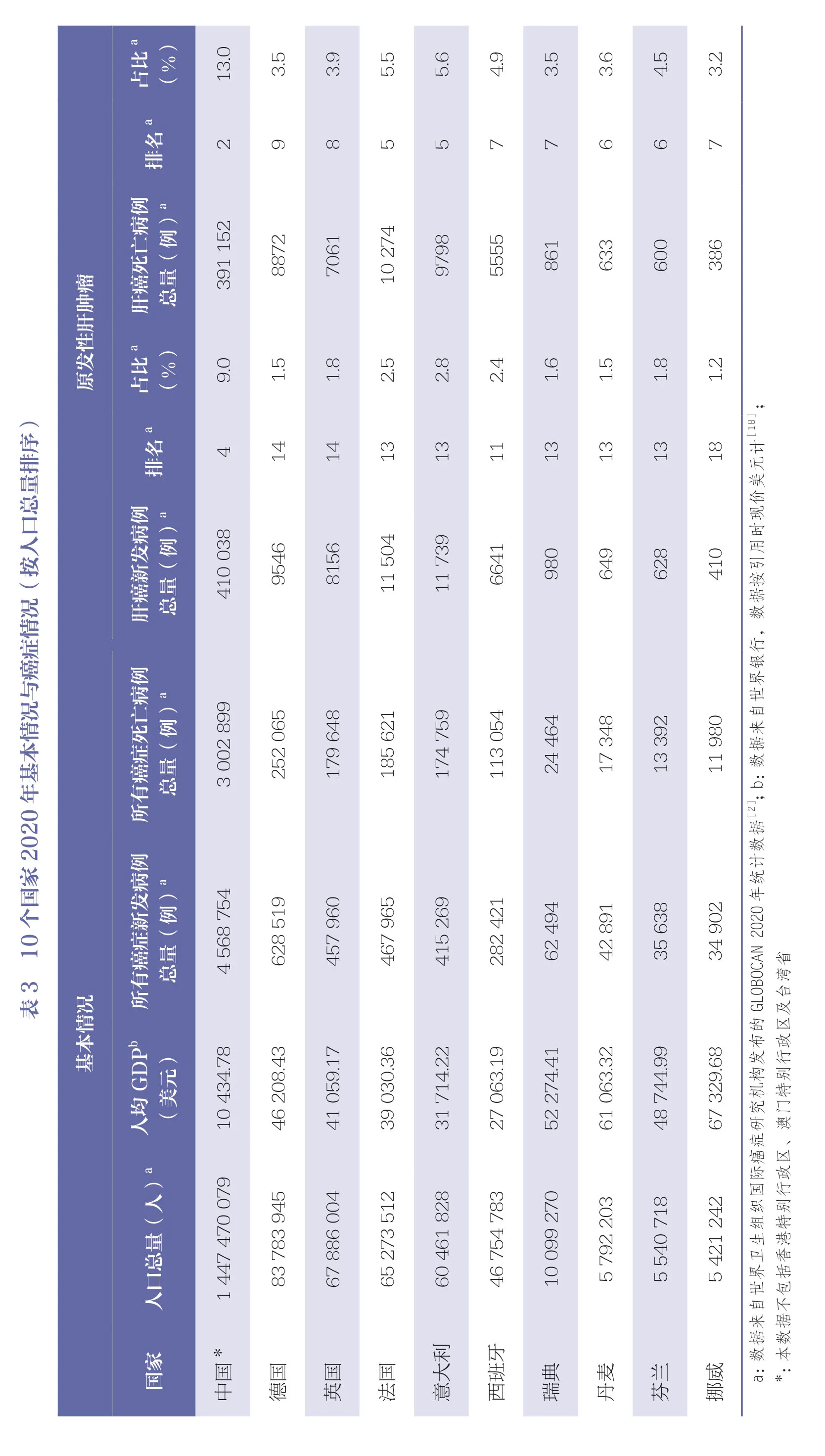
3.2 钇90 微球SIRT 的HCC 和mCRC 2 个适应症诊断编码、操作编码及名称
欧洲9 个国家的疾病诊断编码均以“国际疾病分类(ICD)”为基础,除意大利和西班牙采用ICD-9 版本外,其他国家均以 ICD-10 版本为基础进行修订,见表2。ICD-9 的诊断编码中“155”对应ICD-10 的“C22 肝和肝内胆管恶性肿瘤”;“155.2”对应ICD-10 的“C78.7 肝及肝内胆管继发性恶性肿瘤”;“153”对应ICD-10 的“C18 结肠恶性肿瘤”;“154”对应ICD-10 的“C19 直肠乙状结肠连接处恶性肿瘤”和“C20 直肠恶性肿瘤”。
德国、瑞典、丹麦、芬兰、挪威5 个国家针对钇90 微球SIRT 设置特异性的操作编码或者编码组合;英国和法国针对SIRT 设置特异性的操作编码或者编码组合,但未区分钇90 和其他放射性微球;意大利和西班牙未设置SIRT 的特异性编码,以非特异性编码组合92.28(放射性核素注射或滴入)+38.91(动脉导管插入术)代替。各国操作编码及其名称见表4。
3.3 SIRT 的DRGs 分组、编码、名称
在检索到的诊断编码和操作编码基础上,结合患者基本信息,利用表2 中的分组器分组或者数据库进行手工检索,得到9 个国家的DRGs 分组、编码、名称见表4。
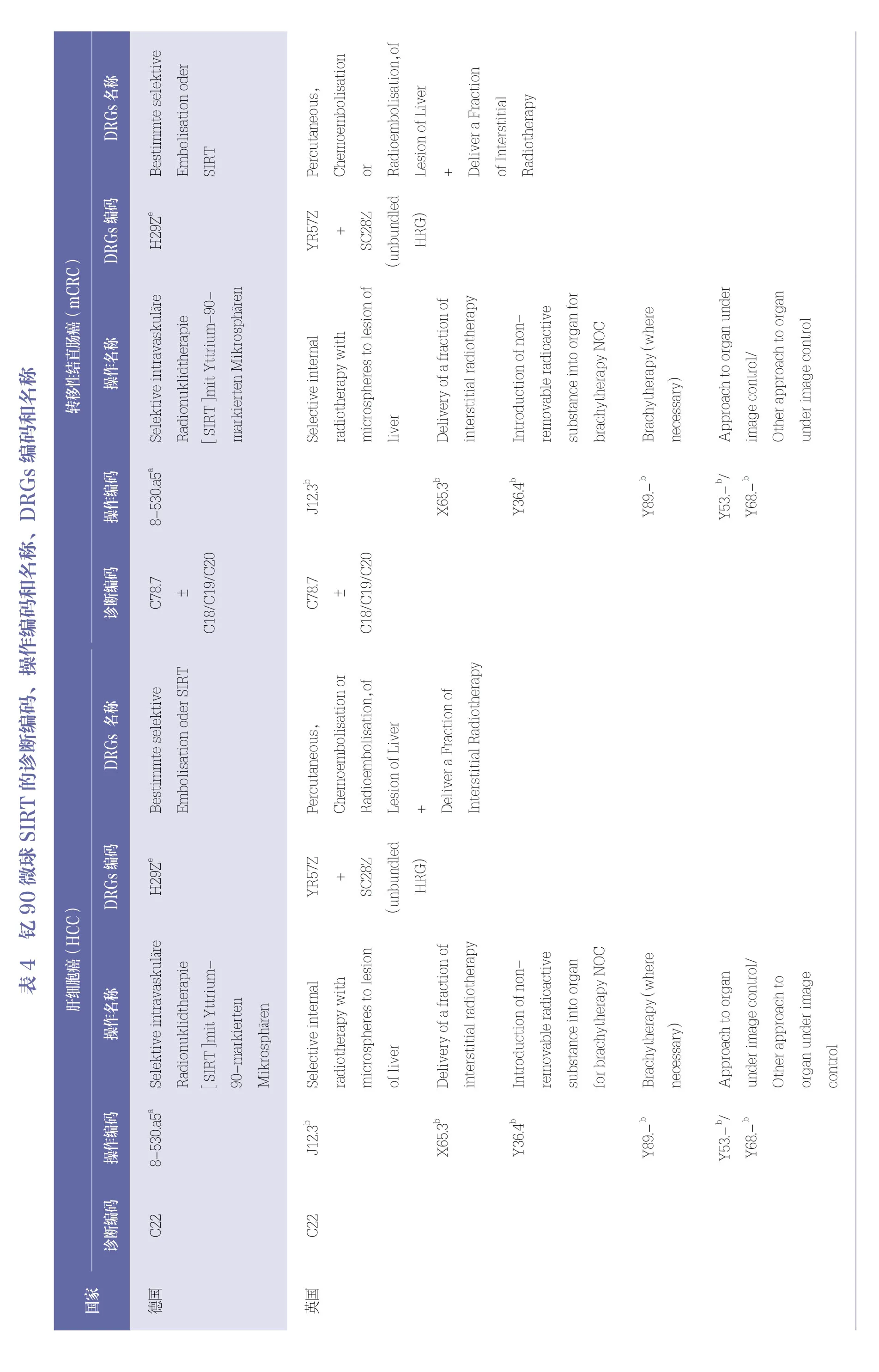
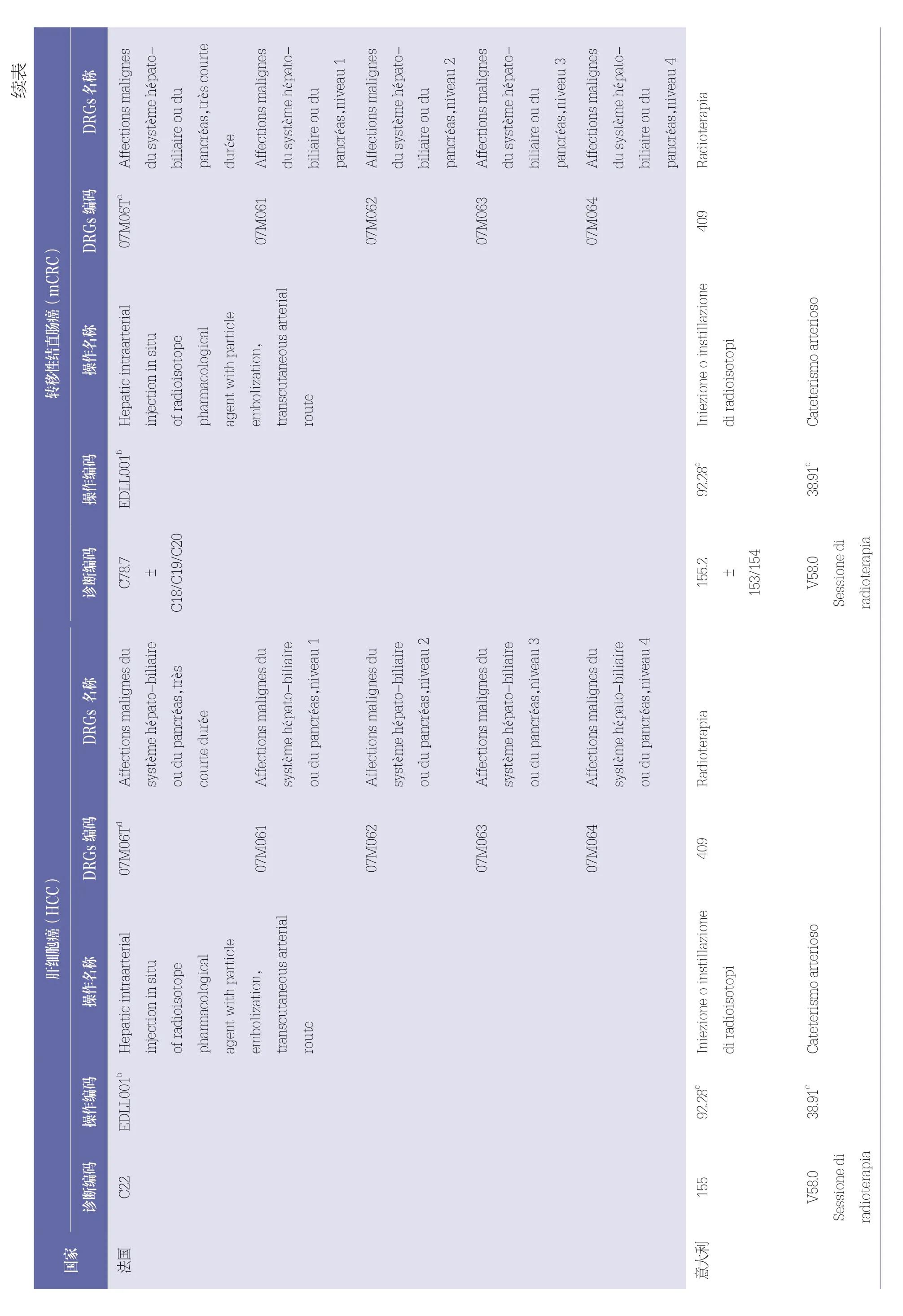
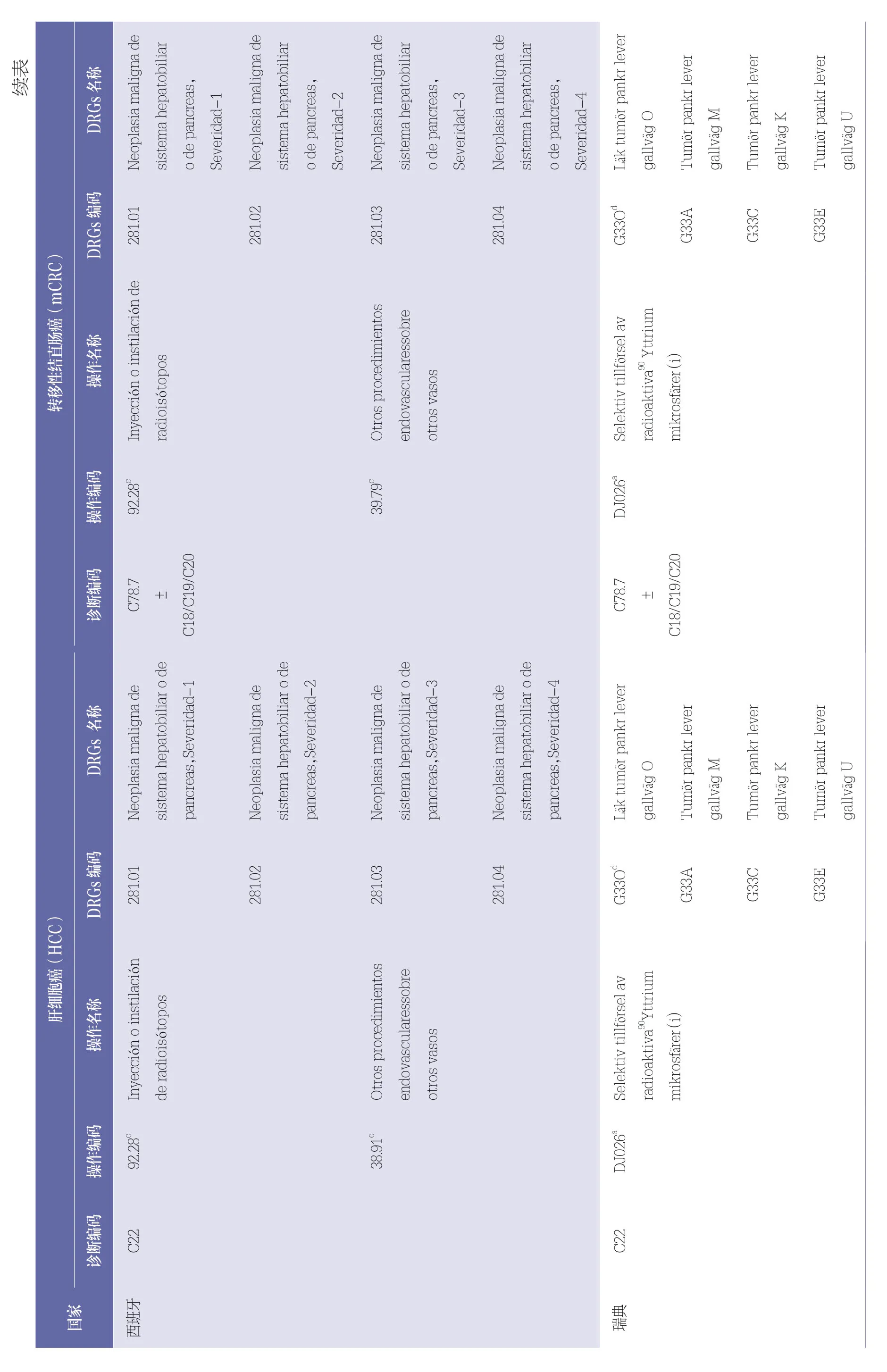
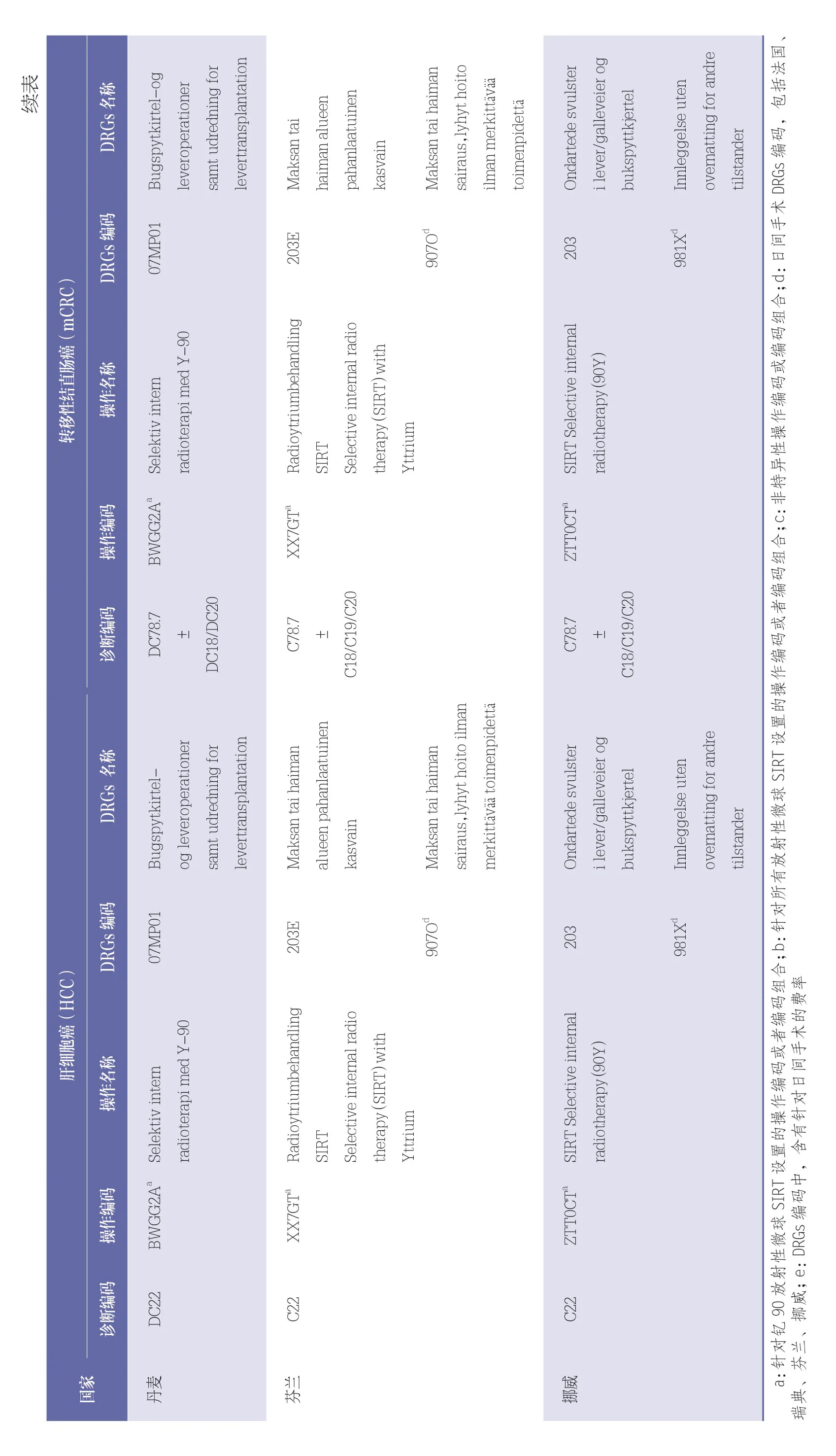
各国对于HCC 和mCRC 2 个适应症均归类为同一个DRGs 组。
德国和英国针对SIRT 设置了特异性的DRGs组;法国、西班牙、瑞典、芬兰、丹麦、挪威生成了“肝胆系统或胰腺的恶性肿瘤”非特异性DRGs 组;丹麦生成了“肝胆系统或胰腺的恶性肿瘤、手术或肝移植”非特异性DRGs 组;意大利归类为“放疗”非特异性DRGs 组。
3.4 SIRT 的DRGs 费率和相关报销方式
大部分国家将SIRT 的报销方式分为2 部分,即针对医疗服务的报销和针对放射性微球产品的报销,本文主要针对SIRT 部分的医疗服务报销进行讨论,不涉及微球产品的价格和报销方式。
德国在SIRT 特异性DRGs 组的固定费率基础上,按照患者住院天数向医院支付护理费,共同报销医疗服务的费用,同时以追加报销(add-on reimbursement)的形式报销放射性微球,其价格由不同医院与生产企业谈判确定。英国采用的是2个DRGs 组费率加和的形式,根据NICE 的评估报告,SIRT 分为2 个阶段,即针对肝病变部位的放射性栓塞和递送放射性治疗物质[19],因此体现在2个不同特异性的DRGs 组中。
未设置特异性SIRT 的DRGs 分组国家中,均未区分SIRT 与肝胆胰腺恶性肿瘤的其他治疗方案。法国区分了日间手术和常规手术DRGs 亚组,并且根据患者的疾病严重程度将常规手术分为4 个亚组,亚组间费率有差异。放射性微球被列入可报销产品和服务清单(liste de produits et prestations remboursables,LPPR)取得相应的编码,以统一全国的报销价格。与法国报销模式相类似的是西班牙和瑞典,由于区域发展差异等因素,西班牙各地区的DRGs 费率不尽相同。西班牙和瑞典各地区对于放射性微球的追加报销价格有所不同。丹麦采用单纯DRGs 报销方式,未区分日间手术与常规手术,亦未区分患者疾病严重程度。同时,由于该DRGs分组中同时包括SIRT、手术治疗和肝移植等,病例平均住院成本差异巨大。芬兰代表医院如芬兰最大的医院赫尔辛基大学医院[20],采用DRGs 费率+按项目付费的形式,在DRGs 的基础上,医院按照SIRT 的操作编码获得报销。意大利和挪威均区分了日间手术与常规手术,但未区分患者疾病严重程度,其针对放射性微球的进一步报销政策未公开。各国报销方式见表5。
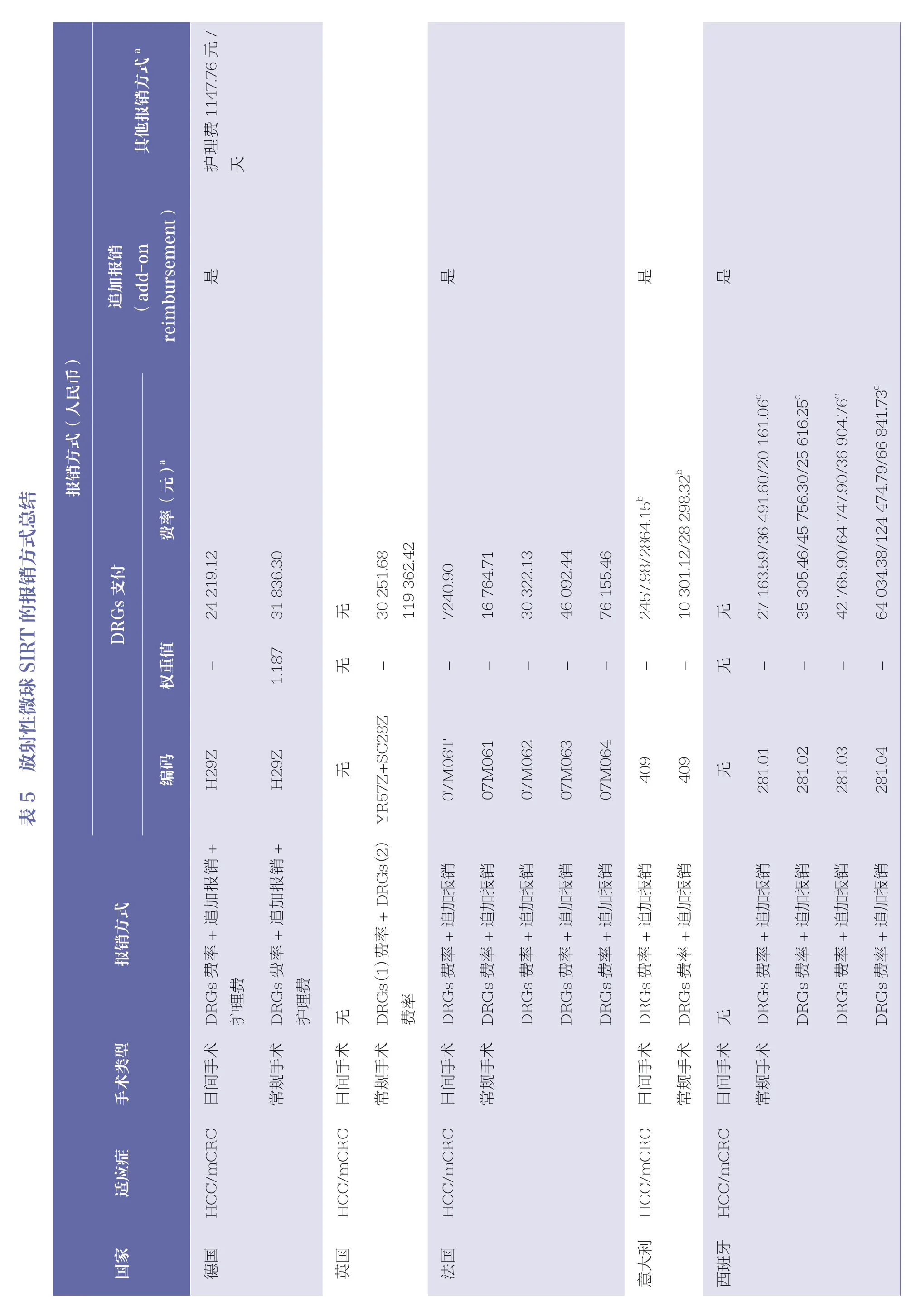
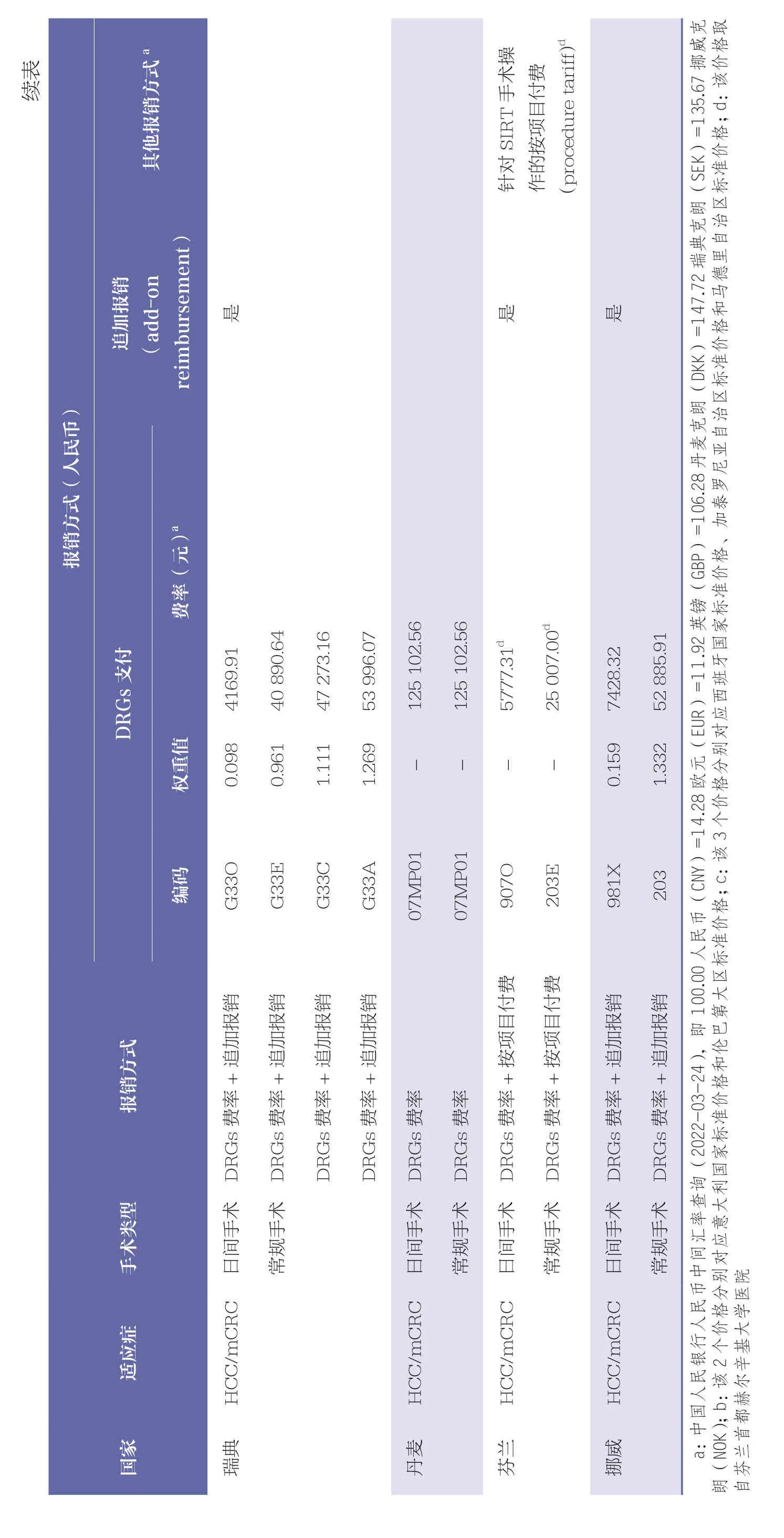
3.5 SIRT 的用量分析
在德国、英国、法国的官方相关数据库以SIRT操作编码为检索词进行2019~2021 年的销量分析,结果见表6。德国2019~2021 年SIRT 手术量均超过1000 例,远超过英国和法国;但是其日间手术占比小于英国和法国。
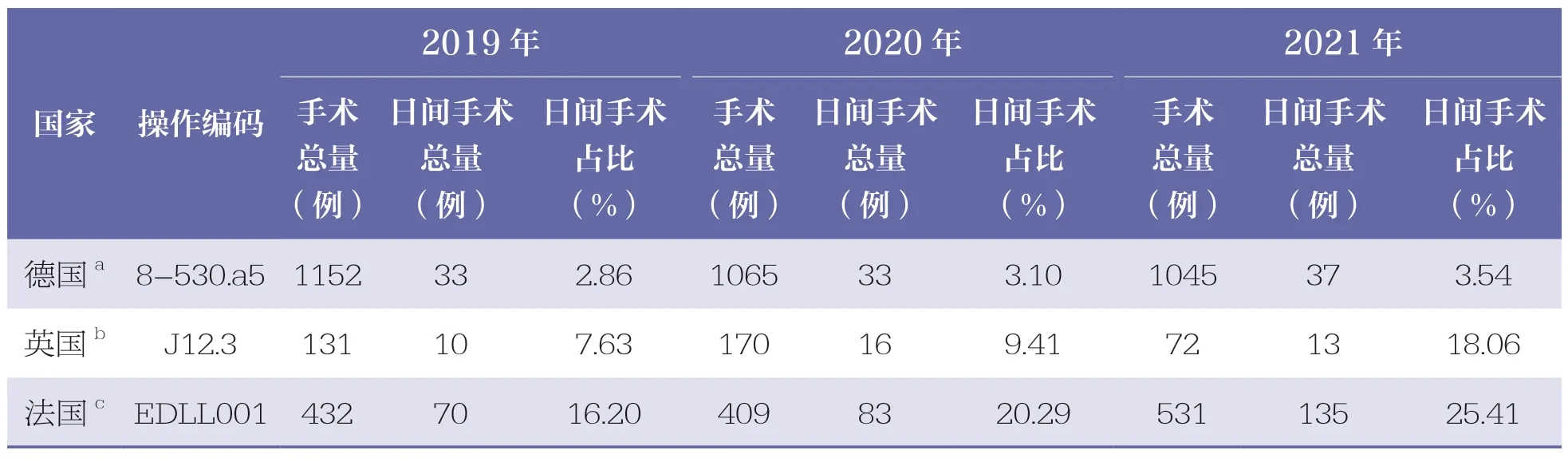
表6 德国、英国、法国SIRT 操作编码2019~2021 年用量分析
德国数据库提供进一步的数据用以分析患者信息,包括男女性别比例、临床复杂水平(patient clinical complexity level,PCCL)和ICD 主诊断编码分类,见表7。超过60%接受治疗的患者为男性;70%以上的患者PCCL 得分为0 分和1 分,代表没有并发症/合并症和有一个轻度的并发症/合并症。ICD 编码的分布反映患者主要集中在原发性或转移性肝癌,少数的其他编码中,包含如C23 胆囊恶性肿瘤等,体现SIRT 潜在的临床应用范围。
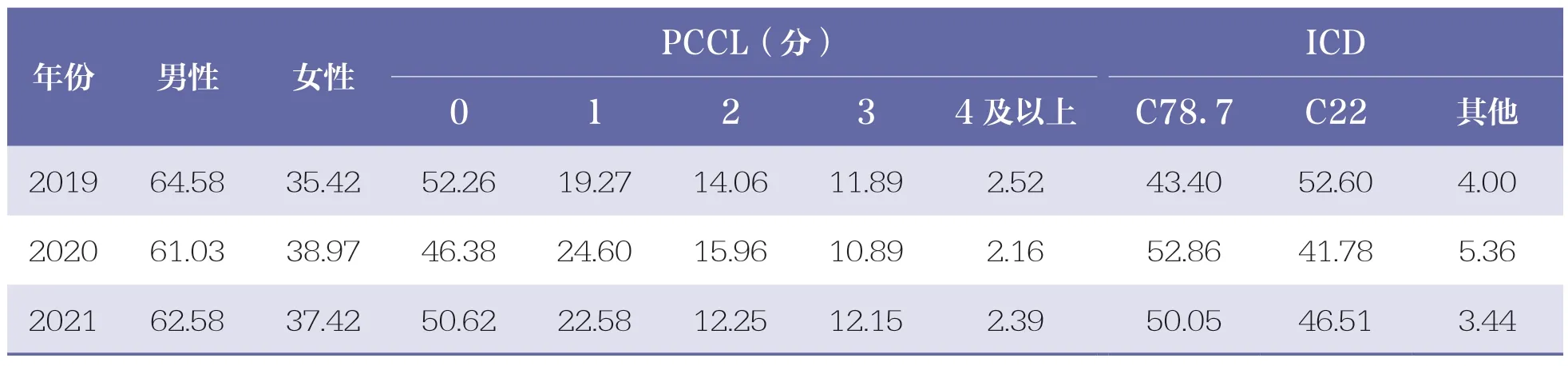
表7 德国接受SIRT 的患者基本信息占比 %
3.6 SIRT 的成本矩阵分析
德国和法国的官方数据库提供以DRGs 代码为检索词进行成本矩阵分析。
德国的成本核算过程建立在模块化方法的基础上,根据成本项和成本中心分别将病例成本进行聚合,其目的是供医疗机构控制资源消耗和提高服务水平[13]。由于德国对于SIRT 设置了特异性的DRGs 组,其成本构成准确地反映出SIRT 的真实资源消耗,及其在各成本项和成本中心的分布。对比德国的H29Z(SIRT,见表8)和H61C(肝胆和胰腺恶性肿瘤的其他治疗方案,见表9)2 个DRGs 组的成本矩阵分布,SIRT 组中医技人员的人力成本占据总成本的17.66%,这与SIRT 需要大量医技人员的劳动消耗的特点相一致;而其他治疗方案(H61C)成本构成中,医技人员人力成本仅占11.16%。SIRT 需要通过介入手术将放射性微球注入患者体内,因此其成本构成中,63.50%的成本归属于“放射科”这一成本中心;而其他治疗方案中归属到“放射科”的仅占总成本的10.51%,差异明显。
法国并未就SIRT 设置特异性DRGs 组,由于07M06(包括日间手术组07M06T 和其他常规手术组07M061/2/3/4,见表10)各组中包括肝胆系统或胰腺恶性疾病的多种治疗手段,包括手术等,其成本构成不能准确地体现到SIRT 的特异性的成本分布,不论是医技人员的人力成本,还是归属到“放射科”成本中心的成本,均低于德国同类项。
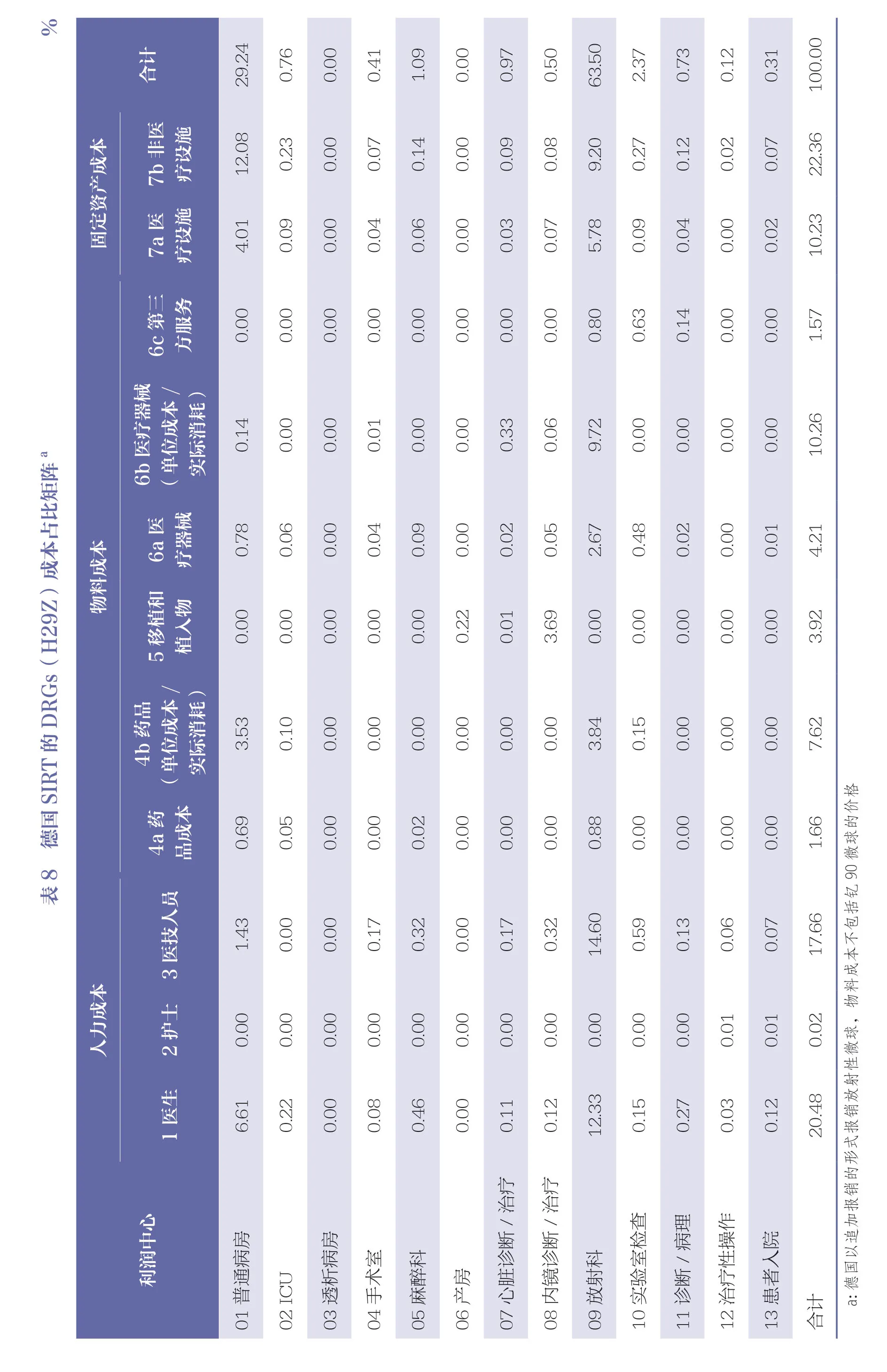
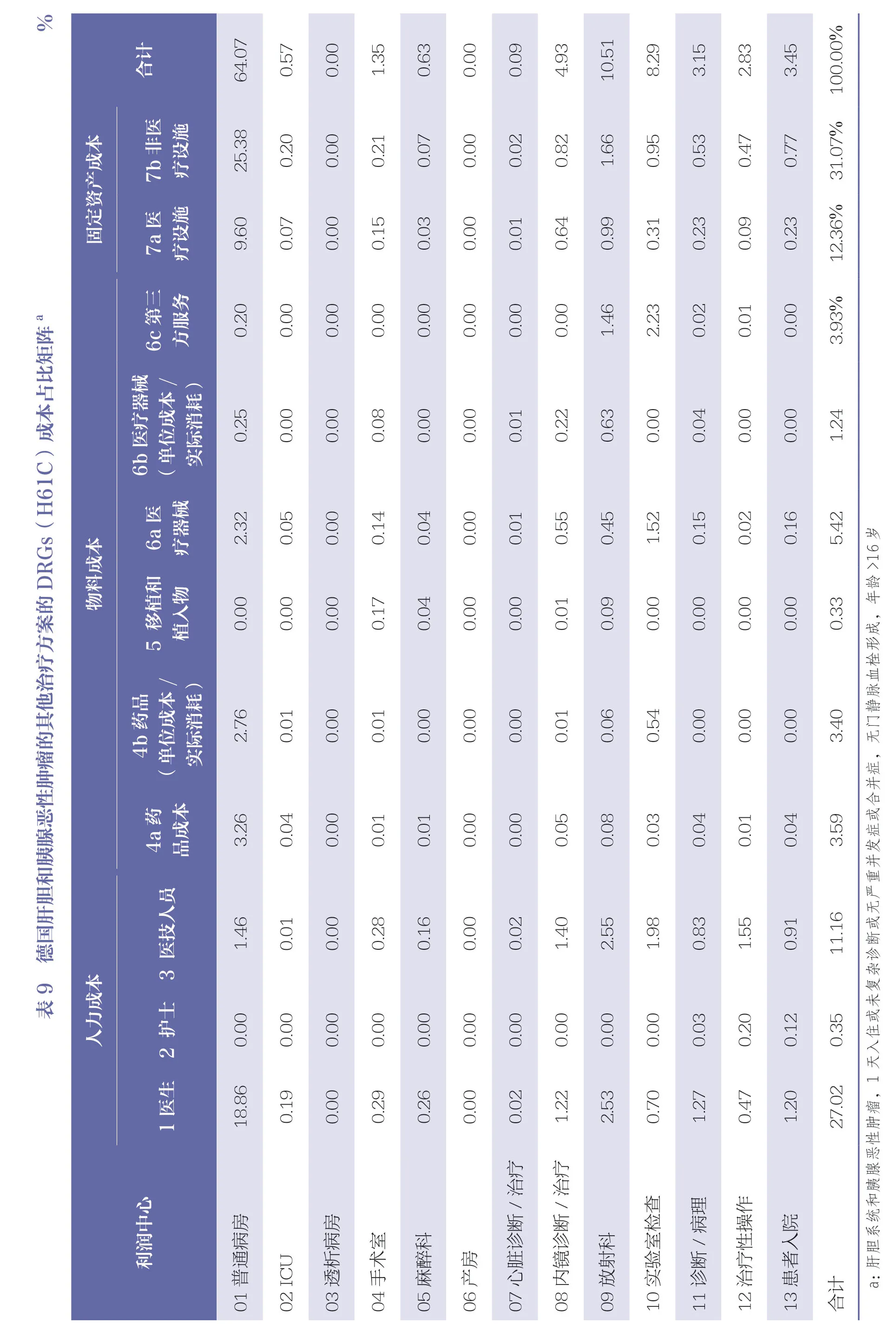
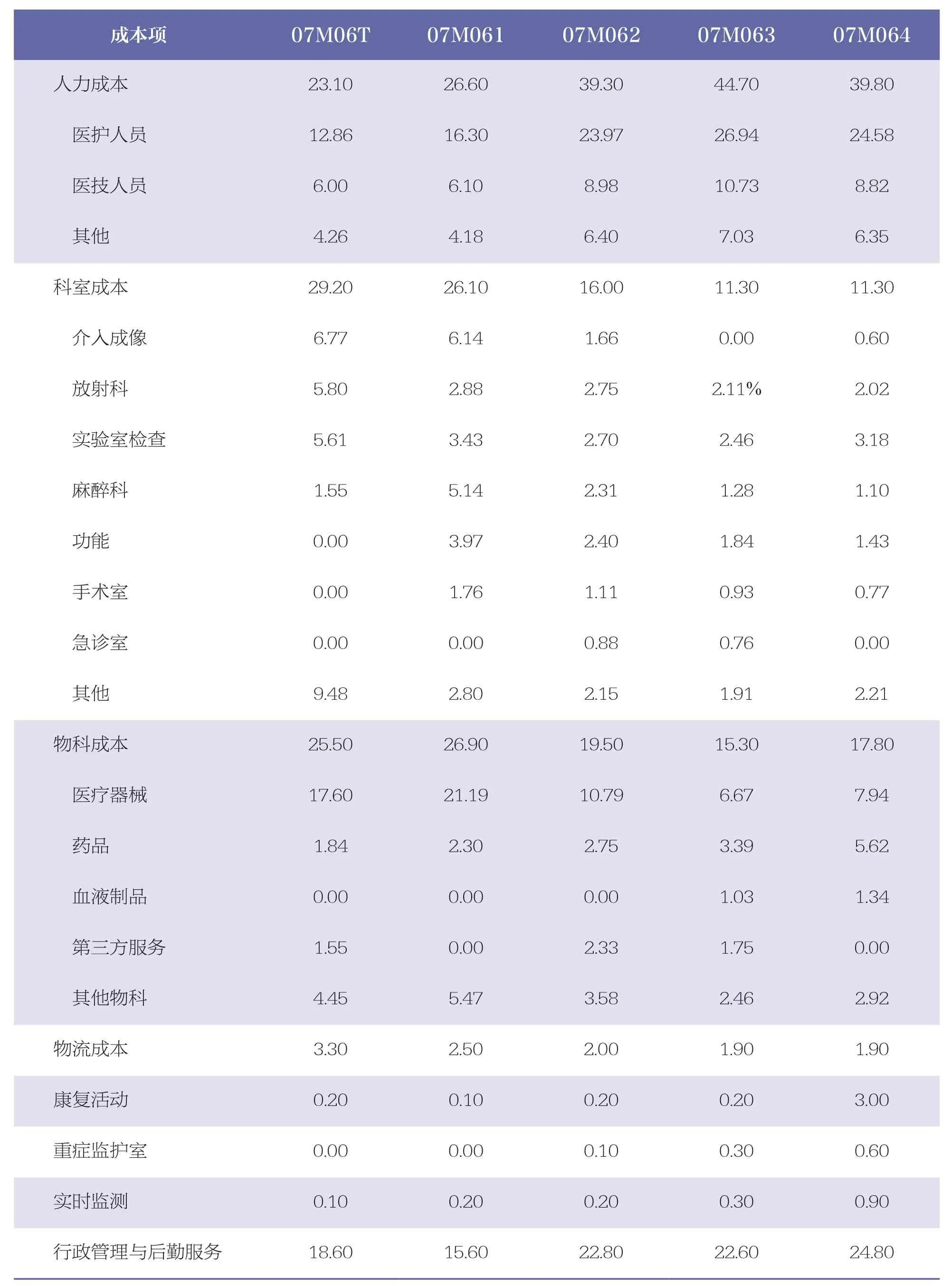
表10 法国“肝胆系统或胰腺的恶性肿瘤”的DRGs(07M06T/1/2/3/4)成本占比矩阵a %
4 讨论
4.1 DRGs 支付方式下对于高价格创新医疗技术的不同报销政策
DRGs 支付方式的实施从源头上改变了医院的成本控制逻辑,药品和医疗器械的临床应用与管理从医院的利润中心转变为成本中心,从重要收入来源转变为主要控费目标。但是DRGs 支付方式并非高价格创新医疗技术获得医保报销的障碍,欧洲各国采用了不同的医保报销政策,以覆盖此类技术,给我国提供了参考:如①DRGs 支付,代表国家:丹麦。②2 种或以上的DRGs 捆绑支付,代表国家:英国。③DRGs 支付+追加报销,代表国家:法国、西班牙、瑞典。④DRGs 支付+追加报销+护理费,代表国家:德国。⑤ DRGs 支付+针对手术操作的按项目付费,代表国家:芬兰。提示大部分国家将医疗服务(SIRT)和放射性微球分别进行报销。
除此之外,各国还有一系列报销政策作为DRGs 支付方式的补充,用以促进创新技术的使用。以德国为例,采用新技术加成(neue untersuchungs-und behandlungsmethoden,NUB)方法鼓励和促进创新型的诊断和治疗手段(包括药品和医疗器械)[13]。德国新技术纳入常规G-DRG 支付系统的典型路径见图2 所示[13]:创新医疗技术首先从医院层级引入;NUB 政策为医院提供资金用以补贴新技术产生的成本,同时在一段时间内收集技术使用产生的数据(包括有效性、安全性、经济性等)。通过NUB 申请并与支付方签署服务协议的医院,以谈判的形式确定追加报销的金额;无操作编码的新技术也将有机会申请特异性的编码。此时的HTA 由区域性机构负责。在此基础上,一旦积累了足够多的患者人数,并且确定了新技术应用的数据,国家级HTA 机构将进行评估,以固定追加报销金额,并最终进入常规G-DRG 支付系统生成特定的DRGs 组。SIRT 现阶段德国处在灰色阴影所在区域,意味着积累了一定的患者人数和使用数据,区域HTA 机构完成评估,以DRGs 费率+追加费用的形式予以报销,放射性微球的报销价格由医院与支付方谈判决定。
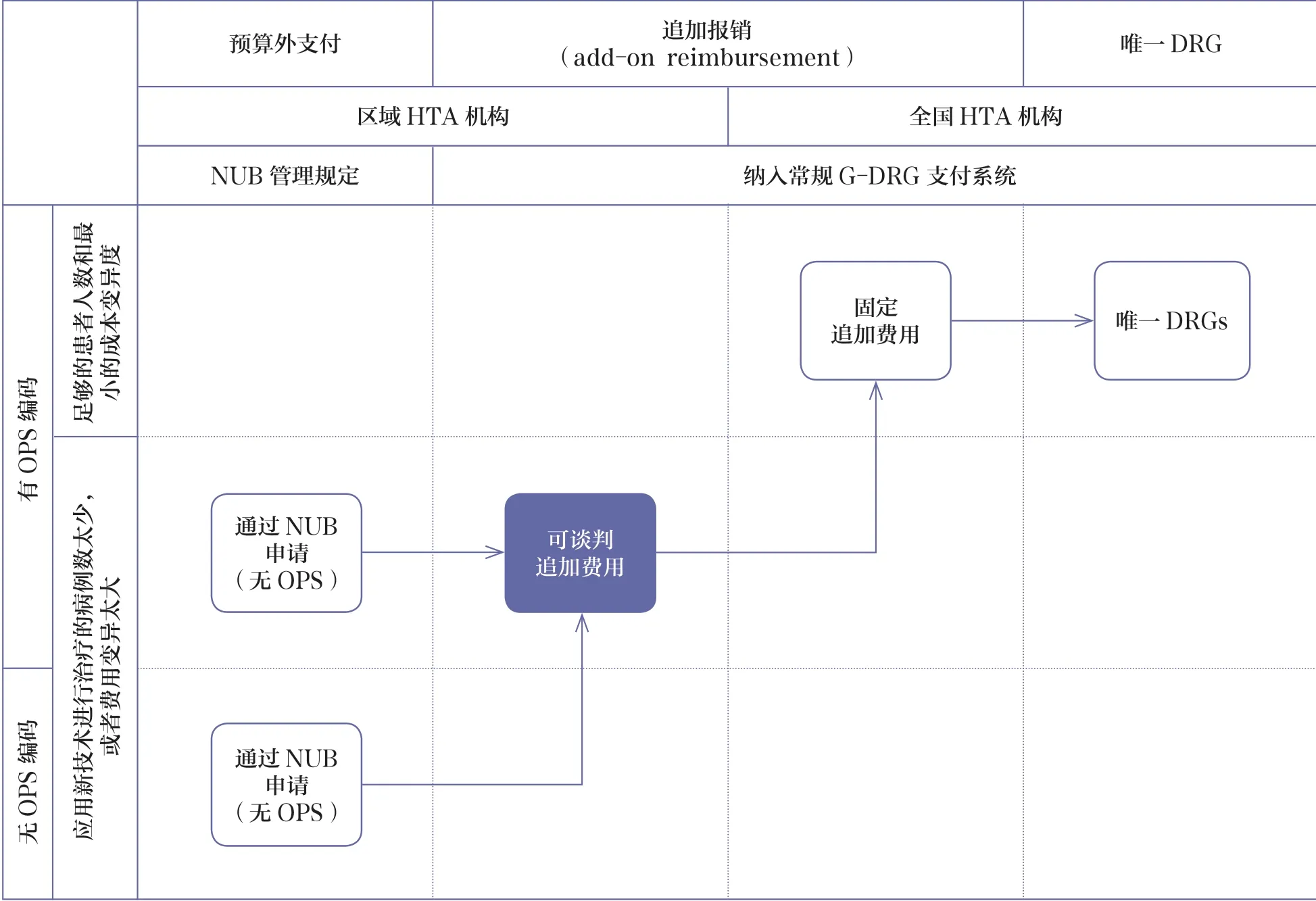
图2 将新技术纳入常规G-DRG 支付系统的典型路径
4.2 DRGs 在各国扮演的不同角色
由表11 可知,欧洲国家引入DRGs 的目的及其演变[13]。DRGs 的应用基于两方面的考虑:第一是通过记录医疗行为,确立绩效考核标杆,规划医院管理等提高医疗服务的透明度;第二是基于DRGs 方式的直接支付,促进医疗资源和医保基金的合理利用。德国、英国、法国现阶段DRGs 支付方式扮演的主要角色是后者,因此通过分析钇90 微球SIRT 报销政策发现,3 个国家均有明确且统一的基于DRGs 的报销形式和金额。瑞典和芬兰等实施的总额预算下的DRGs 支付方式,医院每年的医保报销总额由医院与地方支付方谈判确定,DRGs支付体系作为医院内部资金二次分配(标杆)以及绩效测量的工具,针对放射性微球也未形成全国统一的报销价格。
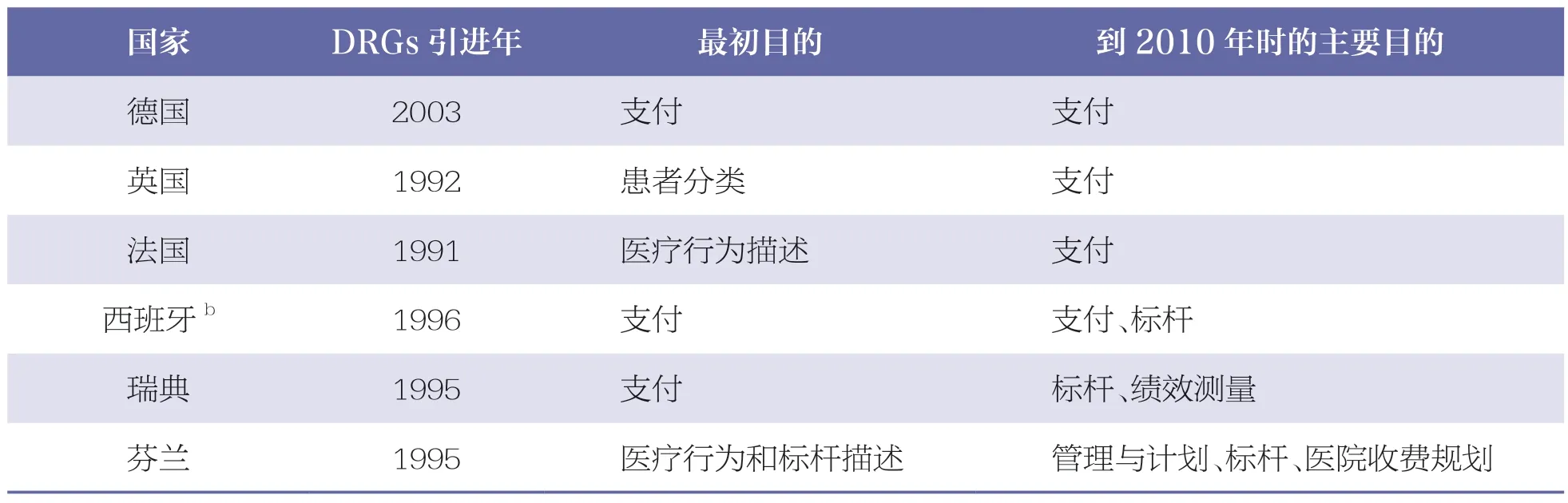
表11 欧洲国家引进DRGs 支付方式的年份和目的 a
4.3 针对创新医疗技术的HTA 与特异性的操作编码和DRGs 分组
创新型医疗技术在欧洲获得医保报销的成功经验包括2 个重要环节,分别是获得HTA 机构正面推荐以及设置特异性的操作编码和DRGs 分组。
在欧洲,HTA 机构就药品进行评估并提供建议,支付方、定价和报销及相关机构依据其结果对比新治疗技术与现有手段的差异;确定报销状态;支持价格谈判过程[21]。德国、英国、法国、意大利、瑞典等国的国家级、区域级、医院级的HTA 机构分别对SIRT 进行了正面推荐,作为其获得医保报销的基础[7-10]。
德国和英国针对SIRT 设置特异性的操作编码,并将SIRT 归类为特异性DRGs 组,以报销和管理该技术;法国等虽然对于SIRT 的操作进行了编码,但将该技术归入“肝胆系统或胰腺的恶性疾病”的DRGs 组进行覆盖,无法区分SIRT 与组内其他治疗技术如手术等的临床资源应用与成本核算方面的差异;意大利和西班牙的操作编码体系尚沿用ICD-9-CM,没有针对SIRT 设置特异性的操作编码,导致了该技术并未有明确的归类。这也与“4.2”中提到的DRGs 支付方式在各国扮演的不同角色有关。
4.4 DRGs 分组对于医疗行为的影响
对比德国、英国、法国的销量分析数据,法国日间手术的占比明显高于其他两国,英国次之。法国设置了独立的日间手术DRGs 亚组:医生在收治患者时,会根据疾病严重程度和手术复杂程度进行区分。德国在DRGs 中针对日间手术和常规手术区分了独立的费率,二者之间存在显著差异(约合人民币7700.00 元)导致归类为日间手术的患者比例相对较小。
这提示我们在设置核心DRG(adjacent-DRGs,ADRGs)组到DRGs 亚组的过程中需要注意颗粒度,重视各DRGs 组权重值的科学设置,以激励医务人员改进技术;合理区分是否需要住院的轻重症患者,从而提高医疗资源的使用效率[15]。
4.5 DRGs 分组对于医院成本核算和医保基金管理的影响
针对德国和法国的DRGs 成本矩阵分析发现,SIRT 的成本构成与肝胆系统或胰腺的恶性疾病其他治疗手段有明显差异。德国设置了针对SIRT的特异性DRGs 组,因此成本矩阵中清晰地体现出其治疗成本在成本项和成本中心的分布;法国将SIRT 归入“肝胆系统或胰腺的恶性肿瘤”非特异性分组,无法区分SIRT 与组内其他治疗手段(如手术治疗等)在临床资源消耗等方面的差异。
SIRT 在临床中应用频次高,不同患者对于医疗成本消耗的差异较大。对于此类治疗手段,根据患者基线水平设置不同的DRGs 亚组,对明确医疗资源消耗、控制医疗机构成本、改善科室绩效考核水平、精准地提高医院成本核算与管理能力和医保基金的管理能力具有重要的现实意义。
4.6 研究的局限性
钇90 微球在国内按照药品管理,而在欧洲按照III 类医疗器械监管[7,22],不同的监管分类导致医保支付政策的差异。本研究中涉及欧洲9 个国家,多语种。语言的障碍给研究带来了一定困难,在此感谢瑞典Synergus RWE AB 公司在数据检索和政策研究方面提供的支持。
5 结论
基于欧洲9 个国家各自医保体系下引入DRGs支付方式的不同目的,各国针对以钇90 微球SIRT为代表的高价格创新医疗技术提供多样的报销政策予以覆盖。
现今我国正处于DRGs支付方式推广落地阶段,分析不同国家针对高价格创新医疗技术进行覆盖的政策,有助于增加新技术的应用,提高医疗产出,规范医疗行为,促进新技术的可及性,同时也对支付方的医保基金管理能力和医疗机构的医院管理能力提出了更高的要求。

