三种基源冰片对不同分子量药物促透效果的差异研究
廖玉瑶 郭淑娟 周晴 杨翠婷 石艳双 戴幸星 史新元
冰片属芳香开窍药,能引药由肌表直达腠理,是目前应用较广泛的中药挥发油类促透剂之一[1-3]。根据2020版《中华人民共和国药典》规定,冰片有三种基源,包括天然冰片(右旋龙脑)、艾片(左旋龙脑)、合成冰片(合成龙脑)[4]。三者性味归经、功能主治、用法用量相近,因此在临床用药上并未严格区分。由于天然冰片与艾片产量少、成本高,在临床应用上主要以合成冰片为主[5]。但是三种基源冰片的旋光性不同,化学成分有差异,不同基源的冰片与待促透药物及角质层之间均存在相互选择,这有可能导致对药物促透效果的差异,叶惠娴等[6]发现天然冰片较合成冰片对大黄素的促透效果更强,而陆洋等[7]发现合成冰片较艾片对栀子苷的促透效果更强。那么这三者在临床应用上是否可以互为替代品,不加区别呢?特别是对于低成本的合成冰片,如果可以相互替代,显然是减少成本并保护植物资源的好选择。因此,研究三种基源冰片对药物促透效果的影响,可为冰片的开发应用提供参考。
药物分子量(molecular weight,MW)是影响其经皮吸收的主要因素之一。有研究认为适宜的经皮吸收药物应该具有较小的MW、较高的溶解度、较低的熔点以及合适的分配系数对数值(logP值,其在1~3范围内更易于透皮)[8-9]。对于MW较大的药物而言,寻找可行的经皮促透方法,是经皮给药系统的一大挑战。因此,本文选择两种logP值一致(logP=1.3),但MW差异较大的药物川芎嗪(MW=136)与秋水仙碱(MW=399)为模型药物,考察三种基源冰片对其促透效果的差异,为冰片在中药外用制剂中的合理应用提供参考,也为川芎嗪和秋水仙碱经皮给药制剂研究提供实验依据。
1 材料与方法
1.1 实验动物
SPF级健康雄性SD大鼠,5~6周龄,体质量(200±10)g,由斯贝福(北京)实验动物科技有限公司提供,合格证号:SCXK(京)2016-0002。
1.2 试剂与仪器
天然冰片(批号:FY24030602)、艾片(批号:FY2403WG09)、合成冰片(批号:FY2035GA01)、秋水仙碱(批号:FY15000715)纯度均≥95%,购自南通飞宇生物科技有限公司;川芎嗪(批号:r03822)纯度≥98%,购自百奥百乐生物科技有限公司;乙腈(色谱纯,批号:175157)、甲醇(色谱纯,批号:155759),购自赛默飞世尔科技(中国)有限公司。无水乙醇(分析纯,批号:20170515),购自北京化工厂;蒸馏水购自广州屈臣氏食品饮料有限公司;PBS缓冲液(pH = 7.2~7.4,批号:20171120),购自北京索莱宝科技有限公司。
高效液相色谱仪(1260,美国安捷伦科技公司),智能透皮扩散仪(TP-6,天津市新天光分析仪器技术有限公司),电子天平(BP211D,德国赛多利斯科学仪器有限公司)。
1.3 川芎嗪和秋水仙碱含量测定方法的建立
1.3.1 色谱条件 川芎嗪:Agilent Extend-C18色谱柱(4.6 mm×250 mm,5 μm),流动相为乙腈—水(40∶60),流速1 mL/分钟,检测波长282 nm,柱温25 ℃,进样量10 μL。秋水仙碱: Agilent Extend-C18色谱柱(4.6 mm×250 mm,5 μm),流动相为甲醇-水溶液(45∶55),流速1 mL/分钟,检测波长353 nm,柱温25 ℃,进样量10 μL。
1.3.2 对照品溶液的配制 川芎嗪:精密称取川芎嗪对照品30.5 mg,置50 mL容量瓶中,加甲醇适量使溶解并定容,即得浓度为610 μg/mL的川芎嗪对照品溶液。秋水仙碱:精密称取秋水仙碱对照品10.3 mg,置25 mL容量瓶中,加适量甲醇使溶解并定容,即得浓度为412 μg/mL的秋水仙碱对照品溶液。
1.3.3 方法专属性考察 分别取透皮实验空白接收液、川芎嗪和秋水仙碱对照品溶液、川芎嗪和秋水仙碱体外透皮实验接收液,按其色谱条件进行分析,结果显示接受液中其他成分对川芎嗪和秋水仙碱的测定无干扰。
1.3.4 线性关系考察 川芎嗪:精密移取川芎嗪对照品溶液0.5、1、3、5、8、10 mL于10 mL容量瓶,加甲醇定容至10 mL,得到系列浓度的川芎嗪对照品溶液,按其色谱条件进行测定,以峰面积(Y)对质量浓度(X)进行线性回归。川芎嗪对照品回归方程为Y= 29.34X+179.89,r= 0.9996,表明川芎嗪在30.05~610.00 μg/mL范围内具有良好的线性关系。秋水仙碱:精密移取秋水仙碱对照品溶液0.01、0.02、0.1、0.2、0.5、1、2 mL于10 mL容量瓶,加甲醇定容至10 mL,得到系列浓度的秋水仙碱对照品溶液,按其色谱条件进行测定,以峰面积(Y)对质量浓度(X)进行线性回归。秋水仙碱对照品回归方程为Y=24.57X+6.77,r= 0.9994,表明秋水仙碱在0.41~82.40 μg/mL范围内具有良好的线性关系。
1.3.5 精密度考察 分别取川芎嗪线性范围内低、中、高三个浓度(30.05、305.00、610.00 μg/mL)和秋水仙碱线性范围内低、中、高三个浓度(2.06、41.20、82.40 μg/mL)的对照品溶液,每个浓度1日内连续进样6次,按其色谱条件进行测定,计算二者的日内精密度;以上样品连续3天内进样,按其色谱条件进行测定,计算二者的日间精密度。川芎嗪低、中、高三个浓度的日内精密度分别为0.13%、0.10%、0.09%,日间精密度分别为0.37%、0.15%、1.39%,均小于2.0%;秋水仙碱低、中、高三个浓度的日内精密度分别为0.90%、0.36%、0.15%,日间精密度分别为1.74%、0.67%、0.40%,均小于2.0%。以上结果表明仪器精密度良好。
1.3.6 稳定性考察 分别取川芎嗪和秋水仙碱体外透皮实验接收液,分别于0、4、8、12、24、36 小时进样分析,测得川芎嗪RSD为1.12%,秋水仙碱RSD为1.56%。表明川芎嗪和秋水仙碱体外透皮接收液在36小时内稳定。
1.4 体外经皮渗透试验
1.4.1 供试品溶液的制备 分别取三种基源冰片和药物适量,置2 mL容量瓶中,加80%丙二醇溶液适量使溶解并定容,即得含冰片30 mg/mL(3%)和含药物 30 mg/mL(3%)的供试品溶液。
1.4.2 体外透皮实验 取雄性SD大鼠处死后,剃除腹部毛发,剪取腹部正中部位皮肤,去除皮下脂肪组织,用PBS缓冲液清洗干净,备用。将处理后的大鼠腹部皮肤固定于Franz扩散池之间(扩散池有效扩散面积为3.14 cm2,接收池体积为20 mL),供给池分别加入2 mL供试品溶液,为使接收池中药物溶解达漏槽条件,接收池中选择含20%乙醇的PBS缓冲液为透皮接收液。温度设置为32℃,接收池搅拌转子转速为300 r/分钟。分别于0、2、4、6、8、10、12小时在接收池取样1 mL,并补充等体积的空白接收液,所得样品过滤后,采用HPLC测定接收液中药物的含量。
1.5 数据处理和统计分析
药物的单位面积累计渗透量Qn,μg/cm2按下式计算:
其中,Cn和Ci为第n个和第i个取样点测得的药物浓度,V0为扩散池接收室体积(20 mL),Vi为每次取样的体积(1 mL),A为皮肤有效面积(3.14 cm2)。
将Qn与时间作图得到药物经皮渗透动力学曲线,其中直线部分(6~12小时)的斜率即为稳态透皮速率[J,μg/(cm·h)],直线部分反向延长线与X轴的交点即为滞后时间(Tlag,h)。促透效率(ER)按下式计算:
ER=Je/J0
其中,Je为加入促渗剂之后的稳态透皮数率,J0为不加促渗剂的稳态透皮速率。
2 结果
2.1 不同基源冰片对川芎嗪经皮渗透的影响
三种基源冰片对川芎嗪的经皮渗透动力学曲线及相关渗透参数见图1和表1。结果显示,对照组川芎嗪的12小时累计渗透量达到(2004.47±351.82) μg/cm2,川芎嗪由于自身分子量小,具有良好的经皮渗透能力。分别加入三种冰片后,川芎嗪的累计渗透量增加到1~2倍,表明三种基源冰片对川芎嗪均有明显的促透作用,但三者促透效果的差异不显著。同时,相比于天然冰片与艾片,合成冰片的滞后时间小于对照组川芎嗪,表明合成冰片能缩短川芎嗪的起效时间。综合促透效率与滞后时间,三种基源冰片促透的效果排序为:合成冰片>天然冰片>艾片。
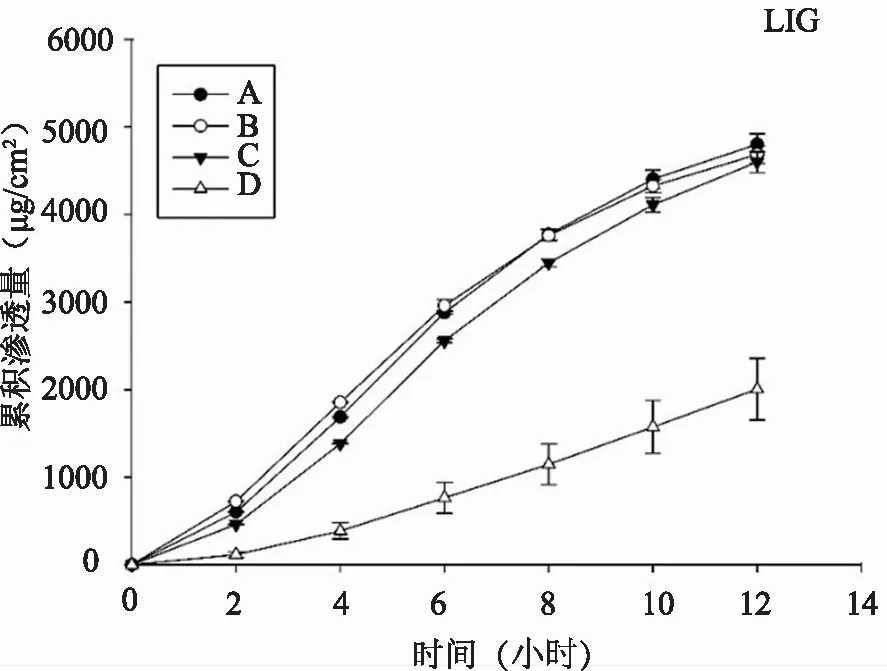
注:A 天然冰片;B 艾片;C 合成冰片;D 对照组。
2.2 不同基源冰片对秋水仙碱经皮渗透的影响
三种基源冰片对秋水仙碱的经皮渗透动力学曲线及相关渗透参数见图2和表2。结果显示,对照组秋水仙碱的12小时累计渗透量为(100.15±59.85)μg/cm2,秋水仙碱由于分子量大,自身的透皮能力较差。分别加入三种冰片后,秋水仙碱的累计渗透量增加到3~6倍,表明三种冰片对秋水仙碱均有明显的促透作用,且三者间存在显著差异。三种冰片的滞后时间均小于对照组秋水仙碱,表明其均能缩短秋水仙碱的起效时间。综合促透效率与滞后时间,三种基源冰片促透的效果排序为:天然冰片>合成冰片>艾片。
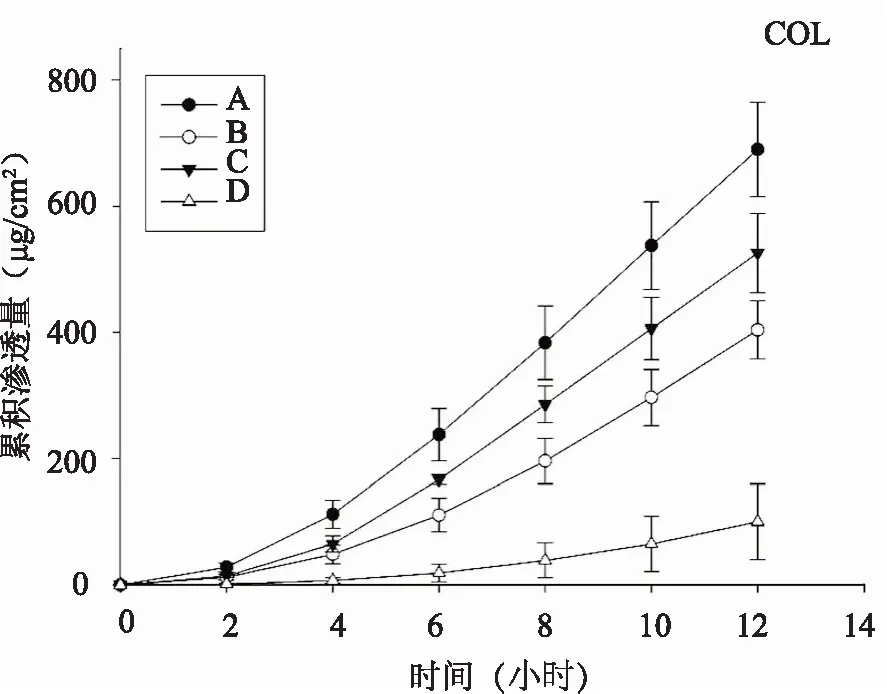
注:A 天然冰片;B 艾片;C 合成冰片;D 对照组。
渗透动力学曲线(n=3)
2.3 不同基源冰片对两种分子量药物促透效率的比较
三种基源冰片对两种分子量大小药物的促透效果如表3所示。对于同一药物,三种基源冰片的促透效率存在差异,尽管三种冰片对川芎嗪促透效果的差异并不显著,但从数值上可以观察到对于两种药物而言,天然冰片与合成冰片的促透效果更强。此外,三种基源冰片对秋水仙碱的促透效率均显著高于川芎嗪的促透效率,表明三种冰片对大分子药物的促透效果更佳。

表3 不同基源冰片对两种分子量药物的促透效率
3 讨论
本文研究结果表明,对于同一药物而言,三种基源冰片的促透效果有所差异,其中天然冰片与合成冰片均显示出较艾片更好的促透效果。不论何种冰片,最主要的功效成份都是龙脑(2-莰醇),但纯度和旋光性有所差别,天然冰片应含右旋龙脑96%以上,艾片应含左旋龙脑85%以上,合成冰片中消旋龙脑含量应在55%以上[10],这造成了三种基源冰片在透皮吸收、黏膜渗透、体内药效等多方面的差异[11-13]。此外,冰片促透的主要作用部位在皮肤的角质层,富含手性物质神经酰胺[14]。因此,基于三种基源冰片的旋光性与角质层神经酰胺的手性中心,促透剂与皮肤之间可能存在立体选择性[15-16],导致三种冰片的促透效果差异。对于不同分子量的药物而言,三种基源冰片对秋水仙碱的促透效率均大于对川芎嗪的促透效率,表明冰片对分子量较大的药物比对分子量较小的药物促透效果更显著。角质层是药物经皮吸收的主要屏障,其脂质排列紧密, 间隙小[17], 分子量较大的药物不易穿透角质层脂质,渗透能力弱。已有研究表明,冰片的促透机制包括扰乱角质层类脂与诱导瞬时孔等[18],从而能有效地促进大分子量药物的经皮渗透[19]。

表1 不同基源冰片对川芎嗪的相关渗透参数

表2 不同基源冰片对秋水仙碱的相关渗透参数
受资源与成本的限制,目前市场上以合成冰片为主,但有研究认为合成冰片在很大程度上效果不及天然冰片[5]。通过本研究发现,三种基源冰片均能显著提高两种分子量药物的体外经皮渗透率。对小分子药物,合成冰片有较好的促透效果;对于难以透皮吸收大分子药物,三种冰片均具有高于小分子的促透效果,合成冰片的促透效果虽不及天然冰片,但高于艾片。因此,从来源与成本角度考虑,在以冰片为促透剂的现代中药外用制剂研发中,合成冰片是可行的选择。

