丙酮溶剂中氯丙烯催化环氧化合成环氧氯丙烷
刘 易,张永强,杜泽学
(中国石化石油化工科学研究院,北京 100083)
环氧氯丙烷(ECH)是一种重要的丙烯衍生物,以它为原料制得的环氧树脂具有黏结性强,耐化学介质腐蚀、收缩率低、化学稳定性好、抗冲击强度高以及介电性能优异等特点,在光伏、风电和电子、涂料等行业应用广泛,消费量不断增长[1]。目前,环氧氯丙烷的工业生产采用皂化法,包括丙烯高温氯化法和甘油法两种工艺[1],其共同的特征是副反应多、物耗高、能耗大,排放大量含有机氯的废水和含氯化钙废渣,环境危害严重,难以治理。2019年国家发展和改革委员会修订发布的《产业结构调整指导目录(2019年)》明确限制发展皂化法环氧氯丙烷生产装置,当年国内环氧氯丙烷装置开工率仅43.2%。因此,开发市场急需的环氧氯丙烷绿色合成新技术势在必行。
以丙烯为原料生产环氧氯丙烷就是向丙烯分子中引入氯原子和氧原子的过程。丙烯高温氯化法合成环氧氯丙烷是先通过高温氯化引入氯原子,然后通过氯醇化引入氧原子,最后通过皂化实现环化。分析这3个过程,发现氯醇化过程是产生大量废水的根源,皂化过程是产生废渣的根源。开发绿色环氧氯丙烷工艺就是要开发新的工艺替代氯醇化和皂化工序,由氯丙烯直接环氧化生产环氧氯丙烷。氯丙烯直接环氧化制环氧氯丙烷的研究始于20世纪80年代,其中采用钛硅分子筛(TS-1)为催化剂,过氧化氢(HPO)直接氧化氯丙烯制备环氧氯丙烷新工艺的开发最受关注[1-2]。中国石化石油化工科学研究院多年来一直致力于这种新技术的开发[3-5],目前正在开展工业试验。
在TS-1催化氯丙烯直接环氧化合成环氧氯丙烷的反应体系中,由于氯丙烯和过氧化氢互溶性差,加上催化剂以固体形式发生作用,导致反应效果差,需要使用溶剂来改善[6]。本课题将丙酮(AC)作为溶剂进行探索,并与甲醇(MeOH)溶剂进行对比。
1 实 验
试验所用的3-氯丙烯、甲醇、丙酮、30%过氧化氢均为分析纯试剂,国药集团化学试剂公司产品;TS-1分子筛,自制。
1.1 3-氯丙烯与过氧化氢的反应
试验所用的反应器是500 mL的玻璃反应釜,电磁控速搅拌。将溶剂、TS-1催化剂和3-氯丙烯(ALC)(或30%过氧化氢,两种反应物选其一)加入到反应釜中,连接好装置后,开动搅拌,使之充分混合;然后,边搅拌边升温至指定反应温度,再将另一种反应物按设定的流量泵入反应釜中,同时冰水浴冷却取热,直至这种反应物加完,保持温度继续搅拌到指定时间。停止加热,用冰水快速冷却反应釜至不高于20 ℃,停止搅拌,取样检测过氧化氢的残余量,同时分析有机物组成。
1.2 分析方法
反应液中的有机物组成采用安捷伦公司生产的6890N气相色谱仪进行分析。色谱柱为Φ0.25 mm×50 m的OV-1毛细管柱,氢火焰离子化检测器。
反应后物料中残余过氧化氢的含量采用碘量法测定。
过氧化氢转化率(XHPO)为:
(1)
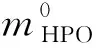
过氧化氢有效利用率(EHPO)为:
(2)
式中:mECH为环氧氯丙烷的生成量,g;MECH和MHPO分别为环氧氯丙烷和过氧化氢的摩尔质量,g/mol。
环氧氯丙烷单程收率为:
(3)

环氧氯丙烷选择性为:
SECH=(mECH/MECH)/[(mECH/MECH)+(mB/MB)]
(4)
式中:mB为副产物的生成量,g;MB为副产物的平均摩尔质量,g/mol。
2 结果与讨论
2.1 丙酮和甲醇对氯丙烯和过氧化氢兼溶能力
溶剂的兼溶能力定义为:一定温度下,一定摩尔比的氯丙烯与过氧化氢(nALC/nHPO)完全互溶时所需溶剂的最少量,以溶剂与氯丙烯的质量比表示,即m溶剂/mALC。常温下,考察甲醇、丙酮对氯丙烯和过氧化氢的兼溶能力,结果如表1所示。由表1可以看出:不论溶剂是丙酮还是甲醇,随着nALC/nHPO的增加,溶剂的需要量依次变小,说明溶剂的兼溶能力增强;丙酮的兼溶能力低于甲醇。此外,升高温度时溶剂的兼溶能力提高,温度从20 ℃升高到40 ℃,丙酮的兼溶能力可以提高约15%,而甲醇的兼溶能力只提高10%。

表1 nALC/nHPO变化对丙酮和甲醇兼溶能力的影响
丙酮和甲醇的一些基本物理性质如表2所示。从表2可以看出,丙酮的沸点、黏度和蒸发热都比甲醇低,特别是丙酮的蒸发热只有甲醇的82.4%。根据表1的结果,丙酮的兼溶能力低于甲醇,用量要比甲醇约增加20%。但由于丙酮的蒸发热也只有甲醇的82.4%,因而,同样条件下,回收丙酮和回收甲醇的能耗基本相当。

表2 丙酮和甲醇的基本物理性质比较
2.2 丙酮和甲醇溶剂对氯丙烯环氧化反应的影响
溶剂丙酮和甲醇对产物组成的影响如图1所示。由图1可以看出:采用丙酮作溶剂时,主要的副产物是环氧氯丙烷的水解开环产物;而采用甲醇作溶剂时,副产物更多,有环氧氯丙烷的醇解开环产物,还有其水解开环产物,而且醇解产物的量比水解产物的量多。由此可见,采用丙酮作溶剂时,由于丙酮与环氧氯丙烷不发生反应,减少了副产物生成。

图1 丙酮与甲醇作溶剂时的产物组成对比
分别在55 ℃和85 ℃下考察丙酮和甲醇作溶剂时不同反应时间下的反应结果,如表3所示。从表3可以看出,不论是55 ℃或是85 ℃,采用甲醇作溶剂时,过氧化氢的转化率均比丙酮作溶剂时略高,但氯丙烯转化率(XHLC)、过氧化氢的有效利用率和环氧氯丙烷的选择性略低。随着反应时间延长,以甲醇为溶剂时过氧化氢有效利用率和环氧氯丙烷选择性与以丙酮为溶剂时的差别越来越大,说明以甲醇为溶剂时副反应随反应时间延长增加得更快。尤其是在85 ℃下,反应120 min后,过氧化氢有效利用率和环氧氯丙烷的选择性分别只有24.5%和26.5%,远远低于同样情况下以丙酮为溶剂时的74.8%和78.8%。
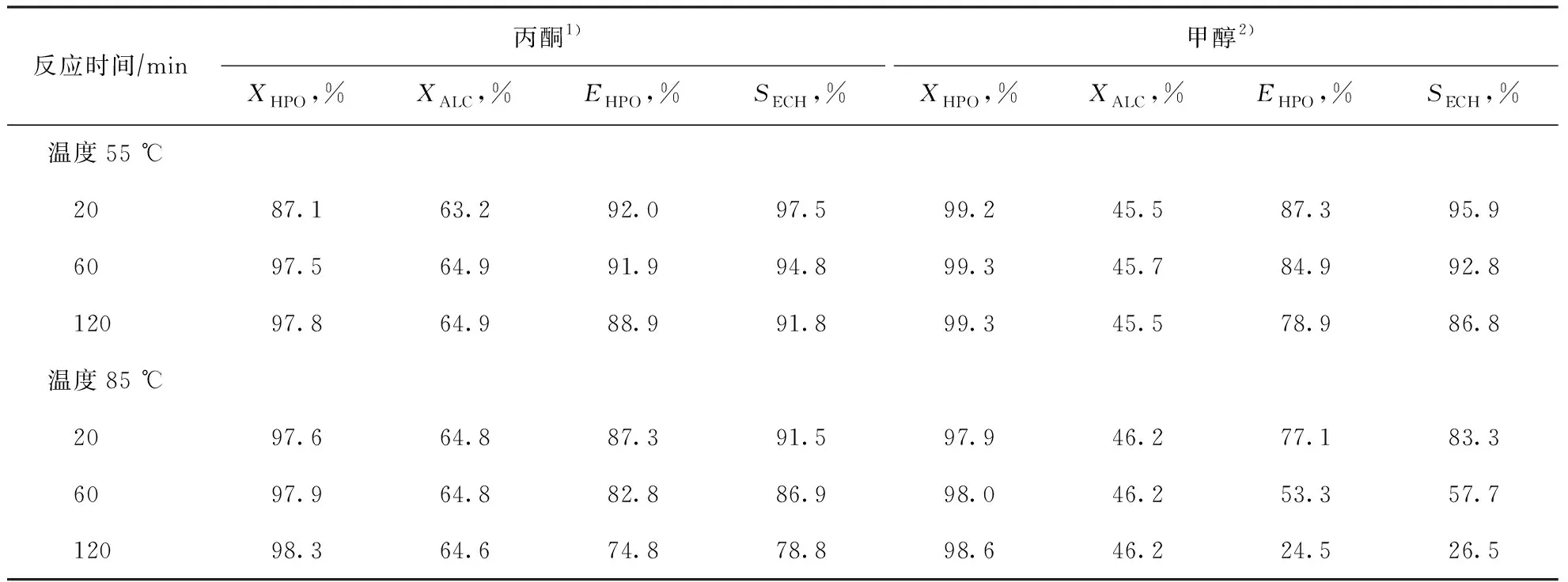
表3 丙酮和甲醇作溶剂时不同反应时间下试验结果的比较
2.3 丙酮溶剂中氯丙烯和过氧化氢环氧化反应的影响因素
2.3.1丙酮用量
常温下,当nALC/nHPO=1.5∶1,过氧化氢浓度约30%,丙酮的用量不小于氯丙烯质量的2.6倍时,能保证各组分相互溶解成单液相。由于单液相条件下增加丙酮用量将稀释催化剂和过氧化氢,对提高反应速率不利,因此试验仅考察丙酮用量不足以形成单液相对,即反应体系是液-液两相情况下,丙酮用量变化对反应的影响,并与形成单液相时的反应情况进行对比,结果如表4所示。由表4可以看出:在相同条件下,减少丙酮的用量,虽然反应体系是液-液两相体系,但反应结果与单液相体系区别不大;如果完全去除溶剂丙酮,过氧化氢转化率和有效利用率明显下降。由此可见,使用溶剂丙酮与否对反应至关重要,当溶剂达到一定用量的条件下,增加溶剂用量对反应结果的影响很小。
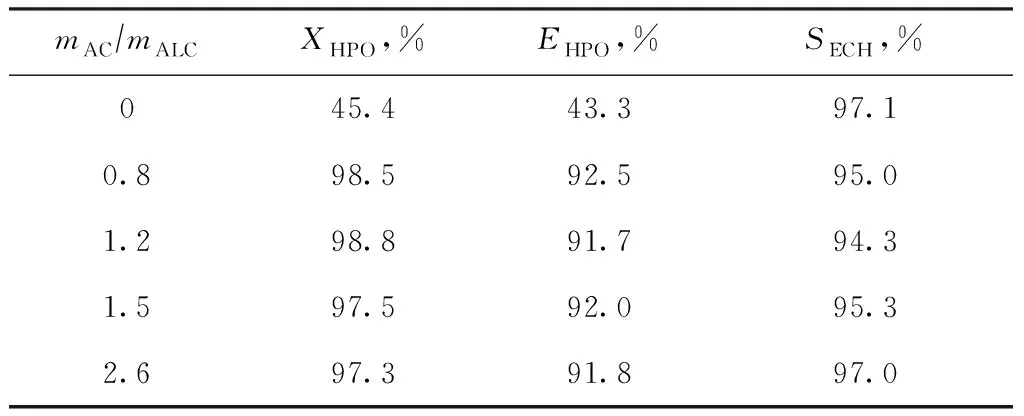
表4 丙酮用量对氯丙烯环氧化反应的影响
由于溶剂需要回收重复利用,因此溶剂的用量在可以满足反应要求的条件下应该越少越好,可以减少回收溶剂的能耗。但在液-液两相状况下,由于两相的性质存在差异,催化剂、溶剂、未反应的反应物以及产物的在两相间的分布对反应体系长时间运转是否会带来一些不利影响,还需要进一步的试验考察。
2.3.2搅拌速率
搅拌速率对有、无丙酮溶剂存在的氯丙烯-过氧化氢液-液两相体系中过氧化氢转化率的影响如图2所示。由图2可以看出,有丙酮的体系,搅拌速率为150 r/min时,过氧化氢转化率在60 min内就可以达到92.3%,到300 r/min时,过氧化氢转化率在反应60 min后可以达到97.1%,再增加搅拌速率,过氧化氢转化率基本不再变化,如增加到1 200 r/min,过氧化氢的转化率只增加了0.7百分点。可见,加入相当于氯丙烯质量0.8倍的丙酮后,尽管反应体系处在液-液两相状况下,但搅拌速率为300 r/min时就可以满足反应的要求。对于无丙酮溶剂的反应体系,搅拌速率从300 r/min增加到1 200 r/min,过氧化氢的转化率从42.19%增加到96.8%。可见,没有溶剂时,提高搅拌速率对传质有明显的促进作用。
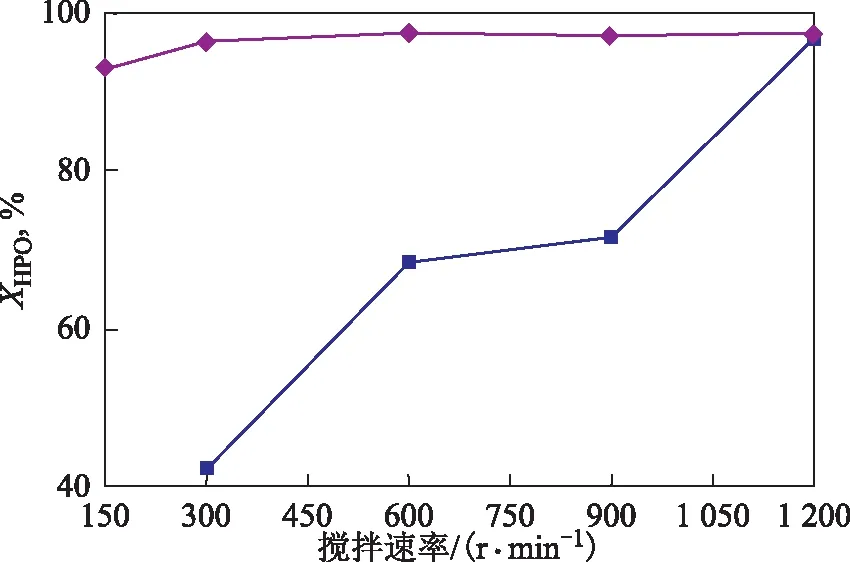
图2 液-液两相体系中搅拌速率对过氧化氢转化率的影响◆—mAC/mALC=0.8; ■—无溶剂反应条件:mALC/mCAT=20,温度55 ℃,时间60 min,添加丙酮溶剂反应体系的nALC/nHPO=1.5∶1,无丙酮溶剂反应体系的nALC/nHPO=7∶1
2.3.3反应温度
反应温度对反应结果的影响如图3所示。从图3可以看出:①在TS-1的催化作用下,反应30 min,过氧化氢转化率随着温度升高而升高,特别是温度从40 ℃到55 ℃,仅升高15 ℃,但过氧化氢的转化率从55.6%增大到91.7%;继续升高温度,过氧化氢转化率略有增加。这说明当反应温度低于55 ℃时,反应温度对催化剂TS-1活性影响明显;温度超过55 ℃后,反应温度对TS-1活性影响较小。②环氧氯丙烷选择性随着温度升高而下降。反应温度从70 ℃升高到85 ℃,环氧氯丙烷选择性下降5.0百分点;而温度从40 ℃升高到70 ℃,环氧氯丙烷选择性仅下降4.4百分点。可见,温度越高,副反应越严重。③过氧化氢有效利用率的高低取决于过氧化氢的转化率和环氧氯丙烷的选择性。反应温度为40 ℃时,尽管环氧氯丙烷选择性为100%,但由于过氧化氢转化率低,过氧化氢有效利用率也较低;温度升高到55 ℃,虽然环氧氯丙烷选择性有所下降,但由于过氧化氢转化率增加得多,因而过氧化氢有效利用率也随之增加,由56.9%增加到90.1%;继续升高温度到70 ℃,过氧化氢转化率与55 ℃时相比增加了近5百分点,但由于环氧氯丙烷选择性下降,过氧化氢有效利用率仅增加1.5百分点;继续升高温度到85 ℃,虽然过氧化氢转化率继续增加,但由于环氧氯丙烷的选择性下降得更多,导致过氧化氢有效利用率下降,甚至比55 ℃时的结果低近3百分点。根据以上结果分析可知,反应温度最好控制在55~70 ℃之间。
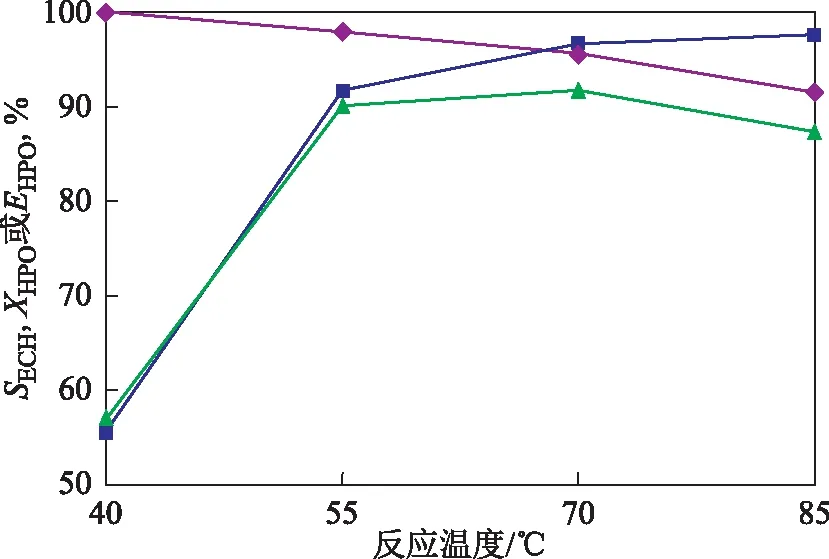
图3 反应温度对氯丙烯环氧化反应的影响◆—SECH; ■—XHPO; ▲—EHPO反应条件:mAC/mALC=2.6,nALC/nHPO=1.5,搅拌速率900 r/min,反应时间30 min
2.3.4催化剂用量
催化剂用量以TS-1与液体的质量比表示。催化剂用量对反应的影响结果如图4所示。从图4可以看出:过氧化氢转化率随着催化剂用量增加而升高,尤其是催化剂用量在0.65%~1.00%范围内变化,对过氧化氢转化率的影响显著,使其从67.1%增加到91.7%;继续增加催化剂用量,过氧化氢转化率略有增加。但若在30 min内,使过氧化氢转化率达到97%以上,需要将催化剂的用量提高到2%。
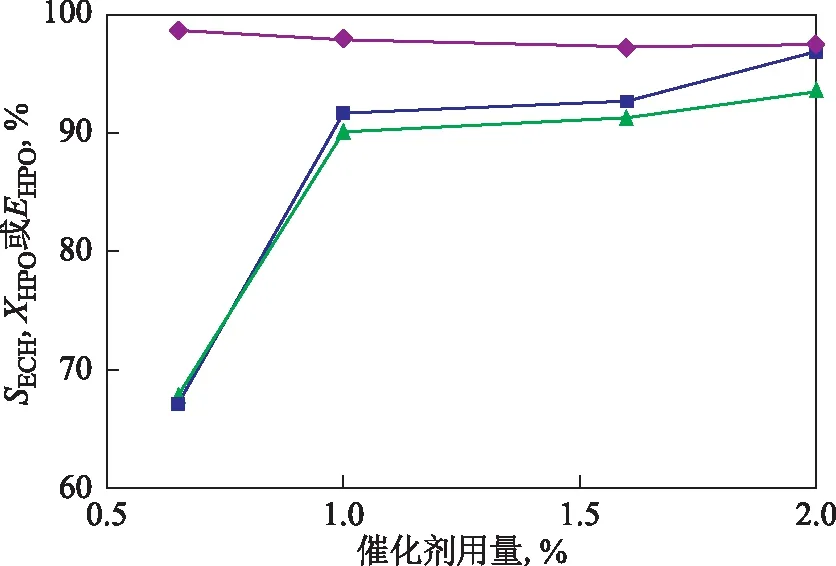
图4 催化剂用量对氯丙烯环氧化反应的影响◆—SECH; ■—XHPO; ▲—EHPO反应条件:mAC/mALC=2.6,nALC/nHPO=1.5,反应温度55 ℃,搅拌速率900 r/min,反应时间30 min
在不同催化剂用量下,考察反应时间对过氧化氢转化率的影响,结果如图5所示。由图5可以看出,虽然催化剂用量不同,但过氧化氢转化率在反应开始后的60 min内均随着反应时间延长明显提高,60 min后再延长时间,过氧化氢的转化率均增加不明显。另外,过氧化氢的转化效果也与催化剂用量有关,催化剂用量越大,在相同时间内过氧化氢转化率越高。由此可见,在确定催化剂用量后,反应时间应以不大于60 min为宜。
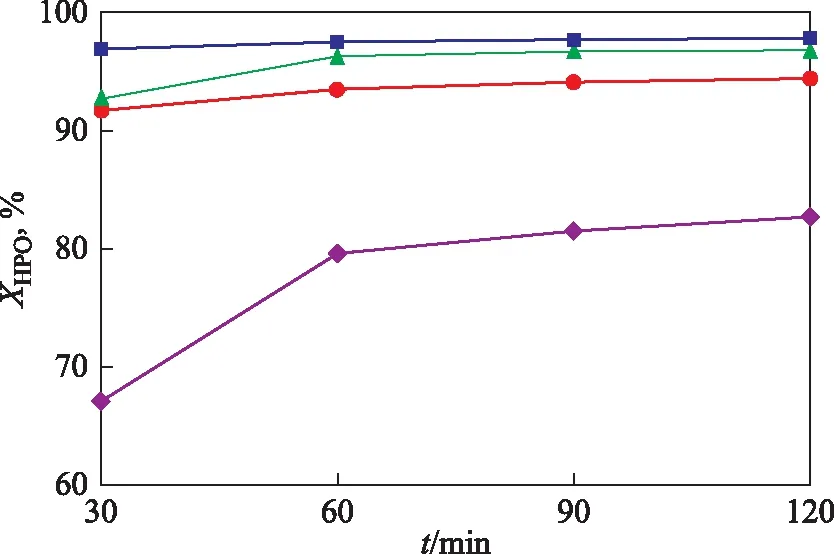
图5 催化剂用量和反应时间对过氧化氢转化率的影响催化剂用量,%:◆—0.65; ●—1.0; ▲—1.6; ■—2.0反应条件:mAC/mALC=2.6,nALC/nHPO=1.5,反应温度55 ℃,搅拌速率900 r/min
图6是不同催化剂用量条件下环氧氯丙烷选择性随着反应时间的变化。由图6可以看出,在相同的反应时间内,催化剂用量越小,环氧氯丙烷选择性越高。这主要是因为催化剂用量少,过氧化氢转化率相应下降,生成的环氧氯丙烷量相对少。不论催化剂用量多少,反应时间延长都将造成环氧氯丙烷的选择性下降,且催化剂用量越大,这种下降趋势越明显。因此,适当增加催化剂的用量,在确保过氧化氢转化率的前提下,尽量缩短反应时间将有利于提高环氧氯丙烷的选择性。

图6 催化剂用量和反应时间对环氧氯丙烷选择性的影响催化剂用量,%:◆—0.65; ●—1.0; ▲—1.6; ■—2.0反应条件:mAC/mALC=2.6,nALC/nHPO=1.5,反应温度55 ℃,搅拌速率900 r/min
2.3.5氯丙烯与过氧化氢配比
氯丙烯与过氧化氢摩尔比(nALC/nHPO)对反应的影响如表5所示。由表5可以看出:①环氧氯丙烷的选择性基本不受nALC/nHPO变化的影响,都保持在95%以上;②当过氧化氢过量时,氯丙烯的转化率仅为90%左右,使得过氧化氢的转化率进一步下降,造成过氧化氢有效利用率只有80%左右;③当氯丙烯过量时,尤其当nALC/nHPO不低于1.5时,过氧化氢转化率不低于97%,过氧化氢有效利用率大于90%;进一步扩大氯丙烯的过量比例,虽然过氧化氢转化率和有效利用率有所增加,但氯丙烯的单程转化率下降,这就意味着将有更多的氯丙烯需要回收利用,势必增加能耗。

表5 nALC/nHPO对氯丙烯环氧化反应的影响
由于过氧化氢过量时并不能实现氯丙烯完全转化,导致过氧化氢有效利用率下降的同时,还必须对未转化的氯丙烯回收利用,因此宜选择氯丙烯过量的方案,nALC/nHPO宜选择在1.2~1.5之间。
2.4 氯丙烯与过氧化氢环氧化反应中的副反应
试验结果发现,氯丙烯与过氧化氢的环氧化反应体系中除主产物环氧氯丙烷外,还有一定量的副产物。反应温度越高、停留时间越长,副产物就越多。采用色谱-质谱联用仪对反应温度85 ℃、停留时间2 h的样品蒸去氯丙烯和大部分丙酮后进行定性分析。结果表明副产物有3个来源:①氯丙烯中杂质的氧化产物及其水解产物。3-氯丙烯中含有1-氯丙烯、2-氯丙烯、1,5-己二烯等可以发生氧化反应的杂质及不能发生氧化反应的氯代烷烃类杂质。1-氯丙烯、2-氯丙烯、1,5-己二烯氧化后分别生成了1-氯丙酮及其衍生物、丙酰氯及其衍生物、己二烯氧化产物的衍生物。②环氧氯丙烷的水解产物。③丙酮氧化分解生成的乙酸。这些副产物中,环氧氯丙烷的水解产物是最主要的副产物,它对环氧氯丙烷选择性的影响显著;氯丙烯中杂质的氧化不影响环氧氯丙烷的选择性,但影响过氧化氢的有效利用率;丙酮氧化生成的产物很少,必须浓缩后才能在色谱中检出。
3 结 论
(1)丙酮对氯丙烯和过氧化氢混合体系具有兼溶作用,与常用的甲醇相比,单位质量丙酮的兼溶能力低于甲醇,用量比甲醇约增加20%,但丙酮的蒸发热只有甲醇的82.4%,丙酮回收和循环利用的能耗与甲醇相当。丙酮作溶剂时环氧化体系主要的副反应是环氧氯丙烷的水解反应,而甲醇作溶剂时的副反应除环氧氯丙烷水解开环反应外,还有醇解开环反应,副产物种类和量更多。
(2)在搅拌釜反应器中,以丙酮为溶剂,在搅拌速率为300 r/min下反应60 min后,过氧化氢转化率可以达到97.1%;但不使用溶剂时,反应体系为液-液-固三相状态,对搅拌强度要求更高,搅拌速率需要增加到1 200 r/min时过氧化氢的转化率才可达到96.8%。温度低、时间短时反应不彻底,而温度高、时间长时则导致产物环氧氯丙烷发生更多的副反应,因此反应温度宜选择55~70 ℃,反应时间约60 min。
(3)nALC/nHPO小于1时,氯丙烯的转化率最高为90%;当nALC/nHPO大于1时,优化条件下可以获得大于97%的过氧化氢转化率和95%以上的环氧氯丙烷选择性,反应进料配比宜选择氯丙烯过量方案,nALC/nHPO控制在1.2~1.5之间。
致谢:感谢研究生张晓宁对本课题试验的贡献。

