一株耐铬真菌的分离鉴定及基于抗氧化酶的耐铬机制研究
朱超,马靓琛,王曼婷,马宏瑞,赵澜博
(1.陕西科技大学,陕西 西安 710021;2.西北工业大学,陕西 西安 710072)
引言
随着现代工业的快速发展,人类活动对环境的影响不断加剧,向环境中释放了大量的重金属,使得重金属污染面积逐步扩大,污染程度不断加深[1]。其中水溶性Cr(VI)的生物毒性是强致突变物质,美国的环境保护机构(USEPA)已将其认定为是严重危害人类健康的17 种化学物质之一[2]。相关研究还指出,高浓度Cr(III)的暴露也会对植物造成明显的毒害作用,影响其萌发过程,甚至抑制光合作用等生理过程[3]。皮革经过浸水、脱毛、鞣制及其他加工工段产生许多皮革废液,铬作为皮革废水的主要污染物之一,主要存在形式为Cr(VI)和Cr(III)[4]。中国制革产量全球第一,据统计制革废水年排放量约为1.38亿吨,其中总铬排放量在6.7 t 左右,在我国各类行业造成的Cr 污染中,制革行业占比超过40%[5-6],潜在环境健康风险较大[7]。
目前,含铬废水的治理方法主要有物理法[8]、化学法[9]和生物法[10]。物理法包括离子交换法,吸附法,膜分离法等[11]。化学法包括还原沉淀法、电解法和光催化还原法等,但都存在一定的局限性。近年来,由于生物法[12]具有经济高效、作用温度低、pH 适应范围宽、污泥量少、无二次污染[13]等优势,成为生物除铬技术和机制研究热点之一[14]。
目前关于生物除铬的研究主要集中在利用真菌或细菌对Cr(VI)进行吸附和还原[15]。王瑜谦[16]在高浓度铬污泥中得到的五种优势菌株在70 h 内对Cr(VI)(600 mg/L)的还原性可达80%以上[17]。王岩等[18]以浮游藻类制成的生物吸附剂在3 h 时对Cr(VI)的吸附可达92.10%。生物法治铬的主要核心在于耐铬机制的研究上,现有研究[19]表明当Cr(III)浓度低于10 mg/L 时,对普通小球藻细胞抗氧化酶系统中的SOD、CAT、POD 表现为促进作用,大于10 mg/L 时具有抑制作用。陈兰等[20]发现长根菇菌丝体对Pb(II)和Cd(II)的耐受能力分别为400 mg/L 和16 mg/L,其中SOD 和CAT 的活性呈现先升后降的趋势。相关研究发现其他重金属胁迫初期,黄孢原毛平革菌抗氧化酶系中的SOD 优先响应,其次是CAT 和GSH-Px[21]。
目前基于抗氧化酶系响应研究微生物耐受高浓度铬的机制研究主要集中在细菌和植物上[22],对于真菌的耐铬机制研究几乎没有,但真菌是制革含铬废水生物处理系统中的常见菌种,将其用于废水中Cr(VI)和Cr(III)的去除很有潜力,故阐明真菌的耐铬机制对优化其应用技术研发具有重要意义[23]。
本研究拟直接从高浓度铬液中分离鉴定耐受高浓度铬真菌,优化其培养条件,并研究其基于抗氧化酶系的耐受机制, 为应用此类菌种进行含铬废水处理或制备重金属铬吸附剂提供理论依据。
1 材料与方法
1.1 试验材料
实验菌种取自实验室被真菌污染的质量浓度为100 mg/L Cr-EDTA 溶液。
蛋白胨、葡萄糖、琼脂,北京奥博星生物技术有限责任公司;总抗氧化能力测试盒、总超氧化物歧化酶测试盒、过氧化氢测试盒、蛋白质测试盒,南京建成生物工程研究所。
ICP,美国THEM 公司;能谱仪,EDAX Octane Prime 公司;Multiskan FC 型酶标仪,赛默飞世尔(上海)仪器有限公司。
液体培养基采用改良马丁培养基:蛋白胨5 g,酵母浸出粉2 g,葡萄糖20 g,磷酸二氢钾1 g,硫酸镁0.5 g;固体培养基采用改良马丁培养基:蛋白胨5 g,酵母浸出粉2 g,葡萄糖20 g,磷酸二氢钾1 g,硫酸镁0.5 g,琼脂2%。
1.2 试验方法
1.2.1 菌种的分离培养
配制液体培养基,根据微生物实验方法,将培养基以及所需仪器进行分装灭菌。于超净工作台中,从真菌污染的100 mg/L 1∶1 Cr-EDTA 溶液中分离提取真菌菌株。将真菌用接种环挑出,分别放入三个装有100 mL 液体培养基的三角瓶中进行扩繁,150 r/min、30 ℃恒温振荡培养72 h,培养成功后,于4 ℃保存,作为接种物备用。
1.2.2 真菌的理化性质研究
观察生长出的菌株,肉眼观察菌株的特征,利用光学显微镜和电子显微镜观察其菌丝、分生孢子梗、分生孢子等形态特征,根据其菌落特征以及形态特征进行菌种的初步鉴定。
分别在培养温度为26,28,30,32,34 ℃时,培养真菌,研究温度对其生长影响,并确定最适生长温度。配制液体培养基,在加热状态下调节pH 分别为4,5,6,7,8,9,在培养皿分别培养真菌,研究pH对其生长影响,确定最适生长pH。根据确定的最适生长温度以及最适生长pH,进行其他因素对菌株生长的影响的研究。
1.2.3 菌株的分子生物学鉴定
液体扩培的菌体经1500 r/min 离心5 min 收集后,采用TSINGKE 植物DNA 提取试剂盒(通用型)进行基因组DNA 的提取,并由北京擎科生物科技有限公司进行18s rRNA 基因测序,所得序列在NCBI 数据库(https://www.ncbi.nlm.nih.gov/)中进行blast 比对分析,获得具有同源序列的菌株信息,下载相关参比序列,以Aspergillus flavus 为外类群,运用MEGA 5 软件通过邻接法(Join-neighbor)构建系统发育树,Bootstrap 检测设置为1000 次重复。
1.2.4 菌种的耐铬浓度梯度实验
(1)Cr(VI)标准溶液的配置
称取重铬酸钾2.835 g,蒸馏水定容至1000 mL,则该溶液中Cr(VI)的最终质量浓度是1 g/L,准确吸取1 g/L 的Cr(VI)标准溶液1,2,3,4,5 mL 分别置于250 mL 的三角瓶中,加液体培养基稀释至100 mL,即可得到Cr(VI)质量浓度为10,20,30,40,50 mg/L 的培养基,同理配制Cr (VI) 质量浓度为60,70,80,90,100 mg/L;200,300,400,500,600,700,800,900,1000 mg/L;2000,3000,4000,5000 mg/L 的培养基。
(2)菌种的驯化
将配制好的培养基以及所需仪器进行分装灭菌,使用接种环将培育出的母种分别接种到配制好的低浓度铬的液体培养基中,150 r/min 30 ℃振荡培养72 h,培养完成后置于冰箱4 ℃保存。
(3)耐铬浓度梯度实验
将配制好的培养基以及所需仪器进行灭菌,将培育出的母种分别接种到配制好的液体培养基中,150 r/min、30 ℃振荡培养72 h,根据菌株生长情况确定菌株的最高耐铬能力。
1.3 分析方法
使用测试盒分别测试T-AOC,T-SOD,CAT,严格按照测试盒要求进行测试,根据各自所需波长下得到的OD 值,计算出菌株的主要抗氧化酶。
COD 的测定严格按照测试盒操作表使用各试剂,于波长550 nm 处,1 cm 光径比色杯,双蒸水调零,比色,根据测定的结果由式1 求出总抗氧化能力。
总抗氧化能力(U/mgprot)=((测定OD 值- 对照OD 值)÷0.01))÷30×((反应液总量(mL)÷(取样量(mL)÷蛋白浓度(mgprot/mL)) (1)
T-SOD 的测定严格按照测试盒操作表使用各试剂,于波长550 nm 处,1 cm 光径比色杯,双蒸水调零,比色,根据测定的结果由式2 求出总SOD 活力。
总SOD 活力(U/mgprot)=((对照OD 值- 测定OD 值)÷对照OD 值)÷50%×((反应液总体积(mL)÷(取样量(mL))÷待测样蛋白浓度(mgprot/mL)(2)
CAT 严格按照测试盒操作表使用各试剂,于波长405 nm 处,1 cm 光径比色杯,双蒸水调零,测定各管吸光度值,根据测定的结果由式3 求出CAT 活力。
CAT 活力(mmol/mgprot)=((测定OD 值-空白OD 值)÷(标准OD 值-空白OD 值))×标准品浓度(163 mmol/L)×(1÷蛋白浓度(gprot/L)) (3)
蛋白浓度严格按照测试盒操作表使用各试剂,于波长550 nm 处,1 cm 光径比色杯,双蒸水调零,比色,根据测定的结果由式4 求出蛋白浓度。
待测样品蛋白浓度(g/L)=((测定OD 值-空白OD 值)÷(标准OD 值-空白OD 值))×标准品浓度(0.563 g/L) (4)
1.3.1 基于抗氧化酶的耐铬机制的研究
根据T-SOD,T-AOC,CAT,蛋白质的测试结果,进行线性拟合,分析出菌株的综合抗氧化能力,根据抗氧化酶活性和Cr(VI)的剂量效应关系,分析其耐铬机制,并通过暴露胁迫去除后培养实验,研究分离菌株的最大Cr(VI)耐受浓度。
1.3.2 菌株对Cr(VI)的吸收量
使用等离子电感耦合原子发射光谱仪(ICP-AES,陕西科技大学轻工学院),测定1000 mg/L Cr(VI)暴露72 h 后,剩余的Cr(VI)浓度,并基于250 mL 培养体系计算溶解态铬的百分比,同时使用环境扫描电子显微镜(分别在1500 kv 和1000 kv 发射电压;放大倍数3000 倍和4000 倍下观察)观察真菌形态,并配合能谱仪扫描测定菌体表面Cr 质量百分比作为吸附态Cr 浓度,依据培养体系中真菌总干重计算吸附态Cr 总量及占培养体系总铬的百分比,其余占比部分的铬则推定为进入真菌细胞内部的铬。
2 结果与讨论
2.1 菌株的理化性质
2.1.1 菌落特征
菌株的形态学鉴定如图1a,1b 所示。在固体培养基中上呈现肉眼可见的绒毛状菌体,菌株形态较大,质地疏松,外观干燥,白色,呈现或松或紧的形状,菌落和培养基间紧密连接,不易挑取,菌落正面为白色,背面为棕红色。
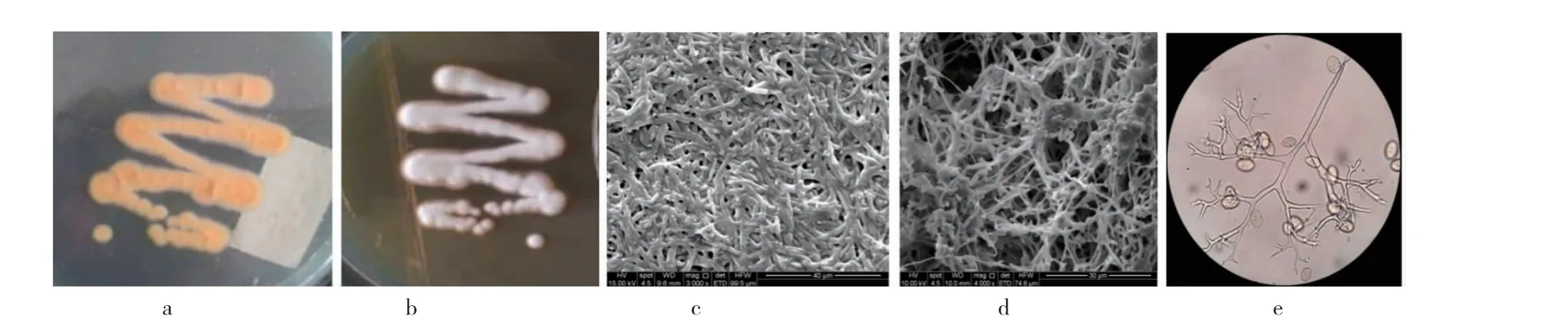
图1 菌株形貌观察(a 为菌体正面形态,b 为菌体背面形态,c 为分离菌株上浮菌体电子显微镜形貌图,d 为为下栖菌体电子显微镜形貌图,e 为分离菌株Cr1000 光学显微镜照片200×)Fig. 1 Morphology observation of strain(a is the front morphology of bacteria,b is the back morphology of bacteria,c is the electron microscope morphology of floating bacteria,d is the electron microscope morphology of benthic bacteria,e is the optical microscope photograph of isolated strain Cr1000 200×)
在液体培养基中,白色菌体上浮连成片,不易分开,不透明状孢子下沉,部分白色菌丝附着于瓶壁,上浮菌体和下栖菌体电子显微镜照片见图1c和1d,分离株光学显微镜观察结果分别见图1e,由图可知上浮菌体为气生菌丝构成的较致密的膜形态,下栖菌体则为基底菌丝和包子囊形成的复合体,光学显微镜显示分离株孢子囊在分枝的孢子囊梗上发育,孢子囊着生在弯曲的锥形分生孢子梗的顶端,具有典型的霜霉属特点,这与分子生物学鉴定的结果相一致。
2.1.2 分子生物学鉴定
图2 为基于分离株18s rRNA 基因序列比对构建的系统发育树,由进化距离和分簇信息可知,分离株Cr1000 和已报道的Peronospora meconopsidis 高度同源,经NCBI 数据库比对可知分离株Cr1000 同Peronospora meconopsidis18s rRNA 基因序列(登录号:KU948930.1)相似度为99.5%,可以确定本研究所得真菌分离株为霜霉属,有研究表明该菌株可通过一般抗性机制、生物吸附和流出机制处理重金属[24]。
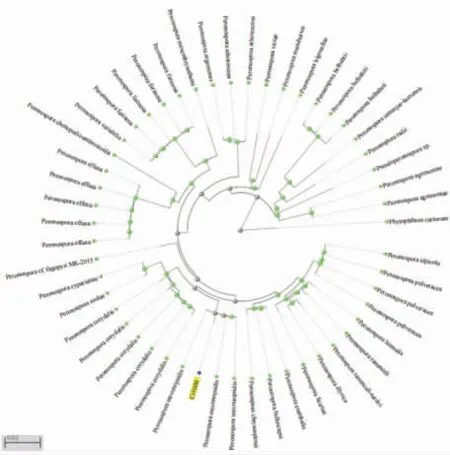
图2 分离株Cr1000 系统发育进化Fig.2 Phylogenetic tree of Cr1000 isolated strain
2.1.3 培养条件优化
根据实验结果得知,该菌株的最高耐铬质量浓度为1000 mg/L、在转速为150 r/min 条件下震荡培养72 h、最适培养温度为30 ℃、最适培养pH 为6。
2.2 菌株对Cr(VI)的吸附
以Cr1000 菌株(培养基含Cr (VI) 质量浓度为1000 mg/L 的菌株)为例,根据ICP-AES 测定结果(图3)可知,Cr1000 菌株培养液中剩余铬质量分数为26.4%,而Cr1000 菌体表面吸附铬量占菌体生物量约为33%,换算为培养体系中总铬质量分数24.3%,可推算Cr1000 菌体吸收的铬占比约为49.3%,说明该菌株有作为重金属铬活性吸附剂的价值。

图3 培养液中剩余Cr(VI)质量分数Fig. 3 Percentage of the residual Cr(VI) concentration in culture medium
2.3 抗氧化酶的耐铬机制
2.3.1 六价铬浓度与抗氧化酶系活性关系
图4 为不同Cr(VI)浓度下分离株抗氧化酶系活性的变化特征。
正常情况下,生物体内会存在一套完整的抗氧化体系清除自由基,使细胞内的自由基维持在适当水平,维持细胞的氧化还原平衡状态,但是当细胞遭遇逆境胁迫时,细胞内活性氧水平可能急剧上升,其产生速度可能超出了细胞平衡状态下的清除能力,造成细胞的氧化损伤。微生物体内活性氧的清除主要由某些酶系统和抗氧化物质来完成,其中T-AOC、T-SOD、CAT 是最重要的活性氧清除酶系统,SOD 将O2-歧化成H2O2,再由CAT 将H2O2分解成H2O 和O2,T-AOC 则为生物细胞整体抗氧化性的评价指标。
由图4 可知,在不同Cr(VI)浓度暴露情况下,分离株的T-AOC、T-SOD、CAT 的活性较之对照均显著增加,其中T-SOD 活性增速最快,在Cr(VI)质量浓度为155 mg/L 时可达到空白对照组的4 倍,CAT为对照组的3.8 倍,T-AOC 是为对照组的2 倍;当铬质量浓度范围在155~750 mg/L 时表现为缓慢增长,当质量浓度范围大于750 mg/L 是时,T-AOC 活力进入平稳期,但T-SOD、CAT 活力仍处于增长期。试验结果肯定了Cr(VI)暴露下该分离株可通过抗氧化系统的应激反应来平衡Cr(VI)导致的氧化胁迫。
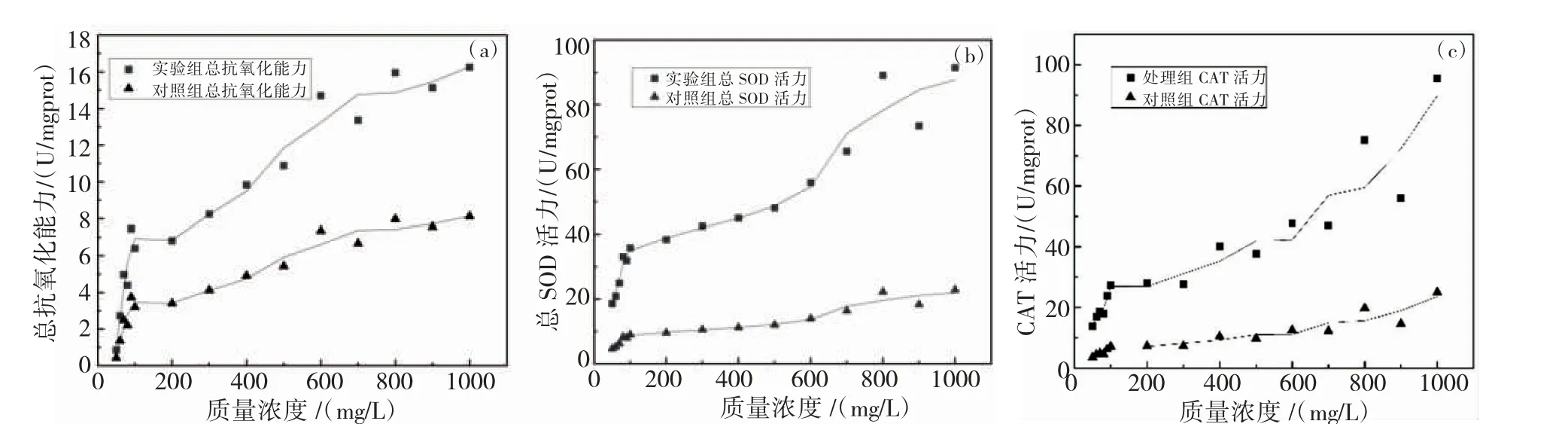
图4 Cr(VI)浓度与抗氧化酶活性响应图Fig.4 Responding variation of the activities of antioxidant enzymes to different Cr(VI) concentrations
2.3.2 各抗氧化酶之间的关系
根据各抗氧化酶的测定结果,T-AOC 与T-SOD 的关系,T-AOC 与CAT 的关系,T-SOD 与CAT 的关系如图5。
由图5a 可得,随着T-SOD 越高,菌株的总抗氧化能力越强,进行线性拟合,各参数如图5a,关系见公式5。
总抗氧化能力(U/mgprot)=0.204×总SOD 活力(U/mgprot)-0.535 (5)
根据T-AOC 与H2O2的测定结果,T-AOC 与CAT 的关系如图5b。
由图可得,随着CAT 越高,菌株的总抗氧化能力越强,进行线性拟合,各参数如图5b,关系见公式6。

图5 各抗氧化酶系之间的关系(a.T-AOC 与T-SOD 的关系,b.T-AOC 与CAT 的关系C.T-SOD 与CAT 的关系)Fig. 5 Relationship between antioxidant enzymes(a.Relationship between T-AOC and T-SOD,;b.Relationship between T-AOC and CAT;C.Relationship between T-SOD and CAT)
总 抗 氧 化 能 力(U/mgprot)=0.1942 ×H2O2(U/mgprot)+1.7782 (6)
根据T-SOD 与CAT 的测定结果,T-SOD 与H2O2的关系如图5c。
由图可得,随着CAT 越高,菌株的总抗氧化能力越强,进行线性拟合,各参数如图5c,关系见公式7。
总SOD 活力(U/mgprot)=0.9686×H2O2(U/mgprot)-7.945 (7)
3 结论
(1)该分离株为霜霉菌菌属,为好氧生长,能在较宽的pH 值(4~9)和温度(25~35 ℃)范围内生长,生长最适环境条件为150 r/min 震荡,pH=7,培养温度为30 ℃。
(2)重铬酸钾质量浓度为50~1000 mg/L 时,菌株生长随Cr (VI) 浓度升高受抑制情况逐渐增强,1000~5000 mg/L 时,菌株生长受到显著抑制,基本不生长,转移到不含铬培养基时,3000 mg/L 铬暴露下的菌株又重新生长,因此该菌的最高耐铬质量浓度为3000 mg/L。
(3)培养液浓度分别与抗氧化酶活性(T-AOC)、总超氧化物歧化酶(T-SOD)和过氧化氢酶(CAT)呈正相关,且活性增速从高到低为T-SOD、CAT、T-AOC,说明本菌对于铬的抗性是由抗氧化酶系协同作用的结果;抗氧化酶活性(T-AOC)与总超氧化物歧化酶(T-SOD)、抗氧化酶活性(T-AOC)与过氧化氢酶(CAT)、总超氧化物歧化酶(T-SOD)与过氧化氢酶(CAT)也分别呈线性正相关。

