神经电生理监测下显微镜和内镜微血管减压术治疗面肌痉挛疗效比较
周 祥,赵锦丽,葛立可,李 凡,孟 磊,王仲伟,金保哲
(新乡医学院第一附属医院神经外科,河南 卫辉 453100)
面肌痉挛(hemifacial spasm,HFS)是面神经运动障碍性疾病,其发病特点是面神经支配的肌肉出现不自主短暂或持续的间歇性抽搐,主要原因是面神经出脑干区(root exit zone,REZ)受到周围血管压迫而产生脱髓鞘变后神经纤维之间的连接异常所致[1-2]。HFS通常单侧发病,多从眼眶周围肌肉开始,随后扩展到面部表情肌、颈阔肌等其他头颈部肌群。虽然HFS不属于器质性病变,但严重时可出现睁眼困难、口角歪斜等症状,长期发作可能导致患者面瘫,严重影响患者生活质量及面部美观,导致社交尴尬和畏惧感,因此患者治疗的欲望强烈。微血管减压术(microvascular decompression,MVD)能通过解除责任血管对面神经REZ区的直接压迫而达到治疗目的,是目前HFS首选的外科治疗方式。通常在显微镜下进行微血管减压术,文献报道,显微镜微血管减压术(microscopic microvascular decompression,MMVD)治疗HFS的有效率为84.0%~94.1%,能明显改善患者的生活质量[3];但术中由于岩骨的阻挡,显微镜成像有一定的视野盲区,容易遗漏责任血管而影响疗效,或者术中为获得理想的REZ区显露而过度牵拉小脑引起术区出血、面瘫和听力下降等术后并发症。内镜具有多角度抵近观察等优势,无需过多牵拉小脑,REZ区即可清晰显示,不易遗漏责任血管,被越来越多地应用到微血管减压术中。本研究比较神经电生理监测下行内镜微血管减压术(endoscopic microvascular decompression,EMVD)与MMVD治疗HFS的效果,以期为临床HFS的治疗提供参考。
1 资料与方法
1.1 一般资料选择2014年12月至2020年6月新乡医学院第一附属医院神经外科收治的106例HFS患者为研究对象,其中男48例,女58例;年龄31~66(43.0±0.7)岁;左侧50例,右侧56例;病程 0.5~6.0(3.1±0.1)a;Cohen Alert面肌痉挛分级[4]:1级0例(外部刺激引起瞬目增多或出现面肌颤动),2级47例(眼睑、面肌自发轻微颤动,无功能障碍),3级55例(痉挛明显,有轻微功能障碍),4级4例(严重痉挛和功能障碍)。病例纳入标准:(1)原发性面肌痉挛患者;(2)Cohen Alert分级2级及以上,影响其日常生活和工作,并且患者手术意愿强烈;(3)病史长达0.5 a以上;(4)术前电生理监测到侧方扩散的患者;(5)未曾接受MVD 治疗的患者。病例排除标准:(1)曾接受诸如肉毒素注射、射频等有创性治疗措施的患者;(2)有开颅手术禁忌证者。根据治疗方法将患者分为对照组(n=54)和观察组(n=52)。对照组:男24例,女30例;年龄31~66(43.1±0.9)岁;左侧28例,右侧26例;病程 0.5~6.0(3.1±0.2)a;Cohen Alert分级1级0例,2级25例,3级27例,4级2例。观察组:男24例,女28例;年龄32~65(42.9±1.1)岁;左侧22例,右侧30例;病程0.5~5.0(3.2±0.1)a;Cohen Alert面肌痉挛分级:1级0例,2级22例,3级28例,4级2例。2组患者的性别、年龄、病程和Cohen Alert分级比较差异无统计学意义(P>0.05),具有可比性。本研究获得医院医学伦理委员会审核批准,患者知情同意并签署知情同意书。
1.2 方法
1.2.1 术前相关检查2组患者均于术前常规行三维时间飞跃法磁共振体层血管造影(three dimensional-time of flight-magnetic resonance tomographic angiography,3D-TOF-MRTA)和磁共振成像(magnetic resonance imaging,MRI)检查,明确面神经REZ区与周围血管的关系,初步判断出责任血管,了解责任血管的走形,同时排除颅内其他病变引起的继发性面肌痉挛(图1);根据MRI判断小脑体积/后颅窝容积比,>90%提示后颅窝容积小,术中脑脊液释放困难,需术前留置腰大池,便于引流脑脊液,降低颅内压,减轻对小脑的牵拉;≤90%提示术中可有效释放脑脊液,术前无需行腰大池引流。术前应用Nicolet EDX神经电生理监测仪(美国Nicolet公司)行双侧面神经肌电图监测,对比了解病灶侧的侧方扩散反应(lateral spread responses,LSR)情况和面神经损伤程度。

A:MRI T2提示右侧桥小脑角区蛛网膜囊肿;B:3D-TOF-MRTA提示右侧面神经根部血管压迫(小脑前下动脉);C:3D-TOF-MRTA提示右侧三叉神经根附近无血管。图1 采用EMVD治疗的右侧面肌痉挛伴桥小脑角区蛛网膜囊肿患者术前MRI和3D-TOF-MRTA检查结果Fig.1 Results of MRI and 3D-TOF-MRTA of patients with right hemifacial spasm and arachnoid cyst in cerebellopontine angle before operation treated by EMVD
1.2.2 手术方法2组患者均取侧卧位,患侧在上,头与上半身抬高15°,颈部稍前屈、头顶下垂约15°并向健侧旋转,使乳突位于最高点。行耳后发髻内0.5 cm竖切口,长约5.0 cm。颅骨钻孔后铣下小游离骨瓣,扩大骨窗外至乙状窦后缘,约2.5 cm×2.0 cm大小,无需暴露横窦,悬吊硬膜后Y形切开。对照组患者采用MMVD:患者在开颅后于显微镜下解剖桥小脑角蛛网膜,释放脑脊液,牵开小脑半球,锐性分离后组颅神经和面听神经周围蛛网膜,探查面神经REZ区,辨认出责任血管,解剖游离血管,取合适大小的Teflon垫棉采用多点位垫入隔开责任血管和面神经REZ区,严密缝合硬膜,骨瓣复位并固定,常规关闭。观察组患者采用EMVD:患者在开颅后由助手持内镜行双手操作,用吸引器和显微剪刀锐性切开桥小脑角区蛛网膜,缓慢释放脑脊液。待脑内压力下降后用薄层明胶海绵和棉片保护小脑半球外侧,用吸引器做适当牵开,显微剪刀依次锐性分离舌咽神经和面听神经周围的蛛网膜,暴露绒球,在其深面探查面神经根REZ区;用常用30°镜头抵近REZ区从不同角度仔细观察神经根周围结构,辨认出责任血管,解剖游离血管,避开穿支血管后取合适大小的Teflon垫棉采用多点垫入的方法隔开责任血管和面神经REZ区(图2),应用内镜潜水技术确认垫棉无移位,严密缝合硬膜,骨瓣复位并固定,常规关闭。术后2组患者均随访12~36(18.0±2.3)个月。

A:术中暴露蛛网膜囊肿;B:显露面神经REZ区和责任血管;C:分离开责任血管;D:垫开责任血管;E:三叉神经根受蛛网膜囊肿压迫向上弧形弯曲。图2 采用EMVD治疗的右侧面肌痉挛伴桥小脑角区蛛网膜囊肿患者术中情况Fig.2 Intraoperative conditions of patients with right hemifacial spasm and arachnoid cyst in cerebellopontine angle treated by EMVD
1.3 观察指标
1.3.1 LSR术中应用Nicolet EDX神经电生理监测仪(美国Nicolet公司)监测LSR。参照Moller和Jannetta方法[5]分为2组监测LSR:一组为刺激电极放置于面神经下颌缘支,接受电极放置在同侧眼轮匝肌,获得的LSR标记为LSR-1;另一组为刺激电极放置于面神经颧支,接受电极位于同侧颏肌,获得的LSR标记为LSR-2。维持麻醉期间不使用肌松剂,麻醉后进行刺激,刺激强度3~50 mA,记录诱发LSR的最小刺激强度,设为诱发阈值;术中垫开血管后出现原有LSR波幅下降或消失,则加大刺激量,最小刺激量为诱发阈值的2倍,最大刺激强度可加至50~70 mA,仍未引出LSR,则判定LSR波形消失。
1.3.2 临床疗效术后1 a评估2组患者的疗效,参考文献[6-7]进行疗效评估:症状完全消失为治愈;症状基本消失仅在情绪紧张等特定情况下偶尔出现为明显缓解;症状减轻但仍有发作为部分缓解;症状无缓解为无效。计算治疗有效率,治疗有效率=(治愈例数+明显缓解例数)/总例数×100%。
1.3.3 并发症观察2组患者继发性颅内出血(包括远隔部位的血肿和术区的血肿)、周围性面瘫(根据House-Brackmann分级[8]分为轻度、中度、重度3个等级)、听力下降和声音嘶哑、感染(包括颅内感染和切口感染)等并发症。
1.4 统计学处理应用SPSS 20.0软件进行统计学分析,计数资料以例数和百分率表示,2组间比较采用χ2检验,P<0.05为差异有统计学意义。
2 结果
2.1 2组患者责任血管判断准确率比较对照组患者术前判断责任血管为小脑前下动脉38例,小脑后下动脉15例,椎基底动脉1例;术中判断责任血管为小脑前下动脉38例,小脑后下动脉14例,小脑后下动脉和椎动脉1例,椎基底动脉1例;术前责任血管判断准确率为98.1%(53/54)。观察组患者术前判断责任血管为小脑前下动脉34例,小脑后下动脉16例,椎基底动脉2例;术中判断责任血管为小脑前下动脉33例,小脑后下动脉16例,小脑前下动脉和小脑后下动脉1例,椎基底动脉2例;术前责任血管判断准确率为98.0%(51/52)。2组患者术前责任血管判断准确率比较差异无统计学意义(χ2=6.914,P>0.05)。
2.2 2组患者临床疗效比较对照组患者治愈40例,明显缓解10例,部分缓解3例,无效1例,有效率为92.59%(50/54);观察组患者治愈43例,明显缓解6例,部分缓解2例,无效1例,有效率为94.23%(49/52);2组患者治疗有效率比较差异无统计学意义(χ2=0.115,P>0.05)。
2.3 2组患者术中电生理监测LSR-1和LSR-2结果及疗效对照组和观察组分别有38例和40例患者术前存在LSR-1和LSR-2,术中LSR-1和LSR-2均消失(图3),术后均临床治愈。对照组12例LSR-1或者LSR-2完全消失且另一LSR波幅降低50%以上患者中,2例治愈,10例明显缓解;观察组9例LSR-1或者LSR-2完全消失且另一LSR波幅降低50%以上患者中,3例治愈,6例明显缓解。对照组术中LSR-1和LSR-2均未消失4例患者中,3例部分缓解,1例无缓解;观察组术中LSR-1和LSR-2均未消失3例患者中,2例部分缓解,1例无缓解。
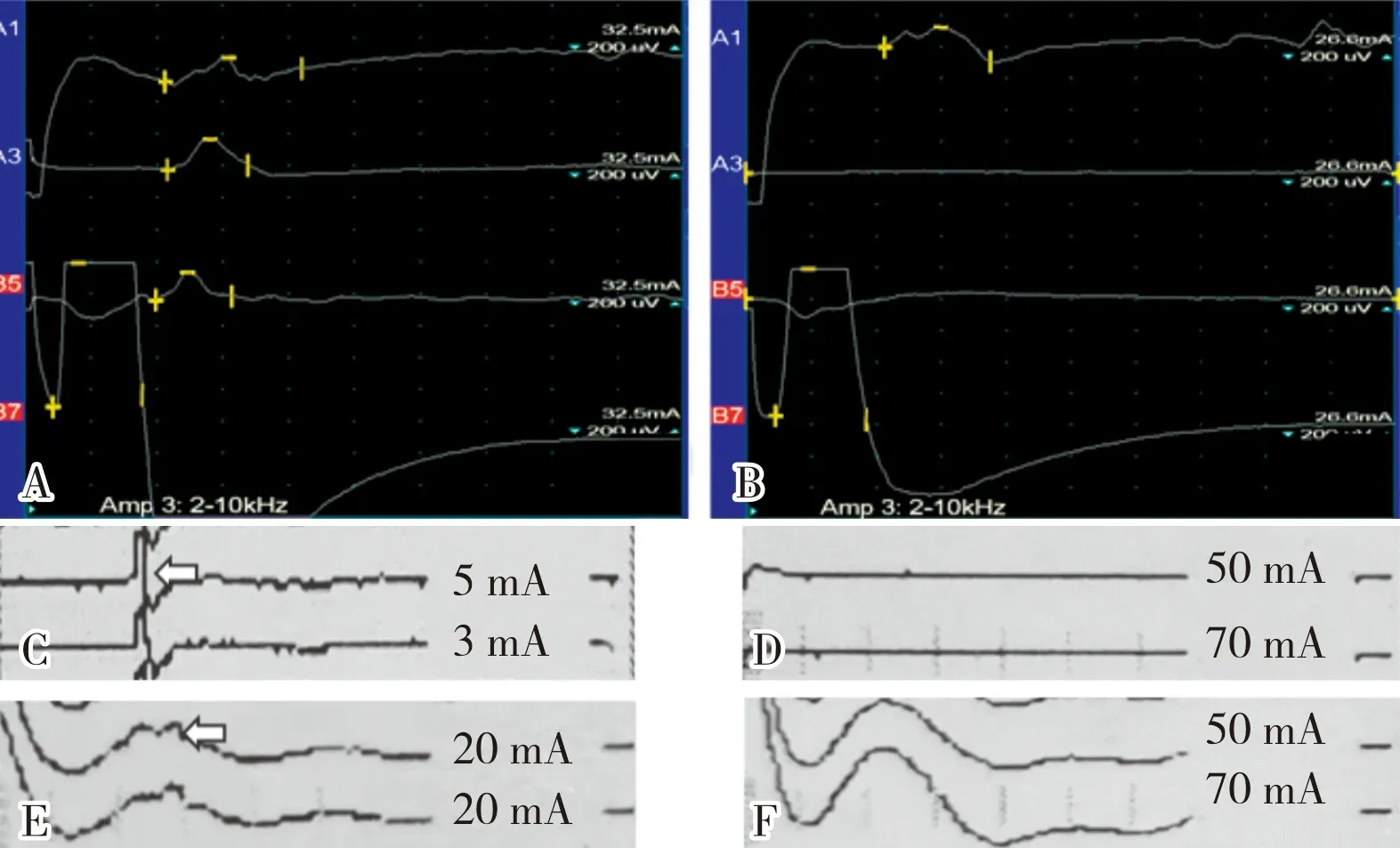
A:术前右侧面神经肌电图提示存在LSR-1(B5)和LSR-2(A3);B:术后右侧面神经肌电图提示LSR-1(B5)和LSR-2(A3)均消失;C:术中电生理监测减压前3~5 mA刺激引起LSR-2;D:减压后50~70 mA刺激LSR-2消失;E:术中减压前20 mA刺激引起LSR-1;F:术中减压后50~70 mA刺激LSR-1消失。图3 采用EMVD治疗的右侧面肌痉挛伴桥小脑角区蛛网膜囊肿患者术前、术中和术后神经电生理监测结果Fig.3 Results of preoperative,intraoperative and postoperative neurophysiological monitoring of patients with right hemifacial spasm and arachnoid cyst in cerebellopontine angle treated by EMVD
2.4 2组患者术后并发症比较对照组患者术后出现术区出血1例,听力中度下降2例,周围性面瘫1例,声音嘶哑1例,无切口和颅内感染患者;对照组患者术后并发症发生率为9.25%(5/54)。观察组患者术后出现幕上对侧的薄层急性硬膜下血肿1例,量约10 mL左右,有轻微头痛(保守治疗1个月后血肿吸收,症状消失),此患者术前肌电图提示面神经运动传导波幅较对侧明显下降,面神经不完全损伤,术前面神经损伤2级,术后无加重;术后听力中度下降1例;无切口和颅内感染及术区出血患者。观察组患者术后并发症发生率为3.84%(2/52)。2组患者术后并发症发生率比较差异无统计学意义(χ2=1.259,P>0.05)。
3 讨论
HFS是神经外科的常见病,发病率较高,其药物治疗效果较差,复发率高。MVD是针对HFS的病因治疗手术方法,手术成功的关键在于辨别责任血管并进行有效减压,其效果确切,术后复发率低,已成为主要治疗方法。目前,显微神经外科手术技术已较为成熟且被广泛应用。研究报道,MMVD治疗HFS患者明显缓解率为50.0%~61.5%,部分缓解率为20%~50%,超过3 a随访的有效率为79%~100%,复发率为1%~4%;但手术通常采用枕下经乙状窦后入路,开颅采用小骨窗,由于显微镜的管状视野特性,且小骨窗限制了显微镜的多角度观察,面神经REZ显露受限,减压过程中为增加显露范围,需要压迫小脑绒球以及牵拉面听神经复合体,术后可出现听力障碍(2%~3%)、面瘫(1%~2%)和后组颅神经功能障碍(0.5%~1.0%)等并发症[9-10]。近年来,随着神经内镜技术的发展,EMVD作为一种新颖的手术方法应用到临床,在脑室病变、脑出血、经鼻垂体瘤等手术中被广泛应用,已经逐步取代显微镜。内镜广角成像及抵近观察等特点可以弥补显微镜下管状视野的不足,能够清晰显示小脑脑桥角区神经、血管的解剖关系,显示细小血管,减少术中损伤面、听神经滋养血管的风险。因此,研究EMVD 治疗HFS的有效性和安全性以及手术优势、术中操作技巧是目前EMVD治疗的研究热点。
有研究报道,EMVD手术治愈率为93.3%,总有效率为97.8%,术后并发症的总发生率仅为4.4%,认为EMVD治疗HFS有效率高,并发症少[7]。本研究结果显示,对照组患者治愈40例,明显缓解10例,部分缓解3例,无效1例,有效率为92.59%(50/54);观察组患者治愈43例,明显缓解6例,部分缓解2例,无效1例,有效率为94.23%(49/52);对照组与观察组患者治疗有效率比较差异无统计学意义。说明MMVD和EMVD治疗HFS术中均可以有效暴露REZ区,正确辨认责任血管,有效性均较好;但2组患者的治疗有效率比较差异无统计学意义,考虑可能与样本量小有关。
HFS患者术前行3D-TOF-MRTA,有利于了解责任血管的走行方向和毗邻关系,制定合适的手术计划,术中可有助于快速找到责任血管。本研究结果显示,对照组患者术前判断责任血管为小脑前下动脉38例,小脑后下动脉15例,椎基底动脉1例;术中判断责任血管为小脑前下动脉38例,小脑后下动脉14例,小脑后下动脉和椎动脉1例,椎基底动脉1例;术前责任血管判断准确率为98.1%(53/54)。观察组患者术前判断责任血管为小脑前下动脉34例,小脑后下动脉16例,椎基底动脉2例;术中判断责任血管为小脑前下动脉33例,小脑后下动脉16例,小脑前下动脉和小脑后下动脉1例,椎基底动脉2例;术前责任血管判断准确率为98.0%(51/52)。对照组与观察组患者术前责任血管判断准确率比较差异无统计学意义,说明术前应用3D-TOF-MRTA了解责任血管,对于MMVD和EMVD 术中确认责任血管均有非常重要的指导作用。
神经电生理检查和监测已经广泛应用到HFS的诊断和治疗中,普遍认为术前电生理检查LSR具有非常重要的辅助诊断意义,术中神经电生理监测LSR的消失可以作为减压充分的实时指标[11-14]。本研究结果显示,2组患者术前神经电生理检查均能检测到LSR-1和LSR-2,证实出现LSR可以作为原发性面肌痉挛的辅助诊断。此外,本研究结果显示,术中电生理监测LSR-1和LSR-2均消失且术后LSR-1和LSR-2亦均消失的78例患者术后均临床治愈,其中对照组38例,观察组40例。对照组12例LSR-1或者LSR-2完全消失且另一LSR波幅降低50%以上患者中,2例治愈,10例明显缓解;观察组9例LSR-1或者LSR-2完全消失且另一LSR波幅降低50%以上患者中,3例治愈,6例明显缓解。对照组术中LSR-1和LSR-2均未消失4例患者中,3例部分缓解,1例无缓解;观察组术中LSR-1和LSR-2均未消失3例患者中,2例部分缓解,1例无缓解。这说明无论采用MMVD还是EMVD治疗,患者术中电生理监测至少LSR-1或者LSR-2消失且另一LSR波幅下降超过50%,术后可以达到治愈或者明显缓解。随访1例右侧面肌痉挛伴桥小脑角区蛛网膜囊肿患者,术前电生理检查LSR-1和LSR-2均存在,术中监测和术后复查LSR-1和LSR-2均消失,这也证明LSR可作为诊断面肌痉挛的相对客观指标。此外,此患者术中发现责任血管上蛛网膜小梁较多,需充分锐性解剖游离责任血管,再进行垫片减压。因此,术中监测LSR可指导正确判断责任血管和适时终止手术;建议术中同时监测LSR-1和LSR-2,将至少LSR-1或者LSR-2消失且另一LSR波幅下降超过50%以上作为减压充分的依据。
MVD术后的常见并发症是听力障碍和面瘫,严重并发症是小脑挫伤和术区出血。本研究结果显示,对照组患者术后出现术区出血1例,听力中度下降2例,周围性面瘫1例,声音嘶哑1例,并发症发生率为9.25%(5/54);观察组患者术后出现远隔部位的出血1例和听力下降1例,并发症发生率为3.64%(2/52)。结果说明,MMVD和EMVD治疗HFS安全性均较好,并发症发生率均低;但2组患者术后并发症发生率比较差异无统计学意义,推测与病例数少有关。文献报道,手术时间长导致听神经缺乏脑脊液保护和手术对小脑的过度牵拉是MVD术后发生听力下降和出血的主要原因,远隔部位的出血和术区出血与脑脊液过快释放导致脑表面和硬膜间的静脉损伤和穿支血管的损伤相关[15-17]。因此,提高操作技术和缩短手术时间是减少术后并发症的关键。通过本研究发现,EMVD存在以下的优势和技巧:(1)内镜深部良好的照明系统和局部放大效果使术者在减少牵拉小脑半球的情况下可以获得良好的全景视野,30°镜头引导下无需牵拉小脑绒球即能清楚地观察到面神经REZ区和血管的解剖关系,用微弯的手术器械进行分离和减压,破坏的蛛网膜界面范围小,损伤小。(2)对面神经REZ区进行近距离、多角度地反复观察,确定血管、神经的关系,更有利于找到并确认责任血管。(3)抵近观察明确责任血管垫入点是否有穿支血管发出,减少术后出血或者梗死的风险。(4)术中应采用多点支撑架桥式分担压力的方法进行垫片[18],先用湿的团状垫棉垫开,然后用干的絮状垫棉固定,确保垫棉不易移动。(5)利用潜水技术判断垫棉是否移位,保障手术效果。
综上所述,MMVD和EMVD治疗HFS的有效性和安全性均较好,且2种术式的有效性和安全性无显著性差异;术前应用3D-TOF-MRTA了解HFS患者REZ区责任血管和面神经根的关系有助于术中确认责任血管,术前和术中神经电生理监测 LSR-1和LSR-2可指导正确判断责任血管和适时终止手术,为手术疗效提供客观判断依据。因此,在技术及条件成熟的单位,EMVD可作为血管减压术的技术手段之一。但本研究为回顾性研究,样本量小,有待大样本、前瞻性随机对照试验进一步验证结论。

