气肿性膀胱炎诱发糖尿病酮症酸中毒一例并文献复习
刘亭亭,王媛,王垚,李理,张云,沙贵明
(北京老年医院老年示范病房,北京100095)
1 临床资料
患者,女性,72岁,主因“口干、多饮、多尿10余年,呕吐、乏力4 d”于2020年12月4日收入北京老年医院。患者10年前无诱因出现口干、多饮,伴夜尿多,体质量变化不详,就诊外院完善糖耐量试验,明确诊断为2型糖尿病,具体不详,未规律服药治疗,未规律监测血糖,血糖控制情况不详。6年前出现视物模糊、手足麻木,外院就诊诊断为糖尿病视网膜病变、糖尿病周围神经病变,予眼底激光治疗,仍未规律服药及监测血糖。入院4 d前患者突发恶心、呕吐,伴乏力、精神萎靡,呕吐物为胃内容物,否认腹痛、发热及腹泻等,进食减少。就诊于我院急诊科,完善相关检查。血气分析:酸碱度7.265,二氧化碳分压13.2 mmHg(1 mmHg=0.133 kPa),氧分压114 mmHg,标准碳酸氢盐10.4 mmol/L,实际碱剩余-19.9 mmol/L,乳酸1.7 mmol/L;尿常规+镜检:尿比重1.025,尿pH 5.0,尿亚硝酸盐+,尿葡萄糖+4,尿酮体+2,尿白细胞(镜检)106/μl,白细胞+1,隐血+1,尿蛋白+1;糖化血红蛋白16.5%;生化:谷丙转氨酶16.4 U/L,血糖32.4 mmol/L,尿素15 mmol/L,肌酐75.1 μmol/L,血钾3.3 mmol/L,血钠123 mmol/L;血常规:白细胞计数27×109/L,中性粒细胞百分比89.3%,血红蛋白、血小板计数均正常。考虑2型糖尿病、糖尿病酮症酸中毒、泌尿系感染、低钾血症、低钠血症,予患者心电监护,监测血糖,补液、胰岛素降糖、氯化钾补钾、浓氯化钠补钠等治疗,头孢他啶抗感染,为求进一步诊治收入我科。患者自病来,精神差、食欲不佳、尿频、排便正常及体质量变化不详。
既往病史:诊断高血压病40余年,最高血压160/90 mmHg,口服北京降压0号1# qd降压,未监测血压,控制不详;诊断高脂血症20余年,未治疗。1年前发现腰椎间盘突出,腰痛行动不便,卧床为主,如厕需搀扶,因无人照料,经常在床上大小便,导致会阴局部皮肤发红。发病前2个月,进食明显减少,体质量变化不详。个人史、婚育史、家族史无特殊。
入院查体:体温37.4 ℃,血压130/63 mmHg,心率94次/min,呼吸20次/min,呼气中有烂苹果味,营养中等,神志清楚,皮肤黏膜干燥,双眼凹陷,会阴部及大腿根部皮肤发红,无破溃,双肺呼吸音清,未闻及干湿性啰音,心率快、律齐,腹软,下腹部压痛,无反跳痛,双下肢不肿。
入院诊断:2型糖尿病、糖尿病性酮症酸中毒、糖尿病性视网膜病变、糖尿病周围神经病变、泌尿系感染、低钠血症、低钾血症、高血压病(2级 极高危)、高脂血症及腰椎间盘突出。
诊疗经过:入院后完善检查。血气分析加离子提示:酸碱度7.439,二氧化碳分压33.1 mmHg,氧分压114 mmHg,标准碳酸氢盐22 mmol/L,实际碱剩余-1.5 mmol/L。尿常规+镜检:尿pH 5.5,尿葡萄糖+4,尿酮体+2,尿镜检白细胞5 400/μl,红细胞180/μl。血常规:白细胞计数19.67×109/L,中性粒细胞百分比83.6%,血红蛋白、血小板计数正常。降钙素原2.48 ng/ml,超敏C反应蛋白95.15 mg/L,血糖23 mmol/L。入院后予患者静脉补液,胰岛素静脉泵入降糖。后患者酮症酸中毒纠正,停用胰岛素泵,予患者糖尿病教育,调整降糖方案为甘精胰岛素8 U于睡前皮下注射,生物合成人胰岛素注射液6 U于三餐前30 min皮下注射降糖,患者空腹血糖波动于7~9 mmol/L,餐后血糖波动于8~11 mmol/L。患者血白细胞计数及中性粒细胞比例升高,超敏C反应蛋白升高,降钙素原升高,结合尿常规白细胞明显升高,考虑泌尿系感染,查体患者下腹部压痛,以膀胱区为著,立即完善全腹部CT检查评估,结果提示:膀胱壁增厚,膀胱壁及膀胱腔内积气(图1)。结合患者年龄、糖尿病病史及辅助检查结果,考虑气肿性膀胱炎,予留取尿管,留取尿液标本送检细菌性检查,经验性予患者头孢噻肟钠舒巴坦抗感染治疗,患者尿白细胞仍多,尿色浑浊。后患者尿培养结果:白色假丝酵母菌(80×103CFU/ml)、光滑假丝酵母菌(>105CFU/ml),药敏结果提示对氟康唑剂量依赖性敏感,两性霉素B敏感,因我院无两性霉素B药物,经与家属商议,对氟康唑剂量依赖性敏感,遂予加倍剂量的氟康唑氯化钠0.4 g qd抗真菌,经抗感染治疗后复查患者尿中白色假丝酵母菌消失,光滑假丝酵母菌菌量较前减少不明显。考虑治疗效果不佳,申购两性霉素B脂质体治疗,后复查尿常规正常,尿培养无细菌、真菌生长。再次复查腹部CT,膀胱内气体消失。查体腹部无压痛,治疗好转后出院随诊。
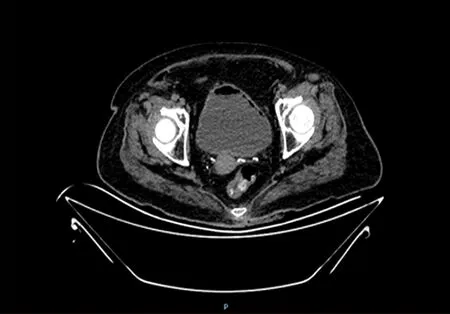
图1 全腹部CT显示膀胱壁增厚,膀胱壁及膀胱腔内积气Figure 1 Whole abdominal CT shows bladder wall thickening, bladder wall and bladder cavity gas
2 讨 论
糖尿病患者容易并发各种感染,感染可诱发糖尿病急性并发症,如糖尿病酮症酸中毒。泌尿系感染是糖尿病常见的感染类型,气肿性膀胱炎是好发于糖尿病患者的一种罕见的泌尿系统感染。气肿性膀胱炎临床表现无明显特异性,经查阅文献大部分为个案报道,临床医护人员对该病认识相对不足,容易漏诊、误诊,严重者可危及患者生命,为提高对该疾病的认识,本文对气肿性膀胱炎进行文献复习。
气肿性膀胱炎是以气体积聚于膀胱壁及膀胱腔内为特征的少见类型的膀胱炎。好发于50~70岁女性糖尿病患者[1],糖尿病患者罹患此病的风险是非糖尿病患者的7倍[2],女性糖尿病患者比男性患者发病率高[3]。其他危险因素包括免疫功能低下、神经源性膀胱、导尿、老年人及尿路梗阻等[4]。目前该病的发病机制尚不明确[5],根据现有报道,主要的机制为大肠埃希菌、肺炎克雷伯菌等产气菌进入膀胱上皮细胞内,发酵糖尿病患者尿液中高浓度的糖,而致局部酸性物质增多,膀胱上皮细胞内pH下降。病原菌在酸性环境下产生的一种特殊的酶,可将酸性底物转化成二氧化碳气体,膀胱上皮细胞内气体积聚,在壁内形成气泡,并破溃进入膀胱腔内形成腔内积气。而这一过程发生在非糖尿病患者中时,致病菌可以以尿液中白蛋白作为产气底物[6]。约有7%的气肿性膀胱炎症患者没有任何临床症状,其他患者可表现为发热、血尿、尿频、尿急、尿痛、排尿困难、下腹部胀痛、恶心、呕吐及腹泻等。体格检查可能有下腹部膨隆、压痛,叩诊膀胱区呈鼓音,气尿是气肿性膀胱炎最典型的临床表现[7]。严重的膀胱感染和气体积聚,膀胱内压力不断增高,可能导致膀胱破裂,压力上升导致输尿管扩张、肾盂积水、梗死,出现肾功能不全、气腹、腹腔感染,甚至脓毒性休克,危及生命[2,8]。实验室检查结果显示,血常规白细胞计数伴中性粒细胞比例升高,血糖升高;尿常规白细胞及红细胞增多,尿蛋白阳性,尿糖升高,尿酮体升高,尿培养可见大肠埃希菌、肺炎克雷伯杆菌、铜绿假单胞菌、产气荚膜梭状芽孢杆菌、粪肠球菌、奇异变形菌、真菌(光滑假丝酵母菌,热带假丝酵母菌)等[8]。膀胱CT提示“气抱球征”是气肿性膀胱炎最具特异性CT征象,对于气肿性膀胱炎诊断敏感度达90.6%,特异度达100%[9],表现为膀胱壁间、内外壁下弥漫分布的串珠样积气,像气体环绕球体,所以称为“气抱球征”。另一常见CT征像为膀胱腔内积气伴气液平面,其诊断灵敏度为87.1%,特异度为50%,表现为膀胱腔内积气伴气液平面。其他间接征像有膀胱壁增厚毛糙、膀胱壁强化、膀胱周围脂肪间隙浑浊模糊、膀胱肿大、气腹、腹盆腔积液及肾盂输尿管积水等[10]。超声检查在诊断气肿性膀胱炎中具有一定的局限性,容易误判为肠气干扰[11],但可以通过泌尿系超声发现是否伴上尿路输尿管扩张表现。膀胱镜下检查可见全膀胱黏膜附着有弥漫性脓苔,黏膜红肿、充血,黏膜层可见小气泡分布,以镜挤压气泡可呈“沼泽样”释放气体,但一些研究认为它对诊断不是必要的[12]。治疗方面,可通过导尿术对膀胱内气体及尿液进行引流,积极抗感染,严格控制血糖;也可通过高压氧辅助治疗厌氧菌感染[13]。复杂的气肿性膀胱炎,若保守治疗不成功,可能需要外科手术干预。对于预后,气肿性膀胱炎的总死亡率是7%[8],若引起更为严重的气肿性肾盂肾炎,则死亡率可高达50%[2]。
综上,气肿性膀胱炎是一种罕见的疾病,好发于老年女性严重或血糖未控制的糖尿病患者。随着我国社会老龄化程度的进展,气肿性膀胱炎的发病率也越来越多,但因气肿性膀胱炎的临床表现缺乏特异性,主要依赖于影像学检查进行诊断。很多临床医师对该病的认识不足,容易出现漏诊,故提高临床医师对该病的认识,在收治老年糖尿病患者或具有相关危险因素的非糖尿病患者时,如合并泌尿系感染,应考虑到该病可能,合理安排影像学检查,以证实或排除气肿性膀胱炎的存在。

