碳中和技术研究进展及对农业碳减排的展望
年琳玉 王梦军 孙笑阳 曹崇江


摘要:为了控制全球气候变化所带来的影响,《巴黎协定》提出将全球平均气温上升限制在1.5℃。要实现这一目标亟须解决CO2排放量攀升的问题,并部署CO2净零排放的技术。其中农业碳排放约占全球温室气体排放总量的1/3,因此推进农业领域减排固碳技术是发展农业碳中和的重要举措。本文主要介绍了CO2捕集、封存及转化技术的研究进展,具体包括:利用化学、材料领域的物理化学等方法对CO2进行捕集,并通过光电催化技术对CO2进行高效转化;地质、海洋封存CO2并通过矿物合成方法实现碳的循环再利用;微生物细胞工厂基于合成生物学技术将CO2转化为燃料及化学物质,并对其在农业碳中和上的研究方向进行展望,以期为碳中和技术在农业中的应用提供理论依据和参考。
关键词:CO2捕集;封存与转化技术;研究进展;农业碳中和;展望;碳减排
中图分类号:S181文献标志码:A
文章编号:1002-1302(2022)11-0001-12
收稿日期:2021-07-28
基金项目:国家重点研发计划(编号:2019YFC1605804)。
作者简介:年琳玉(1993—),女,安徽蚌埠人,博士,主要从事新型智能食品包装材料研制及农产品精准碳调控技术研究。E-mail:nianlinyu0305@163.com。
通信作者:曹崇江,博士,教授,主要从事新型智能食品包装材料研制及在果蔬保鲜品质的精準调控研究。E-mail:ccj33@163.com。
全球气候变化背景下,CO2减排是当今国际社会的共识和一致努力的行动目标。据美国国家海洋和大气管理局(NOAA)统计,温室气体排放每年增长1.5%,2020年大气CO2浓度已达到414 mL/L,造成了严重的温室效应[1]。作为全球最大的温室气体排放国之一,中国在全球气候治理中扮演着至关重要的角色,中国承诺于2030年前CO2排放达到峰值,争取2060年前实现碳中和。随之而来的是对减排技术的需求,其中碳捕集、封存与转化技术能够从源头上避免CO2排放,并能通过CO2移除技术大规模地减少大气中已有的CO2,是将全球升温稳定在低水平的关键技术之一[2]。
联合国粮农报告显示,粮食体系温室气体排放比例日渐增加。据估计,2018年粮食体系排放的CO2当量高达160亿t,目前粮食体系碳排放量占温室气体排放总量的33%,这已经超出了全球粮食体系温室气体的排放预期[3]。因此,推进农业领域减排固碳,降低农业生产温室气体排放强度,是全球碳中和的重要举措。据报道,当前农业领域实现碳中和的途径主要包括3个方面:(1)降低排放强度,如施用缓释肥、节水灌溉以及2种措施配合等技术,可分别减少稻田温室气体排放19%、21%、41%。(2)提高固碳能力。目前主要包括推动保护性耕作、秸秆还田、有机肥施用、人工种草等措施,提高土壤有机质含量,提升温室气体吸收和固定能力。(3)节能与可再生能源替代。大力发展生物质能、太阳能等新能源,抵扣化石能源排放[4-5]。但当前,农业领域要实现碳中和还面临很大挑战。如减排固碳关键技术复杂,成本高,难以快速推广;存在易腐解有机碳被土壤微生物转化为温室气体排放的风险[6-7]。因此,农业领域的碳中和技术需求大但储备不足,亟需发展。
目前材料、地质、生物等领域在碳捕集、封存与利用方面已经取得一些新进展。如材料领域利用物理化学等方法对CO2进行捕获,通过催化等技术实现CO2的高效转化;地质领域利用已有或潜在的地质空间进行CO2封存并通过矿物合成方法实现碳的循环再利用;生物领域通过微生物工程及合成生物学实现CO2向高附加值的化学物质转化[8-13]。这些技术与理论在未来农业实现碳中和过程中具有启示与借鉴意义。因此,本文就当前碳捕集、封存及利用技术的研究进展进行综述,力争为农业碳中和提供几种潜在的技术与路径。
1 CO2捕集技术
随着全球工业与农业的不断发展,温室效应的程度越来越严峻,其中与农业相关的碳排放约占全球碳排放的1/3,农业中的温室气体主要包括CO2、甲烷(CH4)和氧化亚氮(N2O),而CO2是导致全球气候变暖的主要因素,因此,对于农业中CO2的去除显得尤为重要[14]。CO2的捕集、封存与利用技术是解决温室气体排放的有效方法,其中CO2的捕集技术主要包括吸收法、吸附法和膜分离法等。
1.1 吸收法
吸收法按照吸附的原理可以分为化学吸收法、物理吸收法和生物吸收法。化学吸收法是利用碱性溶剂(有机胺、醇胺和氨水等)与酸性气体CO2发生化学反应,生成盐类化合物如碳酸盐等。物理吸附法是指吸收剂不与CO2发生化学反应,而是利用溶剂对CO2的溶解性而达到吸收CO2的效果。而生物吸收法则是利用光合作用将CO2吸收并将其转化为O2和有机物。其中,化学吸收法由于具有处理能力大、吸收效率高和成本低的特点,成为各行业大规模捕集CO2的技术[15]。31A34332-FF5A-4E17-873D-198B4A5FC60E
最近,一些研究将烷醇胺溶剂(包括伯胺、仲胺和叔胺)用于CO2捕获,由于伯胺、仲胺与CO2的反应速度较快,因此得到了广泛的应用,但由于其对CO2吸收能力低、溶剂易降解、腐蚀性高等原因,使其实际应用受到一定限制。叔胺的吸附量大、再生热低等优势引起研究界的广泛关注[16]。有研究将叔链烷醇胺1-二甲氨基-2-丙醇(1DMA2P)作为一种CO2的吸收剂,1DMA2P与最常见的叔胺相比,表现出更好的传质性能和更高的CO2去除动力[17]。将2种或以上的混合胺作为CO2的吸附剂,不仅吸收效果好,而且更加节能。Pasha等将25%的N-甲基二乙醇胺(MDEA)和5%的六亚甲基二胺(HMDA)混合制备水溶性混合胺吸收剂,以金属泡沫为填充材料,研究了其对CO2吸收的传质和动力学特性,结果表明,该混合胺吸附剂在连续3个再生循环中表现出良好的CO2吸收量和再生效率[18]。
除了以上几种化学吸收剂,还有一些新型的CO2吸收剂,包括相变吸收剂、离子液体吸收剂和纳米流体吸收剂,它们整合了化学吸收剂的优点,更有利于大規模应用。
1.2 吸附法
吸附法主要是利用固体吸附剂对CO2进行捕集,目前用于CO2吸附的固体吸附剂包括金属有机框架(MOFs)、沸石、活性炭和生物炭等。它们的吸附原理是通过CO2分子和吸附剂之间形成范德华力,以及CO2分子与固体吸附剂的离子和极性位点之间的离子相互作用来实现对CO2的吸附[8]。
1.2.1 MOFs MOFs是一种由金属离子和有机配体通过自组装的方式制备而成的新型多孔晶体材料。MOFs最主要的特点是比表面积大、孔隙率高、孔道结构有序、结构稳定以及化学性质易调,这些优势使得MOFs在气体的吸附与储存、催化、传感、生物医学等领域显示出独特的应用前景[19]。MOFs的孔径和通道较小,为纳米甚至埃的级别,可以容纳众多的CO2分子,可以在高压条件下储存自身体积10倍以上的CO2[20]。
MOFs有成千上万种,其中沸石咪唑酯骨架(ZIFs)是具有沸石拓扑结构的MOFs的一个子类,有望应用于工业上的CO2捕获和储存。ZIFs通常以粉末的形式被利用,然而ZIFs晶体的加工性差限制了其在工业系统中的实际应用。Ma等采用可生物降解、可循环利用的细菌纤维素(BC)作为氨基功能化的ZIF-8(ZIF-8-NH2)基质,使得ZIF-8-NH2均匀包裹在细菌纤维素上,成功制备出具有高效CO2吸附性能的ZIF-8-NH2@BC气凝胶,并且该气凝胶具有较好的可回收性和便携性[21]。徐国芬等也开发了一种基于ZIF-8的气凝胶,以聚酰胺酸盐(PAS)和聚酰亚胺纳米纤维为原料,制备了具有层状孔结构的聚酰亚胺气凝胶,然后将ZIF-8原位生长在气凝胶孔壁上,得到PI/ZIF-8复合气凝胶,发现该复合气凝胶结合了ZIF-8和气凝胶的高孔隙率的优点,当ZIF-8负载量为44.3%时,对CO2的吸附量为0.79 mmol/g[22]。
1.2.2 沸石 沸石是一种含水的碱金属(K、Na、Li)或碱土金属(Mg、Ca、Ba等)硅铝酸盐,其捕获CO2的优势在于孔隙度、孔径、酸碱度、比表面积等可根据需要和应用情况进行改性。沸石具有均匀的孔径(<2 nm),形成相互连接的通道和网状结构,并且沸石骨架中CO2能与碱金属阳离子之间产生强静电作用,因此,沸石可以将CO2吸附在其通道和网状结构中[23]。
Qiang等以铝土矿尾矿为原料,在110℃、n(SiO2/Al2O3) 固定在3.2的条件下反应16 h合成了高结晶度、正八面体形态的CO2吸附剂沸石X,其在273 K(0℃)和303 K(29.85℃)时的CO2吸附量分别为 7.3 mmol/g 和6.1 mmol/g,而且经过多个吸附循环试验发现沸石X仍然具有良好的CO2捕获能力,由于沸石X的成本较低,因此可广泛用于大规模CO2等温室气体的捕获[24]。有研究称,将碱性溶剂(胺类化合物)浸渍于沸石的表面或孔中可以提高沸石吸附CO2的性能[25]。Tejavath等合成了沸石(13X,4A和5A)负载一系列胺类化合物[二乙烯三胺(DETA)、乙二胺(EDA)、单乙醇胺(MEA)和三乙醇胺(TEA)]的复合材料,吸附动力学研究表明,当胺负载量大于13X-DETA-40时对CO2的吸附能力最大,其对CO2的吸附能力达到1.690 mmol/g[26]。除此之外,该反应器的投资成本与工业上的反应器成本相比减少了84%。因此,该吸附剂具有一定的经济可行性,可以用于工业、农业中CO2的大规模捕集。31A34332-FF5A-4E17-873D-198B4A5FC60E
1.2.3 活性炭 活性炭是一种将有机物在隔绝空气条件下加热、活化制备而成的具有多孔结构的材料,具有制备成本低和比表面积大的特点,可降低CO2捕获的整体能耗和成本[27]。活性炭吸附CO2的原理主要是通过物理吸附和化学吸附2种方式,物理吸附主要是利用活性炭的微孔结构(<2 nm),化学吸附主要是利用活性炭表面的官能团与CO2相互作用。但是活性炭吸附CO2也存在一些局限性,因此,目前研究活性炭吸附CO2最多的是利用碱性官能团和碱性溶剂(胺类化合物、氢氧化钠等)或碱性金属氧化物对其改性,增加其对CO2的吸附性能[28]。郭慧娴等用氢氧化钠浸渍改性活性炭,发现优化改性后的活性炭对烟气中CO2的吸附量是未改性活性炭的3.9倍[29]。Shahkarami等通过一步活化生物炭浸渍法制备氧化镁(MgO)活性炭,即将生物炭浸渍3%和10%的镁盐溶液,然后通过蒸汽活化,当Mg含量从3%增加到10%时,其比表面积更小,但是CO2吸收量更高,表明制备方法和金属含量比样品的比表面积和孔隙率更重要[30]。
1.2.4 生物炭 生物炭是一种富含碳的多孔固体,由生物质(植物、农产品废弃物、牛羊粪便和厨余垃圾等)在反应器中热分解而产生,具有比表面积大、孔隙率高、稳定性强以及表面具有丰富的官能团等特点,在催化、能量存储、污染物去除和CO2捕获等领域具有广阔的应用前景[31]。从结构的角度来看,生物炭和活性炭类似,因为它们都具有丰富孔隙率的无定形碳。然而,生物炭通常具有丰富的表面官能团(C—O、CO、COOH和OH等),因此,它们具有高度的可修饰性,可作为合成各种功能化碳材料的平台[32]。近些年,生物炭由于成本低廉、稳定性强等优势在CO2捕获方面有着巨大的应用潜力。
刘清涛采用超声辅助水热法将聚乙烯亚胺(PEI)接枝到玉米芯生物炭表面制备了PEI改性生物炭材料(PBC),PBC材料具有较高的BET比表面积(928.1 m2/g),并研究了PBC吸附CO2的性能和热力学行为,发现该吸附过程符合Langmuir等温吸附模型,其中PBC-4对CO2吸附效果最佳,最佳吸附量为2.71 mmol/g[33]。而且PBC具有良好的可回收性,易于实现热再生,重复使用10次后,吸附性能无明显变化。王立春等采用浸渍法制备氧化石墨烯(GO)改性的生物炭,该复合材料在900℃时热解得到的生物炭捕获CO2的能力最高(57.4 mg/g),并且当氧化石墨烯的负载量为9%时,复合吸附剂对CO2的最佳捕获量为77.5 mg/g,比未改性生物炭提高了35%,吸附性能的提升归因于含氧官能团的增加以及生物炭芳香化程度的提高[34]。
1.3 膜分离法
膜分离技术是一种新兴的CO2分离、捕获技术,是利用气体渗透率不同实现对气体的分离,与化学溶剂吸收法、物理/化学吸附法和低温蒸馏法等传统分离技术相比,膜分离技术具有能耗低、投资小、操作简单和分离效率高等特点[35]。根据膜材质的不同,通常用于CO2分离和捕获的膜可分为无机膜、有机高分子聚合物膜和混合基质膜3类。
1.3.1 无机膜 无机膜的种类繁多,包括炭膜、金属氧化物膜、沸石、氧化石墨烯和陶瓷膜等,与其他2种膜相比,无机膜最突出的优点是化学稳定性高,可以耐酸、耐碱以及耐高温等,而且无机膜还具有可调的孔径及规则的孔道,因此可适用于大多数气体的分离[36]。其中,炭膜具有机械、化学稳定性强,分离性能高等优点,尤其适用于高温、高压工况,如蒸汽甲烷重整过程中的H2/CO2分离、天然气脱硫过程中的CO2/CH4分离。最近,Cao等采用浸涂和热解工艺制备多层不对称碳分子筛(CMS)中空纤维膜,该无机纤维膜具有优异的气体分离性能,CO2/CH4(50∶50)混合气体的CMS渗透结果表明,CO2/CH4选择性为58.8,渗透率为310 GPU[37]。
虽然已经报道了无机CMS膜具有良好的 CO2/N2和CO2/CH4选择性,但是CMS膜用于碳捕获的应用仍然具有挑战性:(1)与许多需要更大膜面积的聚合物材料相比,其对CO2滲透率相对较低;(2)大多数CMS膜对水蒸气敏感;(3)CMS膜的脆性较大。为了应对这一挑战,可以考虑开发具有高度疏水性膜的超薄支撑CMS膜,例如,基于纤维素的CMS膜和氟化CMS膜。
1.3.2 有机高分子聚合物膜 有机高分子聚合物膜由于具有低成本、加工性能好、工艺简单以及可大规模生产等特点而备受关注,有机高分子聚合物的种类多种多样,包括聚二甲基硅氧烷(PDMS),聚酰亚胺(PI)、醋酸纤维素(CA)、聚氨酯(PU)和聚氧乙烯(PEO)等[38]。根据结构和组成,可以分为普通高分子聚合物膜、微孔有机高分子聚合物膜以及固定载体膜。其中普通高分子聚合膜约占市场份额的90%以上,这主要是由于其价格低廉、易于加工和成膜性能好,但其对酸、碱以及高温的耐受性较差,而且该类型的膜还会受到“trade-off”效应的制约,即气体分离的吸附容量和选择性不能同时兼备[39]。微孔有机高分子聚合物膜是由扭曲结构单体通过缩聚反应制备而成的,其孔隙率高,具有相互连通的微孔,因此表现出十分优异的气体分离性能。微孔有机高分子聚合物膜具有高气体选择性,但是其气体渗透率较低。沈钦通过1个简单的酰氯取代反应,将金刚烷接枝到偕胺肟功能化的微孔有机高分子膜(AOPIM-1)主链上,金刚烷作为一种侧基,用于调节AOPIM-1链的排列方式,从而影响气体的渗透性,特别是CO2的渗透性。结果表明,通过调节接枝的金刚烷分子的摩尔比,可以很好地调节接枝的AOPIM-1膜的间距。AOPIM-1膜的CO2渗透性从980.7 Barrer显著提高到2 483.6 Barrer。而CO2/N2和CO2/CH4的选择性则分别由36.0下降到31.2,由33.8下降到30.1,AOPIM-1膜的综合分离性能大大超过2008年的上限[40]。31A34332-FF5A-4E17-873D-198B4A5FC60E
1.3.3 混合基质膜 混合基质膜(MMMS)是由连续的有机高分子聚合物相和均匀分散的无机填料组成,它融合了有机高分子聚合物膜和无机膜的优点,可以大大提高CO2等气体的分离效果[41]。由于有机聚合物以及无机填料的种类和组成多样,因此,可以通过合理的设计选用合适的无机填料和有机聚合物,使MMMS在气体分离方面发挥独特的优势。目前,有研究者将金属有机框架、金属氧化物、沸石、碳纳米材料和金属氧化物等无机填料掺加到有机聚合物膜材料中,并且取得了良好的分离效果。最近,尚景宏等将高机械强度、高比表面积和高热稳定性的氧化石墨烯和还原性氧化石墨烯(rGO)掺杂到聚酰亚胺(PI)基质膜中制备新型的MMMS,发现与纯聚酰亚胺膜相比,其对CO2的分离性能明显提升,而且渗透系数和分离因数分别比纯PI膜上升了13.52%和24.34%[42]。彦晶晶等通过溶剂挥发法将氧化石墨烯量子点(GOQDs)掺杂到聚醚嵌段共聚酰胺(PEBA)中,制备一种具有良好分散性能和界面结合性能的GOQDs/PEBA混合基质膜,并研究了其对CO2/N2的渗透性能和分离性能,结果表明,GOQDs在PEBA基质膜中的分布较为均匀[43]。同时,GOQDs的加入使PEBA膜的力学性能得到了改善。除此之外,GOQDs中含有大量的羟基和羧基,对CO2有较强的吸附能力,显著提高了CO2/N2分离性能。
2 CO2封存技术
2.1 CO2地质封存
CO2的地质封存是指将高纯的超临界/密相CO2通过特殊管道送入地下指定地点进行封存,主要包括物理和化学方法。物理法借助地下的矿物吸附、地下水动力将CO2捕获在储层的顶隙中,但这种方法受地质结构、水动力等影响较大,不适用于长期储存CO2[44]。化学法是借助地下矿物、水和CO2之间发生的化学反应,生成新的物质固定下来,这种方法固定下来的CO2非常稳定,可达到长期储存的目的[10]。目前,CO2地质封存技术主要包括枯竭油气藏封存、深部咸水层封存和煤层封存。
枯竭油气藏封存是目前地质封存最成熟的技术,随着地质封存技术的发展,目前已掌握代表适宜封存的地质参数,还可借助钻井和地层监测数据综合考察封存情况[45]。深部咸水层封存是利用CO2与咸水层中的矿物质反应产生碳酸盐,从而实现CO2在地下的有效封存。咸水层分布广泛,封存能力强,且此处水质不适宜饮用,所以在CO2封存方面有巨大潜力[46]。煤层封存是利用煤层对CO2的强吸附力,将CH4从煤层中置换出来,既可以提高燃料的利用率,还可以固定CO2,但不足是煤层在吸附过CO2之后会发生溶胀,导致很难再吸附新的CO2,未来仍需进一步研究[45]。
2.2 海洋封存
海洋面积占地球表面积的3/4,海洋的固碳能力远超过陆地生物圈和大气,它所固定的碳约是陆地生物圈的20倍,是大气的50倍,因此海洋对促进大气中CO2的封存具有巨大的潜力[47]。CO2海洋封存主要包括:(1)海洋水柱封存,将捕获的CO2以一定的方式灌入大海中,依靠海洋中的HCO-3、CO2-3和H2CO3等游离的离子通过一系列化学反应将CO2吸收,最终实现海洋水柱封存[47]。CO2在海水中溶解的影响因素有很多,如何提高CO2在海水中的溶解能力且不会在短期内回到大气中是目前技术攻关的关键。(2)海洋沉积物封存,将CO2通过特制的管线送入海底的沉积层储层,通过沉降,将其封存在沉积层储层孔隙水下,其首要任务是确定储层的封存潜力和技术的可行性,可以通过储层岩心孔隙度、渗透性、伽玛射线的辐射记录和原位渗透性数据来评估[48]。同时,研究者发现深海黏土和软泥的渗透性较差,可以考虑沉积层中渗透性和孔隙度更好的高渗砂岩和组成洋壳的火成岩来封存CO2[48]。Marieni等证明了在相同的pH值条件下,富含CO2的盐水溶液与镁铁质岩石的反应速率高于低PCO2的淡水,这表明近海镁铁质岩石对CO2海洋储存可能起到重要作用[49]。(3)海洋增肥,通過向海水中添加营养素,增强浮游植物的光合作用,进而提高海洋对CO2的吸收能力,是目前最重要的CO2封存技术之一[47]。植物叶绿素发育过程中的必需元素是Fe,Fe的作用在“高氮低叶绿素”的海区更为明显,因为Fe可以提高植物的初级生产力,使其更好地吸收CO2。铁的供应控制着浮游植物的生长和群落组成,可提高浮游植物的碳固定速率并且长时间的海水铁增肥是有效的固碳方法[50]。31A34332-FF5A-4E17-873D-198B4A5FC60E
2.3 CO2矿物碳酸化封存
CO2矿物碳酸化封存是利用矿物中Mg2+/Ca2+与CO2发生碳酸化反应,生成稳定无污染的碳酸盐产物,进而达到CO2封存的目的,目前CO2的矿物碳酸化封存大多利用工业固体废物,如钢渣、粉煤灰等作为与CO2反应的原料,主要可分为CO2干法直接碳酸化、CO2湿法直接碳酸化和CO2间接碳酸化[51]。CO2干法直接碳酸化是通过含有Mg2+/Ca2+的硅酸盐与CO2气体直接反应得到碳酸盐,反应速率较慢,且是放热反应,所以考虑采用加压的手段以提高其反应速率[52]。如Fagerlund等使用流化床作为反应器,结果表明在510℃,4 500 kPa条件下,Mg(OH)2颗粒的碳矿化率提高55%[53]。CO2湿法直接碳酸化借助了CO2与H2O的反应,其中Mg2+/Ca2+的溶解速率被认为是该方法的主要限制因素,因此,很多研究者致力于研究如何提高硅酸盐溶解动力学特性[54]。绳昊一等发现温度升高降低了CaSiO3矿化CO2的能力,这与高温导致的CaSiO3表面形成的高温熔融体有关[55]。Wang等证明矿化反应具有扩散控制动力学特征,且在水泥浆体中加入CaSiO3和矿化渣可以增强水泥浆体的CO2吸收能力,并提高水泥的性能,这为未来探寻固碳新路径提供了思路[56-57]。此外,任国宏等发现在60℃、1个标准大气压条件下,粉煤灰固碳率为2%,电石渣固碳率为61.3%,而配合物固碳率比两者之和高19.6%[58]。CO2间接碳酸化就是在对矿石等原料中的Ca2+/Mg2+进行提纯之后,再将其与CO2反应,这种方法提高了反应效率,还回收了矿石中的贵金属。这种方法的主要技术难点是“如何更有效地萃取”和“萃取剂的回收”。包炜军等在乙酸固定CO2过程中加入了有机溶剂磷酸三丁酯(TBP),这种方法使碳酸化反应的转化率提高到40%以上[59]。
2.4 生物质能-碳捕集与封存
生物质能-碳捕集与封存技术(BECCS)是通过对生物质转化或燃烧产生的CO2进行捕集和封存,以长期分隔CO2与大气[60]。目前,规模最大的BECCS项目是捕集玉米制乙醇过程中产生的高浓度CO2,并将其封存于咸水层,该项目的规模已经达到了100万t/年,还有一些小规模的BECCS项目,主要是捕获和封存乙醇工厂产生的CO2[61]。国内的BECCS技术应用主要基于农林废弃物燃烧发电、燃煤耦合生物质发电以及生物天然气[61-62]。樊静丽等基于农林废弃物燃烧发电的BECCS,模拟了秸秆燃烧电厂,结果显示,预计每发电1 kW·h,可实现负碳排放1.570~1.585 kg[61]。基于燃煤耦合生物质发电的BECCS技术有2种途径,第1种是通过碳捕获和封存(CCS)技术对烟气中的CO2进行捕集和封存,第2种是通过生物质替代部分燃煤减少CO2的释放量。基于生物天然气的BECCS技术是指用生物天然气替代传统天然气,并对沼气中的CO2进行捕获和分离,这一过程实现了CO2的间接和直接减排,但目前生物天然气规模普遍较小,所以未来研究重点可能集中于前2项技术。
3 CO2转化技术
除了将农业中排放的CO2捕获、封存减缓其对气候的不利影响外,通过CO2资源化利用将其转化为高价值的化学品,是减少CO2排放以及实现“碳中和”的重要途径之一。CO2资源化利用的方法主要包括化学转化法和生物转化法。化学转化法主要是利用还原反应等将CO2转化为高附加值的化学品,通过化学法可以将CO2转化为甲醇、甲酸、甲烷、汽油、烯烃和可降解的塑料等,包括热化学法、电化学法、光催化法以及等离子体化学法等。生物转化法主要是通过植物、微藻的光合作用,以及通过酶和微生物固碳技术,实现对CO2的资源化利用。
3.1 化学转化法
3.1.1 热化学法 热化学法主要是利用热能驱动CO2直接转化为燃料及化学品,其中利用太阳能作为热量是一种绿色节能的转化方式,该方式不仅可以降低大气中的CO2浓度,还可以将太阳能转变为易于储存与运输的高价值化学品和燃料,这对于CO2的资源化具有重要意义[63]。热化学法转化CO2可以分为直接热分解法和两步热化学循环法,其中后者在实际的CO2转化中的应用更加广泛。两步热化学循环是利用热能通过一系列的化学反应将CO2和H2O转化为合成气如CO、H2和O2,它们是合成甲烷、甲醇等化学品和染料的重要原料。CO2转化过程分为2步,首先是吸热过程,将太阳能聚集并为反应提供充足的热量(>1 273 K),然后将太阳能反应器中的金属氧化物(MxOy)还原为低价态氧化物或金属单质;第2步则是低价态氧化物或金属单质在较低的温度下(>600 K)将CO2和H2O轉化为合成气,金属氧化物在整个反应过程不被消耗,因此,可以实现材料的循环利用[64]。目前,用于CO2热化学转化的金属氧化物多为Fe3O4,ZnO,CeO2和SnO等,研究表明采用Zn/ZnO、Ce2O3/CeO2、FeO/Fe3O4和SnO/SnO2等多种金属氧化物的氧化还原对进行CO2热化学循环时,可以降低反应温度,提高金属氧化物氧化还原对在该循环中的有效循环次数[65]。31A34332-FF5A-4E17-873D-198B4A5FC60E
3.1.2 电化学法 电化学转化CO2,即以电能为能量,在催化剂的协同作用下将CO2还原为高价值化学品或者生物燃料等。CO2的电化学转化有以下几个优点:反应条件如还原电位、电解液和温度可以通过调整来控制反应;可以利用可再生能源驱动反应,电解液可以循环利用,因此整个过程只需要消耗水;电化学系统通常是模块化的,并能够扩大规模并用于工业应用[66]。但是电化学CO2还原过程动力学缓慢、能量效率低、能量消耗高,因此需要具有高催化活性和稳定性的高效催化剂。Siltamaki等采用简易电沉积法合成了具有纳米树枝状结构的铜金合金(CuAu)电极,发现Cu/Au原子比约为 1∶1 的CuAu纳米枝晶对CO2的电化学还原具有良好的催化活性,气相色谱结果表明,CO2电化学转化的主要产物为CO和H2[67]。MOFs具有周期性排列的孤立金属活性位点,是一类很有前景的CO2电化学还原催化剂,但是传统MOFs的导电性较差导致CO2电化学还原的电流密度较低,为了解决这个问题,Yi等利用邻苯二酚酸镍,制备了具有导电性的二维(2D)酞菁基MOFs(NiPc-NiO4)纳米片,并用于CO2电化学还原合成CO,由于酞菁分子与NiO4节点之间的平面全π-d共轭,使得NiO4具有4.8×10-5S/m的良好电导率[68]。因此,所制备的2D NiPc-NiO4纳米片表现出了优异的CO2电还原活性,CO的选择性接近100%,而且该催化剂还表现出优异的长期耐用性。
3.1.3 光催化法 光催化法是通过光催化剂在特定波长下的光激发下产生激发态的电子(e-),然后将催化剂表面的CO2直接转化为燃料和高价值的化学品,这是解决全球能源和环境问题最有前景的策略之一[69]。目前,应用于光催化CO2转化的催化剂多为半导体材料,包括纳米TiO2、g-C3N4、CdS、钙钛矿及MOFs材料等。其中MOFs由于可以与气体分子相互作用以及其丰富而有序的孔隙,成为光催化转化气体分子的候选材料。然而,MOFs或MOFs基复合材料进行CO2光催化还原,CO2转换效率仍远低于先进的固态或分子催化剂。Jiang等通过在MOFs(MIL-101)及其衍生物的不同孔隙中生长TiO2,从而在MOFs晶体中创建分子隔间,这使得吸收光和产生电子的TiO2单元与MOFs中的催化金属簇之间能够发挥协同作用,从而促进光催化CO2高效转化为甲烷,同时产生O2[70]。Kong等采用一种原位生长方法将卤化钙钛矿CsPbBr3QDs封装进沸石咪唑基金屬有机框架(ZIFs)中制备CsPbBr3@ZIFs复合材料,其中,ZIF-8和ZIF-67不仅可以作为CsPbBr3QDs的稳定剂,还可作为促进CO2活化转化的有效助催化剂,因此该复合材料表现出优异的CO2光催化转化为甲烷的性能[71]。Tian等利用ZIF-8包覆的具有S空位的CdS核-壳复合光催化剂(Sv-CdS),在可见光驱动下选择性地将CO2还原为乙烯。S空位既产生电子结构调制,又产生结构弛豫。所得到的Sv-CdS光催化剂不仅能促进*CO的生成,而且通过缩短2个相邻吸附的*CHO的距离和反应能垒,引发它们的二聚[72]。ZIF-8壳层增加了CO局部浓度,进一步降低了反应能垒,因此该复合材料可以在光照条件下高选择性和高效地生产C2H4。
3.1.4 等离子体化学法 作为物质的第四态,等离子体由大量的高能粒子组成,如电子、离子和中性粒子。这些高能粒子通过碰撞可以产生自由基,自由基可以进一步反应得到目标产物。等离子体具有启动快、能量效率高的优点,然而由于组成等离子体的粒子相互作用过程极其复杂,产品的选择性难以控制[73]。因此,等离子体与催化剂相结合的等离子体催化法不仅具有传统催化法产物选择性高的优点,而且具有等离子体反应速度快、能量效率高的优势,不仅可以大规模生产,还可以达到低能耗、高能效减排CO2的目标。
尽管使用了催化剂,但为了克服动力学障碍和避免催化剂失活,需要适当的温度(>350℃)和高压。最近,将催化剂与非热等离子体结合,即介质阻挡放电等离子体(DBD),可以促进低温下的CO2甲烷化。Nizio等采用传统的湿法浸渍法制备了不同Ce/Zr比例的氧化铈-氧化锆混合氧化物中负载15%的Ni,并以Ni-CexZr1-xO2为催化剂的DBD等离子体反应器,在常压和极低温度下将CO2催化加氢成甲烷(甲烷化),发现混合等离子体15NiCZ5842催化剂即使在低温下也能有效地将CO2转化为甲烷[74]。Mikhail等将一系列促进剂(Cu、Co、Mn、La、Y和Sr等)添加到Ni/CeZrOx基催化剂中用于介质阻挡放电(DBD)等离子体催化CO2转化为甲烷,这些元素的存在显著提高了催化剂的物理化学和电气特性,导致不同的等离子体催化性能。其中,NiCZ-Gd的活性最高,在7 W左右CO2完全转化为甲烷的转化率为85%,NiCZ-Gd催化剂的效率由原来的50%提高到72%[75]。31A34332-FF5A-4E17-873D-198B4A5FC60E
3.2 生物法
3.2.1 植物固定法 大气中的CO2可以通过植物的光合作用固定到陆地/水生生态系统中。这种碳储存在植物成分中,包括树干、树枝、树叶和根中,这些物质通过不同的土壤有机体,特别是土壤生态系统中的功能群和凋落物的作用,与微生物群体利用的根部碳分泌物一起进入土壤,共同构成将生物量碳结合到土壤中的自然途径[76]。生物量碳通过分解进入土壤,这是碳循环中的一个关键过程,它包括矿化和腐殖化2个相互关联的过程,其中矿化是有机分子转化为植物可同化的无机形式的过程,腐殖化是维持土壤有机质水平的过程[77]。
大气中CO2浓度的增加会增强光合作用。因此,CO2的增加有望增强植物糖转化的能力,进而增加生态系统中储存在有机物中的碳总量。基于上述基础理论,有研究者对如何通过森林管理来提高其碳捕获和封存能力进行了探索和研究,并提出了3种模型,具体方法见表1。
第1种模型是森林碳保护管理模型,该模型目前可以增设更多的碳含量保护措施,包括延长林木轮伐期,避免在林业作业期间损害树木,通过应用土壤保护技术减少伐木残留物,以及提高木材使用的碳效率[79]。第2种模型是森林碳储存管理模型,该模型的目标是增加森林植被和土壤中的碳量,通过增加耐用木质材料的储存,来增加天然林和人工林生物量的表面积或碳含量,并通过植树造林、促进次生林的自然或人工再生和增加农地或牧场的森林覆盖率等措施提高固碳能力[80]。第3种模型是森林碳替代管理模型,该模型的主要目标是增加从森林生物质转移到其他产品的碳量,这些产品通常直接或间接来自化石燃料,如生物燃料和建筑材料,这种模型主要将林业管理得到的副产品转化为生物质衍生燃料,如木屑颗粒燃料或生物炭,然后用于替代化石燃料,并增强碳捕获和封存[81]。
3.2.2 微生物固定法 固定CO2的微生物可分为自养和异养2类,且CO2是自养微生物唯一的无机碳源。因此,除了植物,微生物在将CO2转化为有机生物质方面也发挥着重要作用。使用微生物作为催化剂实现CO2固定不仅环保,而且还可以生产高附加值的化学物质[82]。自养微生物中只有部分被用作代谢工程的宿主,主要宿主、类型及模式菌株见表2。
目前,微藻是实现商业规模化应用最成功的菌种,每年可生产5 000 t 生物量干藻,并且微藻生物燃料有望成为新能源[86]。除自氧微生物外,异养微生物通过代谢途径中的羧化反应也可固定CO2,代谢途径的底物和能量都来自有机化合物的分解,主要包括戊糖丙酸杆菌、大肠杆菌和酿酒酵母[87-88]。目前,提高微生物CO2转化能力的策略主要分为降低微生物CO2释放和提高微生物CO2固定。微生物的CO2释放有3种途径:产物合成途径中的脱羧反应、氧化失衡、ATP生成[89]。基于此,研究者总结了几种降低CO2释放的方法(表3)[90]。
自养微生物中CO2的固定是由細胞能量(ATP和还原力)驱动的途径,在能量驱动下将非生物碳化合物(HCO-3/CO2)转化为有机代谢物;异养微生物中CO2的固定是由有机化合物分解供应能量和底物,通过代谢途径中的羧化反应固定的。基于自养和异养微生物的固碳机理,研究者提出了几种提高微生物固碳能力的方法(表4)[90]。
鉴于微生物天然固碳途径效率低,且其关键酶存在催化效率低等问题,目前已有学者利用新兴的合成生物学技术开发人工设计的微生物固碳途径。如Zhang等提出了一种辅助模块增强的海洋原绿球藻源羧化体大肠杆菌内重构策略,重构的羧化体具有高效的CO2固定能力。通过合成生物学方法,将这种天然CO2同化体系用于规模化生产多种高附加值代谢中间产物(如乙酰辅酶A、苹果酸、延胡索酸和酪氨酸等)[91]。考虑到目前农业领域的研究主要集中在土壤微生物对大气中CO2浓度变化的响应探究上,而土壤微生物类群调控土壤碳循环的研究较少,因此,探究土壤微生物对农业领域碳循环及微生物固碳的影响,是实现农业碳中和重要的研究方向。
3.2.3 酶固定法 目前已发现的天然生物固碳途径有6条(表5),这些途径主要通过羧化酶或还原酶进行生物固碳[92]。
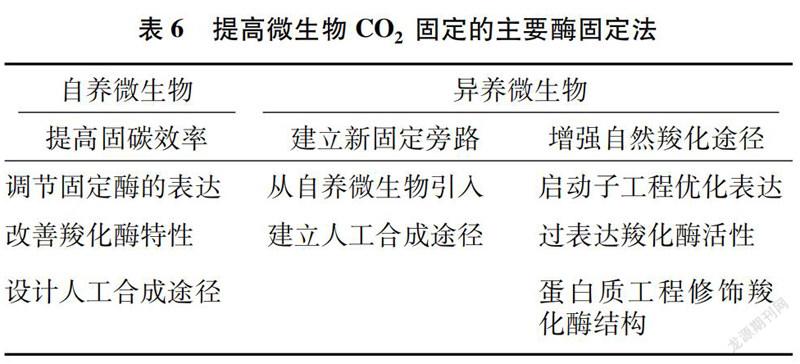
自然界原有的固碳途径存在关键酶催化效果不佳和反应条件苛刻等问题,所以如何对现有的天然固碳途径进行改造或利用合成生物学技术设计新酶、新途径以提高固碳效率成为当前的研究热点,近年来,研究者提出了提高微生物CO2固定的主要酶固定法(表6)[90]。
研究表明,羧化酶(如卡尔文循环中的Rubisco)和碳通量控制酶(如卡尔文循环中的果糖-二磷酸醛缩酶)是较佳的表达调控目标[93]。在集胞藻(Synechocystis sp.) PCC 6803中过表达Rubisco可使乙醇产量增加55%[94]。羧化酶是CO2固定途径中最重要的酶,其中Rubisco的活性较低,且会被空气中存在的O2占用部分活性中心,所以Rubisco人工改造设计具有一定难度,目前最好的改进方案是结合活性大肠杆菌选择和伴侣进化,通过调节伴侣基因GroEL/ES和RbcX的表达,提高Rubisco羧化速率,进而提高集胞藻PCC 6803的光合作用速率[95]。另外,可将现有自然固碳途径移植到异养生物中以提高异养生物的固碳效率,而这种移植主要是通过移植自然途径的关键酶来实现的。Gong等将卡尔文循环路径的2个关键酶移植到大肠杆菌中,使其固碳速率得到提高[96]。增强羧化酶活性也可以有效增强异养微生物CO2的固定。Brown等通过过表达米曲霉中的丙酮酸羧化酶,极大地提高了羧化速率,进而提高了米曲霉的固碳速率和副产物得率[97]。31A34332-FF5A-4E17-873D-198B4A5FC60E
微生物代谢网络具有很强的可塑性,除了能提高微生物CO2固定酶活性之外,通过改造天然代谢途径可以有效降低微生物CO2释放,也是一种重要的固碳方式。Xiong等在蓝藻中设计了一种磷酸酮醇酶途径,该途径极大地提高了蓝藻的碳代谢效率和光合生产力[98]。另外,利用合成生物学设计人工固碳是近年来重要的酶固碳途径之一。研究表明,磷酸烯醇式丙酮酸羧化酶的酶活性较高,因此利用此酶设计人工固碳途径被广泛研究。Bar-Even等围绕磷酸烯醇式丙酮酸羧化酶,通过计算确定了一种新型的高效碳固定途径,但是研究表明低磷/氧(P/O)比和ATP维持损失是导致细胞能量代谢严重不足于CO2固定的重要因素,这些现存问题也为研究者未来继续探索如何提高酶固碳能力提供了方向[99-100]。
4 總结与展望
4.1 总结
农业中CO2的排放对全球温室效应的贡献不容忽视,CO2的捕集、利用与封存是缓解气候变暖、实现分离回收和资源化利用的有效途径,这对于早日实现碳达峰和碳中和的目标具有重要意义。吸附法、吸收法以及膜分离法等捕获CO2的方法存在效果好、CO2回收率和纯度较高等优点,因而得到广泛的研究,但是在实际应用中存在能耗大、腐蚀性强的问题;进而通过封存技术如地质封存和海洋封存,再利用化学法和生物法等CO2转化技术将其转化为高价值的化学品和生物燃料等,这不仅可以减少碳排放,而且可以实现CO2的资源化利用以及可再生能源的储存与转化。
4.2 展望
虽然CO2的CCUS技术在CO2去除以及资源化利用方面取得了不错的成效,但是依然面临一些挑战,如成本偏高不适用于大规模推广应用,且农业中CO2的捕获、封存与转化研究较少。
4.2.1 新型CO2捕获、转化材料的开发 鉴于当前CCUS技术成本高昂,开发低成本、吸附与催化性能的新材料是未来的发展方向之一,沸石和MOFs等多孔材料兼具捕获及催化转化的功能,但是它们的成本仍较高,依然停留于实验室研究阶段,难以大规模地应用于CO2的捕获与转化。因此,开发高性能、低成本的沸石、MOFs材料或者替代物等CO2捕获与转化材料,并借助可再生的清洁能源如光能和电能并将其转化为高价值的化学品和生物燃料是未来的发展方向。
4.2.2 新型CO2转化技术的研发 新型CO2转化技术的开发,对于早日实现CO2规模化资源利用具有重要意义,通过新兴的生物技术如合成生物学技术、微藻技术以及酶固定技术等高效转化CO2是未来的重点研究方向。目前多数研究将CO2转化为化学品和燃料,很少有研究将其拓展到其他领域,将CO2转化为食品、饲料和可降解的生物材料新技术的开发也是未来CO2资源化利用较有前景的发展方向。
总之,开发成本低廉、易于制备、稳定性高、性能优异的CO2捕获与转化材料以及低成本、高效率、具有商业价值的CCUS技术,并能高效且大规模地应用于CO2的转化与资源化利用是加快实现碳中和的重要途径。
参考文献:
[1]Lu X,Cao L A,Wang H K,et al. Gasification of coal and biomass as a net carbon-negative power source for environment-friendly electricity generation in China[J]. Proceedings of the National Academy of Sciences of the United States of America,2019,116(17):8206-8213.
[2]van Vuuren D P,Stehfest E,Gernaat D E H J,et al. Alternative pathways to the 1.5 ℃ target reduce the need for negative emission technologies[J]. Nature Climate Change,2018,8(5):391-397.
[3]Tubiello F N,Rosenzweig C,Conchedda G,et al. Greenhouse gas emissions from food systems:building the evidence base[J]. Environmental Research Letters,2021,16(6):065007.
[4]齐 晔,李惠民,王 晓. 农业与中国的低碳发展战略[J]. 中国农业科学,2012,45(1):1-6.
[5]Adeel M,Zain M,Shafi J,et al. Conservation agriculture,a way to conserve soil carbon for sustainable agriculture productivity and mitigating climate change:a review[J]. 2018,27(9):6297-630831A34332-FF5A-4E17-873D-198B4A5FC60E
[6]曹丽花,刘合满,杨东升. 农田土壤固碳潜力的影响因素及其调控[J]. 江苏农业科学,2016,44(10):16-20.
[7]乐小芳,陈佳淳,苗 璐. 农业土壤碳汇研究综述[J]. 农业与技术,2020,40(22):8-10.
[8]徐永辉,肖宝华,冯艳艳,等. 二氧化碳捕集材料的研究进展[J]. 精细化工,2021,38(8):1513-1521.
[9]Liu M S,Hohenshil A,Gadikota G. Integrated CO2capture and removal via carbon mineralization with inherent regeneration of aqueous solvents[J]. Energy & Fuels,2021,35(9):8051-8068.
[10]李 琦,蔡博峰,陳 帆,等. 二氧化碳地质封存的环境风险评价方法研究综述[J]. 环境工程,2019,37(2):13-21.
[11]王 凯,刘子鹤,陈必强,等. 微生物利用二氧化碳合成燃料及化学品:第三代生物炼制[J]. 合成生物学,2020,1(1):60-70.
[12]李美洁,夏青青,Harwood C S,等. 沼泽红假单胞菌作为微生物细胞工厂的应用[J]. 生物加工过程,2020,18(1):27-34.
[13]胡贵鹏. CO2封存工程改造微生物生产L-苹果酸[D]. 无锡:江南大学,2020:1-13.
[14]尚 杰,杨 果,于法稳. 中国农业温室气体排放量测算及影响因素研究[J]. 中国生态农业学报,2015,23(3):354-364.
[15]梅明灿. CO2在离子液体中化学和物理吸收量定量方法的建立[D]. 上海:华东理工大学,2021:1-3.
[16]邬高翔,田 瑞. 二氧化碳捕集技术研究进展[J]. 云南化工,2020,47(4):22-23.
[17]Ahmadi M,Gomes V G,Ngian K.Advanced modelling in performance optimization for reactive separation in industrial CO2removal[J]. Separation and Purification Technology,2008,63(1):107-115.
[18]Pasha M,Li G X,Shang M J,et al. Mass transfer and kinetic characteristics for CO2absorption in microstructured reactors using an aqueous mixed amine[J]. Separation and Purification Technology,2021,274:118987.
[19]Wang M J,Nian L Y,Cheng Y L,et al. Encapsulation of colloidal semiconductor quantum dots into metal-organic frameworks for enhanced antibacterial activity through interfacial electron transfer[J]. Chemical Engineering Journal,2021,426(1):130832.
[20]Bhatt P M,Belmabkhout Y,Cadiau A,et al. A fine-tuned fluorinated MOF addresses the needs for trace CO2removal and air capture using physisorption[J]. Journal of the American Chemical Society,2016,138(29):9301-9307.
[21]Ma H,Wang Z G,Zhang X F,et al. In situ growth of amino-functionalized ZIF-8 on bacterial cellulose foams for enhanced CO2adsorption[J]. Carbohydrate Polymers,2021,270(8):118376.
[22]徐国芬,董 杰,赵 昕,等. 聚酰亚胺/ZIF-8复合气凝胶的制备及二氧化碳吸附性能[J]. 高分子材料科学与工程,2020,36(12):90-96,102.
[23]Murge P,Dinda S,Roy S. Zeolite-based sorbent for CO2capture:preparation and performance evaluation[J]. Langmuir,2019,35(46):14751-14760.
[24]Qiang Z Q,Li R,Yang Z Q,et al. Zeolite X adsorbent with high stability synthesized from bauxite tailings for cyclic adsorption of CO2[J]. Energy & Fuels,2019,33(7):6641-6649.31A34332-FF5A-4E17-873D-198B4A5FC60E
[25]Bacariza M C,Amjad S,Teixeira P,et al. Boosting Ni dispersion on zeolite-supported catalysts for CO2methanation:the influence of the impregnation solvent[J]. Energy & Fuels,2020,34(11):14656-14666.
[26]Tejavath V,Kasarabada V,Gonuguntla S,et al. Technoeconomic investigation of amine-grafted zeolites and their kinetics for CO2capture[J]. ACS Omega,2021,6(9):6153-6162.
[27]Heidarinejad Z,Dehghani M H,Heidari M,et al. Methods for preparation and activation of activated carbon:a review[J]. Environmental Chemistry Letters,2020,18(2):393-415.
[28]朱 赛. 表面改性对活性炭物理、化学性质及CO2吸附性能的影响[D]. 郑州:郑州大学,2010:9-10.
[29]郭慧娴,李水娥,张 勇,等. 改性活性炭对烟气中CO2吸附性能的影响[J]. 湿法冶金,2020,39(2):156-159.
[30]Shahkarami S,Dalai A K,Soltan J. Enhanced CO2adsorption using MgO-impregnated activated carbon:impact of preparation techniques[J]. Industrial & Engineering Chemistry Research,2016,55(20):5955-5964.
[31]Woolf D,Amonette J E,Street-Perrott F A,et al. Sustainable biochar to mitigate global climate change[J]. Nature Communications,2010,1(1):1-9.
[32]Wang J L,Wang S Z. Preparation,modification and environmental application of biochar:a review[J]. Journal of Cleaner Production,2019,227:1002-1022.
[33]劉清涛. PEI改性生物炭的制备及对CO2吸附性能的评价[J]. 环境科学学报,2021,41(3):932-939.
[34]王立春,马丽萍,彭雨惠,等. 氧化石墨烯修饰蔗渣生物炭吸附CO2的研究[J]. 化工新型材料,2020,48(7):108-113.
[35]Warmuzinski K,Tanczyk M,Jaschik M. Experimental study on the capture of CO2from flue gas using adsorption combined with membrane separation[J]. International Journal of Greenhouse Gas Control,2015,37:182-190.
[36]Lei L F,Bai L,Lindbrthen A,et al. Carbon membranes for CO2removal:status and perspectives from materials to processes[J]. Chemical Engineering Journal,2020,401:126084.
[37]Cao Y H,Zhang K A,Sanyal O,et al. Carbon molecular sieve membrane preparation by economical coating and pyrolysis of porous polymer hollow fibers[J]. Angewandte Chemie International Edition,2019,58(35):12149-12153.
[38]杨珍珍,刘志敏. 功能型微孔有机聚合物吸附及催化转化CO2研究进展[J]. 中国科学(化学),2016,46(10):973-993.
[39]Rungta M,Zhang C,Koros W J,et al. Membrane-based ethylene/ethane separation:the upper bound and beyond[J]. AIChE Journal,2013,59(9):3475-3489.
[40]沈 钦. 高性能自具微孔聚合物气体分离膜的设计与性能研究[D]. 郑州:郑州大学,2019:36-46.
[41]何荣荣. 基于多孔有机聚合物的混合基质膜及气体分离性能优化[D]. 郑州:郑州大学,2020:2-3.31A34332-FF5A-4E17-873D-198B4A5FC60E
[42]尚景宏,臧毅华,罗林军,等. 改性石墨烯材料掺杂聚酰亚胺制备混合基质膜分离CO2/N2[J]. 膜科学与技术,2021,41(3):98-104.
[43]彦晶晶,陈丙晨,白云翔,等. 用于CO2/N2分离的氧化石墨烯量子点混合基质膜的制备及性能研究[J]. 化工新型材料,2020,48(5):90-94.
[44]吕碧洪,金佳佳,张 莉,等. 有机胺溶液吸收CO2的研究现状及进展[J]. 石油化工,2011,40(8):803-809.
[45]陈 兵,肖红亮,李景明,等. 二氧化碳捕集、利用与封存研究进展[J]. 应用化工,2018,47(3):589-592.
[46]薛 博,刘 勇,王 沉,等. 碳捕获、封存与利用技术及煤层封存CO2研究进展[J]. 化学世界,2020,61(4):294-297.
[47]孙玉景,周立发,李 越. CO2海洋封存的发展现状[J]. 地质科技情报,2018,37(4):212-218.
[48]Eccles J K,Pratson L. Global CO2storage potential of self-sealing marine sedimentary strata[J]. Geophysical Research Letters,2012,39(19):L19604.
[49]Marieni C,Matter J M,Teagle D A H. Experimental study on mafic rock dissolution rates within CO2-seawater-rock systems[J]. Geochimica et Cosmochimica Acta,2020,272:259-275.
[50]Buesseler K O,Andrews J E,Pike S M,et al. The effects of iron fertilization on carbon sequestration in the southern ocean[J]. Science,2004,304(5669):414-417.
[51]Ji L,Yu H,Zhang R J,et al. Effects of fly ash properties on carbonation efficiency in CO2mineralisation[J]. Fuel Processing Technology,2019,188:79-88.
[52]Liu W,Su S,Xu K,et al. CO2sequestration by direct gas-solid carbonation of fly ash with steam addition[J]. Journal of Cleaner Production,2018,178:98-107.
[53]Fagerlund J,Teir S,Nduagu E,et al. Carbonation of magnesium silicate mineral using a pressurised gas/solid process[J]. Energy Procedia,2009,1(1):4907-4914.
[54]Olajire A A. A review of mineral carbonation technology in sequestration of CO2[J]. Journal of Petroleum Science and Engineering,2013,109:364-392.
[55]绳昊一,吕 莉,梁 斌,等. 焙烧温度对硅酸钙矿化CO2的影响[J]. 矿产综合利用,2015(5):76-80.
[56]Wang T,Huang H,Hu X T,et al. Accelerated mineral carbonation curing of cement paste for CO2sequestration and enhanced properties of blended calcium silicate[J]. Chemical Engineering Journal,2017,323:320-329.
[57]Huang H,Guo R N,Wang T,et al. Carbonation curing for wollastonite-Portland cementitious materials:CO2sequestration potential and feasibility assessment[J]. Journal of Cleaner Production,2019,211:830-841.
[58]任國宏,廖洪强,吴海滨,等. 粉煤灰、电石渣及其配合物碳酸化特性[J]. 环境工程学报,2018,12(8):2295-2300.
[59]包炜军,李会泉,张 懿. 强化碳酸化固定CO2反应过程分析与机理探讨[J]. 化工学报,2009,60(9):2332-2338.
[60]GCCSI. Bioenergy and carbon capture and storage[R]. Sydney:Global CCS Institute,2019:1-14.31A34332-FF5A-4E17-873D-198B4A5FC60E
[61]樊靜丽,李 佳,晏水平,等. 我国生物质能-碳捕集与封存技术应用潜力分析[J]. 热力发电,2021,50(1):7-17.
[62]常世彦,郑丁乾,付 萌. 2℃/1.5℃温控目标下生物质能结合碳捕集与封存技术(BECCS)[J]. 全球能源互联网,2019,2(3):277-287.
[63]许辰宇,林伽毅,潘富强,等. Ni离子替位掺杂TiO2增强光热化学循环还原CO2研究[J]. 化学学报,2017,75(7):699-707.
[64]许辰宇. 光热协同催化分解H2O和CO2制备燃料反应动力学及能量转化[D]. 杭州:浙江大学,2018:10-11.
[65]Romero M,Steinfeld A. Concentrating solar thermal power and thermochemical fuels[J]. Energy & Environmental Science,2012,5(11):9234-9245.
[66]Novaes L F T,Liu J J,Shen Y F,et al. Electrocatalysis as an enabling technology for organic synthesis[J]. Chemical Society Reviews,2021,50(14):7941-8002.
[67]Siltamaki D,Chen S,Rahmati F,et al. Synthesis and electrochemical study of CuAu nanodentrites for CO2reduction[J]. Journal of Electrochemistry,2021,27(3):278-292.
[68]Yi J D,Si D H,Xie R K,et al. Conductive two-dimensional phthalocyanine-based metal-organic framework nanosheets for efficient electroreduction of CO2[J]. Angewandte Chemie International Edition,2021,60(31):17108-17114.
[69]Nasalevich M A,Becker R,Ramos-Fernandez E V,et al. Co@NH2-MIL-125(Ti):cobaloxime-derived metal-organic framework-based composite for light-driven H2production[J]. Energy & Environmental Science,2015,8(1):364-375.
[70]Jiang Z,Xu X H,Ma Y H,et al. Filling metal-organic framework mesopores with TiO2for CO2photoreduction[J]. Nature,2020,586(7830):549-554.
[71]Kong Z C,Liao J F,Dong Y J,et al. Core@ shell CsPbBr3@ zeolitic imidazolate framework nanocomposite for efficient photocatalytic CO2reduction[J]. ACS Energy Letters,2018,3(11):2656-2662.
[72]Tian F Y,Zhang H L,Liu S,et al. Visible-light-driven CO2reduction to ethylene on CdS:enabled by structural relaxation-induced intermediate dimerization and enhanced by ZIF-8 coating[J]. Applied Catalysis(B:Environmental),2021,285:119834.
[73]刘剑豪. 等离子体催化氢气和甲烷还原CO2[D]. 大连:大连理工大学,2017:10-14.
[74]Nizio M,Albarazi A,Cavadias S,et al. Hybrid plasma-catalytic methanation of CO2at low temperature over ceria zirconia supported Ni catalysts[J]. International Journal of Hydrogen Energy,2016,41(27):11584-11592.
[75]Mikhail M,da Costa P,Amouroux J,et al. Tailoring physicochemical and electrical properties of Ni/CeZrOx doped catalysts for high efficiency of plasma catalytic CO2methanation[J]. Applied Catalysis(B:Environmental),2021,294:120233.31A34332-FF5A-4E17-873D-198B4A5FC60E
[76]Dinakaran J,Rao K S. Carbon sequestration in terrestrial vegetation and soils:a review[J]. Phytomorphology,2012,62(3/4):177-188.
[77]Jiménez J J,Lal R.Mechanisms of C sequestration in soils of Latin America[J]. Critical Reviews in Plant Sciences,2006,25(4):337-365.
[78]Nunes L J R,Meireles C I R,Pinto Gomes C J,et al. Forest contribution to climate change mitigation:management oriented to carbon capture and storage[J]. Climate,2020,8(2):21-42.
[79]Moomaw W R,Masino S A,Faison E K. Intact forests in the United States:proforestation mitigates climate change and serves the greatest good[J]. Frontiers in Forests and Global Change,2019,2:27-37.
[80]Cox P M,Betts R A,Jones C D,et al. Acceleration of global warming due to carbon-cycle feedbacks in a coupled climate model[J]. Nature,2000,408(6809):184-187.
[81]Harmon M E. Have product substitution carbon benefits been overestimated?A sensitivity analysis of key assumptions[J]. Environmental Research Letters,2019,14(6):065008.
[82]Venkata M S,Modestra J A,Amulya K,et al. A circular bioeconomy with biobased products from CO2sequestration[J]. Trends in Biotechnology,2016,34(6):506-519.
[83]Angermayr S A,Gorchs R A,Hellingwerf K J. Metabolic engineering of cyanobacteria for the synthesis of commodity products[J]. Trends in Biotechnology,2015,33(6):352-361.
[84]Qiao K J,Wasylenko T M,Zhou K,et al. Lipid production in Yarrowia lipolytica is maximized by engineering cytosolic redox metabolism[J]. Nature Biotechnology,2017,35(2):173-177.
[85]Schuchmann K,Müller V.Autotrophy at the thermodynamic limit of life:a model for energy conservation in acetogenic bacteria[J]. Nature Reviews Microbiology,2014,12(12):809-821.
[86]Wijffels R H,Barbosa M J. An outlook on microalgal biofuels[J]. Science,2010,329(5993):796-799.
[87]Claassens N J,Sousa D Z,dos Santos V A P M,et al. Harnessing the power of microbial autotrophy[J]. Nature Reviews Microbiology,2016,14(11):692-706.
[88]von Borzyskowski L S,Carrillo M,Leupold S,et al. An engineered Calvin-Benson-Bassham cycle for carbon dioxide fixation in Methylobacterium extorquens AM1[J]. Metabolic Engineering,2018,47:423-433.
[89]Jones S W,Fast A G,Carlson E D,et al. CO2fixation by anaerobic non-photosynthetic mixotrophy for improved carbon conversion[J]. Nature Communications,2016,7(1):1-9.
[90]Hu G P,Li Y,Ye C,et al. Engineering microorganisms for enhanced CO2sequestration[J]. Trends in Biotechnology,2019,37(5):532-547.31A34332-FF5A-4E17-873D-198B4A5FC60E
[91]Zhang Y W,Zhou J A,Zhang Y C,et al. Auxiliary module promotes the synthesis of carboxysomes in E.coli to achieve high-efficiency CO2assimilation[J]. ACS Synthetic Biology,2021,10(4):707-715.
[92]Saini R,Kapoor R,Kumar R,et al. CO2utilizing microbes—a comprehensive review[J]. Biotechnology Advances,2011,29(6):949-960.
[93]Liang F Y,Lindblad P. Effects of overexpressing photosynthetic carbon flux control enzymes in the cyanobacterium Synechocystis PCC 6803[J]. Metabolic Engineering,2016,38:56-64.
[94]Liang F Y,Englund E,Lindberg P,et al. Engineered cyanobacteria with enhanced growth show increased ethanol production and higher biofuel to biomass ratio[J]. Metabolic Engineering,2018,46:51-59.
[95]Huber H,Gallenberger M,Jahn U,et al. A dicarboxylate/4-hydroxybutyrate autotrophic carbon assimilation cycle in the hyperthermophilic Archaeum Ignicoccus hospitalis[J]. Proceedings of the National Academy of Sciences of the United States of America,2008,105(22):7851-7856.
[96]Gong F Y,Liu G X,Zhai X Y,et al. Quantitative analysis of an engineered CO2-fixing Escherichia coli reveals great potential of heterotrophic CO2fixation[J]. Biotechnology for Biofuels,2015,8(1):1-10.
[97]Brown S H,Bashkirova L,Berka R,et al. Metabolic engineering of Aspergillus oryzae NRRL 3488 for increased production of L-malic acid[J]. Applied Microbiology and Biotechnology,2013,97(20):8903-8912.
[98]Xiong W,Lee T C,Rommelfanger S,et al. Phosphoketolase pathway contributes to carbon metabolism in cyanobacteria[J]. Nature Plants,2015,2(1):1-8.
[99]Bar-Even A,Noor E,Lewis N E,et al. Design and analysis of synthetic carbon fixation pathways[J]. Proceedings of the National Academy of Sciences of the United States of America,2010,107(19):8889-8894.
[100]Wu G,Yan Q A,Jones J A,et al. Metabolic burden:cornerstones in synthetic biology and metabolic engineering applications[J]. Trends in Biotechnology,2016,34(8):652-664.31A34332-FF5A-4E17-873D-198B4A5FC60E

