婴儿肝移植术后产金属β-内酰胺酶肺炎克雷伯菌腹腔感染治疗1例及文献复习
刘东华 郭延磊 曲海军 周长凯 全香花 崔萌纳 李静
关键词头孢他啶阿维巴坦;氨曲南;儿童;腹腔感染;器官移植;金属β-内酰胺酶;肺炎克雷伯菌;肠杆菌科细菌
在过去的20 多年中,我国实体器官移植迅猛发展,但同时出现了许多耐药菌,给器官移植带来了巨大的挑战。实体器官移植受者一旦发生耐药菌感染,病死率可高达40.4%[1]。其中耐碳青霉烯酶的肠杆菌科细菌(carbapenemase-resistant Enterobacteriaceae,CRE)感染与严重侵袭性感染、移植物失败以及移植受者的高死亡率显著相关[2]。肠杆菌科细菌对碳青霉烯类抗生素最主要的耐药机制是产生碳青霉烯酶或金属β-内酰胺酶(metallo-β-lactamase,MBL)。对于耐氨曲南的产MBL肠杆菌科细菌,目前可用于治疗其引起感染的抗生素很少,多黏菌素、替加环素、氨基糖苷类等毒性较大的药物成为唯一可用的治疗选择[3]。因此,这对耐氨曲南的产MBL肠杆菌感染的治疗提出了挑战。正如一些病例报告和已发表的研究所见,在成人患者中使用头孢他啶阿维巴坦和氨曲南的组合在治疗耐氨曲南的产MBL肠杆菌感染方面显示出一定前景[4-6]。2021 年7 月,1 名5 个月的女婴在青岛大学附属医院(后称“我院”)行肝移植手术,术后发生腹腔感染,致病菌为耐氨曲南的产MBL肺炎克雷伯菌。据笔者检索,国外有3 篇关于成人器官移植受者对耐氨曲南的产MBL 革兰氏阴性杆菌感染病例报道[3,7-8],目前国内外均无儿童器官移植受者发生相关感染的报道。现将该患儿的具体诊疗过程报道如下并检索相关病例资料进行分析,以期对耐氨曲南的产MBL肠杆菌科细菌感染儿童患者的临床治疗提供参考。
1 病例资料
女婴,5 个月龄,因先天性胆道闭锁在外院行葛西手术后7 周,于2021 年7 月30 日拟行肝移植治疗而收入我院。入院查体示体温36.5 ℃,心率110 次/min,呼吸频率30 次/min,血压84/54 mmHg(1 mmHg=0.133 kPa)。患儿身高61 cm,体质量6 kg,营养良好,皮肤黏膜黄染、无皮疹。专科检查结果示:患儿腹部平坦,对称,可见葛西手术术后瘢痕愈合良好;腹部柔软,未触及异常包块;可触及脾大;肠鸣音正常,约3 次/min,未听到血管杂音。患儿入院诊断如下:肝硬化、脾大、门静脉高压、先天性胆管闭塞性黄疸、胆肠吻合术后。实验室检查示血清天冬氨酸转氨酶(aspartate aminotransferase,AST)588U/L(↑,表示高于正常值上限,下同)、丙氨酸转氨酶(alanine aminotransferase,ALT)275 U/L(↑)、血清肌酐16.56 μmol/L(↓,表示低于正常值下限,下同)、白细胞(white blood cell,WBC)计数4.13×109 L-1(↓)、中性粒细胞计数2.37×109 L-1、全血C反應蛋白(C-reactive protein,CRP)1.52 mg/L、血小板86×109 L-1(↓)。
2 治疗过程
患儿于2021 年7 月31 日在我院行同种异体肝移植手术,术后转入肝移植监护室。患儿围术期预防用抗感染方案为美罗培南(0.1 g,q8 h)、替考拉宁(0.06 g,qd)和卡泊芬净(16 mg,qd)。术后给予他克莫司联合甲泼尼龙免疫抑制方案。术后患儿持续发热,最高体温为39.2 ℃。
术后第4 天,患儿WBC计数8.16×109 L-1,中性粒细胞计数3.82×109 L-1,CRP 145.94 mg/L(↑),降钙素原(procalcitonin,PCT)1.80 ng/mL(↑),ASL 87 U/L(↑),ALT 203 U/L(↑),肌酐20.29 μmol/L(↓),血小板31×109 L-1(↓),血钠151 mmol/L(↑)。患儿腹腔引流液培养结果显示:耐碳青霉烯酶肺炎克雷伯菌肺炎亚种,金属β-内酰胺酶(+);药敏结果显示其仅对替加环素、庆大霉素和妥布霉素敏感,对氨曲南耐药[最低抑菌浓度(minimum inhibitory concentration,MIC)>64 μ g/mL]。但我院微生物实验室无法进行MBL分型检测。临床医师停用美罗培南,调整抗感染方案为多黏菌素B 10 mg,q12 h(负荷剂量2.5 mg/kg 静脉注射,随后每12 h 静脉注射1.67 mg/kg)和替加环素(负荷剂量40 mg,随后每12 h静脉注射20 mg),替考拉宁按原用法用量继续使用。器官保存液培养提示近平滑假丝酵母菌,临床医师停用卡泊芬净,换用氟康唑40 mg,qd,口服。针对患儿血钠高的情况,临床医师给予限钠、补液及鼻饲低渗液的治疗,同时动态监测血钠。患儿术后肠胀气明显、腹内压升高,故暂不给予肠内营养,继续肠外营养支持。调整用药方案后,患儿仍有发热,最高体温稍有下降,为38.3 ℃。
术后第7 天,患儿左侧手术切口愈合不良,出现大量渗出液;期间患儿的多次腹腔引流液、腹水和切口分泌物反复培养为产MBL肺炎克雷伯菌,药敏结果与上述一致。
术后第9 天,临床医师考虑患儿手术切口愈合不良、腹腔感染,故行剖腹探查术,探查原手术切口及腹腔内,并用温盐水冲洗腹腔,冲洗液清亮。
术后第12 天,患儿WBC计数7.66×109 L-1,中性粒细胞计数3.41×109 L-1,CRP 51.69 mg/L(↑),PCT 0.89ng/mL(↑),ASL 26 U/L,ALT 23 U/L,肌酐26.6 μmol/L(↓),血小板80×109 L- 1(↓),血钠142 mmol/L,血钙1.07 mmol/L(↓),最高体温38.6 ℃,感染指标仍高,且双下肢和手臂出现休克花斑。临床医师认为抗感染方案治疗效果不佳,考虑调整抗感染方案。临床药师通过文献检索,建议可以调整方案为头孢他啶阿维巴坦联合氨曲南。临床医师最终停用替加环素,将抗感染方案调整为头孢他啶阿维巴坦0.5 g,q8 h(静脉滴注2 h)和氨曲南0.18 g,q6 h(每日120 mg/kg),同时继续使用多黏菌素B(10 mg,q12 h)。患儿转氨酶恢复正常,但腹内压仍高、存在腹胀,临床医师开始给予其适量糖水、母乳,同时给予益生菌,促进胃肠道功能恢复。患儿高血钠较前纠正,但出现低血钙,故临床医师给予补充钙剂,以维持电解质平衡。
后第14 天,即头孢他啶阿维巴坦联合氨曲南治疗第2 天,患儿腹腔引流液、腹水切口分泌物培养均无细菌生长,AST、ALT和胆红素均恢复至正常。术后第20 天,患儿体温恢复正常,实验室检查结果和临床表现均有明显改善,PCT 降至0.26 ng/mL,因此将患儿从肝移植监护室转入儿童器官移植科,同时停用多黏菌素B,抗感染方案仅采用头孢他啶阿维巴坦联合氨曲南,在给予患儿适量奶粉的同时联合肠外营养支持治疗。
术后第23 天,患儿大便次数增多,并伴有腹泻,粪便常规分析示WBC阴性。大便菌群分析如下:革兰氏阴性杆菌5%,革兰氏阳性球菌90%,革兰氏阳性杆菌5%。临床医师继续给予患儿益生菌调节肠道菌群。患儿的PCT 和CRP 继续稳步下降,术后第24 天分别降至0.08 ng/mL和17.46 mg/L。
术后第26 天,临床医师考虑患儿临床症状及感染指标均好转且稳定,故停用头孢他啶阿维巴坦和氨曲南。停药第2 天,即术后第27 天,患儿又出现发热,临床医师使用美罗培南(0.1 g,q8 h)联合氨曲南(0.18 g,q6 h)的方案,患儿仍发热。在术后第29 天,临床医师重新启用头孢他啶阿维巴坦联合氨曲南治疗方案,未再使用多黏菌素B。
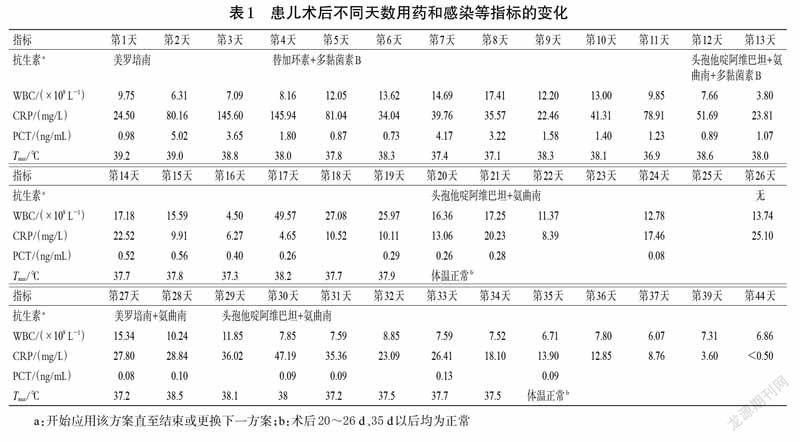
术后第35 天,患儿体温恢复正常,病情平稳,大便正常。患儿逐渐增加奶粉用量,并在术后第48 天停用头孢他啶阿维巴坦和氨曲南。患儿于术后第61 天出院。出院后随访2 个月,患儿未再出现发热和感染等情况。患儿整个治疗期间的用药和感染等指标的变化如表1所示。
3 讨论
3.1 器官移植术后产MBL肠杆菌科细菌感染的治疗
肠杆菌科细菌对碳青霉烯类药物耐药最主要的机制是其可产生碳青霉烯酶[9]。碳青霉烯酶按照Ambler分子分类法,可分为A、B、D 3 类:A类为丝氨酸碳青霉烯酶,B 类为MBL,D 类为OXA-48 型丝氨酸碳青霉烯酶[10]。另外少数菌株对碳青霉烯类药物耐药的机制还包括产生超广谱β-内酰胺酶(extended-spectrum β-lactamase,ESBLs)和/或头孢菌素酶合并外膜孔蛋白表达下调或缺失[10]。头孢他啶阿维巴坦对A 类[如肺炎克雷伯菌碳青霉烯酶(Klebsiella pneumoniae carbapenemase,KPCs)]、头孢菌素酶和一些D类碳青霉烯酶具有活性,目前已被广泛用于治疗移植受者中由CRE 引起的感染[11 - 12]。但阿维巴坦对MBL 没有活性,而氨曲南对MBL稳定。美国移植传染病学会的指南指出,虽然氨曲南对MBL 具有活性,但耐药菌往往同时产生ESBLs、KPCs或其他头孢菌素酶,这些酶会水解氨曲南,氨曲南单独给药可能对产MBL肠杆菌科细菌感染无效[13-14]。
尽管缺乏临床数据,该指南对器官移植受者產MBL肠杆菌科细菌感染仍推荐头孢他啶阿维巴坦联合氨曲南的治疗方案。《桑福德抗微生物治疗指南》针对除氨曲南外的所有β-内酰胺类药物耐药的产金属碳青霉烯酶革兰氏阴性杆菌感染,也推荐首选头孢他啶阿维巴坦联合氨曲南的治疗方案[15]。
本例患儿腹腔引流液、腹水及切口分泌物均培养出产MBL肺炎克雷伯菌,药敏结果显示其对替加环素、庆大霉素和妥布霉素敏感,但对氨曲南耐药。目前的指南和《桑福德抗微生物治疗指南》对耐氨曲南的产MBL革兰氏阴性杆菌感染均未给予推荐药物。笔者检索文献发现,国外有3 篇关于成人器官移植受者对耐氨曲南的产MBL革兰氏阴性杆菌感染的病例报道(表2)。其中,Mojica 等[7]报道了1 例肾移植患者因多重耐药嗜麦芽窄食单胞菌导致菌血症,使用头孢他啶阿维巴坦联合氨曲南成功治愈。Benchetrit 等[8]报道了2 例产新德里金属-β-内酰胺酶1(New Delhi metallo-β-lactamase 1,NDM1)肺炎克雷伯菌致感染性休克的器官移植患者:第1 例为肾移植术后患者,继发于血流感染发生感染性休克,初始方案采用多黏菌素E联合庆大霉素,治疗后血培养仍为阳性,换用头孢他啶阿维巴坦联合氨曲南方案后,患者临床状况迅速好转;第2 例为肺移植术后5 个月的患者,因呼吸机相关性肺炎引起感染性休克,初始方案选用替加环素联合多黏菌素E,由于支气管痉挛停用多黏菌素E,改用头孢他啶阿维巴坦+氨曲南+替加环素的三联方案最终成功治愈。Cairns 等[3]报道了4 例产IMP-4(imipenemase-4)金属酶的阴沟肠杆菌感染移植患者,其中1 例患者最终死于与造血干细胞移植相关的并发症,其他3 例患者均成功治愈。而本文病例中患儿初始方案基于药敏结果选用了多黏菌素B联合替加环素的方案,治疗有一定效果;但使用该方案9 d 后,患儿出现病情反复,同时出现休克性花斑,临床改用头孢他啶阿维巴坦联合氨曲南后最终治愈。与国外报道的案例相似,初始方案选用致病菌敏感的抗生素联合方案,但效果并不好,最终换用头孢他啶阿维巴坦联合氨曲南治愈。该患儿使用头孢他啶阿维巴坦联合氨曲南的治疗长达25 d,这期间多黏菌素B仅在前8 d 中有使用;患儿在术后第26 天病情稳定,但临床停用头孢他啶阿维巴坦联合氨曲南后,出现病情反复;然后又再次启用头孢他啶阿维巴坦联合氨曲南,并没有使用多黏菌素B,最终患儿的感染得到控制。多黏菌素B主要适应于其敏感菌导致的泌尿系感染、肺部感染、脑膜炎和血流感染,其组织扩散较差,在对肺部感染及脑膜炎患者静脉应用的同时应辅助局部用药治疗[16]。本文病例中患儿为腹腔感染,考虑多黏菌素B组织扩散较差,对患儿的感染真正起作用的药物主要为氨曲南和头孢他啶阿维巴坦。
3.2 头孢他啶阿维巴坦联合氨曲南对耐氨曲南的产MBL肠杆菌科细菌感染治疗有效的机制及给药方式Davido 等[17]进行了头孢他啶阿维巴坦和氨曲南的联合药敏试验,结果表明在头孢他啶阿维巴坦存在的条件下,氨曲南的MIC从12 mg/L 降至2 mg/L。体外药敏试验证明,对于耐氨曲南的产MBL肠杆菌科细菌,头孢他啶阿维巴坦联合氨曲南方案可以逆转其耐药性。这种组合对产MBL 细菌有效的机制可能是:氨曲南对MBL 酶具有活性,但耐药菌往往同时产生ESBLs、KPCs 或其他头孢菌素酶,这些酶会水解氨曲南,从而使氨曲南耐药;头孢他啶阿维巴坦联合氨曲南时,该方案中的阿维巴坦可灭活A类酶、头孢菌素酶或D类酶,从而恢复细菌对氨曲南的敏感性[3,7-8]。
Lodise 等[18]研究表明,同时给予高剂量氨曲南(2 g,q6 h)与头孢他啶阿维巴坦静脉滴注2 h 可完全清除细菌;并且发现同时给药方式优于交替给药方式(先静脉滴注头孢他啶阿维巴坦,再静脉滴注氨曲南),但该结果尚需要更多临床试验来验证。在本文的案例中,该患儿采用的是交替给药方式,最终治疗有效。
3.3 头孢他啶阿维巴坦的剂量选择基于2 项针对3 个月~18 岁的尿路感染及腹腔感染儿童使用头孢他啶阿维巴坦治疗的Ⅱ期随机对照研究[19-20],2019 年美国FDA批准头孢他啶阿维巴坦用于治疗3 个月及以上儿童患者的复杂尿路感染和腹腔感染[21]。不同月(年)龄段及肾功能情况儿童给药剂量[21]如表3和表4 所示。
针对儿童(3 个月~<18 岁)腹腔感染治疗的Ⅱ期临床研究结果表明,头孢他啶阿维巴坦联合甲硝唑具有良好的耐受性,其安全性与单独使用头孢他啶相似,并且對由革兰氏阴性菌(包括头孢他啶不敏感菌株)引起的儿科腹腔感染患者有效。FDA说明书中推荐,对于6个月~18 岁儿童,头孢他啶阿维巴坦给药剂量为62.5 mg/kg(50 mg/kg 头孢他啶+12.5 mg/kg 阿维巴坦),q8 h。因此,本案例中临床药师建议该患儿的头孢他啶阿维巴坦给药剂量采用62.5 mg/kg,q8 h。但临床医师考虑患儿感染严重,并处于免疫抑制状态,考虑加大剂量使用。临床药师依据《桑福德抗微生物治疗指南》对年龄>28 d的患儿推荐头孢他啶剂量为150~200 mg/(kg·d),且该患儿肾功能正常,故建议临床医师最终剂量以头孢他啶计不超过200 mg/(kg·d)。最终临床医师基于头孢他啶200 mg/(kg·d)的剂量,将头孢他啶阿维巴坦的剂量确定为0.5 g(83.4 mg/kg),q8 h。调整抗感染方案时,患儿已满6 月龄,体质量6 kg,该剂量大于FDA 说明书推荐的使用剂量(62.5 mg/kg,q8 h)[20],因此根据我院超说明书用药的管理规定,与患者家属签署了知情同意书。
3.4 不良反应监护国外2 项针对3 个月~18 岁尿路感染和腹腔感染儿童使用头孢他啶阿维巴坦治疗的Ⅱ期随机对照研究中,67 例和61 例患儿应用头孢他啶阿维巴坦的安全性与成人患者使用头孢他啶阿维巴坦的安全性一致[19-20]。头孢他啶阿维巴坦常见的不良反应包括胃肠道反应(如腹泻、恶心、呕吐、腹痛)、神经系统不良反应(如头痛、眩晕)、艰难梭菌相关性腹泻、肝功能异常、外周水肿、超敏反应等[22]。本病例用药期间,患儿仅出现过腹泻,经治疗后好转,未观察到其他不良反应的发生。患儿肝移植术后第12 天开始使用头孢他啶阿维巴坦,此时患儿的肝功基本恢复正常,整个用药期间患儿的肝肾功能无异常改变。
4 结语
本例患儿为肝移植术后耐氨曲南的产MBL肺炎克雷伯菌腹腔感染的婴儿,初始方案选用致病菌敏感的抗生素联合方案,治疗效果不佳,临床药师通过文献检索,协助临床医师选用头孢他啶阿维巴坦联合氨曲南的方案。对于头孢他啶阿维巴坦,美国FDA已经批准其用于治疗3 个月及以上儿童患者的复杂尿路感染和腹腔感染[21]。在多药耐药革兰氏阴性菌日益严重以及儿童用药种类选择有限的情况下,头孢他啶阿维巴坦联合氨曲南为耐氨曲南的产MBL肠杆菌感染的器官移植患儿提供了一种有价值的治疗选择。

