痰热清注射液特征图谱建立及4种成分测定
张静娴, 孙 健, 陈 军, 吴清臣, 毛秀红, 胡 青*, 季 申*
(1.上海市食品药品检验研究院,国家药品监督管理局中药质量控制重点实验室,上海 201203;2.上海凯宝药业股份有限公司,上海 200030)
痰热清注射液由黄芩、熊胆粉、山羊角、金银花、连翘5味药材组成,具有清热解毒、止咳化痰的作用,临床上广泛用于治疗发热、急性支气管炎、急性肺炎、慢性阻塞性肺炎等[1-7],还具有抗病毒、抗菌作用[8-10],其主要成分有黄酮、酚酸、氨基酸、胆酸等[11-14]。该制剂现行国家药品标准中有2项特征图谱[15],分别反映山羊角、金银花中氨基酸、酚酸类成分,但尚无反映君药黄芩所含成分的特征图谱,仅测定了黄芩苷、野黄芩苷含量,另外只有文献[7]报道了同时测定芦丁、白杨素-7-O-葡萄糖醛酸苷等6种成分的含量。因此,本实验建立痰热清注射液特征图谱,并以黄芩苷为内标,通过一测多评法测定野黄芩苷、千层纸素-7-O-葡萄糖醛酸苷、白杨素-7-O-葡萄糖醛酸苷含量,为该制剂质量标准的完善提升提供参考。
1 材料
Agilent 1260高效液相色谱仪(美国Agilent公司,配置四元泵、光电二极管阵列检测器、柱温箱、自动进样器、ChemStation工作站);BP211D电子天平(0.01 mg,德国Sartorius公司)。黄芩苷(批号110715-201619)、野黄芩苷(批号110842-200102)对照品购自中国食品药品检定研究院;千层纸素-7-O-葡萄糖醛酸苷(批号100286)、白杨素-7-O-葡萄糖醛酸苷(批号100271)对照品购自江苏永健医药科技有限公司。痰热清注射液样品共33批,包括2016年13批(编号S1~S13,批号分别为1605205、1605206、1607115、1607116、1608216、1608217、1610210、1610211、1611315、1611316、1612219、1612220、1612311)、2017年10批(编号S14~S23,批号分别为1711218、1711219、1711220、1711221、1711222、1711223、1711224、1711225、1711216、1712201)、2018年10批(编号S24~S33,批号分别为1802210、1802211、1802212、1803209、1803207、1803208、1804314、1803210、1803220、1803221),由上海凯宝药业股份有限公司提供。乙腈、甲醇、甲酸为色谱纯,购自德国Merck 公司;其余试剂均为分析纯;水为超纯水,由美国Milli-Q超纯水系统制备。
2 方法与结果
2.1 特征图谱建立
2.1.1 色谱条件 Diamonsil Plus C18色谱柱(5 μm,4.6 mm×25 cm);流动相乙腈(A)-0.1%甲酸(B),梯度洗脱(0~30 min,15%~30%A;30~60 min,30%A);体积流量0.8 mL/min;柱温25 ℃;检测波长280 nm。
2.1.2 对照品溶液制备 精密称取野黄芩苷、黄芩苷、千层纸素-7-O-葡萄糖醛酸苷、白杨素-7-O-葡萄糖醛酸苷对照品适量,甲醇制成质量浓度分别为25、80、50、25 μg/mL的溶液,即得。
2.1.3 供试品溶液制备 精密量取本品5 mL,置于20 mL量瓶中,加水稀释至刻度,摇匀,即得。
2.1.4 方法学考察
2.1.4.1 专属性试验 通过与对照品保留时间比对,确定5、10~12号峰分别为野黄芩苷、黄芩苷、千层纸素-7-O-葡萄糖醛酸苷、白杨素-7-O-葡萄糖醛酸苷,阴性无干扰,见图1。
2.1.4.2 精密度试验 取供试品溶液(S1)适量,在“2.1.1”项色谱条件下进样测定6次,去除黄芩苷峰后导出AIA数据,采用“中药色谱特征图谱相似度评价系统”(2012版)软件计算相似度,发现均大于0.99,表明仪器精密度良好。
2.1.4.3 重复性试验 取本品(S1)6支,按“2.1.3”项下方法制备供试品溶液,在“2.1.1”项色谱条件下进样测定,去除黄芩苷峰后导出AIA数据,采用“中药色谱指纹图谱相似度评价系统”(2012版)软件计算相似度,发现均大于0.99,表明该方法重复性良好。
2.1.4.4 稳定性试验 取供试品溶液(S1)适量,室温下于0、4、8、12、16、20、24 h在“2.1.1”项色谱条件下进样测定,去除黄芩苷峰后导出AIA数据,采用“中药色谱指纹图谱相似度评价系统”(2012版)软件计算相似度,发现均大于0.98,表明溶液在24 h内稳定性良好。
2.1.5 图谱生成与相似度评价 取33批样品,按“2.1.3”项下方法制备供试品溶液,在“2.1.1”项色谱条件下进样测定,获得特征图谱,以保留时间适中的黄芩苷(10号峰)为参照,共确定了12个特征峰。去除黄芩苷峰后导出AIA数据,导入“中药色谱指纹图谱相似度评价系统”(2012版)软件进行色谱峰匹配,采用平均值法生成对照特征图谱,见图2。再计算相似度,结果见表1,可知均大于0.97。
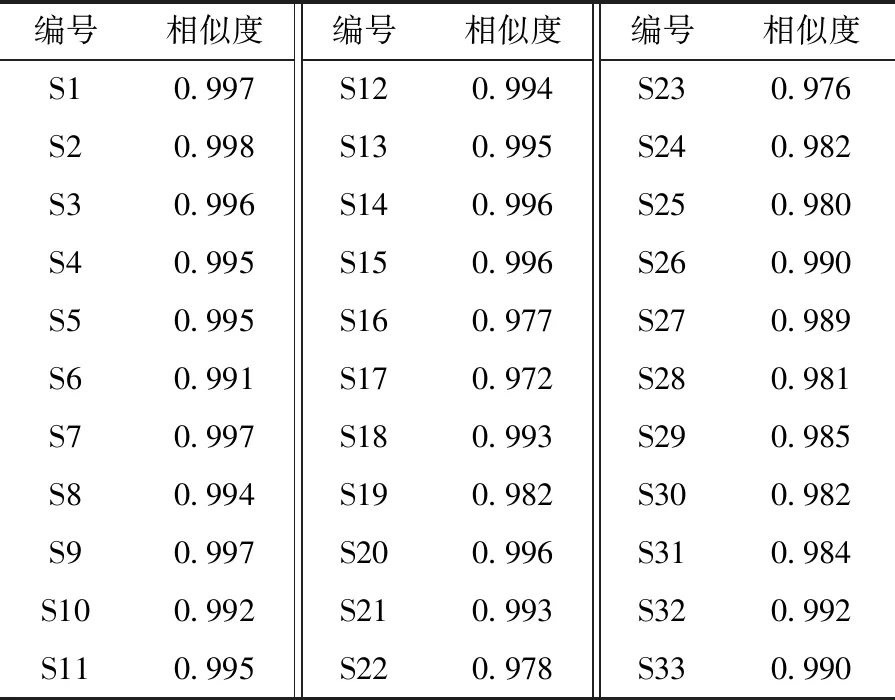
表1 33批样品相似度Tab.1 Similarities of thrity-three batches of samples
2.2 一测多评法测定各成分含量
2.2.1 色谱条件 同“2.1.1”项。
2.2.2 对照品溶液制备 精密称取野黄芩苷、黄芩苷、千层纸素-7-O-葡萄糖醛酸苷、白杨素-7-O-葡萄糖醛酸苷对照品适量,甲醇制成质量浓度均为1 mg/mL的贮备液,分别精密量取2.5、8.0、5.0、2.5 mL至同一量瓶中,制成质量浓度分别为125、400、250、125 μg/mL的对照品溶液,分别吸取0.2、0.4、2、4、5 mL至5 mL量瓶中,即得[野黄芩苷、白杨素-7-O-葡萄糖醛酸苷质量浓度(L1~L5)分别为5、10、50、100、125 μg/mL,黄芩苷质量浓度(L1~L5)分别为16、32、160、320、400 μg/mL,千层纸素-7-O-葡萄糖醛酸苷质量浓度(L1~L5)分别为10、20、100、200、250 μg/mL]。
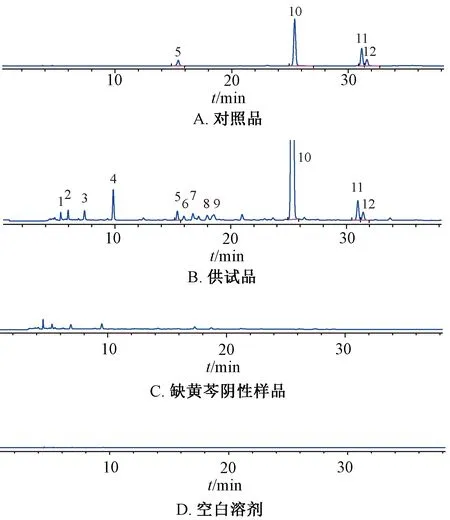
5. 野黄芩苷 10. 黄芩苷 11. 千层纸素-7-O-葡萄糖醛酸苷12.白杨素-7-O-葡萄糖醛酸苷5. scutellarin 10. baicalin 11. oroxylin A-7-O-glucoronide12.chrysin-7-O-glucoronide图1 各成分HPLC色谱图Fig.1 HPLC chromatograms of various constituents
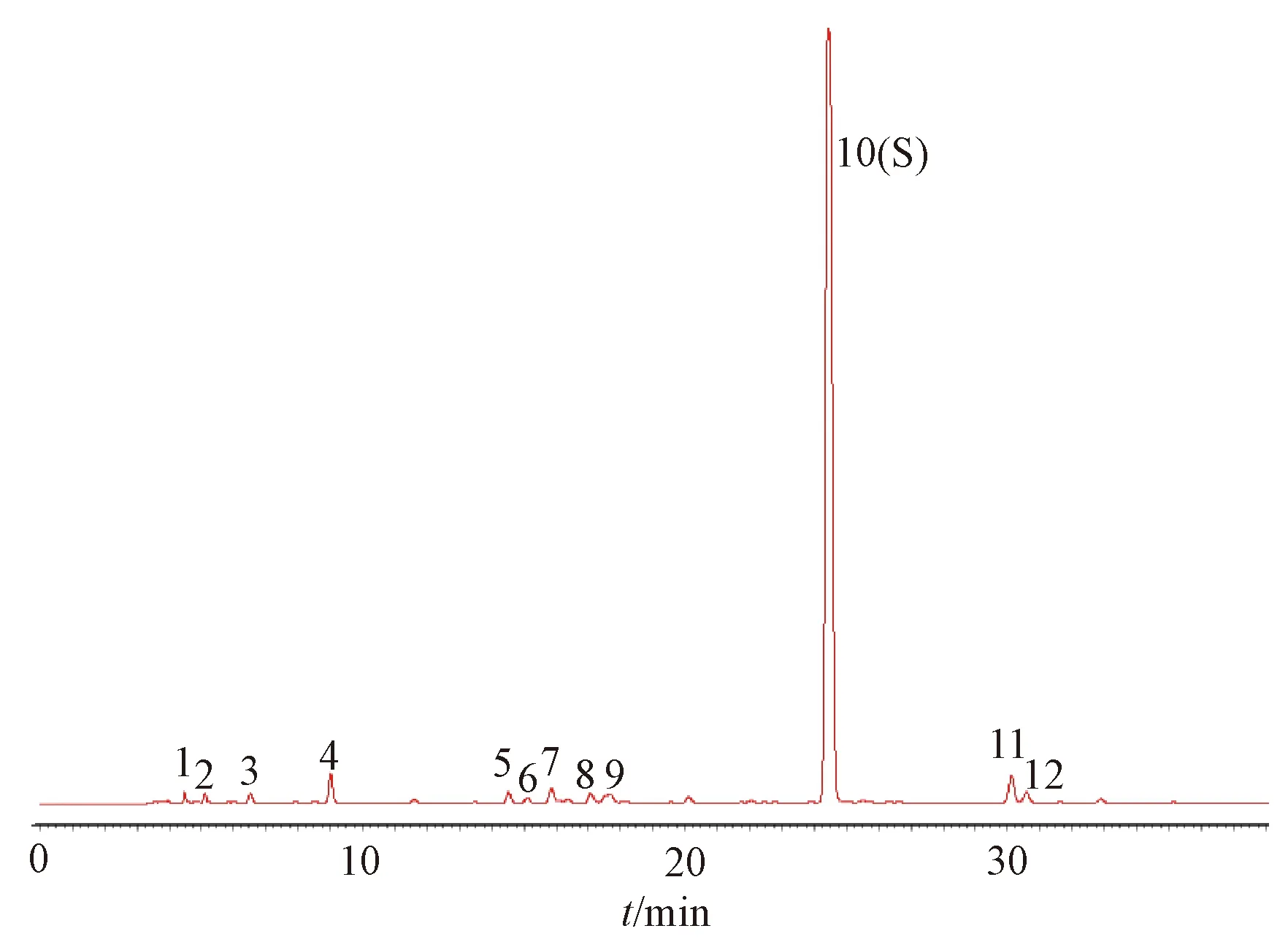
5. 野黄芩苷 10. 黄芩苷 11. 千层纸素-7-O-葡萄糖醛酸苷 12. 白杨素-7-O-葡萄糖醛酸苷5. scutellarin 10. baicalin 11. oroxylin A-7-O-glucoronide 12. chrysin-7-O-glucoronide图2 对照特征图谱Fig.2 Reference characteristic chromatogram
2.2.3 供试品溶液制备 取“2.1.3”项下供试品溶液,用于野黄芩苷、千层纸素-7-O-葡萄糖醛酸苷、白杨素-7-O-葡萄糖醛酸苷含量测定。另精密量取“2.1.3”项下供试品溶液1 mL至20 mL量瓶中,加水溶解置刻度,摇匀,用于黄芩苷含量测定。
2.2.4 方法学考察
2.2.4.1 线性关系考察 精密吸取“2.2.2”项下对照品溶液10 μL,在“2.1.1”项色谱条件下进样测定。以对照品质量浓度为横坐标(X),峰面积为纵坐标(Y)进行回归,结果见表2,可知各成分在各自范围内线性关系良好。

表2 各成分线性关系Tab.2 Linear ranges of various constituents
2.2.4.2 精密度试验 精密吸取对照品溶液10 μL,在“2.1.1”项色谱条件下进样测定6次,测得野黄芩苷、黄芩苷、千层纸素-7-O-葡萄糖醛酸苷、白杨素-7-O-葡萄糖醛酸苷峰面积RSD分别为0.48%、0.29%、0.37%、0.38%,表明仪器精密度良好。
2.2.4.3 重复性试验 取本品(S1)适量,按“2.2.3”项下方法平行制备6份供试品溶液,在“2.1.1”项色谱条件下进样测定,测得野黄芩苷、黄芩苷、千层纸素-7-O-葡萄糖醛酸苷、白杨素-7-O-葡萄糖醛酸苷含量RSD分别为1.27%、0.69%、1.02%、1.13%,表明该方法重复性较好。
2.2.4.4 稳定性试验 取供试品溶液(S1)适量,室温下于0、4、8、12、16、20、24 h在“2.1.1”项色谱条件下进样测定,测得野黄芩苷、黄芩苷、千层纸素-7-O-葡萄糖醛酸苷、白杨素-7-O-葡萄糖醛酸苷峰面积RSD分别为1.32%、0.31%、0.39%、0.39%,表明溶液在24 h内稳定性良好。
2.2.4.5 加样回收率试验 黄芩苷:由于本品中黄芩苷含量高,故在加样回收率试验中适当减量,即供试品制备方法更改为“精密量取本品0.5 mL,置于2 mL量瓶中,加水稀释至刻度,摇匀,精密量取上述溶液1 mL至20 mL量瓶中,加水至刻度,摇匀,即得”。同时,取样量减半,即精密量取本品0.25 mL(S1)9份,置于2 mL量瓶中,分别精密加入对照品溶液(约1.6 mg/mL)0.5、1.0、1.5 mL各3份,分别相当于原有量的50%(低质量浓度)、100%(中质量浓度)、150%(高质量浓度),加水至刻度,摇匀,精密量取1 mL至20 mL量瓶中,加水至刻度,摇匀,在“2.1.1”项色谱条件下进样测定,计算回收率,结果见表3。
野黄芩苷、千层纸素-7-O-葡萄糖醛酸苷、白杨素-7-O-葡萄糖醛酸苷:精密量取本品2.5 mL(S1)9份,置于20 mL量瓶中,精密量取对照品溶液1.0、2.0、3.0 mL各3份,分别相当于原有量的50%(低质量浓度)、100%(中质量浓度)、150%(高质量浓度),加水稀释至刻度,在“2.1.1”项色谱条件下进样测定,计算回收率,结果见表3。

表3 各成分加样回收率试验结果(n=9)Tab.3 Results of recovery tests for various constituents(n=9)
2.2.5 内标选择 黄芩苷、野黄芩苷对照品容易获取,而千层纸素-7-O-葡萄糖醛酸苷、白杨素-7-O-葡萄糖醛酸苷对照品目前仅江苏永健医药科技有限公司有售,价格昂贵。由于黄芩苷色谱峰保留时间适中,故选择其作为内标。
2.2.6 相对保留时间、相对校正因子测定 精密吸取对照品溶液10 μL,在“2.1.1”项色谱条件下进样测定,以黄芩苷为内标计算其他3种成分的相对保留时间ti/s和相对校正因子fi/s,公式分别为ti/s=ti/ts(ti为其他成分保留时间,ts为内标保留时间)、fi/s=fi/fs=As×Ci/(Ai×Cs)(Ci为其他成分含量,Ai为其他成分峰面积,Ci为内标含量,As为内标峰面积),结果见表4,可知两者RSD均小于1.5%,表明其稳定性良好。
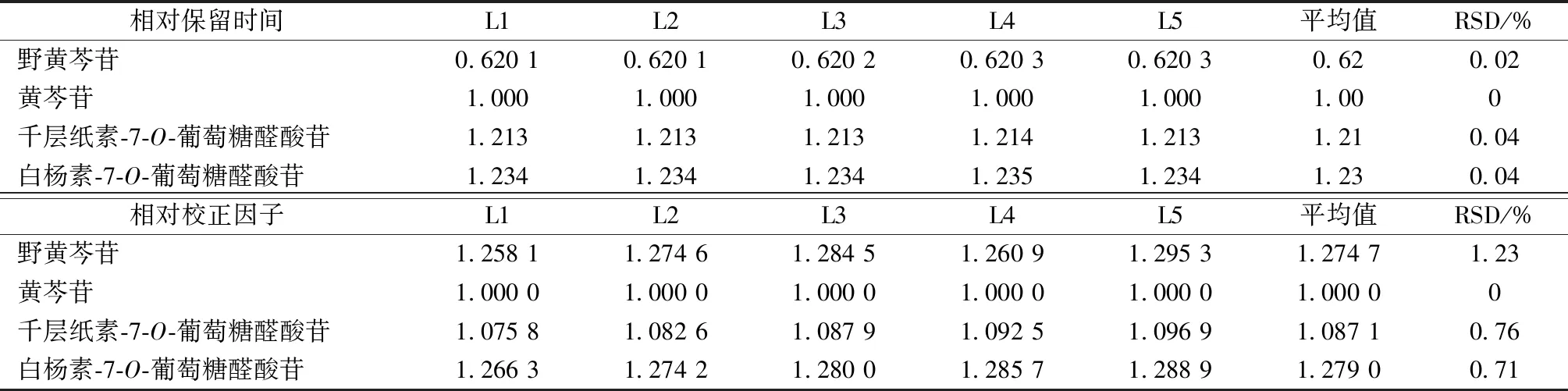
表4 各成分相对保留时间、相对校正因子测定结果(n=2)Tab.4 Results of relative retention time and relative correction factor determination of various constituents
2.2.7 耐用性试验
2.2.7.1 体积流量 本实验取对照品溶液(野黄芩苷、白杨素-7-O-葡萄糖醛酸苷质量浓度为25 μg/mL,黄芩苷质量浓度为80 μg/mL,千层纸素-7-O-葡萄糖醛酸苷质量浓度为50 μg/mL)适量,考察了体积流量0.7、0.8、0.9 mL/min对相对保留时间和相对校正因子的影响,结果见表5。由此可知,野黄芩苷受体积流量影响较大,其他2种成分受其影响较小,但为了保证千层纸素-7-O-葡萄糖醛酸苷、白杨素-7-O-葡萄糖醛酸苷色谱峰的分离度,故体积流量不高于0.9 mL/min。
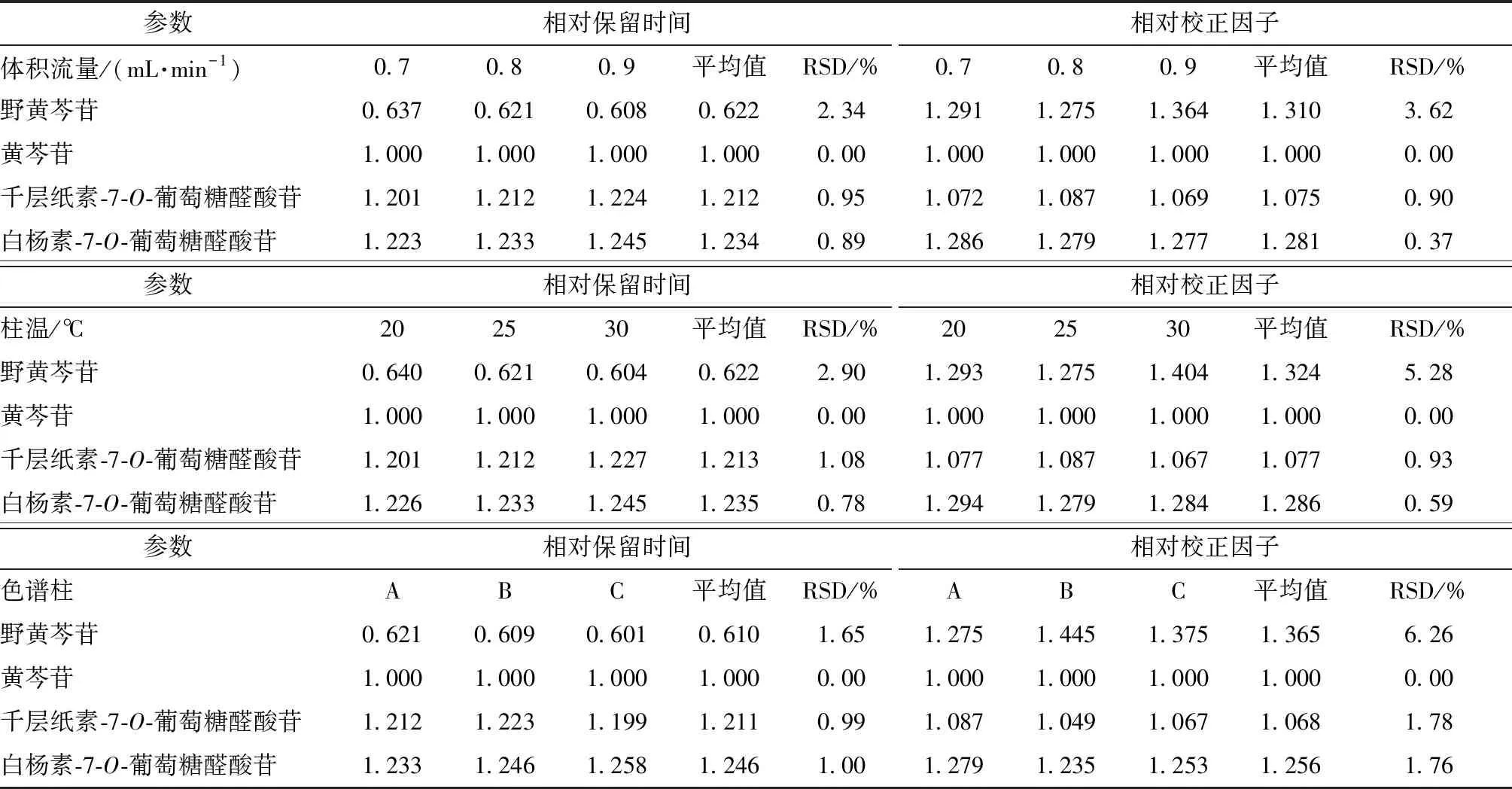
表5 各成分耐用性试验结果Tab.5 Results of durability tests for various constituents
2.2.7.2 柱温 本实验考察了柱温20、25、30 ℃对相对校保留时间和相对校正因子的影响,结果见表5。由此可知,野黄芩苷受柱温影响较大,其他2种成分受其影响较小,并且在20、25 ℃时相对校正因子接近,故柱温不高于25 ℃。
2.2.7.3 色谱柱 本实验考察了Diamonsil Plus C18(5 μm,4.6 mm×25 cm)(A)、Agilent Eclipse Plus C18(5 μm,4.6 mm×25 cm)(B)、Agilent SB-C18(5 μm,4.6 mm×25 cm)(C)色谱柱对相对保留时间和相对校正因子的影响,结果见表5。由此可知,各成分相对保留时间相对稳定;野黄芩苷相对校正因子受色谱柱影响较大,其他2种成分也有一定程度影响;当采用色谱柱B、C时,千层纸素-7-O-葡萄糖醛酸苷、白杨素-7-O-葡萄糖醛酸苷色谱峰的分离度略有降低,可能是其RSD偏大的原因,故在选择色谱柱时两者色谱峰必须达到基线分离。
2.2.7.4 仪器 本实验考察了Agilent 1260(A)、Agilent 1290(B)色谱仪(均配置二元泵)对相对保留时间和相对校正因子的影响,发现各成分两者RSD均小于1.6%,可见色谱仪对其无明显影响。
2.2.7.5 结论 当检测条件发生变化时,各成分相保留时间相对稳定;千层纸素-7-O-葡萄糖醛酸苷、白杨素-7-O-葡萄糖醛酸苷相对校正因子耐用性较好,而野黄芩苷相对校正因子受条件变化的影响较大,不适合采用一测多评法。由于野黄芩苷对照品易得,故采用外标法测定其含量。
2.2.8 样品含量测定 取9批样品(S3~S4、S12、S14、S17、S20、S24~S25、S28),按“2.2.3”项下方法制备供试品溶液,在“2.1.1”项色谱条件下进样测定,分别采用外标法、一测多评法测定含量,结果见表6。由此可知,2种方法所测野黄芩苷含量相对偏差较大,其中一测多评法偏低;其他2种成分含量基本一致,表明可以用一测多评法代替外标法测定两者含量。

表6 各成分含量测定结果(Ⅰ)Tab.6 Results of content determination of various constituents(Ⅰ)
同法测定33批样品中各成分含量,结果见表7,可知同一年份不同批次样品中各成分含量RSD均小于10%(2016年样品中野黄芩苷含量除外),表明其一致性较好。现行国家药品标准中,黄芩苷、野黄芩苷含量限度规定为“本品每1 mL含黄芩以黄芩苷(C21H18O11)计,应为5.0~8.0 mg;以野黄芩苷(C21H18O12)计,应为50~150 μg”,本实验33批样品均满足上述要求。以各成分含量平均值的±50%为上下限范围,规定每1 mL本品含千层纸素-7-O-葡萄糖醛酸苷100~300 μg、白杨素-7-O-葡萄糖醛酸苷50~150 μg。

表7 各成分含量测定结果(Ⅱ)Tab.7 Results of content determination of various constituents(Ⅱ)
3 讨论
本实验根据痰热清注射液制备工艺[15],将黄芩水煎液经调节pH值、醇沉后得提取物,再将其与其他药材提取物合并,通过调节pH值、超滤、灭菌等步骤制得成品,主要保留了黄芩中大极性黄酮苷类成分。再对中间体黄芩提取物进行分析,发现黄芩素含量较高,但在制备过程中该成分已基本不存在,而千层纸素-7-O-葡萄糖醛酸苷、白杨素-7-O-葡萄糖醛酸苷被进一步富集,故在痰热清注射液质量标准提升中很有必要增加这2种成分的含量测定,但两者对照品难以获取,价格昂贵,故本实验建立一测多评法[16-18],以容易获取的黄芩苷为内标,并对相对保留时间、相对校正因子的耐用性进行考察。
痰热清注射液中黄芩苷、野黄芩苷含量相差100倍,其现行质量标准需要2种测定方法,费时费力。因此,本实验通过稀释供试品溶液,在同一个色谱条件下进行含量测定,可大大提高分析效率。
4 结论
本实验针对痰热清注射液中黄芩所含成分质量控制不够全面的问题,建立了特征图谱和一测多评含量测定方法,进行了全面的方法学考察,并根据33批样品中野黄芩苷、黄芩苷、千层纸素-7-O-葡萄糖醛酸苷、白杨素-7-O-葡萄糖醛酸苷含量测定结果,给新增成分制订了限度,对该制剂质量标准的完善提升具有重要参考价值和指导意义。

