巯基螯合剂治疗重金属中毒研究进展
姚 青,杨国宝,王 皓,郭永学,杨 阳,高春生
(1.沈阳药科大学制药工程学院,辽宁 本溪 117000;2.军事科学院军事医学研究院毒物药物研究所,北京 100850)
重金属中毒是一种常发生于工业、农业及矿业活动的职业病,主要由强毒性重金属如汞、铅、铬、砷及镉等中毒引起。重金属密度较大,一般均>4.5 g·cm-3,其进入机体后可竞争体内特定酶上的巯基,使酶失去催化活性,造成细胞膜表面转运载体功能障碍,也会使肌球蛋白和肌动蛋白无法完成肌肉收缩,体内细胞无法获得营养,进而引起细胞结构异常和细胞功能丧失,最终出现中毒症状[1]。重金属中毒救治问题一直备受国内外关注。目前,临床上常用的解毒剂主要包括二巯丙醇(dimercaptopropanol,BAL)、二巯丁二酸(dimercaptosuccinic acid,DMSA)、二巯丙磺钠(sodium dimercaptopanesulfonate,DMPS)、青霉胺(penicillamine,DPEN)和硫辛酸(alpha lipoic acid,LA)等巯基螯合剂及依地酸二钠钙(disodium-calcium edetate,Na2CaEDTA)和二乙烯三胺五乙酸(diethylenetriaminepentaacetic acid,Na3CaDTPA)等非巯基螯合剂[2],其中巯基螯合剂是重金属中毒主要的解毒剂[3]。不同的巯基螯合剂对不同种类重金属中毒的解毒疗效有所不同。本文主要综述重金属中毒的主要类型、巯基螯合剂的解毒机制及不同解毒剂的临床应用,并提出联合用药的方式治疗重金属中毒可实现快速、安全、高效的解毒效果,提高患者用药顺应性,为重金属中毒的临床治疗提供参考。
1 重金属中毒机制、临床表现和解毒剂
1.1 汞中毒
汞主要以金属汞、无机汞和有机汞3种形式存在。甲基汞亲脂性强,极易穿透血脑屏障,引起脑组织汞中毒。汞进入血液及人体组织中,可与蛋白质及酶系统中的巯基结合,抑制其功能,甚至使其失活;汞与体内蛋白结合后可由半抗原成为抗原,引起变态反应,出现肾病综合征;高浓度的汞还可直接引起肾小球免疫损伤[4]。汞中毒患者的临床症状差异较大。急性汞中毒主要表现为发热和呼吸困难等症状;而慢性汞中毒主要表现为失眠、记忆力衰退及食欲不振等反应[5]。目前,临床上驱汞治疗首选二巯丁二钠注射液。
1.2 铅中毒
铅对人体无任何生理功能且有严重危害。铅暴露对造血系统、神经系统、消化系统、肾及心脏均有影响。一旦被吸收,就会被血液输送,与血红蛋白结合并抑制其合成,引起贫血;也可直接作用于胃黏膜,破坏其再生能力,出现炎症性变化[6]。铅暴露会影响肾小管上皮细胞线粒体的功能,抑制酶活性,导致尿肌酐排出减少,血肌酐和血尿素氮含量增加,尿糖排泄增加[7]。铅中毒主要表现为恶心、腹泻、血压升高和昏迷,甚至会有癫痫的发作。Na2CaEDTA对铅中毒具有较好的治疗效果。
1.3 铬中毒
在自然界中,铬(Ⅱ)和铬(Ⅲ)对人体几乎无毒,但铬(Ⅵ)为剧毒,易通过吸入或食入的方式侵入人体并蓄积,使机体代谢速度变缓。铬进入红细胞后,与血红蛋白结合,使血红蛋白变成高铁血红蛋白而失去携氧能力,对细胞造成损害。研究表明,铬通过抑制Bcl-2蛋白表达和增加促凋亡基因表达而诱导细胞凋亡[8]。铬中毒主要表现为呕吐、腹部灼烧和血水样便,严重者出现休克、面色发紫和呼吸困难等症状。对于铬中毒,目前最有效的治疗手段是注射二巯丁二钠。
1.4 砷中毒
无机砷主要通过空气、水和食物等媒介、经呼吸系统、消化系统和皮肤吸收,进入血液并随之进入全身各组织器官[9]。砷主要蓄积在肝,当含量达到一定限度时,就会引起砷中毒。砷会诱导脂质过氧化,产生多种自由基和非自由基,引起细胞功能紊乱,自由基进入细胞核,直接攻击DNA和RNA,引起DNA突变并致细胞癌变[10]。砷也可抑制大多数酶的活性,影响酶的空间构型与构象,从而使细胞的呼吸代谢受到抑制。食入性砷中毒急性期会有恶心、低血压、溶血、急性肾衰竭等症状;而亚急性期会伴有周边神经炎等症状出现。吸入性砷急性中毒常表现为呼吸困难、肺水肿和急性呼吸衰竭;慢性中毒会引起皮肤角质化、皮肤癌、白血病、四肢坏死和肝功能异常等症状。目前,砷中毒主要使用特效解毒剂BAL进行治疗。
1.5 镉中毒
镉分布广泛,毒性持久,多以二价形式存在,如氧化镉和硫化镉等。矿石开采及含镉垃圾的燃烧,使大量的镉颗粒释放到大气中。镉一旦被吸收,会迅速从血液分布到全身各处,引起机体功能紊乱,特别是肝和肾。镉进入组织,与钙竞争结合钙调素,干扰钙调素及其所调控的生理、生化体系,抑制多种酶的活性[11-12]。镉在肾蓄积,会引起肾小球屏障功能损害,肾小管细胞损害和功能障碍。镉中毒主要临床症状有呕吐、腹泻、咳嗽、急性肾衰竭和骨骼病变;部分患者出现鼻、牙齿异常,骨质疏松及休克的并发症。目前临床上常用特效解毒剂Na2CaEDTA治疗。
2 巯基螯合剂的解毒机制
巯基螯合剂是临床上应用最多的重金属中毒解毒剂。不同的巯基螯合剂所含的巯基数目与所处位置不同,便表现出不同的性质,其与重金属离子的作用机制也有所不同。通过研究不同巯基螯合剂的化学特征及其与重金属离子的络合反应,可探究巯基螯合物的解毒机制。
2.1 巯基螯合剂的化学特征
结构决定性质,性质体现用途。质子化常数对药物的生物学特性如溶解性、细胞穿透性和生物利用度等具有显著作用,对所形成螯合物的形态也具有重要意义。BAL、DMSA、DMPS、DPEN、LA和二氢硫辛酸(dihydrolipoic acid,DHLA)等巯基螯合剂的结构、名称、缩略词、分子式、相对分子质量和质子化常数等特征见表1,其随pH的形态变化如图1。
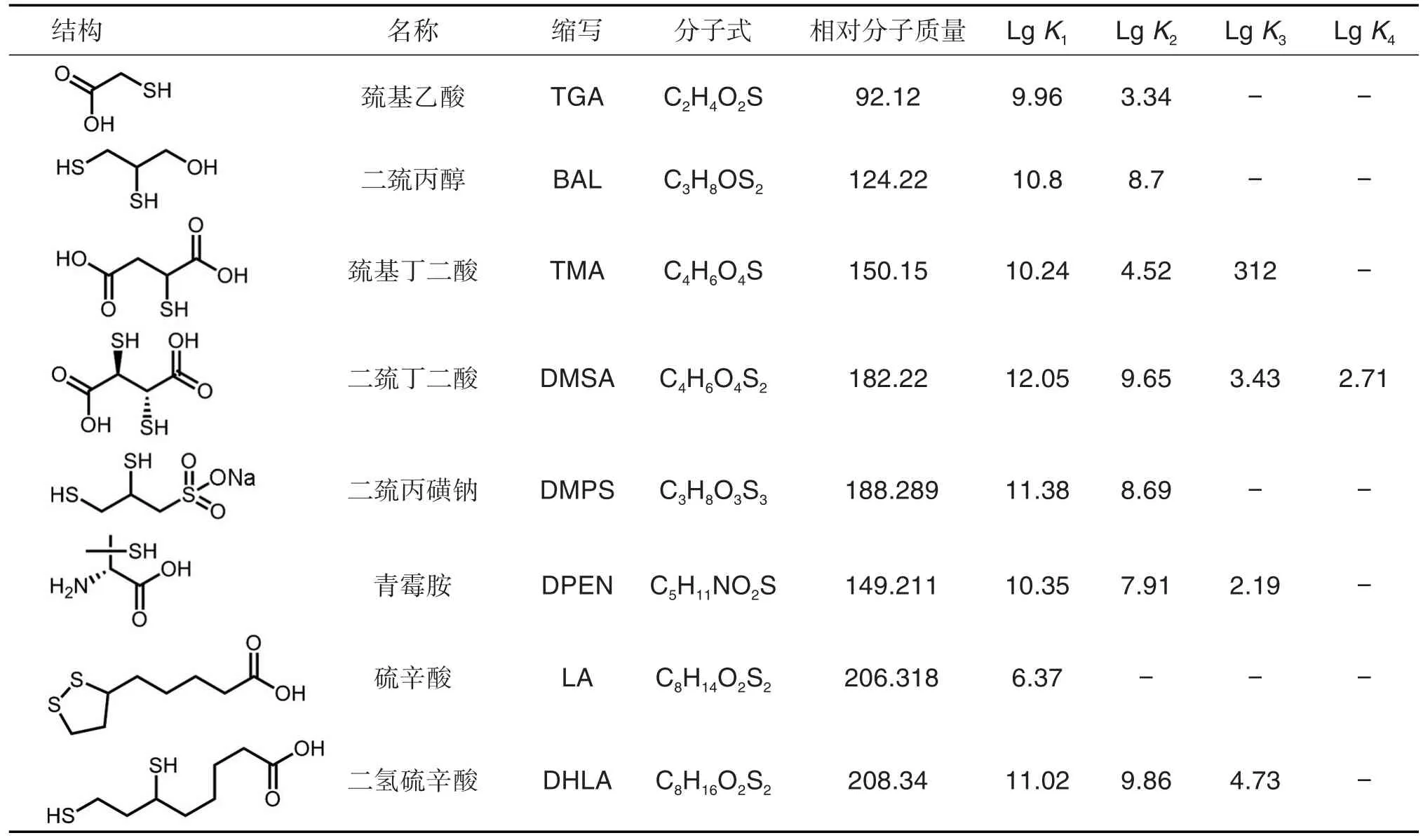
表1 巯基螯合剂的化学特征
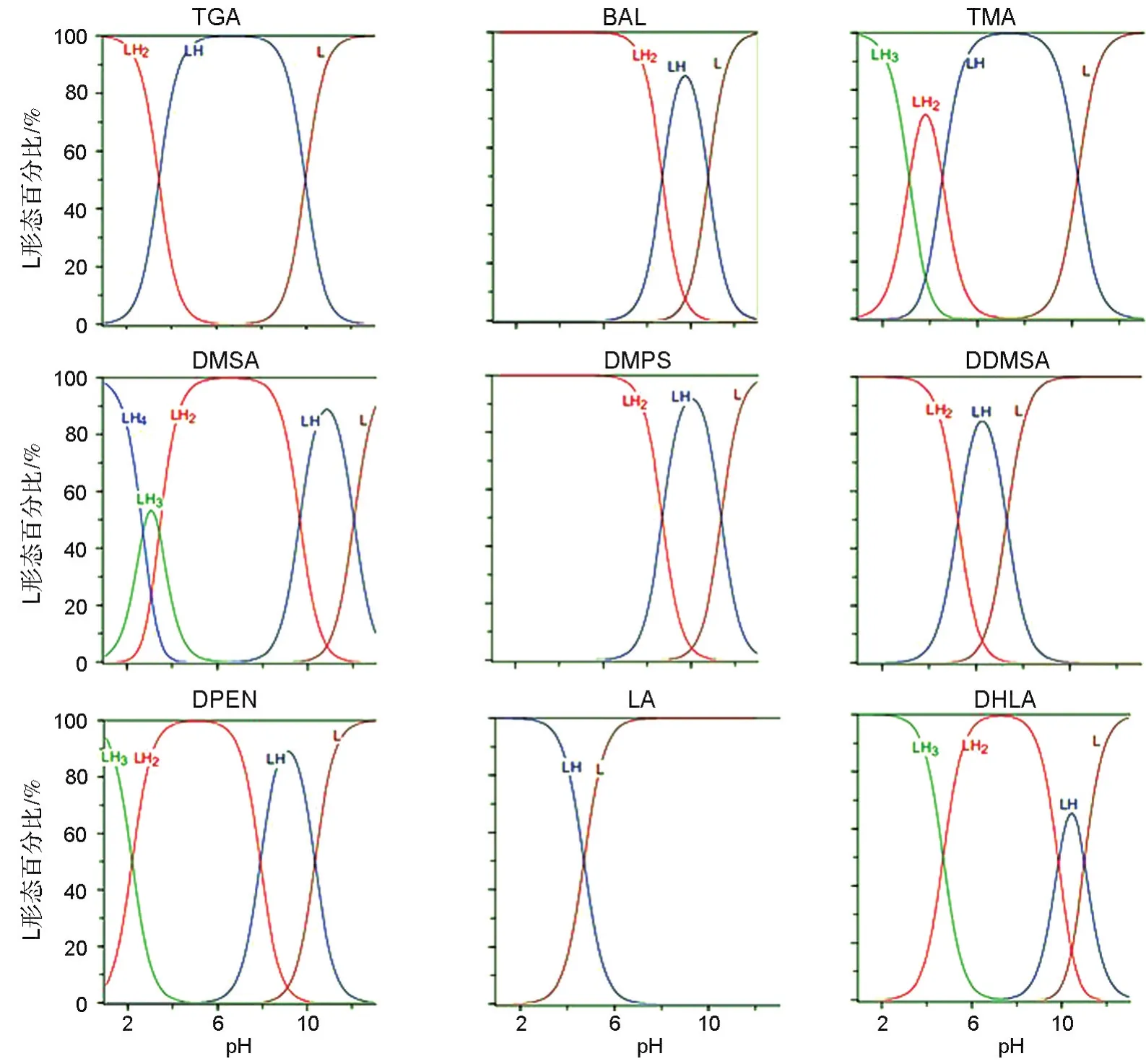
图1 巯基螯合剂在不同pH下的形态百分比.DDMSA:二甲二巯丁二酸.
由表1可看出,各巯基螯合剂巯基数目和相对位置不同,所含羧基、羟基的数目和相对位置也有所不同,使得各分子间所产生的范德华力不同。再者,对于结构相似的有机分子,相对分子质量越大,范德华力越大。综合来说,各巯基螯合剂的范德华力有很大差异,导致其质子化常数差异显著。由图1可知,巯基螯合剂在不同pH条件下的形态占比不同,表明在不同pH条件下,其会先后失去不同类别和数量的质子,表现不同的性质。
2.2 巯基螯合剂与重金属离子的络合反应
各重金属离子与同一类型螯合剂的络合反应相似,但不同类型的螯合剂因其所产生的范德华力不同其络合反应的相互结合能力也会不同。对于汞配合物,据Lenz等[13]研究,除Hg-TMA配合物的pM值为8.24外,其他Hg配合物不论分子中巯基数量多少,其pM值均非常高。然而,对于其他重金属配合物,含有2个巯基配体配合物的pM值均高于只含1个巯基配体的配合物。
在DMSA与Hg2+络合的电位平衡研究中,2个巯基参与了反应。Morales等[14]提出DMSA与Hg2+存在1∶1复合体。6年后,Avdeef等[15]在此基础上提出两者以1∶1比例配合形成的稳定配合物结构(图2)。
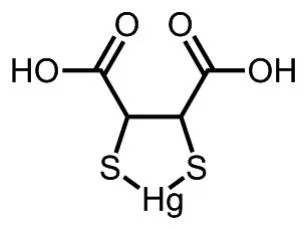
图2 DMSA-Hg配合物(1∶1)的结构式.
2004年,George等[16]利用X射线吸收光谱和密度泛函理论研究了Hg2+与DMSA或DMPS的络合。二者主要形成1∶1的配合物,也存在部分比例为1∶4形式。与Avdeef等[15]的报道相反,George等[16]指出,由于DMSA或DMPS分子中2个硫原子之间的距离不允许S-Hg-S键的线性调节,1个螯合剂分子上的2个巯基不能结合在共同的Hg上,并提出DMSA或DMPS与Hg2+络合的近线性结构(图3)。
Chekmeneva等[17]采用微分脉冲伏安法(dif-fertial pulse voltammetry,DPV)和电喷雾电离质谱(electrospray inoization mass spectrometry,ESIMS)技术研究了DMSA,DMPS和DPEN与Hg2+的结合。首先通过伏安滴定法获得络合方案的结果,形成的主要配合物为Hg(DPEN)2,Hg2(DMSA)2和Hg(DMPS)2。之后,通过DPV及ESI-MS技术证实了这些络合物的存在。
Chekmeneva 等[18]还报道了 Hg2+与 DHLA 的线性配位,通过DPV技术研究二者1∶1和1∶2配合物的形成,并通过ESI-MS技术为它们的络合给出了充分证据。由于2个巯基间距短,只有存在几个配体基团时才能为每个Hg2+提供具有2个巯基基团的稳定线性构象。图4为由2个DHLA、1个Hg2+和2个苯基汞基团形成的配合物结构图,呈现出类似的线性结合配位模式[19]。
其他重金属巯基配合物呈现的特点与Hg2+相似,含有单个巯基配体和2个邻巯基配体,其pPb值具有显著差异;可能是由于氨基或羧基存在的结果。Gale等[20]介绍了用循环伏安法和DPV技术研究DMSA和DMPS络合铅的方法,将多元曲线分辨率应用于伏安法生成配合物的化学计量和稳定性常数。
3 巯基螯合剂的临床应用
最早应用的巯基螯合剂是BAL,主要用于治疗汞或砷中毒,但由于其不良反应较大,逐渐被DMSA和DMPS取代。特别是DMSA为口服剂型,便于服用,得到了较快的普及。DPEN可与体内的铜形成无毒复合物,也可诱导肝细胞合成金属硫蛋白,促进排铜。2,3-二巯丁二酸咪唑啉异戊酯(2,3-dimercaptosuccinate imidazoline iso-amylester,MiADMSA)目前正在开发中,未来可作为潜在的解毒剂。对于不同的重金属中毒,需要选择不同种类的巯基螯合剂进行治疗,必要时可考虑将螯合剂进行联合用药,以快速高效达到解毒效果。
3.1 二巯丙醇
BAL主要用于含砷或汞毒物的解毒。BAL与路易斯气反应,可生成稳定、无毒的砷化合物,常被称为英国抗路易斯气剂[21]。此外,BAL也可与其他有毒金属形成稳定的配合物。二战后的几十年里,人们一直使用BAL用于无机汞、砷、锑、金和铋等重金属的解毒[22]。大剂量BAL可导致严重的不良反应,如小动脉收缩、血压升高、头痛、视力模糊和手麻等反应。由于高毒性,BAL目前仅在危及生命或急性砷中毒时使用几天。BAL的安全治疗窗小,且会将有毒元素重新分布到大脑,一般情况下会被DMSA或DMPS取代[23]。
3.2 二巯丁二酸
DMSA分子中含有2个巯基,1个可结合在白蛋白的半胱氨酸残基上,另1个可夺取已与组织中酶系统结合的金属离子,形成稳定的水溶性螯合物由尿排出,使含有巯基的酶恢复活性,解除重金属引起的中毒。DMSA可特异性地与铅结合,减少铅在胃肠道的吸收和滞留,降低血铅浓度,但短时间用药后,易使铅从骨中游离出来重新分布,引起血铅反跳性升高[24],故应视情况多疗程用药。DMSA也可与汞、铬和砷等形成螯合物。DMSA安全有效,是有机汞中毒的首选解毒药物,可通过改变甲基汞在大脑与血液中分布间接减轻其在大脑的聚积[16]。与其他二硫醇解毒剂相比,DMSA毒性较小,几乎无人体必要的金属元素丢失。由于DMSA为口服剂型,在重金属中毒解毒治疗中得到较快普及。
3.3 二巯丙磺钠
DMPS对汞中毒解毒效力较BAL好,毒性也较低,对砷、铬、铋、铜和锑等中毒亦有效,许多研究证明其可有效螯合有毒金属。DMPS被认为是无机汞中毒的最佳解毒剂。对于铅和有机汞中毒,其解毒效力低于DMSA,但DMPS比DMSA能更有效地去除肾中的汞。DMPS的使用常伴随机体中锌和铜的部分流失,因此建议在治疗前后监测这些微量元素[25]。DMPS也伴随一定的不良反应,如恶心、心动过速、头晕等,但很快可消失。
3.4 青霉胺
DPEN是青霉素的代谢产物,能络合汞、铅、砷、铜、铁等重金属。DPEN驱铅作用不及EDTA,驱汞作用不如BAL;但其可口服,不良反应少,可供轻度重金属中毒或对其他螯合剂有禁忌时选用。本药口服后约57%经胃肠道吸收,分布至全身各处,但主要分布在血浆和皮肤。DPEN主要在肝代谢,服药24 h内由尿排出80%的二硫化物,粪便排出20%[26]。DPEN也有一定的不良反应,与给药剂量有关,发生率较高且较为严重。最初的不良反应多为胃肠道功能紊乱和味觉减退。长期大剂量服用,会导致皮肤胶原和弹性蛋白受损,有时出现穿孔性组织瘤。但大多数不良反应可在停药后自行缓解和消失。
3.5 硫辛酸和二氢硫辛酸
早期LA被当作重金属中毒的解毒剂使用,现也被用于治疗糖尿病性神经病变。LA进入人体后易被还原成DHLA。DHLA含有1对硫醇基团,其R-对映体是解毒治疗的活性形式。LA或DHLA无论在细胞内或细胞外均能发挥其药理作用,促进维生素C和E的再生,发挥抗氧化作用。DHLA对汞有很高的亲和力,被认为是一种有效的汞解毒剂[27]。
3.6 2,3-二巯丁二酸咪唑啉异戊酯
与DMSA和DMPS相比,MiADMSA可有效去除机体中的镉,比DMSA更有效地减轻亚慢性和急性砷中毒的负担[28]。当与N-乙酰半胱氨酸一起使用时,可显著减少螯合治疗中的氧化应激。
3.7 联合用药
巯基螯合剂对重金属中毒的解毒疗效非常显著,是目前临床上的主要解毒剂。但目前常是各解毒剂单独使用,往往需要患者大量、多次服药,为患者及医护人员带来极大不便。故本文提出联合用药的方式,对不同重金属中毒,可选择将≥2个螯合剂一起服用或先后服用,以快速、安全、高效地达到解毒效果,提高患者用药顺应性。研究表明,DMSA与莫能菌素(monensin)联合使用,比单独使用DMSA更有效,特别是在去除沉积在大脑中的铅方面。在与DMSA联合用药时,离子载体莫能菌素对铅离子(Pb2+)在磷脂膜上的转运具有较高的活性和选择性,可显著加速Pb2+与胞外DMSA的螯合,增加铅在大脑、心脏、肝和肾中的去除量[29]。莫能菌素通过将Pb2+和OH-与外部Na+交换而促进胞内铅向胞外转运,加速胞内铅与DMSA的螯合,从而提高其有效性。在此过程中,莫能菌素作为DMSA的载体存在[30],二者相辅相成,快速高效地起到解毒效果。此外,MiADMSA和DMSA的联用比其单用对促进镉清除更有效。汞蒸气中毒时,建议DMPS与BAL联合用药。根据DMPS与BAL的化学结构可知,二者联合用药时,巯基数量增多,易使更多的中毒重金属离子同时被螯合,并形成稳定的线性配合物;DMPS中的磺酸基与BAL中的羟基可形成氢键,也会使配合物的结构更稳定。根据巯基解毒剂的安全性可知,BAL安全治疗窗小,毒性大,但对汞中毒解毒效力更佳;而DMPS毒性较小,且不良反应可自行消失。总之,DMPS与BAL联合用药比二者单用解毒效果更好。对最新联合用药配对以应对不同重金属中毒总结见表2。

表2 重金属中毒的联合用药
4 结语
针对重金属中毒的快速高效解毒一直为临床所关注。目前上市的各种含巯基解毒剂在临床上均为单用,往往会产生一定的毒性,对患者造成严重的不良反应。然而,在充分考虑各巯基螯合剂理化性质和实验研究基础上,采用联合用药的方式来应对不同的重金属中毒,可安全、快速、高效达到解毒效果。也就是说,可通过使用相同解毒功效的其他解毒剂作以辅助,以减少主药用量,从而降低主药的毒性和不良反应。也可采用其他类型的非巯基螯合剂辅助治疗,使各螯合剂间相互作用产生范德华力,并与重金属离子形成线性稳定结构,进而相互促进各自的解毒功效,使解毒更高效、更安全。DMPS与BAL联合用药治疗无机汞盐和汞蒸气中毒及DMSA与MiADMSA联合用药治疗镉中毒等新颖的螯合剂联合用药方式均具有较好的解毒效果。当然,通过临床深入应用和研究,应还能发现更多、更理想的联合用药配方和用药方式用于重金属中毒的高效救治。

