牙源性始基瘤1例
唐月阳 万梓欣 姚莉洪 吴兰雁 何志秀 汤亚玲
口腔疾病研究国家重点实验室 国家口腔疾病临床医学研究中心四川大学华西口腔医院病理科,成都 610041
牙源性始基瘤(primordial odontogenic tumour,POT)是世界卫生组织2017年头颈部肿瘤分类中新描述的一种罕见良性牙源性肿瘤[1]。此型肿瘤少见,目前国外文献报道18 例,国内报道5 例[2-4]。以儿童及青少年常见,无性别差异,好发生于下颌骨内,临床表现为无痛性肿块。本文报道1例牙源性始基瘤,并结合文献探讨其临床病理表现及治疗原则,以增强对该疾病的认识,提高诊断和治疗水平。
1 病例报道
1.1 病例资料
患者,男,11 岁,2020年12月以“右下颌包块”为主诉就诊。
专科检查:患者面形不对称,右颊部膨隆,张口度开口型正常。口内可见右下颌颊侧膨隆,可触及质硬包块,偏向颊侧,前至43 牙,后至右下颌升支,口外可触及包块偏向颊舌侧,无触痛。双侧颌下及颈部未触及明显增大淋巴结。
口腔颌面锥形束CT(cone beam CT,CBCT)示:右下颌46 牙区及其远中颌骨内见类圆形囊腔样病变,与正常边界清晰,边缘光滑,颌骨膨隆明显,46 牙远中牙槽突侧骨质不连续,47 牙移位至囊腔远中下份,牙冠缺损,囊腔中心见不规则钙化团片、有包膜,右下颌神经管受推挤移位。影像诊断:右下颌骨良性占位(成釉细胞纤维牙瘤?),请病理明确诊断(图1)。

图1 术前CBCTFig 1 Preoperative CBCT
完善术前检查后,对患者行右下颌骨病灶刮治术。
1.2 病理检查
病灶刮治术后送检组织经10%甲醛充分固定,脱水后石蜡包埋切片(约4 μm 厚),经常规苏木精-伊红(hematoxylin-eosin staining,HE)染色和SP法免疫组织化学染色后,光学显微镜下观察。
1.2.1 大体检查 带部分颌骨的包块一个,大小4.5 cm×4 cm×3 cm,周围可见牙齿1 枚,有包膜,包膜易剥脱,有囊性腔隙,包块表面凹凸不平,周围有许多淡黄色颗粒,切面灰白灰黄、质韧、分叶状,中央发白有光泽(图2)。

图2 大体形态Fig 2 Gross morphology
1.2.2 镜下表现 镜下肿瘤部分被纤维包膜包裹。由间充质纤维黏液样组织组成,内含大量梭形和星形细胞,类似于牙乳头,周围被类似于成釉器的内釉上皮所包围,呈立方到柱状伴核极性倒置,部分区域可观察到细胞呈星网状层样分化,上皮细胞常局灶性内陷入间质中,可见到上皮岛成分。上皮下间质细胞聚集增多。肿瘤内未见成牙本质细胞分化、无牙体硬组织形成,间质中存在小钙化灶,钙化为圆形小硬块,呈球形、同心圆状(图3)。
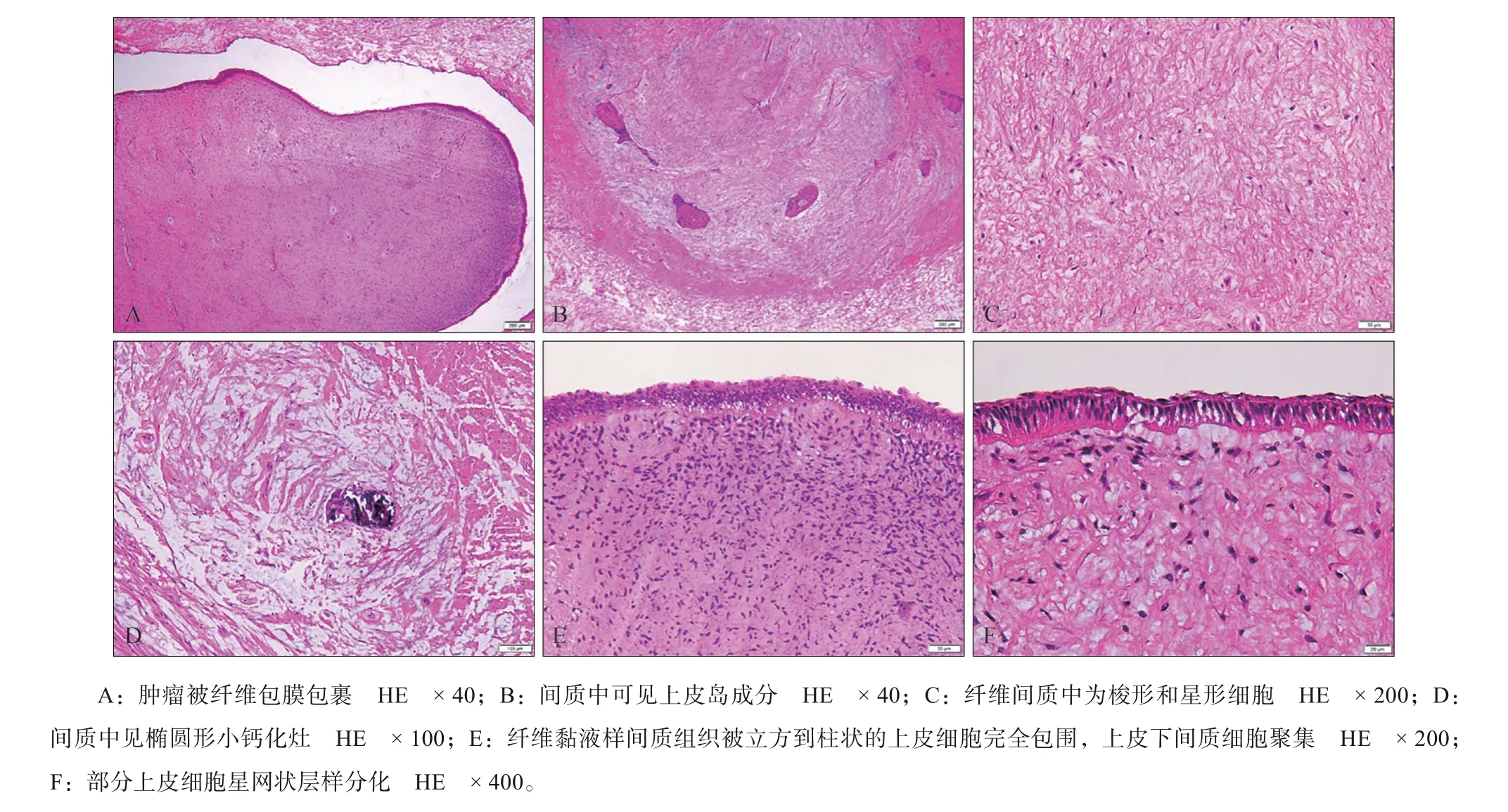
图3 牙源性始基瘤的组织学特征Fig 3 Histological features of primordial odontogenic tumour
1.2.3 免疫组织化学染色 肿瘤上皮成分广谱细胞角蛋白(pan cytokeratin,PCK)、CK14、CK19 及P63 均阳性(图4),间质细胞波形蛋白(Vimentin)阳性。S100、平滑肌肌动蛋白(smooth muscle actin,SMA)阴性。肿瘤组织Ki-67 的增殖指数<1%。
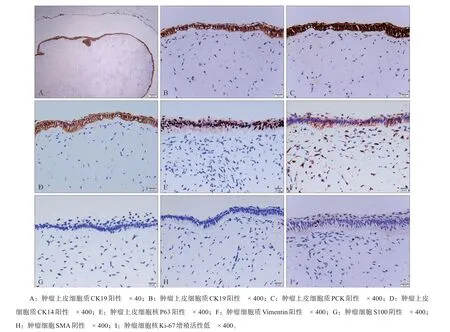
图4 免疫组织化学染色Fig 4 Immunohistochemical results
1.3 预后
术后随访3个月无复发。
2 讨论
2014年,牙源性始基瘤首次由Mosqueda-Taylor 等[5]报道,这是一种罕见的良性牙源性肿瘤。2017年世界卫生组织第4 版头颈部肿瘤分类中列入新型的混合型上皮间质牙源性肿瘤[1]。据文献[6]报道,牙源性始基瘤患者普遍年轻,年龄2~19岁,平均11.6 岁,无性别差异,通常为单发,最常见于下颌骨内。因为其镜下特征类似于正常牙胚中的组织,特别是在帽状到钟状晚期,所以有学者[7]称其病变起源于牙齿发育的早期,但具体的发病机制尚不完全清楚。
牙源性始基瘤患者早期常无明显的症状,通常在拍片时偶然发现,但随着病变逐步发展,可导致患者面形不对称,颌骨膨隆。影像学上常包含一颗未萌出牙,环绕牙冠形成境界清楚的放射影,类似含牙囊肿,其内可见散在高密度影,骨皮质膨隆、变薄或穿孔,相邻牙移位和牙根吸收[8]。有些病例是包裹未萌出牙的根部而不是牙冠[6]。本例影像主要表现是右下颌骨内见类圆形囊腔样病变,与正常边界清晰,边缘光滑,颌骨膨隆明显,46 牙远中牙槽突侧骨质不连续,47 牙移位至囊腔远中下份,牙冠缺损,囊腔中心见不规则钙化团片,有包膜,与之前文献报道基本一致,包含一颗牙。
从大体标本上看,牙源性始基瘤是一个实性的、多分叶的白色和光滑的肿块,有或无囊腔,肿瘤被包膜包围,与周围的组织分界清楚[9]。镜下,肿瘤由间充质纤维黏液组织组成,细胞密度不均匀,呈梭形和星形,多数情况下与牙乳头相似,周围环绕着类似于内釉上皮的立方到柱状上皮,可见基底细胞呈星网状,上皮下间质细胞聚集增多。肿瘤周围上皮可凹陷入间质成分内,导致因切面不同而出现成釉细胞纤维瘤样岛屿。肿瘤被一层薄薄的纤维包膜包裹具有一定的诊断意义。肿瘤中一般无牙齿硬组织,文献[10]中描述了上皮组织中存在小的钙化灶,特别是星网状区。然而,到目前为止,还没有证据表明这些上皮细胞可以分化或诱导牙齿硬组织沉积,上皮内钙化是圆形的硬组织团块,呈球状或同心圆状[11]。本例镜下特点符合牙源性始基瘤组织学表现。
本例病例免疫组织化学染色显示:肿瘤上皮成分PCK、CK14、CK19及P63均阳性,间质细胞Vimentin 阳性,S100、SMA 阴性,肿瘤组织Ki-67的增殖指数<1%。Bologna-Molina 等[10]研究表明,牙源性始基瘤肿瘤上皮成分中CK14、CK19、成釉蛋白和牙本质唾液磷蛋白(dentin salivary phosphoprotein,DSPP)均呈一致阳性,而其他标记物,如Vimentin、半乳糖凝集素3(galectin-3)、p53、Bcl-2 和PTEN 也有不同程度的局部表达。Sun 等[12]报道,POT 的间质组织Vimentin、细胞周期蛋白D1(Cyclin D1)、Bcl-2、和p53 呈强阳性表达,S100、SMA 及CD56 阴性。CK19 通常在牙源性囊肿和肿瘤的上皮细胞中呈阳性表达,特别是在前成釉细胞和分泌性成釉细胞中,在既往和目前的POT 病例中,CK19在立方和柱状上皮细胞中呈强阳性,表明这些衬里上皮有不同程度的成熟分化,肿瘤可能起源于釉质器官的原始细胞成分[7,12]。Ki-67 检测细胞增殖指数<5%,说明细胞增殖活性不高,POT 为生长缓慢的良性肿瘤,其细胞增殖可能不是肿瘤生长和扩张的主要机制[10]。然而,Bologna-Molina 等[13]研究表明,浓缩的上皮下层区域表现出更高的血管化,葡萄糖转运蛋白(glucose transporter 1,GLUT-1)和抗凋亡标志物的阳性,表明代谢、抗凋亡和血管生成是参与肿瘤生长的主要因素。分子遗传学方面,已经通过下一代测序在POT 中分析了151 个与癌症相关的基因和42 个与成牙相关的基因,并且未检测到突变[10]。研究[14]还发现了Amelx、Ambn和Enam的釉质蛋白编码基因以及Col1a1、Dspp、Nes 和Dmp1的牙本质蛋白编码基因的表达。然而,与牙本质发生相关的基因Bglap、Ibsp 和Nfic 的表达为阴性或非常弱,这可能是由于表观遗传沉默机制所致,表明成牙本质细胞分化后POT 中牙本质形成受到抑制,这提示POT 中釉质和牙本质形成的抑制是由于牙本质形成过程中的缺陷引起的[14]。
在病理组织学上,牙源性始基瘤的主要鉴别诊断包括成釉细胞纤维瘤、中央型牙源性纤维瘤、牙源性黏液瘤和增生性牙囊。1)成釉细胞纤维瘤是由牙源性上皮和类似于牙乳头的牙源性间充质所组成,不含牙体硬组织的良性肿瘤[15]。上皮细胞的形态类似于成釉细胞,可排列成条索状、小梁状、岛状,间质成分呈黏液状,可见幼稚纤维结缔组织聚集并形成少量的胶原纤维。POT 包含少量的条索状上皮或巢,类似于成釉细胞纤维瘤。但是,POT 的上皮条索或巢仅存在于肿瘤周围附近。成釉细胞纤维瘤的间质成分细胞更多,成釉细胞上皮成分更明显,而在POT 间质主体中少见成釉细胞上皮岛。2)中央型牙源性纤维瘤是一种罕见的牙源性良性肿瘤,多发生于上下颌,镜下由成纤维细胞基质之间的牙源性上皮细胞巢组成[16]。在中央型牙源性纤维瘤松散成熟的纤维结缔组织内,存在数量不等上皮岛和上皮条索。与POT 相比,其缺乏牙源性上皮的外部覆盖。3)牙源性黏液瘤又称黏液瘤或黏液纤维瘤,是一种良性但存在局部浸润生长特征的牙源性间充质来源肿瘤[17]。镜下肿瘤边界不清,见大量蓝色黏液基质,其中可见少量上皮剩余条索,瘤细胞呈星形或梭形疏松排列,核分裂象罕见。由于肿瘤周围无包膜,因此往往具有很强的侵袭性,会渗入邻近的颌骨内,并且牙源性黏液瘤周围无类似于POT 的内釉上皮覆盖。4)增生性牙囊在组织学上与POT 相似,在纤细且致密的胶原纤维结缔组织中表现出程度不同的黏液样区域,并且通常包含小的牙源性上皮巢;但POT 中的致密胶原和黏液基质主要由肥大的梭形和星形细胞增殖形成。增生性牙囊的内表面还可衬有退化的釉质上皮,呈薄层状鳞状上皮,有时表面有立方状或柱状细胞[11,18]。
迄今为止,所有报道的POT 病例均已通过外科手术摘除,随访3个月~20年均未复发[19]。因此,牙源性始基瘤的治疗方式仍是完整手术切除,应避免不必要的大范围手术。POT 的临床过程缓慢,口腔放射科医生、外科医生和病理医生应该根据其独特的放射与组织学表现形式,诊断这种罕见肿瘤,以避免误诊和不适当的治疗。
利益冲突声明:作者声明本文无利益冲突。

