双渣转炉炼钢低碱度脱磷工艺实验研究



摘 要:对1 350 ℃下的转炉炼钢新工艺低碱度渣对铁水的脱磷效果进行了研究。当脱磷时间为20 min时,脱磷率达到最高值84.3%。脱磷时间分别为4、8 min时,脱磷渣的主要物相为黑色富磷相和白色富铁相;脱磷时间分别为12、16和20 min时,主要物相为富磷相、富铁相和基体相;脱磷时间为24 min时,主要相为富铁相、基质相和含镁铝尖晶石相,但不含富磷相。随脱磷时间的延长,渣中富铁相的面积不断减小,基体相的面积不断增加。
关键词:双闸转炉;脱磷;低碱度
中图分类号:TF713 文献标识码:A 文章编号:1001-5922(2022)05-0009-05
Experimental research on low-alkalinity dephosphorization process of double slag converter steelmaking
Abstract: Through experimental research, we studied the dephosphorization effect of low-alkalinity slag on molten iron at 1 350 ℃.When the dephosphorization time is 20 min, the dephosphorization rate reaches the highest value of 84.3%. When the dephosphorization time is 4 and 8 min, the main phases of the dephosphorization slag are black phosphorus-rich phase and white Fe-rich phase. When the dephosphorization time is 12, 16 and 20 min, the main phases are P-rich phase, Fe-rich phase and matrix phase. When the dephosphorization time is 24 min, the main phases are Fe-rich phase, matrix phase and magnesium-aluminum spinel phase, but no phosphorus-rich phase. With the extension of the dephosphorization time, the area fraction of the iron-rich phase in the slag keeps decreasing, and the area fraction of the matrix phase keeps increasing.
Key words: double-switch converter;dephosphorization;low alkalinity
磷在鋼材中是一种杂质元素,磷含量过高会对钢的焊接性能产生不利影响,并会显著降低钢的低温冲击韧性。一般来说,一级钢的磷质量分数不能超过0.02%。钢材脱磷主要采用加入石灰石的方式进行,然而,也带来了冶炼成本的升高,并且脱磷效率不高。因此,钢材脱磷过程中如何降低转炉石灰消耗和渣量已成为人们非常感兴趣的研究课题。双渣转炉炼钢工艺(NDSP)的脱磷工艺分2步进行,首先在转炉内进行脱硅和脱磷操作,然后用倾斜炉浇注脱磷渣。近年来,人们对双渣转炉炼钢工艺(NDSP)的脱磷工艺展开了大量的研究,取得了丰硕的成果,如在转炉冶炼过程中,对脱磷反应的重要热力学和动力学方面进行了研究,结果发现:转炉渣在长时间的吹炼过程中以及在大多数情况下吹炼结束时都是非均质的,炉渣中固相的形成,特别是溶解磷的C2S-C3P相,是成功模拟和控制脱磷的关键[1]。在此基础上发展了一种新的热力学模拟方法,用于模拟转炉全吹炼周期内非均质渣铁液之间的磷分布,并将其纳入动力学脱磷模型中,非均相渣中磷的分布不仅与温度有关,而且还与固相数量和液态渣相的碱度有关。通过工业实践和理论计算,对精炼过程中碳、硅的氧化和脱磷优化进行了研究。结果表明,第一造渣阶段钢液中硅的最佳残留量为0.05%~0.07%。当温度为1 340~1 360 ℃时,除渣时钢液中的磷含量可控制在较低水平(0.055%~0.060%),除渣时的渣碱度应控制在1.5左右;FeO含量应控制在15%以内,碱度应高于3.4,温度应低于1 640 ℃[2]。有研究低温、低碱度双渣转炉炼钢过程中脱磷终点温度对铁水脱磷的影响,在温度1 350~1 450 ℃内,随着脱磷终点温度的升高,脱磷率和磷分配率先升高后降低,在脱磷温度1 385~1 410 ℃内,脱磷率大于55%,脱磷渣中P2O5含量为3.74%~4.25%。铁水中磷进入脱磷渣富磷相的路径可以合理推断为:铁水→富铁相→富磷相。考虑双渣脱磷工艺工业试验的实验结果和热力学计算结果,中间除渣的最佳温度约为1 400~1 420 ℃[3]。
有研究表明,脱磷渣中的 C2S和NC2SiO4-Ca3(PO4) 2颗粒都有利于铁水的脱磷。C2S能与液相渣中的Ca3(PO4)2(C3P)迅速结合形成富磷相,导致液相渣中P2O5活性降低,促进铁水中的磷被氧化并进入液相渣中,从而提高脱磷效率[4-5]。如前所述,之前关于低温1 350 ℃和低碱度下NDSP铁水脱磷时间变化和脱磷渣成分的研究较少。因此,研究铁水脱磷过程中炉渣的脱磷、形态和物相的变化是十分必要的。
1 实验部分
1.1 实验方法
本文采用2种方法研究铁水脱磷行为随时间的变化。方法1:在每次脱磷实验中控制不同的反应时间。该方法的优点是每次试验中的脱磷渣量足以进行后续的成分分析和相表征,但很难完全保证初始铁水成分的一致性。方法2:在同一实验中,在不同反应时间取样。其优点是初始铁水的成分完全一致,但是在铁水取样过程中,会有少量熔渣粘附在硅管上,导致熔渣量减少。此外,每次很难确定这些炉渣的数量,这将影响后续脱磷过程中熔渣与铁水的比例。由于每次试验仅使用400 g铁水和40 g矿渣。因此,脱磷过程中很难采集矿渣样品,并对矿渣样品进行分析和表征。因此,第1种方法用于研究脱磷渣的矿物学形态和相组成以及脱磷效率随时间的变化;第2种方法主要用于验证铁水脱磷的实验结果,仅取铁水样品,以减少熔渣量损失对脱磷的影响。
方法1:将大约400 g生铁放入氧化铝坩埚中,并加热至1 350 ℃。然后,用小硅管通过抽吸方式获取初始铁水样品。之后,立即添加25 g脱碳渣和35 g Fe2O3的混合物。通过理论计算,脱磷后最终渣的碱度(CaO/SiO2)约为1.5。当脱磷反应时间为4、8、12、16、20和24 min时,从熔炉中取出坩埚并立即在水中淬火。
方法2:生铁质量为500 g。脱碳渣和Fe2O3的量分别调整为30 g和42 g。当反应时间为4、8、12、16、20和24 min时,分别从坩埚中取出铁水样品。最后,从熔炉中取出坩埚,并在反应时间达到24 min时在水中淬火。
1.2 分析方法
在原子发射光谱分析的基础上,使用直读光谱仪分析铁水的成分。分析前,使用类似成分的标准样品校准光谱仪。采用玻璃熔丝技术,用X射线荧光(XRF)分析了熔渣样品的成分。利用扫描电子显微镜(SEM)矿渣的矿物学形态和相组成进行了表征。
2 结果与讨论
2.1 铁水含量随脱磷时间的变化
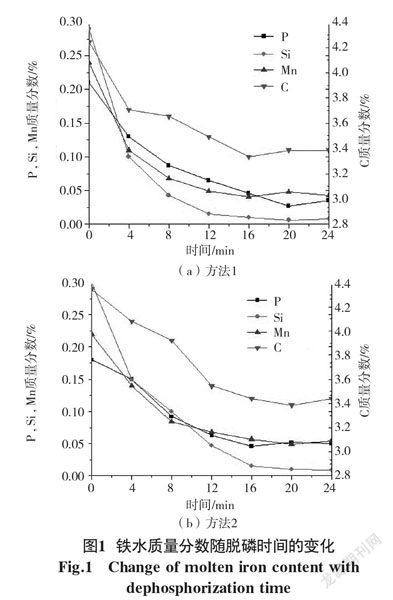
图1(a)和图1(b)分别显示了第1种方法和第2种方法中铁水中C、Si、Mn和P含量随脱磷时间的变化。可以看出,在这2种方法中,铁水中的元素含量随着脱磷时间的增加而降低。当脱磷时间超过16 min时,C、Si和Mn的含量基本保持不变,在相同脱磷时间下,第1种方法的铁水中元素含量略低于第2种方法。这是因为在第2种方法中,部分熔渣粘附在取样过程中要取出的取样管上,从而减少了后續反应中的熔渣量。结果表明,第2种方法的铁水中元素含量高于第1种方法。
在图1(a)中,当脱磷时间为15 min时,铁水中的P含量达到最低值。随着反应时间进一步增加到18 min,铁水中的P含量略微增加,这是由于液相熔渣中P含量的增加和氧化铝坩埚的溶解引起的再磷化。结合图1(a)、(b)可以确定,当反应时间达到15 min左右时,脱磷反应将达到准平衡状态。
2.2 铁水中元素去除率随脱磷时间的变化
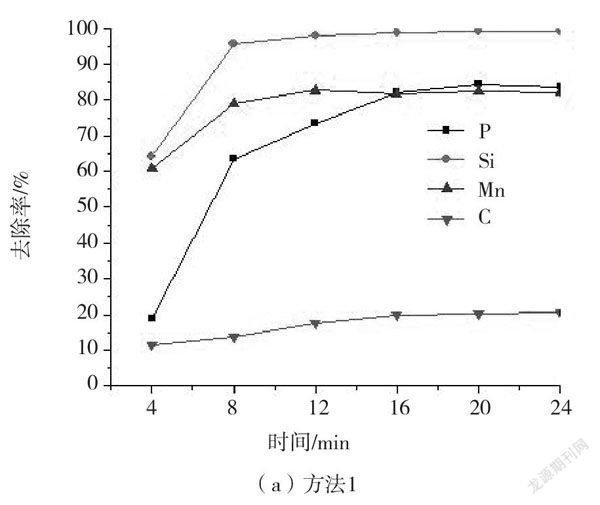
图2(a)、(b)分别显示了方法1和方法2中铁水中C、Si、Mn和P的去除率随脱磷时间的变化。
在图2(a)中,当脱磷时间超过9 min以后,铁水中Si和Mn的去除率基本接近最高值,P和C的去除率继续增加。当脱磷时间为15 min时,脱磷率达84.3%。当脱磷超过18 min以后,由于液相炉渣中磷含量的增加和氧化铝坩埚的溶解,导致脱磷率略有下降,出现再磷化现象。可以看出铁水中Si的去除率最大,其次是Mn、P和C。
2.3 炉渣中氧化物含量随脱磷时间的变化
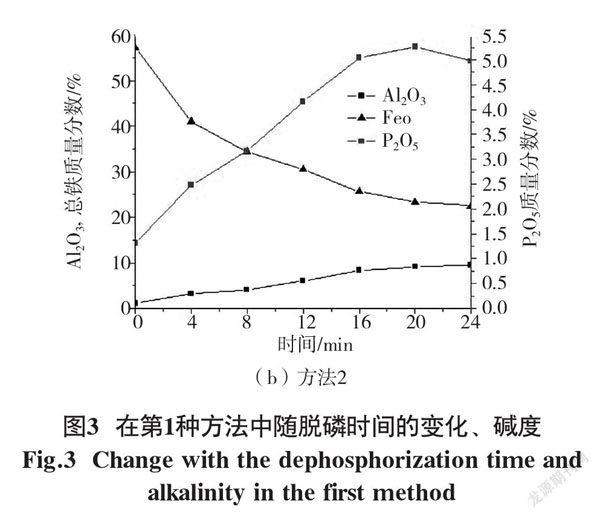
图3(a)显示了CaO和SiO2含量以及炉渣碱度随脱磷时间的变化。
由图3(a)可知,0 min对应的值是脱碳渣和Fe2O3粉末混合物中氧化物的含量。随着反应时间的延长,炉渣中CaO和SiO2的含量先增加后基本保持不变。碱度先降低后基本保持不变。随着反应时间的增加,铁水中各种元素氧化所消耗的炉渣中的FeO量逐渐增加,尤其是在C和FeO之间的反应中,熔渣中没有形成新的氧化物。因此,炉渣中FeO的含量不断减少,导致炉渣中CaO和SiO2的含量逐渐增加。当反应时间为16 min时,铁水中各元素与炉渣中FeO之间的反应基本结束,如图2(a)所示,因此炉渣中CaO和SiO2含量的变化非常小。
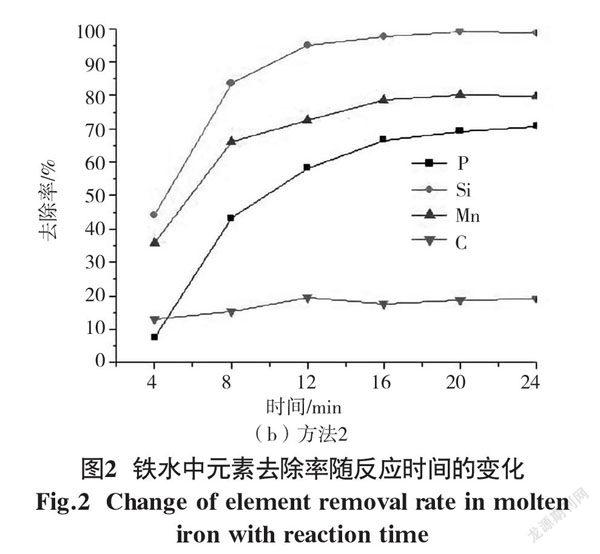
由于炉渣中CaO总量保持不变,碱度的变化主要取决于炉渣中SiO2含量的差异。随着反应时间的延长,铁水中硅氧化形成的炉渣中二氧化硅的含量逐渐增加。根据图2(a)中的结果,当反应时间大于9 min时,炉渣中SiO2的增加量变小。结果表明,随着反应时间的延长,炉渣碱度先降低后保持不变。这主要是由于初始铁水中硅含量偶尔波动所致。图3(b)显示了炉渣中P2O5、Al2O3和总Fe含量随脱磷时间的变化。随着反应时间的增加,炉渣中Al2O3含量增加,P2O5含量先增加后略有下降,铁粉含量先降低后基本保持不变。
随着脱磷时间的增加,熔渣对氧化铝坩埚的腐蚀程度逐渐增加,导致熔渣中Al2O3含量增加,熔渣中总Fe的消耗量随着反应时间的增加而增加,相应的熔渣中总Fe含量降低。当反应接近准平衡态时,铁含量变化不大。炉渣中P2O5含量的变化与图2(a)中铁水中磷去除率的变化基本一致。不同之处在于,当反应时间为20 min时,炉渣中的P2O5含量与12 min时相比没有增加,而是减少了,即使在20 min的较高脱磷率下,炉渣中的P2O5含量也有所降低。
2.4 不同反应时间脱磷渣矿物学形态的变化
在放大200倍和1 000倍的情况下,脱磷渣在不同反应时间的SEM图像变化分别如图4和图5所示。
由图4、图5可知,当反应时间为3、6 min时,发现脱磷渣中存在两相。黑色富磷相A以nC2S-C3P固溶体的形式含有高含量的P2O5以及少量溶解的FeO。白色富铁相B主要含有FeO、MnO和MgO。当反应时间为9、12和15 min时,脱磷渣中的主要相为富磷相A、富铁相B和基体相C。基体相C为液相,主要含有CaO、SiO2、Al2O3、FeO、MnO和MgO,富磷相A的磷含量远高于基质相C。当反应时间为18 min时,发现脱磷渣的主要相为富铁相B、基质相C和含有MgO和Al2O3的尖晶石相D,但不含富磷相A。
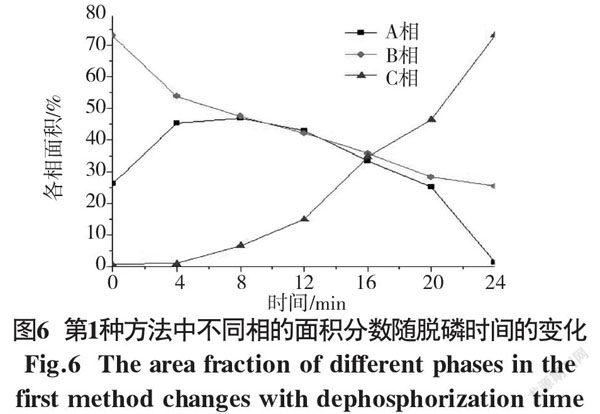
选择图4中200倍SEM图像的放大倍数来分析不同相的面积,如图6所示。
由图6可知,方法1中不同相的面积随脱磷时间的变化。随着反应时间的延长,渣中富铁相B的面积不断减小,富磷相A的面积先增大后减小直至消失,基体相C的面积增大。随着反应时间的延长,铁水中元素的去除率增加,导致渣中FeO含量降低。此外,FeO主要集中在富铁相B。因此,随着反应时间的增加,富铁相B的面积降低,对应的富铁相B中的FeO含量也降低。
随着反应时间增加到9 min,铁水中氧化成基体相C的磷含量逐渐增加。随后,P2O5与炉渣中的C2S颗粒结合形成nC2S-C3P固溶体,从而使富磷相A的面积逐渐增加。表明富磷相A面积的增加有利于脱磷。
当反应时间增加到12 min时,可以发现炉渣中富磷相A的面积减少。由于熔渣熔化和Al2O3坩埚腐蚀,熔渣中基体相C的面积增加,更多的P2O5溶解到基体相C,导致富磷相A的面积减少。随着反应时间增加到15和18 min,富磷相A的面积进一步减小并逐渐消失。这表明富磷相A将持续分解为基体相C,反应时间在低碱度炉渣中约为1.4 min。
3 结语
本文通过NDSP高温实验室试验,研究了1 350 ℃下的低碱度炉渣对铁水的脱磷以及脱磷炉渣随时间的变化规律。主要结论:
(1)研究了2种NDSP脱磷方法中铁水脱磷行为随时间的变化。第1种方法是在每次脱磷试验中控制不同的反应时间;第2种方法是同一试验中在不同的反应时间取样;
(2)随着反应时间的延长,铁水中碳、硅、锰、磷的含量降低。当反应时间为20 min时,铁水中磷含量最低,脱磷率最高,为84.3%。渣中总铁含量和碱度先降低后保持不变,P2O5含量先升高后略有降低;
(3)从渣的SEM分析结果和XRD结果来看,当脱磷时间为4和8 min时,脱磷渣的主要相为黑色富磷相和白色富铁相。当脱磷时间为12、16和20 min时,脱磷渣中的主要相为富磷相、富铁相和基体相。当反应时间为24 min时,脱磷渣的主要相为富铁相、基体相和含有MgO和Al2O3的尖晶石相,但不含富磷相;
(4)随着反应时间的延长,渣中富铁相的面积不断减小,基体相的面积不断增大。富磷相的面积先增大,然后减小,直到消失.因为富磷相在低碱度熔渣中将持续溶解为基体相。
【参考文献】
[1] KHADHRAOUI S,ODENTHAL H J,DAS S,et al.A new approach for modelling and control of dephosphorization in BOF converter[J].La metallurgia italiana,2018(11-12):5-16.
[2]DAI Yuxiang,LI Jing,SHI Chengbin, et al. Dephosphorization of high silicon hot metal based on double slag converter steelmaking technology[J].Ironmaking & Steelmaking,2021,48(4):447-456.
[3]SUN Han,YANG Jian, LU Wanshan,et al.Dephosphorization in double slag converter steelmaking process at different temperatures by industrial experiments[J].Metals,2021,11(7):1 030.
[4]XUE Yuekai,TIAN Peng,LI Chengxiao,et al.Dephosphorization mechanism and phase change in the reduction of converter slag[J]. High Temperature Materials and Processes,2021,40(1):253-264.
[5]YAN L Z, MING G, FENG S L,et al.Enrichment,Separation,and Recovery of Phosphorus from Dephosphorization Slag[J]. Archives of Metallurgy and Materials,2018,63(4).
[6]ZHAO A,ZHANG L,FU Y,et al.Study on duplex process with a single converter[J]. La Metallurgia Italiana,2020:36.
[7]LI Jiansheng,ZHAO Dingguo, LIU Hongwei,et al.Practical Research on Dephosphorization in Converter[C].International Applied Mechanics, Mechatronics Automation & System Simulation Meeting (AMMASS2012),2012.
[8]ZHAO A,ZHANG L,FU Y,et al.Study on duplex process with a single converter[J]. La Metallurgia Italiana,2020:36.
收稿日期:2021-11-02;修回日期:2022-03-08
作者簡介:郑恩文(1974-),男,高级工程师,研究方向:冶金工程。

