基于miR-34a/SIRT1 轴研究柚皮素对H2 O2 诱导的人视网膜色素上皮细胞氧化损伤的保护作用
魏抗抗 ,董伟华 ,帖红艳 ,何章彪 ,赵 琳
(1.商丘医学高等专科学校五官科教研室,河南 商丘 476006;2.郑州大学基础医学院人体解剖学教研室,郑州 450001)
年龄相关性黄斑变性(age-related macular degeneration,AMD)是一种累进性和变性性眼病,会影响视网膜的黄斑区域,是导致老年人严重和永久性视力障碍及失明的常见原因[1]。AMD 发生率较高,据估计全球范围内AMD 的人数到2040 年将增加到3 亿[2],严重影响患者的生活质量,也给经济造成沉重负担。AMD 的主要表现为视网膜色素上皮细胞(retinal pigment epithelial cells,RPE)对视细胞外节盘膜吞噬消化能力降低,导致未被完全消化的盘膜残余小体存在,形成玻璃膜疣,从而导致视力受损甚至失明[3]。虽然AMD 的发病机制尚未完全了解,但RPE 功能障碍在AMD 的进展中发挥中心作用[4-6]。
据报道,miR-34a 在调节细胞增殖、迁移、分化和凋亡中至关重要,可抑制RPE 细胞的增殖和迁移[7];miR-34a 的调节功能与年龄相关性疾病(包括AMD)中的沉默信息调节因子1(silence information regulator 1,SIRT1)有关,研究显示miR-34a 的显著上调,可导致细胞中SIRT1 表达降低,使ARPE-19细胞对氧化应激的耐受性降低[8]。氧化应激在AMD 的发展进程中起关键作用,抗氧化系统组分活性与AMD 的严重程度有关,补充抗氧化剂可以保护RPE 免受氧化应激损伤,可预防或治疗AMD[9]。柚皮素是一类黄酮类化合物,在柑橘类物种中含量丰富,具有强大的抗炎[10]和抗氧化活性[11]。研究发现柚皮素可抑制视网膜组织神经节细胞凋亡,降低糖尿病视网膜病变大鼠氧化应激损伤[12];然而,目前尚不清楚柚皮素是否可以预防AMD,且柚皮素在氧化应激诱导的RPE 损伤中的作用尚未可知。为此,本研究采用H2O2诱导人RPE 氧化损伤,初步探讨柚皮素能否通过调控miR-34a 减轻RPE 氧化应激损伤。
1 材料和方法
1.1 细胞
人视网膜色素上皮细胞系ARPE-19(ATCC)购自上海青旗生物技术发展有限公司,货号:BFN60807591。
1.2 主要试剂与仪器
柚皮素(≥95%,货号:67604-48-2)、过氧化氢(H2O2,≥98%,货号:247079-84-1)均购自美国Sigma-Aldrich 公司;miR-34a 模拟物(mimics)和阴性对照(NC) 购自上海GenePharma 公司;TRIzol RNA 分离试剂(日本TaKaRa,货号:9108-1);SYBR®Premix Ex TaqTM试剂盒(日本TaKaRa,货号:HRR041A-1);PCR 引物的设计合成由美国赛默飞世尔科技公司完成;Lipofectamine 2000(11668019)购自美国Invitrogen 公司;胎牛血清、DMEM 培养基、胰蛋白酶(美国Gbico 公司,货号:16000044、10569-044、25200056),MTT、BCA、JC-1法线粒体膜电位检测及Annexin V-FITC 细胞凋亡检测试剂盒、RIPA 裂解液均购自碧云天生物科技公司(碧云天生物科技公司,货号:C0009 S、P0010、C2006、C1062 L、P0013B);活性氧(ROS)检测试剂盒DCFH-DA(北京索莱宝科技有限公司,货号:CA1410-500);WST -1 法超氧化物歧化酶(superoxide dismutase,SOD)、TBA 法丙二醛(malondialdehyde,MDA)及微板法还原型谷胱甘肽(glutathione,GSH)测定试剂盒(南京建成生物工程研究所,货号:A001-3-2、A003-1-2、A006-2-1);兔抗 人SIRT1 (ab32441)、Bcl-2 (ab32124)、Bax(ab182733)、Caspase-3 (ab32150)、β-actin(ab8227)、山羊抗兔IgG H&L(HRP)(ab205718)购自英国abcam 公司。
细胞培养箱购于美国赛默飞世尔科技公司;IX73 倒置荧光显微镜购于日本奥林巴斯公司;ABI Prism®7300 型荧光定量PCR 仪购于美国应用生物系统公司;BD FACSCanto II 流式细胞仪、iMark680多功能酶标仪及蛋白转膜装置均来于美国Bio-Rad公司。
1.3 实验方法
1.3.1 柚皮素浓度的筛选
ARPE-19 细胞置于DMEM 培养基(100 U/mL青霉素、100 mg/L 链霉素及10%胎牛血清)中培养,条件为37℃,5% CO2。取对数期生长的ARPE-19细胞,以6×103细胞/孔的浓度接种到96 孔板中,待细胞贴壁后,向培养基中添加不同浓度(0、5、10、20、40 μg/mL)的柚皮素预处理24 h,然后用200 μmol/L H2O2处理12 h,每个浓度设置6 个复孔。在37℃的5% CO2中继续培养,随后将MTT 溶液(5 mg/mL,20 μL)在12、24、48 h 时加入各孔并孵育4 h,吸去上层清液后每孔加入150 μL 的DMSO,490 nm波长处测定各孔吸光度(OD),计算细胞存活率。选取可增加ARPE-19 细胞活性的柚皮素浓度为后续实验浓度。细胞存活率=(用药组OD 值-调零孔的OD 值)/(对照组OD 值-调零孔的OD值)×100%。
1.3.2 实验分组及转染
将对数期生长的ARPE-19 细胞分成5 个处理组:(1)对照组:未经处理的ARPE-19 细胞;(2)H2O2组:ARPE-19 细胞用200 μmol/L H2O2处理12 h[3];(3)20 μg/mL 柚皮素组:ARPE-19 细胞用20 μg/mL 柚皮素预处理24 h,再用200 μmol/L H2O2处理12 h;(4) 20 μg/mL 柚皮素+NC 组:用Lipofectamine 2000 将100 nmol/L miR-34a 阴性对照(NC)转染ARPE-19 细胞,转染24 h 后,给予20 μg/mL 柚皮素预处理24 h,再用200 μmol/L H2O2处理12 h;(5)20 μg/mL 柚皮素+miR-34a mimics组:用Lipofectamine 2000 将100 nmol/L miR-34a mimics 转染ARPE-19 细胞,转染24 h 后,给予20 μg/mL 柚皮素预处理24 h,再用200 μmol/L H2O2处理12 h。在37℃的5% CO2中继续培养48 h。
1.3.3 RT-qPCR 检测mRNA
48 h 后从培养ARPE-19 细胞中提取总RNA,后反转录为cDNA 并扩增。20 μL 反应体系:cDNA(200 ng/μL)2 μL,SYBR®Premix Ex TaqTM(2×)10 μL,上下游引物各0.4 μL,ddH2O 7.2 μL。反应条件:40 个循环,先预变性10 min(94℃),后变性15 s(95℃),随后退火20 s(60℃),最后延伸20 s(75℃)。相对miR-34a(对照U6)和SIRT1 mRNA(对照GAPDH)的表达量采用2-ΔΔCt方法计算,引物序列见表1。
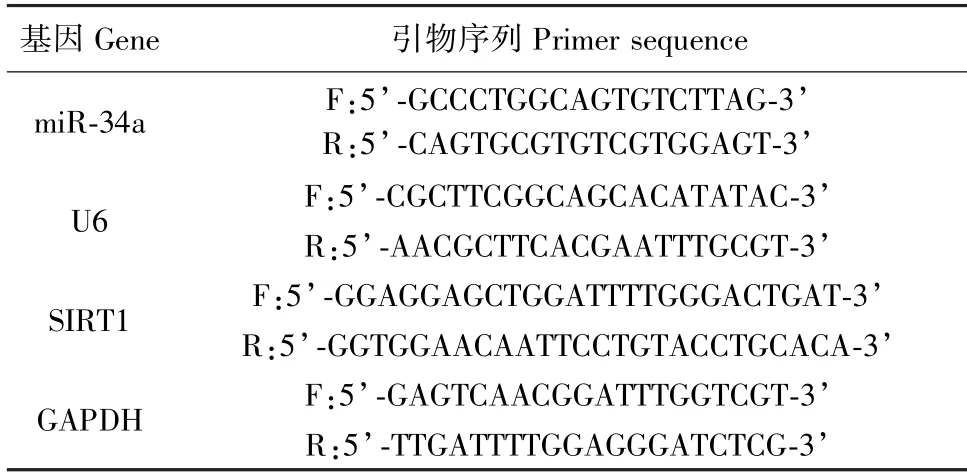
表1 RT-qPCR 引物序列Table 1 Primer sequence of RT-qPCR
1.3.4 MTT 法检测细胞活力
对数期生长ARPE-19 细胞接种到96 孔板,浓度6×103细胞/孔,按照1.3.2 项步骤处理,48 h 后每孔中加入20 μL 的MTT 溶液(5 mg/mL),于培养箱中孵育4 h,吸去上层清液后加入150 μL 的DMSO,各孔吸光度(OD)在490 nm 波长处测定,计算细胞存活率。
1.3.5 流式细胞术检测细胞凋亡
取对数期生长的ARPE-19 细胞,按照1.3.2 项步骤处理,将培养的ARPE-19 细胞用0.25%胰蛋白酶进行消化处理,离心,去除上清液,PBS 洗涤,随后将细胞重悬,密度为每毫升1×106细胞,避光孵育15 min(需加入5 μL Annexin V-FITC 及5 μL PI),细胞凋亡率用流式细胞仪分析并依步骤操作。
1.3.6 荧光探针检测细胞内ROS 水平
取对数期生长的ARPE-19 细胞,按照1.3.2 项步骤处理,ARPE-19 细胞用PBS 洗涤3 次,与10 mmol/L 的2’,7’-二氯荧光黄双乙酸盐(DCFHDA)于37℃避光孵育30 min。后用酶标仪检测二氯荧光素(DCF)荧光(激发波长488 nm、发射波长525 nm),其荧光强度代表ROS 水平。
1.3.7 生化法检测SOD 活性、MDA 和GSH 水平
按照1.3.2 项步骤处理ARPE-19 细胞,收集细胞培养上清液,按照试剂盒说明书的操作检测SOD活性、MDA 和GSH 水平。
1.3.8 JC-1 法检测线粒体膜电位(MMP)
按照线粒体膜电位检测试剂盒(JC-1 法)说明书步骤进行染色。按照1.3.2 项步骤处理,向每孔加入JC-1(DMSO 溶解为浓度5 mg/mL),使终浓度为10 μg/mL,于培养箱中避光孵育20 min,将96 孔板置于多功能荧光酶标仪检测荧光值,激发光为488 nm,发射光为530 nm 时(绿色荧光,检测JC-1单体)的荧光值为A1;激发光为529 nm,发射光为590 nm 时(红色荧光,检测JC-1 聚合物)的荧光值为A2。各组的荧光值A=A2/A1,最终以相对荧光值对MMP 进行定量分析。相对荧光值=实验组A/对照组A。
1.3.9 Western blot 检测SIRT1 和凋亡相关蛋白表达
使用RIPA 裂解液提取ARPE-19 细胞中蛋白质并测定蛋白浓度(BCA 法),随后取等量蛋白质样品上样,每条泳道30 μg/泳道,SDS-PAGE 凝胶电泳,转膜封闭,加入一抗SIRT1、Bcl-2、Bax、Caspase-3、βactin(1 ∶1000),孵育过夜(4℃)后加入二抗(1 ∶5000),室温孵育1 h,ECL 显色。内参均为β-actin,并计算目的条带相对表达水平。
1.4 统计学方法
SPSS 22.0 和Image-Pro Plus 分析数据。平均数± 标准差() 表示,采用单向方差分析(ANOVA)和Tukey 事后检验比较多组测量数据之间的差异。以上所有实验均重复3 次,P<0.05 为差异有统计学意义。
2 结果
2.1 柚皮素的浓度筛选
MTT 结果显示,柚皮素在浓度为10、20 μg/mL时培养48 h 后可显著提高H2O2诱导的ARPE-19细胞活力(P<0.05),且浓度为20 μg/mL 时对ARPE-19 细胞活力的促进作用优于10 μg/mL,而40 μg/mL 柚皮素处理的细胞活性较20 μg/mL 柚皮素明显降低,见图1;因此选择20 μg/mL 柚皮素为后续实验药物干预浓度。

图1 不同浓度的柚皮素对细胞活性的影响Note.Compared with the control group,*P<0.05.Compared with the H2O2 group,#P<0.05.Figure 1 Effects of naringenin at different concentrations on cell viability
2.2 柚皮素对H2O2 诱导的ARPE-19 细胞miR-34a 和SIRT1 mRNA 表达的作用
与对照组相比,H2O2组miR-34a 表达明显升高,而SIRT1 mRNA 表达明显降低(P<0.05);与H2O2组相比,20 μg/mL 柚皮素组和20 μg/mL 柚皮素+mimics NC 组细胞中miR-34a 表达明显降低,SIRT1 mRNA 表达明显升高(P<0.05);与20 μg/mL柚皮素组相比,20 μg/mL 柚皮素+miR-34a mimics组细胞中miR-34a 表达明显升高,SIRT1 mRNA 表达明显降低(P<0.05),见图2。
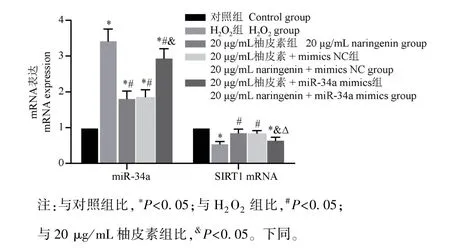
图2 各组细胞中miR-34a 和SIRT1 mRNA 的表达Note.Compared with the control group,*P<0.05.Compared with the H2O2 group,#P <0.05.Compared with the 20 μg/mL naringenin group,&P<0.05.The same as below.Figure 2 Expression of miR-34a and SIRT1 mRNA in each group
2.3 柚皮素对H2O2 诱导的ARPE-19 细胞活力的作用
与对照组相比,H2O2组细胞存活率明显降低(P<0.05);与H2O2组相比,20 μg/mL 柚皮素组和20 μg/mL 柚皮素+mimics NC 组细胞存活率明显升高(P<0.05);与20 μg/mL 柚皮素组相比,20 μg/mL 柚皮素+miR-34a mimics 组细胞存活率明显降低(P<0.05),见图3。

图3 各组细胞中细胞存活率Figure 3 Cell viability in each group of cells
2.4 柚皮素对H2O2 诱导的ARPE-19 细胞凋亡的作用
与对照组(3.28±0.41)%相比,H2O2组ARPE-19 细胞凋亡率(17.85±1.23)%明显升高(P<0.05);与H2O2组相比,20 μg/mL 柚皮素组(9.63±0.95)%和20 μg/mL 柚皮素+mimics NC 组(10.07±1.03)%细胞凋亡率明显降低(P<0.05);与20 μg/mL 柚皮素组相比,20 μg/mL 柚皮素+miR-34a mimics 组(14.86±1.17)%细胞凋亡率明显升高(P<0.05),见图4。

图4 各组ARPE-19 细胞凋亡率Note.A,Control group.B,H2O2 group.C,20 μg/mL naringenin group.D,20 μg/mL naringenin+mimics NC group.E,20 μg/mL naringenin+miR-34a mimics group.Figure 4 Apoptotic rate of ARPE-19 cells in each group
2.5 柚皮素对H2O2 诱导的ARPE-19 细胞内ROS、SOD、MDA 和GSH 含量的作用
与对照组相比,H2O2组ARPE-19 细胞内ROS、MDA 含量明显升高,SOD、GSH 含量明显降低(P<0.05);与H2O2组相比,20 μg/mL 柚皮素组和20 μg/mL 柚皮素+mimics NC 组细胞内ROS、MDA 含量明显降低,SOD、GSH 含量明显升高(P<0.05);与20 μg/mL 柚皮素组相比,20 μg/mL 柚皮素+miR-34a mimics 组细胞内ROS、MDA 含量明显升高,SOD、GSH 含量明显降低(P<0.05),见图5。
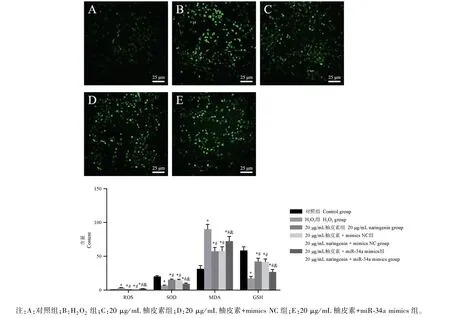
图5 各组ARPE-19 细胞内ROS、SOD、MDA 及GSH 含量Note.A,Control group.B,H2O2 group.C,20 μg/mL naringenin group.D,20 μg/mL naringenin+mimics NC group.E,20 μg/mL naringenin+miR-34a mimics group.Figure 5 Contents of ROS,SOD,MDA and GSH in ARPE-19 cells of each group
2.6 柚皮素对H2O2 诱导的ARPE-19 细胞MMP的作用
与对照组(1.00±0.00)相比,H2O2组ARPE-19细胞内MMP 水平(0.45±0.05) 明显降低(P<0.05);与H2O2组相比,20 μg/mL 柚皮素组(0.83±0.07)和20 μg/mL 柚皮素+mimics NC 组(0.85±0.08)细胞内MMP 水平明显升高(P<0.05);与20 μg/mL 柚皮素组相比,20 μg/mL 柚皮素+miR-34a mimics 组(0.69±0.06)细胞内MMP 水平明显降低(P<0.05),见图6。

图6 各组ARPE-19 细胞MMPFigure 6 MMP in ARPE-19 cells of each group
2.7 柚皮素对H2O2 诱导的ARPE-19 细胞SIRT1和凋亡相关蛋白表达的作用
与对照组相比,H2O2组ARPE-19 细胞SIRT1、Bcl-2 表达明显降低,而Bax、Caspase-3 表达明显升高(P<0.05);与H2O2组相比,20 μg/mL 柚皮素组和20 μg/mL 柚皮素+mimics NC 组细胞SIRT1、Bcl-2 表达明显升高,而Bax、Caspase-3 表达明显降低(P<0.05);与20 μg/mL 柚皮素组相比,20 μg/mL 柚皮素+miR-34a mimics 组细胞SIRT1、Bcl-2 表达明显降低,而Bax、Caspase-3 表达明显升高(P<0.05),见图7。

图7 各组细胞SIRT1、Bcl-2、Bax、Caspase-3 蛋白表达Figure 7 Protein expression of SIRT1,Bcl-2,Bax and Caspase-3 in each group
3 讨论
眼睛持续暴露于环境刺激中,如辐射、化学物质、大气中的氧气[13]。在正常情况下,这些刺激引起的氧化应激可以通过机体的抗氧化系统消除[14]。然而,随着人口老龄化,年龄介导的氧化应激和抗氧化剂水平下降导致蛋白质修饰和氧化,引起RPE功能障碍和随后的细胞凋亡[15],RPE 细胞介导的氧化应激在AMD 的发病机理和进程中起着重要作用。氧化应激是ROS 水平在机体内大量产生和积累的结果。在各种ROS 中,H2O2被确定为可以介导各种细胞作用的第二信使分子,其过量产生是氧化还原信号传导和氧化应激的中心枢纽[16]。因此,H2O2通常在体外实验中用于诱导氧化应激[17]。据报道,用200 μmol/L 的H2O2处理ARPE-19 细胞12 h,可显著抑制ARPE-19 细胞活力,促进ARPE-19细胞ROS 产生和凋亡,并诱导细胞出现氧化应激损伤[3]。因此,本研究使用200 μmol/L 的H2O2诱导建立RPE 细胞氧化损伤模型。有文献报道,阿霉素会诱导心肌细胞损伤,产生大量的ROS,柚皮素可升高GSH 含量及SOD 酶活力,降低ROS 水平,产生抗氧化应激作用,减轻心肌细胞损伤[18-19]。本研究发现H2O2诱导后细胞活力下降,而ROS 水平增加,柚皮素减轻了RPE 细胞中H2O2对细胞活力和ROS产生的影响。此外,柚皮素还可以降低H2O2诱导的RPE 细胞中MDA 水平,增加内源性抗氧化剂GSH 及抗氧化酶SOD 活性。表明柚皮素处理提高了H2O2诱导的RPE 细胞中的GSH 水平和SOD 活性。提示柚皮素处理逆转了RPE 细胞中H2O2诱导的氧化应激。
ROS 介导的氧化应激可能导致RPE 细胞凋亡[20]。而柚皮素可以降低Caspase-3 蛋白表达,升高Bcl-2 蛋白水平及Bcl-2/Bax 比值,抑制细胞凋亡,减轻心肌细胞损伤[18-19]。本研究结果显示,柚皮素处理可抑制H2O2诱导的RPE 细胞凋亡,Western blot 结果进一步显示柚皮素抑制了RPE 细胞中促凋亡Bax 蛋白的表达,并诱导抗凋亡蛋白Bcl-2 的表达。此外,柚皮素还阻止了H2O2诱导的RPE 细胞中Caspase-3 的活化。MMP 参与细胞凋亡的发展和进程,MMP 的降低是细胞凋亡的特异性标志[21]。JC-1 是一种碳氰化合物类阳离子荧光染料,广泛用于检测MMP。正常情况下,JC-1 能依赖跨膜电位聚集在线粒体的基质中,形成红色荧光的聚合物;当发生凋亡则降低跨膜电位,释放线粒体中的JC-1,在胞质内以单体的形式存在发绿色荧光[22];柚皮素可明显升高红/绿荧光比值,升高MMP 水平。这些结果均提示柚皮素可抑制H2O2诱导的RPE 细胞凋亡。
此外,本研究发现H2O2诱导的RPE 细胞中miR-34a 水平显著增加,而SIRT1 mRNA 水平显著降低。有报道显示miR-34a 是RPE 细胞中高度表达的调节因子之一,miR-34a 上调可通过直接或间接抑制c-Met 和其他细胞周期相关分子的表达来抑制RPE 细胞的增殖和迁移[7],证实了其可调节RPE细胞功能。SIRT1 已被证明是miR-34a 的靶基因,在细胞分化、衰老、凋亡、转录调节、氧化应激等多种重要的生物学过程中发挥重要作用;既往研究已经证实SIRT1 可通过抗炎、抗氧化、减少凋亡等机制发挥细胞保护作用[23-24]。Tong 等[8]发现过表达miR-34a 可显著抑制SIRT1 转录后表达,同时H2O2诱导的ARPE-19 细胞对氧化应激的耐受性降低。本研究结果显示柚皮素可下调miR-34a,促进SIRT1 mRNA 和蛋白表达;采用Lipofectamine 2000 将miR-34a 转染ARPE-19 细胞上调miR-34a,结果显示miR-34a 转染ARPE-19 细胞后,miR-34a 水平明显增加,而SIRT1 的表达降低,明显逆转了柚皮素对H2O2诱导的RPE 细胞氧化损伤的保护作用。提示,柚皮素的保护作用可能是由miR-34a/SIRT1 信号通路介导的。
综上所述,柚皮素可通过下调miR-34a,促进SIRT1 表达,抑制RPE 细胞凋亡,保护H2O2诱导的RPE 细胞氧化应激损伤。然而,本研究存在一定的局限性,H2O2诱导氧化损伤后柚皮素是否能发挥较长时间的保护作用需要进一步的实验,且需要进行体内动物研究以及柚皮素与其他药物相比的功效进一步明确柚皮素的保护作用。

